Serviços Personalizados
Journal
Artigo
Indicadores
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Hidrobiológica
versão impressa ISSN 0188-8897
Hidrobiológica vol.18 no.2 Ciudad de México Ago. 2008
Efecto de la salinidad sobre la fisiología energética del camarón blanco Litopenaeus vannamei (Boone)
Effect of salinity on physiological energetics of white shrimp Litopenaeus vannamei (Boone)
Gustavo Valdez1, Fernando Díaz1*Ana Denisse Re1 y Elizabeth Sierra1
1 Laboratorio de Ecofisiología de Organismos Acuáticos, Departamento de Biotecnología Marina. Centro de Investigación Científica y de Educación Superior de Ensenada (CICESE), Ensenada Baja California México.
*Autor para correspondencia:
Fernando Díaz.
Laboratorio de Ecofisiología de Organismos Acuáticos.
E–mail: fdiaz@cicese.mx
Recibido: 23 de marzo de 2007.
Aceptado: 15 de mayo de 2008.
RESUMEN
Se determinó el balance energético en juveniles de Litopenaeus vannamei, aclimatados a la salinidad como hiperosmóticos (20 ups), isosmóticos (26 ups), o hiposmóticos (32 ups). Además, se calculó la razón atómica O:N. La tasa de ingestión, el consumo de oxígeno, la excreción de amonio y el campo de crecimiento fueron afectados significativamente (p < 0.05) cuando los organismos fueron aclimatados a 20, 26 y 32 ups. La mayor cantidad de energía ingerida contenida en el alimento se determinó en los organismos mantenidos en condiciones de 26 ups de salinidad. El menor gasto energético derivado a metabolismo de rutina y la excreción de productos nitrogenados se obtuvo en los animales mantenidos con 26 ups. La mayor cantidad de energía canalizada al campo de crecimiento (671.1 J g–1 dia1 p.s.) se encontró en los camarones aclimatados a la salinidad de 26 ups. La razón O:N calculada para los juveniles indicó un catabolismo de carbohidratos para los organismos mantenidos en la condición isosmótica. El incremento de calor aparente, la producción de heces y la energía derivada hacia la formación del exoesqueleto, no fueron diferentes significativamente (p > 0.05) en los camarones expuestos a las tres salinidades. Para optimizar las condiciones de cultivo de Litopenaeus vannamei se recomienda mantener a los juveniles en la salinidad para la cual es isosmótico (26 ups), evitando el estrés ambiental, lo que desde el punto de vista fisiológico se canaliza en una mayor cantidad de energía hacia el campo de crecimiento.
Palabras clave: Fisiología energética, Litopenaeus vannamei, salinidad, razón atómica O:N.
ABSTRACT
The energy balance was determined with in Litopenaeus vannamei, juveniles acclimated to salinity where they were hyperosmotic (20 ups), isosmotic (26 ups), and hypo–osmotic (32 ups). Also O:N atomic ratio was calculated. The ingestion rate, oxygen consumption, ammonium excretion and scope for growth were affected significantly (p < 0.05) when the organisms were acclimated at 20, 26 and 32 ups. The highest energy contained from the food consumed was obtained in the organisms maintained in 26 ups. The lowest energy expense derived to routine metabolism, and excretion of nitrogenous products was obtained in the animals maintained at 26 ups. The high quantity of energy channeled to the scope for growth (671.1 J g–1 day–1 d.w.) was obtained in the shrimps acclimated to salinity of 26 ups. The O:N atomic ratio calculated for the juveniles indicated a catabolism of carbohydrates for the organisms maintained in the isosmotic condition. The apparent heat increment, the feces production, and energy lost by exuviae, not were significantly different (p > 0.05) in the shrimps exposed to the three salinities. We recommend maintaining Litopenaeus vannamei juveniles at the salinity level which is isosmotic (26 ups), where they are free of environmental stress, these conditions for white shrimp juveniles would enhance production in the cultivation of this species.
Key words: Physiological energetics, Litopenaeus vannamei, salinity, O:N atomic ratio.
INTRODUCCIÓN
En las respuestas fisiológicas de los peneidos eurihalinos, los factores ambientales considerados con mayor influencia son la temperatura y la salinidad, porque les provocan efectos biológicos de gran complejidad (Chen et al., 1995; Wyban et al., 1995). Se han realizado estudios acerca del efecto de la temperatura y salinidad sobre diferentes respuestas fisiológicas en peneidos como Farfantepenaeus aztecus (Ives) (Howe et al., 1982; Hernández Rodríguez & Díaz Herrera, 1995; Re et al., 2005), Litopenaeus setiferus (Linnaeus) (McFarland & Lee, 1963; Castille & Lawrence, 1981; Brito et al., 2000), Farfantepenaeus duorarum (Burkenroad) (Williams, 1960; Castille & Lawrence, 1981), Farfantepenaeus brasilensis (Latreille) (Brito et al., 2000), Penaeus monodon (Fabricius) (Cawthorne et al., 1983), Litopenaeus stylirostris (Stimpson) (Castille & Lawrence, 1981; Lignot et al., 1999; Rosas et al., 2000; Chim et al., 2003; Díaz et al., 2004; Re et al., 2004 y 2006), Fenneropenaeus indicus (Milne–Edwards) (Parado Estepa et al., 1987), Penaeus semisulcatus (De Hann) (Clark, 1992), Fenneropenaeus chinensis (Osbeck) (Chen et al., 1995; Chen & Lin, 1998) y Litopenaeus vannamei (Boone) (Ponce Palafox et al., 1997; Jiang et al., 2000; Díaz et al., 2001; Gong et al., 2004).
Sin embargo, la información disponible no siempre es consistente con los datos de campo (Venkataramaiah et al., 1974). Esto se debe a que, frecuentemente, los estudios se enfocan en el efecto de un solo factor ambiental y además en la mayoría de los estudios se han usado postlarvas, prestando menor atención a las respuestas de juveniles y adultos (Ponce Palafox et al., 1997).
El camarón blanco del Pacífico, Litopenaeus vannamei, se distribuye naturalmente a través de la costa del Pacífico desde el Golfo de California al norte de Perú. Esta especie es conocida por habitar en un amplio intervalo de salinidades desde 1–2 ups hasta 40 ups (Menz & Blake, 1980). L. vannamei exhibe un patrón de regulación hiperosmótico en bajas salinidades y un patrón de regulación hipoosmótico en altas, con un punto isosmótico entre 25–26 ups (Castille & Lawrence, 1981; Díaz et al., 2001; Gong et al., 2004). Es uno de los peneidos más estudiados; ya que es el soporte de muchas pesquerías comerciales y es la especie de cultivo más importante a lo largo de la costa este del Pacífico y algunas zonas de Asia. Esto último se debe a que este decápodo presenta características tales como un requerimiento relativamente bajo de proteína en la dieta, entre el 25 y 35%; tiene una supervivencia y crecimiento aceptables en altas densidades de cultivo (Rosenberry, 1994; Treece, 2000). Resultados de diferentes investigaciones muestran que la supervivencia y la tasa de crecimiento de este organismo dependen de la temperatura (Wyban et al., 1995), la salinidad (Bray et al., 1994) y de la interacción temperatura–salinidad (Ponce Palafox et al., 1997; Díaz et al., 2001; Zhang et al., 2006).
Se ha mencionado que el trabajo osmótico de un organismo es mínimo cuando el medio externo y los fluidos corporales están en equilibrio; además de que bajo condiciones isosmóticas es posible cultivar el máximo número de organismos (Panikkar, 1968).
Los estudios de bioenergética permiten describir, explicar y predecir la condición o estado fisiológico de los organismos en condiciones de cultivo a través de la ecuación modificada de Klekowski y Duncan (1975):
C = P + R + F + U + ICA +M.
Donde C es la energía ingerida a través del alimento consumido, P es la fracción de la energía que corresponde al campo de crecimiento en los organismos juveniles o producción de gametos en los adultos, R es la proporción de energía que se canaliza a metabolismo respiratorio, F es la energía contenida en la materia no digerida, U es la energía que se excreta como productos nitrogenados, ICA es el costo energético asociado con la digestión y utilización del alimento y M es la energía que se utiliza en el proceso de la ecdisis (Rosas et al., 2003).
En juveniles y postlarvas de Litopenaeus vannamei Pascual et al. (2004), Zhu et al. (2004), Wang et al. (2004), Cheng et al. (2006) y Jiménez–Yan et al. (2006) realizaron estudios de balance energético para conocer el efecto de diferentes niveles proteicos, de carbohidratos, condición inmunológica, iones y mineralización de los tejidos, así como de la inclusión de diferentes niveles de de proteína de origen animal y vegetal en la dieta.
Se ha reportado por Lemos et al. (2001) que la variación de la salinidad causó cambios en la composición bioquímica en postlarvas de Farfantepenaeus paulensis (Pérez–Farfante) lo que provocó modificaciones en el contenido energético de los organismos.
Así mismo, Rosas et al. (2002) mencionaron que en juveniles de L. vannamei la salinidad es capaz de influenciar el metabolismo y utilización de algunos nutrimentos, como los carbohidratos.
El presente estudio fue diseñado para determinar el efecto de tres salinidades sobre los diferentes elementos del balance energético en juveniles de Litopenaeus vannamei y evaluar si en la condición isosmótica se propicia la mayor eficiencia energética, lo que promoverá un incremento en la supervivencia y el crecimiento de los organismos.
MATERIALES Y MÉTODOS
Las postlarvas Pl21 de L. vannamei (n = 10,000) fueron obtenidas del laboratorio de producción AQUANOVA ubicado en Mazatlán, Sinaloa, México. Las postlarvas permanecieron en 4 estanques de 2000 L, con flujo continuo de agua de mar, aireación constante y calentadores sumergibles de 1000 W, lo que permitió mantener condiciones de 35 ups de salinidad y 28 °C de temperatura hasta que alcanzaron la etapa juvenil (considerada como tal una vez que los ejemplares alcanzaron 1 gramo). Durante este periodo los organismos fueron alimentados diariamente con el producto comercial Rangen con 40% de proteína, en dos raciones que en conjunto equivalían al 5% de la biomasa total de los organismos.
Los juveniles con un intervalo de peso húmedo de 8.36 ± 0.79 g fueron distribuidos en tres estanques circulares de 500 L. Las condiciones experimentales fueron la salinidad del punto isosmótico de L. vannamei (26 ups), determinada por Díaz et al. (2001) y Gong et al. (2004), así como una salinidad de 20 ups donde los organismos estuvieron en un medio hiposmótico y otra de 32 ups, en la que estuvieron en un medio hiperosmótico. Para obtener el agua con la salinidad deseada se realizaron diluciones de agua de mar (34 ups) con agua dulce, la tasa de disminución fue de 2 ups por día. Cuando se alcanzó la salinidad deseada, los organismos permanecieron en esas condiciones durante 15 días, para su aclimatación. La salinidad en los estanques se midió diariamente con un salinometro YSI modelo Y30 SCT, la temperatura fue de 28 ºC, definida por Valdez (2002) como la óptima para esta especie. Para mantener la calidad del agua y compensar las pérdidas causadas por la evaporación, se efectuaron recambios del 50% del volumen total de agua de los estanques experimentales mediante un sistema de dilución semiautomático a base de válvulas milimétricas. De esta forma se mantuvo también la salinidad deseada. La tasa de recambio fue de 10.5–11.0 L h–1. Los parámetros fisicoquímicos del agua para todas las condiciones experimentales fueron oxígeno disuelto 6.4 ± 0.5 mg L–1, pH 7.9 ± 0.2, amonio 0.74 ± 0.032 mg L–1, temperatura 28.0 ± 0.85 °C.
Para conocer el efecto de la salinidad sobre las diferentes respuestas fisiológicas de los organismos se realizó un balance energético, utilizando la ecuación modificada de Klekowski y Duncan (1975):
C = P + R + F + U + ICA + M.
Para ello se utilizaron 156 organismos provenientes de cada salinidad experimental, los cuales se distribuyeron de manera individual en 26 recipientes plásticos de tres litros que se colocaron dentro de cada estanque circular de 500 L, lo que equivale a una densidad de 0.1 camarones L–1. Para cada condición experimental de salinidad se realizaron dos repeticiones. Dichos recipientes tenían ventanas laterales cubiertas con malla de nytex de 500 μm para permitir el intercambio de agua con el estanque y a su vez impedir la salida del organismo, así como del alimento y de las heces.
Se les proporcionó aireación constante y se practicaron recambios de agua del 50% diariamente, en la forma descrita anteriormente. A los camarones se les proporcionó diariamente, de manera individual, una ración de 0.4 g de alimento comercial Rangen con 40% de proteína (Tabla 1).
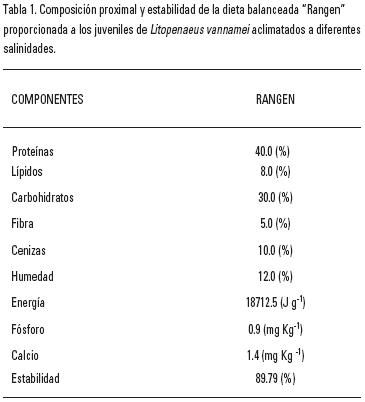
Los componentes de la ecuación se calcularon de la siguiente manera:
Se suministró la ración diaria de alimento (C) y se dejó durante 2 horas en los recipientes que contenían a los organismos. Pasado este período se recogió el alimento no consumido por medio de un sifón acoplado a un sistema de succión por vacío utilizando una malla de 80 µm colocada en el extremo distal del mismo. El alimento remanente proveniente de cada condición experimental fue lavado con formiato de amonio al 4% para eliminar las sales adsorbidas. Se colocó en una estufa a 60 °C durante cuatro días para obtener su peso seco. Para conocer la estabilidad de la dieta debido al movimiento del agua, aireación y sifoneo, se utilizó una modificación de la metodología descrita por Obaldo et al. (2002), se colocó 1 g de alimento en 10 cubetas dentro de los estanques de 500 L para cada condición de salinidad, pero sin organismos y el alimento permaneció en ellas durante dos horas (método estático). El alimento fue recolectado, de la forma descrita anteriormente, se colocó en una estufa a 60 °C para obtener su peso seco y se calculó la estabilidad del alimento mediante la fórmula de retención de materia seca (RMS):
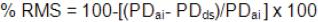
Donde:
PDai = Peso de la dieta antes de la inmersión.
PDds = Peso seco de la dieta después del tiempo de inmersión.
Los datos del alimento consumido fueron corregidos por el factor de dilución de la dieta para cada condición experimental.
Para medir el consumo de oxígeno de rutina (R) los camarones provenientes de cada condición experimental (20, 26 y 32 ups), se colocaron individualmente 12 horas antes de realizar las mediciones en 20 matraces de 2.8 L conectados a un sistema respirométrico semiabierto como el descrito por Díaz et al. (2007). Para evitar variaciones en el consumo de oxígeno debidas al estatus nutricional (Beamish & Trippel, 1990), los camarones fueron mantenidos sin alimentar durante 48 h antes de las mediciones. Se realizaron dos repeticiones para cada condición experimental. Se obtuvieron muestras iníciales de agua de 3 mL de cada uno de los matraces por medio del desplazamiento de agua al inflar un globo en el interior de cada matraz, a través de un sistema de mangueras (para no tener cambios en el contenido de oxígeno disuelto), que se conectaron a una cámara cerrada herméticamente provista de un sensor polarográfico; la concentración inicial del gas se midió con un oxímetro digital (YSI 52 ± 0.01 mg L–1), a continuación los matraces permanecieron cerrados durante dos horas ya que de acuerdo a Stern et al. (1984) es el tiempo adecuado para que el oxígeno disuelto no disminuya por debajo del 30% de saturación y no cause estrés en los organismos. Transcurrido este tiempo se tomaron nuevamente muestras de agua de cada matraz para medir la concentración final de oxígeno disuelto. La diferencia entre la concentración inicial y final del gas fue el consumo de oxígeno de los organismos y se expresó en mg O2 consumido h–1 g–1 de peso seco.
Las heces (F) fueron recolectadas 2 horas después de proporcionar el alimento, esta operación se repitió 6 horas después y antes de volver a alimentar a los organismos al día siguiente. La recolecta y lavado de heces se realizó de igual manera que la descrita para el alimento. De la misma forma que con el alimento se determinó el peso seco. El contenido calórico de la dieta y heces provenientes de cada condición experimental, fue calculado en un calorímetro semimicro PARR modelo 1425 estandarizado con ácido benzoico como lo describen Phillipson (1964) y Prus (1975).
La excreción de amonio (U) de los organismos provenientes de cada condición experimental se midió de manera simultánea a la determinación de consumo de oxígeno. Para ello se tomaron 10 mL de agua de cada uno de los matraces. La concentración de amonio en las muestras se cuantificó con el método de azul de indofenol (Rodier, 1981) empleando un espectrofotómetro ELIPTICA 2000. Los valores de excreción de amonio de los camarones en las diferentes condiciones experimentales se transformaron a unidades de energía empleando el equivalente nitrocalórico de 5.73 cal mg–1 NH4+ de amonio excretado (Clifford & Brick, 1979).
Durante esta fase experimental se mantuvo un control en un matraz sin organismos, para medir el consumo de oxígeno y la producción de amonio de los microorganismos presentes en el sistema respirométrico y hacer las correcciones pertinentes.
El incremento de calor aparente (ICA) se evaluó como la diferencia entre el consumo de oxígeno de los organismos recién alimentados y el consumo de oxígeno de los organismos sin alimentar.
Al finalizar los experimentos de respirometría, inmediatamente los organismos se sacrificaron, se etiquetaron y se colocaron en una estufa a 60 °C durante 6 días. A continuación se pesaron para obtener su peso seco. El consumo de oxígeno de rutina y el incremento de calor aparente se transformaron a unidades de energía mediante el uso del equivalente oxicalórico de 3.53 cal mg–1 de O2 consumido (Elliot & Davison, 1975).
La energía destinada a la formación de exoesqueleto (M) se calculó a partir del análisis del contenido calórico de las exuvias, que fueron recolectadas diariamente de los recipientes; las mudas completas se colocaron en una estufa a 60 °C durante cuatro días para su secado.
El campo de crecimiento (P) se estimó como la diferencia entre la energía del alimento consumido y la suma de la energía utilizada en la producción de heces, respiración, excreción de amonio, incremento de calor aparente y mudas.
P = C – (R + F + U + ICA + M)
El alimento consumido, la producción de heces, el consumo de oxígeno de rutina, la excreción de amonio, el incremento de calor aparente, y las mudas, se transformaron a Joules con el factor de conversión de 1 caloría = 4.1840 Joules (Gnaiger, 1983) y se expresaron en J g–1 día–1 peso seco.
El índice O:N se estimó con los valores del consumo de oxígeno y la excreción de amonio de los camarones obtenidos en el sistema respirométrico con las diferentes salinidades experimentales. Las tasas fisiológicas determinadas para ambos componentes fueron transformadas a átomos–gramo para el cálculo de la razón O:N, utilizando los principios de la termoquímica respiratoria (Brody, 1954; Gnaiger, 1983). Este índice se utilizó para estimar la relación de proteínas, lípidos y carbohidratos que fueron utilizados como fuente energética por los organismos en las diferentes condiciones experimentales. Se consideró que valores de esta razón que fueran de 3 a 16 indicaron oxidación netamente proteica, valores entre 50 y 60 indicaron catabolismo de la misma cantidad de proteínas–lípidos y valores superiores a 60 el empleo de carbohidratos (Mayzaud & Conover, 1988).
Previo cálculo de la normalidad y homoscedasticidad de los datos (Sigma Stat) se aplicó la prueba no paramétrica de Kruskal–Wallis (Zar, 1999) para evaluar el efecto de la salinidad sobre los diferentes parámetros que conforman la ecuación del balance energético de los juveniles del camarón blanco. Cuando se encontraron diferencias significativas se utilizó el método de Dunn para aislar los grupos que diferían entre sí (Sokal & Rohlf, 1979; Zar, 1999).
RESULTADOS
La energía ingerida en el alimento por los organismos mantenidos en 20 ups fue de 1039.9 J g–1 día–1, de 1232.2 J g–1 día–1 para los aclimatados a 26 ups y 1054.0 J g–1 día–1 peso seco para los expuestos a la condición de 32 ups. Se obtuvieron diferencias significativas (p < 0.05) entre la energía ingerida a través del alimento por los juveniles de L. vannamei expuestos a las diferentes condiciones experimentales (Tabla 2).
En los camarones sometidos a las distintas salinidades experimentales, la pérdida de energía por producción de heces mostró un intervalo de 138.6 a 170.2 J g–1 día–1 peso seco, lo que representó del 10.9 a 16.5% de la energía incorporada en el alimento (Tabla 2). No se encontraron diferencias significativas (p > 0.05) entre la cantidad de energía eliminada en la producción de heces en los organismos expuestos a las diferentes salinidades.
La energía que los camarones aclimatados a 26 ups derivaron al metabolismo de rutina fue de 208.2 J g–1 día–1 peso seco (Tabla 2), significativamente menor (p < 0.05) que la de los organismos expuestos a las otras salinidades experimentales. La mayor demanda energética se obtuvo en los camarones mantenidos en la salinidad de 32 ups y fue de 264.0 J g–1 día–1 peso seco (Tabla 2).
Cuando los organismos fueron alimentados, el incremento aparente de calor (ICA) representó un aumento en la energía invertida en los procesos metabólicos del 31.6 al 37.5% en las tres condiciones de salinidad (Tabla 2). Dicho aumento representó una pérdida del 7.64 al 8.92% de la energía ingerida a través del alimento por los organismos. No se obtuvieron diferencias significativas (p > 0.05) entre el ICA de los organismos expuestos a las salinidades de 20, 26 y 32 ups (Tabla 2).
La energía derivada a la excreción de amonio por los juveniles de L. vannamei fue mayor en los organismos expuestos a la salinidad de 20 ups, y disminuyó en los aclimatados a 26 y 32 ups (Tabla 2). Se obtuvieron diferencias significativas (p < 0.05) en el gasto energético que los camarones destinaron a este proceso fisiológico.
La energía invertida en las exuvias por los camarones aclimatados a las diferentes salinidades mostró un intervalo de 141.9 a 152.6 J g–1 día–1 peso seco (Tabla 2). No se encontraron diferencias significativas (p > 0.05) entre la cantidad de energía destinada a la formación de este tejido por los juveniles de L. vannamei.
La energía potencial de crecimiento que destinaron los camarones mantenidos en salinidad de 20 ups fue del 36.5%, los que estuvieron en la condición isosmótica destinaron el 54.4%, y los que se mantuvieron en 32 ups canalizaron a este proceso el 38.8% de la energía ingerida con el alimento (Tabla 2). La salinidad causó que se apreciaran diferencias significativas (p < 0.05) en la energía potencial para crecimiento de los juveniles en las diferentes condiciones experimentales.
Los valores de la razón atómica O:N estimados para los juveniles de L. vannamei mantenidos en condiciones isosmóticas presentaron el valor mayor para esta razón, el cual fue de 153.3. En los organismos expuestos a 32 ups esta razón fue de 95.6. El valor mínimo para la razón O:N se registró en los juveniles aclimatados a 20 ups, siendo de 49.7 (Fig. 1).
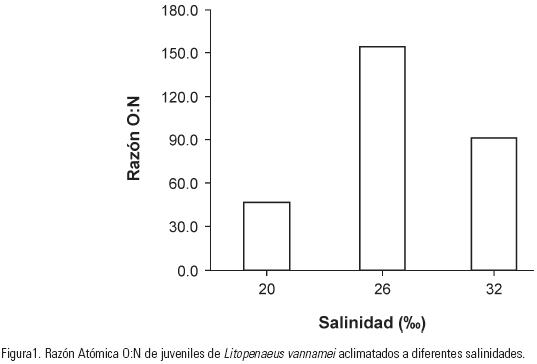
DISCUSION
La habilidad de los peneidos para obtener reservas energéticas y distribuirlas de manera efectiva entre los requerimientos para mantenimiento y crecimiento depende del efecto de los factores ambientales, la salinidad es uno de los que influye sobre el metabolismo de estos organismos (Rosas et al., 2001; Zhu et al., 2006).
La exposición de los juveniles de L. vannamei a condiciones teóricamente favorables (26 ups) causó un efecto significativo en la ingestión de energía a través del consumo de alimento con respecto a los organismos mantenidos en las salinidades de 20 y 32 ups. Se han descrito efectos similares de la salinidad sobre la tasa de ingestión en otros crustáceos. Guerin y Stickle (1997) reportaron que la tasa de energía consumida por juveniles de Callinectes similis (Williams) fue significativamente mayor cuando las jaibas se encontraron en la salinidad óptima de 35 ups. En juveniles de L. vannamei expuestos a salinidades de 15 y 40 ups, y alimentados con diferentes niveles de carbohidratos en la dieta, Rosas et al. (2002) obtuvieron un mayor consumo de energía a través del alimento ingerido en los organismos mantenidos en condiciones de 15 ups. Esto indicó que esta especie opera en su óptimo fisiológico en salinidades donde es isosmótica, acumulando el máximo de energía para canalizarlo a crecimiento.
La salinidad en que los juveniles de L. vannamei utilizaron menos energía destinada a cubrir los procesos metabólicos de rutina fue la condición de 26 ups. Lo anterior era de esperarse, ya que esta salinidad es la que Díaz et al. (2001) y Gong et al. (2004) reportaron como a la que los juveniles de L. vannamei se encuentran en un medio isosmótico y por lo tanto, no requieren de procesos activos para compensar los cambios en la presión osmótica del medio interno (Panikkar, 1968). La mayor demanda energética se registró en la salinidad de 32 ups, en la que los organismos fueron hiposmóticos, y se obtuvieron valores intermedios en 20 ups, donde fueron hiperosmóticos. De manera similar Rosas et al. (2001) describieron en juveniles de esta especie que las mayores demandas energéticas para cubrir el metabolismo de rutina ocurrieron cuando fueron expuestos a condiciones de salinidad de 40 ups. En los juveniles de L. vannamei mantenidos en las tres salinidades, el consumo de oxígeno aumentó después de consumir alimento, alcanzando su valor máximo, en la mayoría de los casos, a las dos horas posteriores de haber sido alimentado. Este periodo de tiempo coincide con el reportado por Rosas et al. (2002) para que juveniles de esta especie de camarón alcancen el máximo consumo de oxígeno después de consumir alimento.
En este estudio no se apreciaron diferencias entre la magnitud del incremento aparente de calor (ICA) de los juveniles ocasionadas por las condiciones experimentales a las que fueron expuestos. Resultados similares obtuvieron Rosas et al. (2002) cuando se mantuvo a juveniles del camarón blanco en salinidades de 15 y 40 ups, no determinándose diferencias significativas en el incremento aparente de calor después de alimentarlos con la misma dieta.
En juveniles de P. monodon aclimatados a tres salinidades y alimentados con el producto comercial Du Preez et al. (1992) obtuvieron un aumento en el consumo de oxígeno del 2 al 17% y no encontraron diferencias significativas en el ICA en los organismos mantenidos en las tres salinidades. Beamish yTrippel (1990) mencionan que los factores que modifican la magnitud del incremento aparente de calor, resultado de la ingestión de alimento, dependen de la naturaleza de la dieta, el tamaño, la ración y la composición química del alimento. Por lo que no existen diferencias entre el incremento aparente de calor y su duración, debido a que los organismos se alimentaron con la misma dieta.
En crustáceos, la mayor parte del amonio excretado es producto del catabolismo de aminoácidos obtenidos a través de la dieta. La excreción amoniacal de los juveniles de L. vannamei en este trabajo estuvo relacionada con la salinidad, ya que se observaron diferencias significativas entre la energía invertida en este proceso por los organismos en las tres condiciones de salinidad.
Se observó que las mayores concentraciones de amonio fueron producidas por los camarones en la salinidad donde fueron hiperosmóticos, los organismos mantenidos en condiciones isosmóticas excretaron las menores concentraciones. Valores intermedios fueron registrados en los juveniles que estuvieron en condiciones hiposmóticas. Tendencias similares para esta tasa fisiológica con respecto a la salinidad fueron descritas por Jiang et al. (2000) para juveniles de esta especie, cuando expusieron a los organismos a salinidades de 10 a 40 ups. Se reportó por Jiang et al. (2000) que la menor tasa de excreción nitrogenada se obtuvo a 26.6 ups, lo cual coincide con los datos de este estudio y con lo mencionado por Díaz et al. (2001), ya que en ambos trabajos el menor gasto energético por excreción amoniacal se determinó en los organismos expuestos en el punto isosmótico de 26 ups. Rosas et al. (2002) observaron una mayor excreción de amonio en juveniles de L. vannamei mantenidos en 15 ups con respecto a otros cultivados en 40 ups de salinidad. Chen y Nan (1993) reportaron un descenso significativo de la tasa de excreción de amonio en F. chinensis cuando fueron transferidos de 15 a 30 ups. En Scylla serrata (Forskal), Chen y Chia (1996) describieron que la excreción de amonio de esos cangrejos disminuyó cuando fueron expuestos al intervalo de salinidad de 15–25 ups.
El aumento en la tasa de excreción nitrogenada de los juveniles de L. vannamei aclimatados a bajas salinidades puede ser explicado por un aumento en el catabolismo de los aminoácidos involucrados en la regulación de la presión osmótica de la hemolinfa. Lo anterior sucede porque se necesita una absorción activa de sodio para compensar su pérdida en organismos que se encuentran en medios diluidos. El incremento en la excreción de amonio favorece la captación de sodio mediante el funcionamiento de la bomba de intercambio Na+ / NH4+, para mantener la concentración osmótica de la hemolinfa (Péqueux, 1995). Hernández Rodríguez y Díaz Herrera (1995), Díaz et al. (2001), Re et al. (2004) y Díaz et al. (2004) han sugerido a este mecanismo fisiológico como responsable principal del mantenimiento de la concentración osmótica en camarones peneidos cuando éstos se encuentran en medios hiperosmóticos.
Los juveniles de L. vannamei destinaron un intervalo de 11.5 a 14.8% de la energía obtenida en el alimento a la formación del exoesqueleto cuando se aclimataron a las diferentes salinidades. Valores similares han sido reportados para otros decápodos, como Carcinus maenas (Linnaeus) y Crangon crangon (Linnaeus) quienes invirtieron el 10 y 17%, respectivamente, de la energía ingerida a través del alimento en la formación del exoesqueleto (Klein–Breteler, 1975; Vernberg, 1987). Logan y Epifanio (1978) mencionaron que la perdida energética durante la muda de Homarus americanus (Milne–Edwards) fue del 10% de la energía ingerida. En los juveniles del camarón blanco el gasto energético que destinaron al proceso de la muda no fue afectado por la salinidad, ya que estuvieron dentro del intervalo reportado para varias especies de crustáceos.
El componente del balance energético que se refiere a la inversión de energía en el campo de crecimiento representó para los organismos que estuvieron aclimatados a la salinidad de 26 ups el 54.4% de la energía ingerida a través del alimento. Se ha demostrado que en otras especies de peneidos el crecimiento ha sido afectado de diferente manera por la salinidad, en juveniles de Fenneropenaeus merguiensis (De Man) alcanzaron un máximo aumento en biomasa, crecimiento y supervivencia cuando fueron cultivados en 25 ups (Staples & Heales, 1991). Postlarvas de Melicertus kerathurus (Forskal) mantenidas en 25 ups tuvieron valores menores de peso (húmedo y seco), talla e índices de condición que cuando fueron expuestas a 35 ups (Mourente & Rodríguez, 1997).
Para poblaciones de Callinectes sapidus (Rathbun) de Louisiana expuestas a un gradiente de salinidad el mayor campo de crecimiento fue obtenido cuando los organismos estuvieron expuestos a 10 y 25 ups que es el intervalo de salinidad optima para esta especie de hábitos estuarinos (Guerin & Stickle 1992). En Callinectes similis, Guerin y Stickle (1997) encontraron que el mayor campo de crecimiento se obtuvo cuando las jaibas fueron aclimatadas a 30 ups de salinidad, que es la óptima reportada para esta especie.
Rosas et al. (2002) al mantener a juveniles de L. vannamei a salinidades de 15 y 40 ups y alimentados con una dieta con 0% de carbohidratos obtuvieron el mayor campo de crecimiento.
Zhu et al. (2006), al aclimatar a juveniles de L. vannamei a 15 y 40 ups y enfrentarlos a diferentes proporciones de Na/K encontraron que la mayor tasa de crecimiento de los organismos ocurrió en la salinidad de 15 ups.
Boyd (1989) considera que las salinidades de 15 a 25 ups pueden ser ideales para el cultivo de L. vannamei. Bray et al. (1994) mencionaron que la exposición del camarón blanco a las salinidades de 5 y 15 ups produjeron incremento de peso mayores que cuando los organismos fueron aclimatados a otros intervalos de salinidad (25, 35 y 49 ups). Sin embargo, Ponce Palafox et al. (1997) concluyeron que el crecimiento de L. vannamei no se redujo cuando fueron expuestos a un intervalo de salinidad de 25–45 ups. Teniendo en cuenta las inconsistencias en la información publicada en relación con el efecto de la salinidad sobre el crecimiento y supervivencia de L. vannamei, consideramos con base en los resultados obtenidos en el presente trabajo que la salinidad óptima para cultivar a esta especie deberá ser la de 26 ups, ya que corresponde al punto isosmótico. De acuerdo a Panikkar (1968) el máximo crecimiento y supervivencia de un organismo debería ocurrir al encontrarse en un medio isosmó–tico, ya que el animal no gastará energía en trabajo osmótico al no hacer uso de procesos activos para mantener el equilibrio del medio interno en relación con el externo. Tomando en cuenta lo anterior, es de suponer que en estas condiciones los organismos optimizarían sus procesos fisiológicos de tal forma que el gasto energético se reduciría, lo que representaría un ahorro energético que podría destinarse al campo de crecimiento.
La relación de la tasa de consumo de oxígeno y excreción de amonio, expresadas en equivalentes atómicos, permite conocer los cambios en la utilización del sustrato metabólico cuando los organismos están expuestos a varios regímenes ambientales (Corner & Cowey 1968; Mayzaud & Conover 1988). Para los juveniles de L. vannamei se observó una modificación en la razón atómica O:N lo que indicó un cambio en la utilización del sustrato energético en respuesta a la variación de la salinidad del medio. La razón O:N estimada para los organismos aclimatados a la salinidad de 26 ups fue 3.3 y 1.7 veces mayor, respectivamente, que la determinada cuando los organismos estuvieron en las salinidades de 20 y 32 ups. Esto indica que los camarones mantenidos en la salinidad del punto isosmótico utilizaron como sustrato energético a los carbohidratos, cuando se encontraron en condiciones hiposmóticas el principal sustrato energético utilizado fue una mezcla proteínas–lípidos y en la salinidad de 32 ups, en la que fueron hiperosmóticos, utilizaron una mezcla de lípidos–carbohidratos como sustrato energético.
Estos resultados son similares a los reportados por Rosas et al. (2002) para juveniles de esta especie cultivados en 15 y 40 ups, ya que los valores más altos para la razón O:N se obtuvieron en los organismos mantenidos en las salinidades bajas, siendo de 2 a 3 veces mayores que los determinados para los organismos expuestos a 40 ups. Lemos et al. (2001) reportaron que para postlarvas de Farfantepenaeus paulensis mantenidos en salinidades de 25 a 34 ups la razón O:N fue significativamente más alta que la registrada cuando fueron cultivadas en 5 y 15 ups.
Los resultados de los valores de la razón O:N obtenidos en L. vannamei concuerdan con los registrados para muchas especies estuarinas y marinas en donde la razón O:N es mayor cuando los organismos se encuentran en salinidades óptimas y disminuye en las salinidades bajas, indicando esto un cambio de un metabolismo predominante de carbohidratos en las salinidades óptimas, a un metabolismo dominado por una mezcla de proteínas–lípidos en bajas salinidades.
Estudios sobre los efectos de la salinidad sobre el balance energético de crustáceos sometidos a diferentes salinidades son escasos, a pesar de que se ha llegado a demostrar que este tipo de análisis proporciona información que permite cuantificar, describir y explicar la condición o estado fisiológico de los organismos.
La exposición de los camarones a la salinidad de 26 ups redujo la inversión energética destinada a cubrir los procesos del metabolismo de rutina así como la excreción de productos nitrogenados, incrementándose el campo de crecimiento, los valores de la razón atómica O:N indicaron que los camarones utilizaron con sustrato energético carbohidratos, lo que significa que en esa salinidad estuvieron libres de estrés ambiental, por lo que desde el punto de vista fisiológico es recomendable mantener a juveniles de L. vannamei en estas condiciones.
AGRADECIMIENTOS
A José M. Domínguez y Francisco Javier Ponce del Departamento de Dibujo del CICESE.
REFERENCIAS
Beamish, F. W. H. & E. A. Trippel. 1990. Heat increment: a static or dynamic dimension in bioenergetic models? Transactions of American Fisheries Society 119: 649–661. [ Links ]
Boyd, C. E. 1989. Water quality management and aeration in shrimp farming. In: Fisheries and Allied Aquacultures Departmental Series, Vol. 2. Alabama Agricultural Experimental Station, Auburn University, Auburn, AL, USA. 83 p. [ Links ]
Bray, W. A., A. L. Lawrence & J.R. Leung–Trujillo. 1994. The effect of salinity on growth and survival of Penaeus vannamei, with observations on the interaction of IHHN virus, and salinity. Aquaculture 122: 133–146. [ Links ]
Brito, R., M. A. Chimal & C. Rosas. 2000. Effect of salinity in survival, growth and osmotic capacity of early juveniles of Farfantepenaeus brasilensis (Decapoda Peneidae). Journal of Experimental Marine Biology and Ecolology 244: 253–263. [ Links ]
Brody, S. 1954. Bioenergetics and Growth. Reinhold Publ. Corp., New York, USA. pp. 307–313. [ Links ]
Castille, F. L. & A. L. Lawrence. 1981. The effect of salinity on the osmotic and chloride concentration in the haemolymph of euryha–line shrimp of the genus Penaeus. Comparative Biochemistry and Physiology 68A: 75–85. [ Links ]
Cawthorne, D. F., T. Beard, J. Davenport, & J.F. WiCkins. 1983. Responses of juvenile Penaeus monodon (Fabricius) to natural and artificial seawaters of low salinity. Aquaculture 32: 165–174. [ Links ]
Chen, J. C & P. G. Chia. 1996. Oxygen uptake and nitrogen excretion of juvenile Scylla serrata at different temperature and salinity levels. Journal of Crustacean Biology 16: 437–442. [ Links ]
Chen, J. C. & J. N. Lin. 1998. Osmotic concentration and tissue water of Penaeus chinensis juveniles reared at different salinity and temperature levels. Aquaculture 164: 173–181. [ Links ]
Chen, J. C & F. H. Nan. 1993. Changes in oxygen consumption and ammonia–N excretion by Penaeus chinensis Osbeck at different temperature and salinity levels. Journal of Crustacean Biology 13: 706–713. [ Links ]
Chen, J. C., M. N. Lin, Y. Y. Ting, & J.N. Lin. 1995. Survival, haemolymph osmolality and tissue water of Penaeus chinensis juveniles acclimated to different salinity and temperatures levels. Comparative Biochemistry and Physiology 3: 253–258. [ Links ]
Cheng, K., C. Hu., Y. Liu., S. Zheng, & X. Qi. 2006. Effect of dietary calcium, phosphorus and calcium/phosphorus ratio on the growth and tissue mineralization of Litopenaeus vannamei reared in low–salinity water. Aquaculture 251: 472–483. [ Links ]
Chim, L., R. Bouveret., P. Lemaire, & J. L. Martin. 2003. Tolerance of the shrimp Litopenaeus stylirostris Stimpson 1894 to environmental stress. Interindividual variability and selection potential for stress–resistant individuals. Aquaculture Research 34: 629–632. [ Links ]
Clark, J. V. 1992. Physiological responses of adult Penaeus semisulcatus (De Haan) to change in salinity. Comparative Biochemistry and Physiology 101A: 117–119. [ Links ]
Clifford, H. C. & R. W. Brick. 1979. A physiological approach to the study of growth and bioenergetics in the freshwater shrimp Macrobrachium rosenbergii. Proceedings of World Mariculture Society 10: 710–719. [ Links ]
Corner, E. D.S & C. B. Cowey . 1968. Biochemical studies on the production of marine zooplankton. Biological Reviews 43: 393–426. [ Links ]
Díaz, F., C. Farfán., E. Sierra, & A. D. Re. 2001. Effects of temperature and salinity fluctuation on the ammonium excretion and osmoregu–lation of juveniles of Penaeus vannamei, Boone. Marine Freshwater Behavior and Physiology 34: 93–104. [ Links ]
Díaz, F., A. D. Re., E. Sierra, & E. Díaz–Iglesias. 2004. Effects of temperature and salinity fluctuation on the oxygen consumption, ammonium excretion and osmoregulation of the blue shrimp Litopenaeus stylirostris (Stimpson). Journal of Shellfish Research 23: 903–910. [ Links ]
Díaz, F., A. D. Re., R. A. González., L. N. Sánchez., G. Leyva, & F. Valenzuela. 2007. Temperature preference and oxygen consumption of the largemouth bass Micropterus salmoides (Lacepede) acclimated to different temperatures. Aquaculture Research 38: 1387–1394 [ Links ]
Du Preez, H. H., H. Y. Chen, & C. S. Hsieh. 1992. Apparent specific dynamic action of food in the grass shrimp, Penaeus monodon (Fabricius). Comparative Biochemistry and Physiology 103A: 173–178. [ Links ]
Elliot, J. M. & W. Davison. 1975. Energy equivalents of oxygen consumption in animal energetics. Oecología 19: 195–201. [ Links ]
Gnaiger, E. 1983. Calculations of energetic and biochemical equivalents for respiratory oxygen consumption. In: Gnaiger, E & H. Forstner (Eds.). Polarographic oxygen sensor. Springer, Berlin. pp.337–345. [ Links ]
Gong, H., D. H. Jiang., D.V. Lightner, C. Collins, & D. Brock. 2004. A dietary modification approach to improve the osmoregulatory capacity of Litopenaeus vannamei cultured in the Arizona desert. Aquaculture Nutrition 10: 227–236. [ Links ]
Guerin, J. L. & W. B. Stickle. 1992. Effects of salinity gradients on the tolerance and bioenergetics of juvenile blue crabs (Callinectes sapidus) from waters of different environmental salinities. Marine Biology 114: 391–396. [ Links ]
Guerin, J. L. & W. B. Stickle. 1997. Effect of salinity on survival and bioenergetics of juvenile lesser blue crabs, Callinectes similis. Marine Biology 129: 63–69. [ Links ]
Hernández Rodríguez, .M. & F. Díaz Herrera. 1995. Interacción de la temperatura y la salinidad sobre la excreción de amonio y osmorregulación en Penaeus aztecus (Crustacea: Penaeidae). Caribbean Journal of Science 31: 284–288. [ Links ]
Howe, N. R., W. D. Quast, & L. M. Cooper. 1982. Lethal and sub lethal effects of a simulated salt brine effluent on adults and sub adults of the shrimps Penaeus setiferus and P. aztecus. Marine Biology 68: 37–47. [ Links ]
Jiang, D. H., A. L. Lawrence, W. H. Neill, & H. Gong. 2000. Effects of temperature and salinity on nitrogenous excretion by Litopenaeus vannamei juveniles. Journal of Experimental Marine Biology and Ecology 253: 193–209. [ Links ]
Jiménez–Yan, L., A. Brito, G, Cuzon, G. Gaxiola, T. García, G. Taboada, L. A. Soto, & R. Brito. 2006. Energy balance of Litopenaeus vannamei postlarvae fed on animal or vegetable protein based compound feeds. Aquaculture 260: 337–345. [ Links ]
Klein Breteler, W. C. M. 1975. Food consumption, growth and energy metabolism of juvenile shore crabs, Carcinus maenas. Netherlands Journal of the Sea Research 9: 255–272. [ Links ]
Klekowski, R. Z. & A. Duncan. 1975. Physiological approach to ecological energetics. In: W. Grodzinski, R.Z. Klekowski y A. Duncan (Eds.). Methods for Ecological Energetics. Blackwell Scientific Publications. Oxford. pp. 15–64. [ Links ]
Lemos, D., V. N. Phan, & G. Álvarez. 2001. Growth, oxygen consumption, ammonia–N excretion, biochemical composition and energy content of Farfantepenaeus paulensis Pérez–Farfante (Crustacea, Decapoda, Penaeidae) early postlarvae in different salinities. Journal Experimental Marine Biology Ecology 261: 55–74. [ Links ]
Lignot, J. H., J. C. Cochard, C. Soyez, P. Lemaire, & G. Charmantier. 1999. Osmoregulatory capacity according to nutritional status, molt stage and body weight in Penaeus stylirostris. Aquaculture 170: 79–92. [ Links ]
Logan, D. T & C. E. Epifanio. 1978. A laboratory energy balance for the larvae and juveniles of the American lobster Homarus americanus. Marine Biology 47: 381–389. [ Links ]
Mayzaud, P. & R. J. Conover. 1988. O:N atomic ratio as a tool to describe zooplankton metabolism. Marine Ecology Progress Series 45: 289–302. [ Links ]
McFarland, W. N. & B. D. Lee. 1963. Osmotic and ionic concentration of penaeidean shrimps of the Texas coast. Bulletin of Marine Science Gulf & Caribbean 13: 391–417. [ Links ]
Menz, A. & B. F. Blake. 1980. Experiments on the growth of Penaeus vannamei Boone. Journal of Experimental Marine Biology and Ecology 48: 99–111. [ Links ]
Mourente, G. & A. Rodríguez. 1997. Effects of salinity and dietary DHA (22:6n–3) content on lipid composition and performance of Penaeus kerathurus postlarvae. Marine Biology 128: 289–298. [ Links ]
Obaldo, L. G., S. Divakaran. & A.G. Tacon. 2002. Methods for determining the physical stability of shrimp feeds in water. Aquaculture Research: 369–377. [ Links ]
Panikkar, N. K. 1968. Osmotic behaviour of shrimps and prawns in relation to their biology and culture. FAO Fisheries Report 57: 527–538. [ Links ]
Parado Estepa, F. D., R. P. Ferraris, J. M. Ladja, & E.G. de Jesús. 1987. Responses of intermolt Penaeus indicus to large fluctuations in environmental salinity. Aquaculture 64: 175–184. [ Links ]
Pascual, C., E. Zenteno, G. Cuzon, A. Sánchez, G. Gaxiola, G. Taboada, J. Suárez, T. Maldonado, & C. Rosas. 2004. Litopenaeus vannamei juveniles energetic balance and immunological response to dietary protein. Aquaculture 236: 431–450. [ Links ]
Péqueux, A. 1995. Osmotic regulation in crustaceans. Journal of Crustacean Biology 15: 1–60. [ Links ]
Phillipson, J. 1964. A miniature bomb calorimeter for small biological samples. Oikos 15: 130–139. [ Links ]
Ponce Palafox, J., C. A. Martínez Palacios, & L. G. Ross. 1997. The effects of salinity and temperature on the growth and survival rates of juvenile white shrimp Penaeus vannamei Boone 1931. Aquaculture 157: 107–115. [ Links ]
Prus, T. 1975. Calorimetry and body composition. 5A Measurement of calorific value using Phillipson microbomb calorimeter. In: W. Grodzinski, R.Z. Klekowski y A. Duncan (Eds.). Methods for ecological energetics. Blackwell Scientific Publications. Oxford. pp. 149–160. [ Links ]
Re, A. D., F. Díaz, E. Sierra, & S. Gómez–Jiménez. 2004. Oxygen consumption, ammonium excretion and osmoregulatory capacity of Litopenaeus stylirostris (Stimpson) exposed to different combinations of temperature and salinity. Ciencias Marinas 30: 443–453. [ Links ]
Re, A. D., F. Díaz, E. Sierra, J. Rodríguez, & E. Pérez, 2005. Effect of salinity and temperature on thermal tolerance of brown shrimp Farfantepenaeus aztecus (Ives) (Crustacea,Penaeidae). Journal of Thermal Biology. 30: 618–622. [ Links ]
Re, A. D., F. Díaz, & G. Valdez. 2006. Effect of salinity on the thermo–regulatory behavior of juvenile blue shrimp Litopenaeus stylirostris Stimpson. Journal of Thermal Biology 31: 506–513. [ Links ]
Rodier, J. 1981. Análisis de las aguas: aguas naturales, aguas residuales y agua de mar. Omega, Barcelona. 138–140 p. [ Links ]
Rosas, C., G. Cuzon, G. Gaxiola, L. Arena, P. Lemaire, C. Soyez, & A. Van Wormhoudt. 2000. Influence of dietary carbohydrate on the metabolism of juvenile Litopenaeus stylirostris. Journal of Experimental Marine Biology and Ecology 249: 181–198. [ Links ]
Rosas, C., G. Cuzon, G. Gaxiola, Y. L. Priol, C. Pascual, J. Rossignyol, F. Contreras, A. Sánchez & A. V. Wormhoudt. 2001. Metabolism and growth of juveniles of Litopenaeus vannamei: effect of salinity and dietary carbohydrate levels. Journal of Experimental Marine Biology and Ecology 259: 1–22. [ Links ]
Rosas, C., G. Cuzon, G. Gaxiola, C. Pascual, G. Taboada, L. Arena, & A. V. Wormhoudt. 2002. An energetic and conceptual model of the physiological role of dietary carbohydrates and salinity on Litopenaeus vannamei juveniles. Journal of Experimental Marine Biology and Ecology 268: 47–67. [ Links ]
Rosas, C., A. Sánchez., M. E. Chimal & R. Brito. 2003. Manual de Métodos para la Evaluación del Balance Energético en Crustáceos. [ Links ]
Rosenberry, R. 1994. WorldShrimpFarming. Aquaculture Digest, San Diego, USA. 52 p. [ Links ]
Sokal, R. R. & F. J. Rohlf. 1979. Biometria. Principios y Métodos Estadísticos en la Investigación Biológica. Blume, España. 832 p. [ Links ]
Staples, D. J. & D. S. Heales. 1991. Temperature and salinity optimum for growth and survival of juvenile banana prawns Penaeus merguiensis. Journal of Experimental Marine Biology and Ecology 154: 251–274. [ Links ]
Stern, S., A. Borut, & D. Cohen. 1984. The effect of salinity and ion composition on oxygen consumption and nitrogen excretion of Macrobrachium rosenbergii (De Man). Comparative Biochemistry and Physiology 79A: 271–274. [ Links ]
Treece, G. D. 2000. Shrimp culture. In: Stickney, R. R. (Ed). Encyclopedia of aquaculture. John Wiley & Sons, Inc. New York, USA, pp.798–868. [ Links ]
Valdez, S. G. 2002. Determinación de la preferencia térmica y fisiología energética de juveniles de Litopenaeus vannamei aclimatados a diferentes salinidades. Tesis de Maestría en Ciencias con Orientación en Acuicultura. CICESE. 68 p. [ Links ]
Venkataramaiah, A., G. J. Lakshmi, & J. Gunter. 1974. Studies on the effects of salinity and temperature on the commercial shrimp, Penaeus aztecus, Ives, with special regard to survival limits, growth, oxygen consumption and ionic regulation. Contract report H–74–2. Gulf Coast Research Laboratory, Ocean Springs, MS, USA. 134 pp. [ Links ]
Vernberg, F. J. 1987. Crustacea. In : T.J. Pandian & F.J. Vernberg (Eds.). Animal energetics, protozoa through insect. Academic Press Inc. New York. pp. 301–372. [ Links ]
Wang, X., S. Ma., S. Dong & M. Cao. 2004. Effect of salinity and dietary carbohydrate levels on growth and energy budget of juvenile Litopenaeus vannamei. Journal of Shellfish Research 23: 231–236. [ Links ]
Williams, A. B. 1960. The influence of temperature on osmotic regulation in two species of estuarine shrimp (Penaeus). Biological Bulletin 119: 560–571. [ Links ]
Wyban, J., W. A. Walsh, & D. M. Godin. 1995. Temperature effects on growth, feeding rate and feed conversion of the pacific white shrimp (Penaeus vannamei). Aquaculture 138: 267–279. [ Links ]
Zar, J. H. 1999. Biostatiscal Analysis. Prentice Hall. USA. 25–150 p. [ Links ]
Zhang, P. , X. Zhang., J. Li. & G. Huang. 2006. The effect of body weight, temperature, salinity, pH, light intensity and feeding condition on lethal DO levels of whiteleg shrimp, Litopenaeus vannamei (Boone, 1931). Aquaculture 256: 579–587. [ Links ]
Zhu, C., S. Dong., F. Wang, & G. Huang. 2004. Effects of Na/K ratio in seawater on growth and energy budget of juvenile Litopenaeus vannamei. Aquaculture 234: 485–496. [ Links ]
Zhu, C. B., S. L. Dong, & F. Wang. 2006. The interaction of salinity and Na/K ratio in seawater on growth, nutrient retention and food conversion of juvenile Litopenaeus vannamei. Journal of Shellfish Research 25: 107–112. [ Links ]














