INTRODUCCIÓN
El tratamiento del agua residual con sistemas biológicos anaerobios se ha incrementado durante los últimos 30 años en comparación con los tratamientos aerobios, debido principalmente a su bajo requerimiento energético, la escasa formación de lodo residual y la producción de metano que representa una potencial fuente de energía (Parawira et al. 2006).
En las últimas tres décadas se han desarrollado reactores anaerobios de alta tasa, tales como el proceso anaerobio de contacto (ACP, por sus siglas en inglés), filtros anaerobios (AF, por sus siglas en inglés), el reactor anaerobio de flujo ascendente y manto de lodo (UASB, por sus siglas en inglés), el reactor de lecho fluidizado (FB, por sus siglas en inglés), el reactor de cama de lodo granular expandida (EGSB, por sus siglas en inglés) y el reactor anaerobio con deflectores (ABR, por sus siglas en inglés).
El reactor UASB de alta tasa es el más utilizado en el tratamiento del agua residual. Al comienzo de 2007, cerca 1750 reactores UASB a gran escala se pusieron en marcha alrededor del mundo para tratar agua residual agroindustrial, química y municipal (Henze et al. 2008).
El éxito del reactor UASB se puede atribuir a su capacidad para retener altas concentraciones de lodo en condiciones anaerobias; lo anterior permite tratar altas cargas orgánicas volumétricas aplicadas (COVapl), mientras mantiene un tiempo de retención celular (TRC) largo y un tiempo de retención hidráulico (TRH) relativamente corto (Henze et al. 2008).
La temperatura de operación de reactores biológicos influye directamente en dos aspectos de las reacciones biológicas de las bacterias presentes: la velocidad de las reacciones catalizadas enzimáticamente y la velocidad de difusión del sustrato a las células. La mayoría de los coeficientes de velocidad de reacción aumentan a medida que se incrementa la temperatura, pero eventualmente disminuyen a medida que la temperatura empieza a inactivar las enzimas de las células.
La baja temperatura dificulta el transporte de sustrato dentro de las células (Grady et al. 1999) e influye en las actividades metabólicas de la población microbiana, mostrando un efecto negativo en la tasa de transferencia de gas, en las características de sedimentación de los sólidos biológicos (Tchobanoglous et al. 2014) y en las propiedades fisicoquímicas del agua residual (Lettinga et al. 2001).
La temperatura recomendable de operación en reactores anaerobios es de 25 a 35 ºC para obtener las velocidades de las reacciones biológicas óptimas y proporcionar un tratamiento más estable (Tchobanoglous et al. 2014). Por lo anterior, los trabajos de investigación con reactores UASB comúnmente se han realizado a temperaturas > 30 ºC (Atuanya y Chakrabarti 2004, Chou et al. 2004, Diamantis y Aivasidis 2007, Sponza y Uluköy 2008, Yetilmezsoy y Sakar 2008, Nacheva et al. 2009, El-Sheikh et al. 2011, Senthilkumar et al. 2011, Wang et al. 2011, Wang y Han 2012, Qiu et al. 2013, Hinken et al. 2014, Li et al. 2015a, b, Lu et al. 2015).
La operación de reactores UASB a temperatura mesofílica representa un costo energético considerable y sobre todo en regiones de clima frío, como la ciudad de Toluca, Estado de México, donde la temperatura del agua varía de 12 a 20 ºC, dependiendo de la estación del año.
La mayoría de los trabajos encontrados en la literatura realizados en reactores UASB a baja temperatura (< 20 ºC) emplearon agua residual sintética o municipal (Singh y Viraraghavan 2002, Mahmoud et al. 2004, Álvarez et al. 2006, Akila y Chandra 2007, Bandara et al. 2011, 2012, Turkdogan-Aydino et al. 2011, Farajzadehha et al. 2012, Donoso-Bravo et al. 2013, Zhang et al. 2013, Rizvi et al. 2015, Saha et al. 2015). Sin embargo, se han realizado pocos estudios sobre el tratamiento de agua residual industrial en reactores UASB a baja temperatura (Kalyuzhnyi et al. 2001, Sato et al. 2006, Tawfik et al. 2008, López y Borzacconi 2009, El-Kamah et al. 2011, Esparza-Soto et al. 2011, 2013).
El objetivo del presente trabajo fue evaluar la eficiencia de remoción (ER) de la demanda química de oxígeno soluble (DQOs), la producción del biogás (PB) y el rendimiento celular experimental (Y exp ) en un reactor UASB a escala de laboratorio durante el tratamiento de agua residual industrial con dos COVapl y temperatura psicrofílica en la ciudad de Toluca, Estado de México.
MATERIALES Y MÉTODOS
El reactor UASB se construyó a escala de laboratorio con acrílico trasparente de un espesor de 0.8 cm y un volumen de 4.5 L (10 × 10 × 45.5 cm). La parte inferior interna del reactor fue cónica para tener una distribución uniforme del influente. En la salida del reactor se instaló un sedimentador de lamelas para ayudar a la retención de sólidos suspendidos dentro del reactor. El reactor fue alimentado con una bomba peristáltica (marca Cole Palmer, modelo Masterflex, EUA) para mantener el flujo constante y continuo durante las dos etapas experimentales (Fig. 1).

Fig. 1 Diagrama del reactor anaerobio de flujo ascendente rectangular a escala de laboratorio, con volumen total de 4.5 L
El reactor UASB a escala de laboratorio de esta investigación se inoculó con lodo anaerobio procedente del sedimentador secundario de un reactor UASB piloto, que trato el mismo tipo de agua residual y operó a un rango de temperatura similar a la empleada en esta investigación (18 ± 0.6 ºC) (Esparza-Soto et al. 2013).
El agua residual con la que se alimentó el reactor a escala de laboratorio procedió de una industria chocolatera (Cuadro I). El reactor UASB a escala de laboratorio se operó con dos COVapl, que se identificaron como etapa experimental I (1.8 ± 0.8 kg DQOs/m3/d) y II (3.5 ± 0.9 kg DQOs/m3/d).
CUADRO I CARACTERIZACIÓN DEL AGUA RESIDUAL INDUSTRIAL CRUDA
| Parámetro | Valor ± DER |
| pH | 4.6 ± 0.8 |
| Temperatura (ºC) | 22.0 ± 0.1 |
| DQOT (mg/L) | 6470.0 ± 537 |
| DQOs (mg/L) | 4660.0 ± 367.7 |
| Sólidos suspendidos totales (mg/L) | 785.6 ± 62.1 |
| Sólidos suspendidos volátiles (mg/L) | 750.6 ± 53.8 |
| Ácidos grasos volátiles (mg ácido acético/L) | 313.8 ± 13.6 |
| Alcalinidad (mg CaCO3/L) | 679.8 ± 95.9 |
| N-NH3 (mg/L) | 11.0 ± 1.3 |
| Ptotal (mg/L) | 268.1 ± 59 |
DQOT: demanda química de oxígeno total, DQOs: demanda química de oxígeno soluble, N-NH3: nitrógeno amoniacal, PTotal: fósforo total, DER: desviación estándar relativa
El reactor operó con un TRH de 6 h y a un rango de temperatura de 18 a 21 ºC. Las COVapl se obtuvieron diluyendo el agua residual industrial cruda con agua potable, y tuvieron fluctuaciones debidas a variaciones en el flujo y a la degradación de la DQOs del influente con el paso del tiempo. Las etapas experimentales I y II duraron 83 y 110 días, respectivamente.
Los parámetros físicos y químicos medidos y analizados fueron pH, temperatura, alcalinidad, DQOs, ácidos grasos volátiles (AGV), sólidos suspendidos totales (SST) y volátiles (SSV). Los métodos analíticos empleados para la medición y el análisis de los parámetros físicos y químicos se muestran en el cuadro II.
CUADRO II PARÁMETROS FÍSICOS Y QUÍMICOS Y MÉTODOS ANALÍTICOS UTILIZADOS DURANTE LAS ETAPAS EXPERIMENTALES
| Parámetros | Método analítico | Material y equipo |
| pH | NMX-AA-008-SCFI-2016 (SE 2016) | Medidor multiparamétrico (marca YSI, modelo 63) |
| Temperatura | NMX-AA-007-SCFI-2013 (SECOFI 2014) | |
| Alcalinidad | NMX-AA-036-SCFI-2001 (SE 2001a) | Bureta de 50 mL |
| DQOT y DQOs | Método 8000, Método de digestión de reactor (Hach 2000). | Digestor (marca HACH, modelo DRB 200) Espectrofotómetro (marca Hach, modelo DR 5000) |
| SST y SSV | NMX-AA-034-SCFI-2001(SE 2001b) | Estufa (marca Lab-Line, modelo Imperial V) y mufla (marca Barnstead, modelo F6010) |
| AGV | Método de destilación (APHA 2012) | Parrilla eléctrica, material de destilación y titulación |
DQOT: demanda química de oxígeno total, DQOs: demanda química de oxígeno soluble, SST: sólidos suspendidos totales, SSV: sólidos suspendidos volátiles, AGV: ácidos grasos volátiles
Los parámetros de control (pH, temperatura y flujo) se midieron por triplicado seis días por semana durante toda la experimentación. Los parámetros de control se midieron para regular la operación del reactor. El pH debe mantenerse cerca de la neutralidad debido a que el nivel de pH óptimo de la digestión anaerobia es de 6.3 a 8.5 (O´Flaherty et al. 2006). La temperatura se midió para conocer en qué rango se operó el reactor y el flujo para mantener el TRH deseado en la presente investigación.
La DQOs, SST y SSV se analizaron tres veces por semana. La DQOs se analizó para determinar su eficiencia de remoción dentro del reactor. La alcalinidad y los AGV se cuantificaron una vez por semana. Los AGV, SST y SSV se determinaron solamente en el efluente para monitorear una posible acidificación del reactor y calcular el TRC, respectivamente. Los SSV dentro del reactor se determinaron al inicio y final de las etapas experimentales (excepto al inicio de la etapa experimental I) por sextuplicado.
La PB se cuantificó por el método de desplazamiento de líquido (Álvarez et al. 2006, Esparza-Soto et al. 2013) y los resultados obtenidos se corrigieron para condiciones estándar de presión y temperatura (1 atm, 273 K [0 ºC]) (ecuación 1).
donde PB STD es la producción de biogás en condiciones estándar (L/d), PB la producción de biogás medido (L/d), P op la presión atmosférica de operación (0.74 atm), P la presión estándar (1 atm), T la temperatura estándar (273 K) y T op la temperatura de operación (K).
La producción de biogás teórica (PBT) se determinó para obtener una aproximación de la cantidad de biogás esperada (ecuación 2). A partir de la ecuación de la ley de los gases ideales se calculó la PBT (Esparza et al. 2013, Tchobanoglous et al. 2014).
donde n es el número de moles del gas (1 mol CH4), R la constante universal de los gases ideales (0.082057 atm L/mol K), T op la temperatura de operación (K), P op la presión atmosférica de operación (0.74 atm), Q el flujo (L/d), So la DQO s del influente (mg/L), S la DQO s del efluente (mg/L), Y exp el rendimiento celular experimental (0.11 mg SSV/mg DQO rem , valor obtenido en esta investigación), b H el coeficiente de decaimiento endógeno (0.03 1/d, Tchobanoglous et al. 2014) y TRC el tiempo de retención celular (81 y 95 días para las etapas experimentales I y II, respectivamente).
Los SST y SSV dentro del reactor y del efluente se utilizaron para calcular el TRC al final de cada etapa experimental con la ecuación 3 (Tchobanoglous et al. 2014):
donde V r es el volumen del reactor (L), X r la biomasa del reactor (mg SSV/L), Q el flujo (L/d), y X e la biomasa del efluente (mg SSV/L).
El rendimiento celular experimental (Y exp ) se calculó para el periodo de tiempo comprendido entre dos cuantificaciones consecutivas de SSV del reactor con la ecuación 4 (Esparza-Soto et al. 2013):
donde ∆X r es la masa total del lodo acumulado en el interior del reactor durante el periodo de tiempo entre dos cuantificaciones de biomasa del reactor (kg SSV), ∆X e la masa total del lodo perdido en el efluente durante el periodo de tiempo entre dos cuantificaciones de X r (kg SSV) y ∆DQO rem la masa total del DQO s removida (kg DQO s rem ) durante el periodo de tiempo entre dos cuantificaciones de X r .
RESULTADOS Y DISCUSIÓN
Los resultados de los parámetros analizados en el reactor UASB se presentan en el cuadro III. El flujo se mantuvo entre 18.1 ± 3.4 y 18.6 ± 2.6 L/d durante las dos etapas experimentales. El control del flujo permitió mantener el TRH deseado en el presente trabajo.
CUADRO III CONDICIONES DE OPERACIÓN Y PARÁMETROS MEDIDOS Y ANALIZADOS EN EL REACTOR ANAEROBIO DE FLUJO ASCENDENTE
| Parámetro | Promedio ± DER | n | ||
| Influente | Efluente | |||
| Etapa I | ||||
| pH | 7.2 ± 0.2 | 7.6 ± 0.2 | 73 | |
| Temperatura (ºC) | 19.2 ± 1.7 | 19.0 ± 1.8 | 73 | |
| Q (L/d) | NA | 18.1 ± 3.4 | 73 | |
| TRH (h) | NA | 6.1 ± 1.1 | 73 | |
| AGV (mg ácido acético/L) | ND | 31.3 ± 4.1 | 2 | |
| Alcalinidad (mg CaCO3/L) | 1134.4 ± 158.8 | 1108.9 ± 82.4 | 5 | |
| COVapl (kg DQOs/m3/d) | 1.8 ± 0.8 | NA | 19 | |
| COVrem (kg DQOs/m3/d) | NA | 1.2 ± 0.6 | 19 | |
| DQOs (mg/L) | 426.5 ± 133.8 | 125.9 ± 80.6 | 22 | |
| ER (%) | NA | 70.4 | 22 | |
| ER (%)* | NA | 90.3 ± 1.3 | 4 | |
| Duración del periodo (d) | 83 | NA | NA | |
| PB (L/d) | NA | 1.6 ± 0.8 | 51 | |
| Etapa II | ||||
| pH | 7.2 ± 0.2 | 7.7 ± 0.2 | 92 | |
| Temperatura (ºC) | 18.2 ± 2 | 17.8 ± 2 | 92 | |
| Q (L/d) | NA | 18.6 ± 2.6 | 92 | |
| TRH (h) | NA | 5.9 ± 0.8 | 92 | |
| AGV (mg ácido acético/L) | ND | 189.1 ± 20.9 | 6 | |
| Alcalinidad (mg CaCO3/L) | 1449.8 ± 336.3 | 1603.0 ± 172 | 11 | |
| COVapl (kg DQOs/m3/d) | 3.5 ± 0.9 | NA | 26 | |
| COVrem (kg DQOs/m3/d) | NA | 2.6 ± 0.7 | 26 | |
| DQOs (mg/L) | 830.6 ± 162 | 198.6 ± 147 | 28 | |
| ER (%) | NA | 77.1 | 28 | |
| ER (%)* | NA | 90.6 ± 3.1 | 13 | |
| Duración del periodo (d) | 110 | NA | NA | |
| PB (L/d) | NA | 3.5 ± 1.3 | 68 | |
Q: caudal, TRH: tiempo de retención hidráulico, AGV: ácidos grasos volátiles, COVapl: carga orgánica volumétrica aplicada, COVrem: carga orgánica volumétrica removida, DQOs: demanda química de oxígeno soluble, ER: eficiencia de remoción, PB: producción de biogás, DER: desviación estándar relativa, n: número de muestras, NA: no aplica, ND: no determinado
*En estado estacionario; en la etapa experimental I comprende del día 71 al 83 de operación, y en la etapa experimental II del día 151 al 193 de operación
El pH del efluente estuvo cercano al neutro en las dos etapas experimentales, mientras que los AGV fueron más bajos (de 31.3 ± 4.1 a 189.1 ± 20.9 mg ácido acético/L) que la concentración máxima sugerida (250 mg ácido acético/L) (Crites y Tchnobanoglous 2000); la alcalinidad fue alta (de 1109 ± 82 a 1603 ± 172 mg CaCO3/L) respecto de la concentración mínima recomendada (1000 mg CaCO3/L) (Crites y Tchnobanoglous 2000).
El pH del efluente cercano a la neutralidad, los AGV bajos y la alcalinidad alta indicaron que el tratamiento anaerobio se mantuvo estable, lo cual se debió a que la alcalinidad fue suficiente para amortiguar los cambios de pH causados por la formación de AGV durante la digestión anaerobia (Isik y Sponza 2005, Henze et al. 2008). Por lo tanto, el monitoreo del pH, el control de la alcalinidad y la determinación de los AGV permitieron evitar la acidificación del reactor (Cuadro III).
Los SST y SSV en el efluente fueron bajos durante las dos etapas experimentales de las dos etapas experimentales (Cuadro IV). Los SSV en el efluente durante las etapas experimentales I y II fueron de 56.6 ± 14.9 y de 45.3 ± 11.0 mg/L, respectivamente. Los SST en el efluente durante las dos etapas experimentales fueron menores a la concentración recomendada por Foresti et al. (2006) (50 a 100 mg/L).
CUADRO IV CONCENTRACIONES DE SÓLIDOS SUSPENDIDOS TOTALES Y SÓLIDOS SUSPENDIDOS VOLÁTILES DEL EFLUENTE Y DENTRO DEL REACTOR (AL FINAL DE LA ETAPA EXPERIMENTAL) Y TIEMPO DE RETENCIÓN CELULAR
| Etapa/COVapl | Efluente | SSV/SST | Reactor | SSV/SST | TRC | ||
| (kg DQOs/m3/d) | (mg SST/L) | (mg SSV/L) | (%) | (mg SST/L) | (mg SSV/L) | (%) | (d) |
| I (1.8 ± 0.8) | 44.1 ± 21.0 | 35.6 ± 18.4 | 79.9 | 16175 | 11550 | 71.4 | 81 |
| II (3.5 ± 0.9) | 56.6 ± 14.9 | 45.3 ± 11.0 | 80.5 | 33175 | 23900 | 72.0 | 95 |
COVapl: carga orgánica volumétrica aplicada, DQOs: demanda química de oxígeno soluble, SST: sólidos suspendidos totales, SSV: sólidos suspendidos volátiles, TRC: tiempo de retención celular
La baja concentración de SST y SSV en el efluente en el presente trabajo se debió a la presencia de un sedimentador de lamelas en la salida del reactor y a la baja velocidad ascensional (0.05 m/h) dentro de éste. Por otro lado, los SST y SSV en el efluente tuvieron concentraciones similares a los reportados por Turkdogan-Aydinol et al. (2011).
La calidad del efluente respecto a la concentración de SST y SSV en el presente trabajo fue satisfactoria y comparable con la literatura (Foresti et al. 2006, Turkdogan-Aydinol et al. 2011). La relación SSV/SST en el efluente de las dos etapas experimentales fue de 79.9 y 80.5 %. Esta alta relación indicó que la mayor parte de los SSV fugados en el efluente provenían del lodo biológico anaerobio presente dentro del reactor.
La concentración de SST y SSV dentro del reactor se incrementó al doble durante la etapa experimental II. La baja concentración de SSV en el efluente favoreció el aumento de la cama de lodo dentro del reactor, y esto a su vez permitió tener un tratamiento anaerobio estable.
La relación SSV/SST dentro del reactor en las etapas experimentales I y II fue de 71.4 y 72.0 %, respectivamente. Esta relación indicó que la cama de lodo estuvo conformada mayormente por lodo biológico anaerobio (Tchobanoglous et al. 2014) y no hubo acumulación de sólidos suspendidos inertes dentro del reactor.
El TRC se incrementó cuando la COVapl aumentó (Cuadro IV). El TRC de las dos etapas experimentales (81 y 95 días) fue más largo que el mínimo requerido para mantener la actividad metanogénica a baja temperatura (TRC 75 días) (Lettinga et al. 2001). El TRC largo fue provocado por la baja concentración de SSV en el efluente, lo cual incrementó los SSV dentro del reactor. El TRC largo permitió obtener una ER alta (90 %) durante el estado estacionario de las dos etapas experimentales.
La ER del reactor UASB se evaluó durante las dos etapas experimentales (Fig. 2). La ER durante toda la etapa experimental I fue variable, mientras que en la etapa experimental II se incrementó con el paso del tiempo de operación del reactor UASB, independientemente de la fluctuación de la DQOs del influente.

Fig. 2 Eficiencia de remoción de la demanda química de oxígeno (DQOs) del influente y efluente durante 193 días de operación en un reactor anaerobio de flujo ascendente
El estado estacionario de las etapas experimentales I y II se alcanzó a partir de los días 71 y 151 de operación, respectivamente. El reactor UASB tardó en alcanzar el estado estacionario en ambas etapas experimentales debido a la baja concentración inicial de SSV en su interior. En estado estacionario, la ER de las etapas experimentales I y II fue de 90.3 ± 1.3 y 90.6 ± 3.1 %, respectivamente.
La ER fue mayor que el valor teórico de van Haandel et al. (2006) (80 %) y que lo reportado en la literatura por Sato et al. (2006) y Tawfik et al. (2008), quienes operaron sus reactores en condiciones similares de COVapl y temperatura. La ER del presente trabajo posiblemente fue mayor porque se trató un solo tipo de agua residual industrial, a diferencia de los autores mencionados, quienes usaron una mezcla de diferentes tipos de aguas residuales.
Trabajar con un solo tipo de agua residual industrial evitó posibles variaciones en la calidad del agua, la cual puede influir en el tratamiento anaerobio. Además, el lodo anaerobio del presente trabajo estaba adaptado previamente al mismo tipo de agua residual industrial y a la baja temperatura de operación. Con lo antes descrito se favoreció la ER del presente trabajo.
La correlación lineal entre la COVapl y la carga orgánica volumétrica removida (COVrem) de las etapas experimentales I y II se muestran en la figura 3. El alto coeficiente de determinación (R2 = 0.7605) indica que los datos experimentales de COVapl y COVrem estuvieron relacionados entre sí.

Fig. 3 Correlación lineal entre la carga orgánica volumétrica aplicada (COVapl) y la carga orgánica volumétrica removida (COVrem) del reactor anaerobio de flujo ascendente durante las etapas experimentales I y II
La COVrem aumentó cuando la COVapl se incrementó. La pendiente de la correlación lineal indicó el porcentaje de ER global de las dos etapas experimentales. La ER global mostrada en la figura 3 (74 %) fue igual a la calculada con la DQOs del influente y efluente y cercana al valor teórico de van Haandel et al. (2006) (80 %).
La ER global obtenida indicó que el tratamiento anaerobio para este tipo de agua residual industrial fue eficiente y comparable con ER teóricas para reactores operados a temperaturas mayores de 20 ºC (van Haandel et al. 2006).
La PB y la COVrem durante ambas etapas experimentales se muestran en la figura 4. En general se observa que la PB se incrementó conforme la COVrem aumentó. Los días 48 y 68 de operación se presentaron dos disminuciones de la PB debido a problemas operativos. La PBSTD promedio de las etapas experimentales I y II fue de 1.6 L/d (0.3 Lbiogás/L/d) y 3.5 L/d (0.8 Lbiogás/L/d), respectivamente.

Fig. 4 Producción de biogás y carga orgánica volumétrica removida (COVrem) en las etapas experimentales I y II
En el presente trabajo se obtuvo mayor PBSTD que Sponza y Uluköy (2008), quienes trabajaron con la misma COVapl de la etapa experimental II (0.3 Lbiogás/L/d a 3.5 ± 0.9 kg DQOs/m3/d) y una temperatura de operación mayor (37 ºC). La ER y el origen alimenticio del agua residual pudieron favorecer a la PBSTD del presente trabajo a diferencia de lo reportado por Sponza y Uluköy (2008), quienes utilizaron agua residual sintética con un contaminante.
La correlación lineal entre la PB y la COVrem muestra que la PB se incrementó cuando la COVrem aumentó (Fig. 5). La pendiente de esta correlación indicó que se produjeron 1.79 L de biogás por cada kg DQOs removida (DQOs rem/m3 d) (R2 = 0.6566). A partir de la pendiente de la correlación lineal entre la COVrem y la PB se calculó el rendimiento de metano.

Fig. 5 Correlación entre la carga orgánica volumétrica (COVrem) y la producción de biogás durante la operación del reactor anaerobio de flujo ascendente
La pendiente de la correlación lineal se dividió entre el volumen del reactor y se consideró que el 84 % del biogás fue metano (valor determinado por Ávila-Arias [2015] para el mismo lodo anaerobio, el mismo tipo de agua residual y temperatura de operación). El rendimiento del metano fue de 231.6 L CH4/kg DQOs rem (1 atm y 0 ºC), siendo este valor menor al teórico (350 L CH4/kg DQOs rem) (Henze et al. 2008) y mayor a los reportados en la literatura de 167 L CH4/kg DQOs rem (Singh y Viraraghavan 2004) y 174 L CH4/kg DQOs rem (Esparza-Soto et al. 2013).
La diferencia entre los valores de rendimiento del metano del presente trabajo y la literatura puede atribuirse a la composición del metano en el biogás, que puede variar dependiendo del tipo y concentración de materia orgánica presente en el agua residual (Noyola et al. 2006).
La correlación lineal entre la PB y la PBT se observa en la figura 6. La pendiente de la correlación lineal indicó el porcentaje de biogás teórico recuperado en el reactor UASB. En la presente investigación se recuperó el 68 % de la PBT (R2 = 0.7075). Este bajo porcentaje de recuperación puede atribuirse principalmente a pérdidas de metano disuelto en el efluente ocasionadas por la baja temperatura de operación, ya que la solubilidad de un gas en un fluido aumenta cuando la temperatura disminuye (Brown et al. 2009). Sin embargo, el porcentaje de biogás recuperado fue cercano al 65 % reportado por Ávila-Arias (2015), al 74 % reportado por Lara-Domínguez (2013) con las mismas condiciones de operación que las del presente trabajo y al 71 % informado por Bandara et al. (2011) con agua residual sintética a 15 ºC.
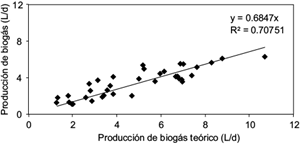
Fig. 6 Correlación lineal entre la producción de biogás teórico y la producción de biogás durante las etapas experimentales I y II
El Y exp calculado para la etapa de experimentación II fue de 0.11 kg SSV/kg DQOs rem a 17.8 ºC. El Y exp fue más alto que el valor clásico reportado por Tchobanoglous et al. (2014) (0.08 kg SSV/kg DQO). El Y exp alto del presente estudio pudo deberse a que la tasa de crecimiento de los microorganismos anaerobios se incrementó en condiciones psicrofílicas, tal como fue reportado por van Lier et al. (1997).
El incremento de los SSV dentro del reactor durante la etapa experimental II (11 550 a 23 900 mg SSV/L) y la baja concentración de SSV en el efluente (45.3 ± 11.0 mg SSV/L) indicaron una alta tasa de formación de microorganismos anaerobios, la cual es controlada por el Y exp . La literatura reporta valores elevados similares de Y exp de 0.18 kg SSV/kg DQO a 20 ºC (Singh y Viraraghavan 2002) y de 0.2 ± 0.04 kg SSV/kg DQO a 18 ºC (Esparza-Soto et al. 2013).
CONCLUSIONES
El pH del efluente cercano al neutro, los AGV bajos y la alcalinidad alta permitieron obtener un tratamiento anaerobio estable porque los microorganismos estuvieron en equilibrio entre sí, evitando la acidificación del reactor.
La baja concentración de SST y SSV del efluente favoreció la acumulación de SSV en la cama de lodo anaerobio. Lo anterior benefició la estabilidad de la ER durante la operación del reactor UASB.
El reactor UASB trató eficientemente el agua residual industrial con COVapl intermedia (1.8 ± 0.8 a 3.5 ± 0.9 kg DQOs/m3/d) y un TRH corto (6 h) a temperatura psicrofílica de operación (18-19 ºC).
El TRC largo y el lodo anaerobio adaptado previamente a la temperatura y al tipo de agua residual industrial, permitieron alcanzar ER altas en el estado estacionario (90.3 ± 1.3 % y 90.6 ± 3.1 % durante las etapas experimentales I y II, respectivamente).
La PB se incrementó cuando la COVrem aumentó. La PBSTD de las etapas experimentales I y II fue 0.3 y 0.8 Lbiogás/L/d, respectivamente.
El bajo porcentaje de biogás recuperado (68 %) en el presente trabajo se debió a que la solubilidad del metano en el efluente aumentó a temperatura baja.
El Y exp fue alto comparado con el valor de Tchobanoglous et al. (2014), lo cual puede atribuirse a la influencia de la baja temperatura de operación sobre la tasa de crecimiento de los microorganismos anaerobios.











 nova página do texto(beta)
nova página do texto(beta)


