INTRODUCCIÓN
El aumento anual del parque automotor a escala mundial tiene un impacto importante en el consumo total de energía primaria y la contaminación atmosférica urbana. Lo anterior, unido a la preocupación general por el carácter no renovable de los combustibles fósiles, ha promovido el desarrollo de combustibles alternativos, en especial los de origen renovable (CEPAL 2007, Delgado et al. 2011, Gaurav et al. 2017).
Desde la perspectiva según la cual lo ideal es reducir la emisión de CO2, el uso de aceites extraídos de plantas oleaginosas como combustibles constituye una opción ecológica, dadas las ventajas inherentes a la utilización de biocombustibles, como su carácter biodegradable y atóxico, la reducción de emisiones de CO y CO2, la ausencia de azufre y su poder lubricante (Agarwal 2007, Demirbas 2007, Mata et al. 2010, Atabani et al. 2012, Sitepu et al. 2014, Habibullah et al. 2015, Morone y Cottoni 2016).
La transesterificación o alcohólisis es la vía más usada para la producción de biodiésel. Durante este proceso, los triglicéridos del aceite vegetal reaccionan con un alcohol de cadena corta, usualmente metanol, en presencia de un catalizador alcalino, para producir alquil ésteres de ácidos grasos (biodiésel) y glicerol como subproducto. El biocombustible que se obtiene con este método es de menor viscosidad con relación al aceite vegetal de partida, lo cual disminuye los problemas relacionados con la inyección de combustible en el motor y su fluidez a bajas temperaturas (Rashid y Anwar 2008, Atabani et al. 2012, Malins et al. 2014, Habibullah et al. 2015, Kuss et al. 2015, Rathore et al. 2016).
El biodiésel se puede producir a partir de cualquier aceite vegetal (virgen o usado) o de grasas animales, mediante el proceso de transesterificación. Incluso nuevas investigaciones informan sobre su generación a partir de microalgas y otras describen el uso de oleorresinas para tal fin. Se dice que debido a la naturaleza de la composición química de la oleorresina extraída del árbol de copaiba, es posible utilizarla directamente como combustible o en mezclas con gasóleo para motores de combustión interna (Calvin 1980, 1983, 1987, Veiga-Junior y Pinto 2002, Chen et al. 2009, Pieri et al. 2009).
La oleorresina de copaiba se obtiene del tronco de árboles pertenecientes a la especie Copaifera officinalis (de la familia Fabaceae, subfamilia Caesalpinioideae), la mayor parte de los cuales se hallan en zonas tropicales de América Latina, particularmente en la región amazónica. Está compuesta principalmente por sesquiterpenos, sobre todo hidrocarburos sesquiterpénicos como α-copaeno, trans β-cariofileno y α-humuleno, y diterpenos como los ácidos copaíbico, copálico y copaiférico. Sin embargo, su composición puede variar considerablemente dependiendo de la especie y de los factores medioambientales (Herrero-Jáuregui et al. 2011, Leandro et al. 2012, Gelmini et al. 2013).
En general, la cantidad de oleorresina que se puede extraer de un árbol puede estar sujeta tanto a factores bióticos como abióticos. Algunos autores afirman que aspectos como el diámetro del árbol, la edad, la estación y la infestación de termitas pueden influir en la cantidad de oleorresina que es factible recolectar en cada cosecha (Da Silva Medeiros y Vieira 2008, Herrero-Jáuregui et al. 2011).
De acuerdo con el estudio realizado por Klauberg et al. (2014), en promedio se pueden recolectar 2.1 L por árbol en cada cosecha, cantidad que disminuiría en el siguiente ciclo dependiendo de la capacidad de regeneración del árbol, relacionada con la actividad fisiológica de los especímenes -mucho mayor en árboles jóvenes- y con su diámetro. Según Da Silva Medeiros y Vieira (2008), la producción de oleorresina podría ser ecológicamente sostenible para árboles con diámetros de 30 a 41 cm respecto de árboles de diámetro superior, en relación con el volumen de oleorresina extraído en cada cosecha y en cuanto a su capacidad de regeneración.
La oleorresina de copaiba se utiliza tradicionalmente en el tratamiento de múltiples enfermedades como analgésico, antiinflamatorio, cicatrizante y protector gástrico, entre otros, y en la atención primaria de salud en poblaciones indígenas (Da Silva Medeiros y Vieira 2008, Santos et al. 2008, Rodrigues et al. 2011, Gonçalves et al. 2014, Bardají et al. 2016). Sin embargo, su uso en actividades menos convencionales, como el funcionamiento de pequeñas embarcaciones y la iluminación en comunidades indígenas, ha despertado el interés sobre sus propiedades como combustible (Silva et al. 2010).
En el presente trabajo se analizó el potencial de la oleorresina de copaiba para la producción o formulación de biocombustibles. Se utilizó oleorresina extraída de árboles de Copaifera reticulata para la producción de biodiésel y se analizaron las variaciones en las propiedades de flujo en frío, su estabilidad oxidativa y su capacidad calorífica en las etapas del proceso.
MATERIALES Y MÉTODOS
La oleorresina de copaiba (OC) se obtuvo de incisiones en árboles de Copaifera reticulata en la amazonia brasileña, a una altitud menor de 300 msnm en clima ecuatorial selvático, en junio de 2016. Se utilizó papel de filtro para eliminar sólidos en suspensión (retención de partículas: 6 μm) y sulfato de sodio anhidro de grado analítico para reducir la humedad.
Neutralización
La oleorresina secada, filtrada y precalentada se mezcló en proporción 2:1 con una disolución de NaOH al 10 % y a 30 ºC durante 10 min. Terminada la reacción, la temperatura se aumentó a 75 ºC para separar las fases. Finalmente, la oleorresina refinada se lavó con agua desionizada hasta lograr que su pH fuera neutro. La humedad en el aceite refinado se eliminó con la adición de Na2SO4 anhidro en proporción 4:1 con relación al aceite. La eficiencia del proceso de neutralización se estimó según su capacidad para reducir la acidez en la oleorresina, mediante la ecuación (1):
donde Pi es la acidez inicial y Pr es la acidez de la oleorresina posterior a la etapa de refinado.
Transesterificación
La oleorresina refinada y precalentada a la temperatura de operación (T = 60 ºC) se mezcló con una disolución de alcohol metílico e hidróxido de sodio. Se empleó una relación másica 4:1 oleorresina/metanol y 1.1 % de NaOH como catalizador. La mezcla de reacción se mantuvo a 60 ºC durante 90 min a 600 rpm. El montaje empleado para la transesterificación se presenta en la figura 1. Finalizado el tiempo de reacción, se depositó la mezcla en un embudo de decantación, separándola en dos fases, a saber: la fase superior rica en metil ésteres, y la fase inferior que contenía la glicerina, el exceso de alcohol, trazas de catalizador e impurezas.
La fase rica en metil ésteres o biodiésel se lavó con agua desionizada seis veces, con una relación 1:1/3 para neutralizar las trazas de catalizador presentes en la mezcla. Finalmente, el agua residual en el biodiésel se eliminó con la adición de Na2SO4 anhidro. El rendimiento en la producción de biodiésel se calculó con la ecuación (2):
Caracterización física y química de la oleorresina
Se determinaron el índice de acidez (NTC 218-99 [ICONTEC 1999]), índice de yodo (AOC920 159), índice de saponificación (AOAC 920 160), humedad (ASTM E203 [ ]) y el contenido de fósforo (ET ISO 10540-1-12 [ESA 2012]). El análisis del contenido de ácidos grasos en la oleorresina fue realizado por laboratorios Mol Labs mediante cromatografía de gases (CG) (método FAMES, Mol Labs Ltda.). En la caracterización se determinaron la viscosidad cinemática (ASTM D445 [ASTM 2015a]), el punto de inflamación (ASTM D92 [ASTM 2005a]), la capacidad calorífica (Cp) (ASTM E1269 [ASTM 2005b]) y el punto de fluidez (ASTM D97 [ASTM 2005c), propiedades que se compararon con los valores estándar para el biodiésel, según las normas de la Sociedad Americana para Pruebas y Materiales (ASTM, por sus siglas en inglés) y valores encontrados en la literatura.
Análisis estructural por espectroscopia FTIR
Se realizó el análisis de la composición estructural de la oleorresina por espectroscopia infrarroja con transformada de Fourier (FTIR), empleando un espectrómetro Nicolet iS10 (Thermo Fisher Scientific), equipado con un sistema de muestreo de reflectancia total atenuada horizontal (HATR). Los espectros FTIR-HATR se obtuvieron con una resolución de 4 cm-1 en el rango espectral de 4000-650 cm-1, con 32 barridos en cada caso. Se empleó el programa OMNIC 9.1.27 (Thermo Fisher Scientific Inc.) para el análisis de los espectros.
En el estudio de las propiedades térmicas de la OC se utilizó un calorímetro diferencial de barrido (DSC, por sus siglas en inglés) serie Q20 (TA Instruments). Para el análisis del comportamiento de la oleorresina a bajas temperaturas, las muestras se purgaron con flujo de N2 de 50 mL/min. Posteriormente, la muestra se mantuvo en condiciones isotérmicas (50 ºC) durante cinco minutos. Transcurrido ese tiempo, el sistema se enfrió a -60 ºC a una velocidad de 10 ºC/min. Cuando las muestras alcanzaron esta temperatura, se calentó el sistema a 50 ºC a una velocidad de 10 ºC/min. Las curvas de enfriamiento y calentamiento obtenidas se emplearon para determinar los puntos de cristalización y fusión, así como las entalpías asociadas a los cambios de fase, cristalización (ºΔH c ) y fusión (ºΔH m ), respectivamente.
Para analizar la degradación termooxidativa de la oleorresina, las muestras se depositaron en un crisol de aluminio abierto y se purgaron con un flujo 50 mL/min de aire. Posteriormente se calentaron de 10 a 250 ºC a una velocidad de calentamiento de 10 ºC/min. A partir de las curvas de calentamiento, en presencia del flujo de aire, se determinaron las temperaturas de inicio de oxidación. Los datos se analizaron utilizando el programa Universal Analysis 2000, versión 4.5 A (TA Instruments). Cada prueba se realizó tres veces.
RESULTADOS Y DISCUSIÓN
Propiedades físicas y químicas
Se determinaron las siguientes propiedades físicas y químicas de la OC: índice de acidez, índice de yodo, índice de saponificación y porcentaje de humedad (Cuadro I). De acuerdo con los parámetros para el biodiésel y según las normas de la ASTM se determinó que la viscosidad, el índice de acidez y la humedad en la oleorresina exceden los límites permitidos por la normativa. Entonces, para desarrollar la producción de biodiésel de OC es necesario reducir estos valores, con el propósito de garantizar el funcionamiento eficaz y seguro del motor. Dado el contenido de fósforo en la OC se descartó la etapa de desgomado.
CUADRO I PROPIEDADES FÍSICAS Y QUÍMICAS DE LA OLEORRESINA DE COPAIBA CRUDA
| Propiedad | Unidades | Valor |
| Densidad a 23 ºC | (g/mL) | 0.966 |
| Viscosidad a 40 ºC | (mm2/s) | 53.3 |
| Acidez | (%p/p A, oleico) | 17.99 |
| Índice de yodo | (g yodo/100 g) | 189.1 |
| Índice de saponificación | (mg KOH/g) | 48.6 |
| Contenido de fósforo | (ppm) | < 0.1 |
| Contenido de humedad | (%) | 1.7 |
En el cuadro II se muestra el perfil de ácidos grasos de la OC. Se aprecia que los ácidos en mayor proporción son el oleico (14.72 %), linoleico (7.43 %) y el palmítico (4.45 %). En general, el 30 % de la OC corresponde a ácidos grasos. El porcentaje restante corresponde a la fracción de sesquiterpenos y diterpenos presentes en la oleorresina.
CUADRO II PERFIL DE ÁCIDOS GRASOS DE LA OLEORRESINA DE Copaifera reticulata
| Ácido graso | Resultado (g/100 g) | Ácido graso | Resultado (g/100 g) | ||
| Ácido hexanoico | C6:0 | 0.53 | Ácido cis-9 oleico | C18:1 | 14.72 |
| Ácido caprílico | C8:0 | 0.03 | Ácido linolelaidico | C18:2t | 0.07 |
| Ácido caproico | C10:0 | 1.52 | Ácido linoleico | C18:2 | 7.43 |
| Ácido mirístico | C14:0 | 0.23 | Ácido araquídico | C20:0 | 0.08 |
| Ácido pentadecanoico | C15:0 | 0.11 | Ácido linolénico | C18:3 | 0.06 |
| Ácido cis-10 pentadecanoico | C15:0 | 0.64 | Ácido cis 11-14 eicosadienoico | C20:2 | 0.08 |
| Acido palmítico | C16:0 | 4.45 | Ácido erúcico | C22:1 | 0.06 |
| Ácido palmitoleico | C16:1 | 0.08 | Ácido nervónico | C24:1 | 2.24 |
| Acido esteárico | C18:0 | 0.8 | |||
En la literatura se ha reportado la presencia de ácidos resínicos para la especie Copaifera reticulata, como el kaurenoico (3.6 %) y el copálico (2.4 %), este último considerado como el diterpeno característico del género Copaifera; asimismo, de hidrocarburos sesquiterpénicos como el β-cariofileno, bergamoteno y α-copaeno en 40.9 %, 4.1 % y 3.0 %, respectivamente, como principales constituyentes de la oleorresina (Santos et al. 2008). Sin embargo, este resultado difiere de otras investigaciones, en las que se afirma que el bisaboleno y el α-bergamoteno son los principales constituyentes de la oleorresina de Copaifera reticulata (Herrero-Jáuregui et al. 2011, Leandro et al. 2012, Bardají et al. 2016). Como se mencionó, factores ambientales como luminosidad, calidad del suelo, estacionalidad, así como la infección por hongos y diversos patógenos, pueden afectar la composición química de la oleorresina y hacer aún más compleja la determinación de sesquiterpenos y ácidos resínicos constituyentes (Herrero-Jáuregui et al. 2011, Leandro et al. 2012).
Neutralización
Con el método empleado para el refinado de la OC se logró reducir en un 97 % la acidez de la oleorresina después del tratamiento con NaOH. Sin embargo, este método dio lugar a la formación de jabones, con lo cual se redujo la cantidad de aceite disponible para la transesterificación. La neutralización por vía química junto con los procesos de desecado y filtrado redujeron en 55.3 % la masa inicial de oleorresina. Se presentó una reducción del 5.7 % y 63 % en los valores de densidad y viscosidad, respectivamente. La OC refinada tiene una densidad de 0.911 g/mL y una viscosidad cinemática de 19.8 mm2/s. Estos resultados demuestran que a partir del proceso de refinado es posible reducir la viscosidad de la oleorresina, con miras a aplicarla como biocombustible.
Transesterificación
Luego de la transesterificación, la viscosidad de la muestra (8.5 mm2/s) fue superior en comparación con el diésel de petróleo y el biodiésel según las normas ASTM, característica determinada por la estructura química de los metil ésteres de ácidos grasos producidos, en particular el grado de instauración y largo de cadena carbonada.
El uso de NaOH en el refinado y como catalizador en el proceso de transesterificación, puede aumentar la viscosidad del producto. Es preciso aclarar que, pese a compensar los niveles de acidez en la oleorresina, la neutralización de los ácidos grasos libres y la hidrólisis de los triglicéridos y posterior neutralización generan jabones inactivos catalíticamente que afectan la viscosidad del aceite (Narváez-Rincón et al. 2004). Aunque se esperaba reducir en mayor proporción la viscosidad del biocombustible para garantizar el cumplimento de la norma, la formación de jabones no lo permitió.
Si bien el uso de este biocombustible favorecería la lubricidad de las piezas en el motor como resultado de una viscosidad ligeramente superior al patrón estándar, podría generar complicaciones en el funcionamiento de los inyectores de la máquina, en particular a bajas temperaturas. En tal caso, es posible que un incremento en la viscosidad afecte la fluidez del combustible, por lo que no se aconseja su uso directo como combustible (Demirbas 2008, Atabani et al. 2012). Para asegurar una inyección adecuada del combustible en el motor y mantener un funcionamiento adecuado de los inyectores, se podría considerar el uso del biocombustible obtenido en mezclas con gasóleo.
El rendimiento global para la producción de biodiésel a partir de la OC cruda, mediante el método aplicado fue del 10 % aproximadamente. Se aclara que los procesos de refinado y transesterificación del aceite generaron pérdidas en la materia prima disponible del 55.3 y 89.8 %, respectivamente (Cuadro III). La inducción de reacciones de saponificación durante la transesterificación afectó la eficiencia del NaOH como catalizador, así como el rendimiento en la producción de metil ésteres y dificultó los procesos de separación y purificación del biodiésel de copaiba (Encinar et al. 2005, Tacias-Pascacio et al. 2016).
CUADRO III CANTIDADES DE MATERIA PRIMA EN CADA UNA DE LAS ETAPAS DEL PROCESO DE PRODUCCIÓN DE BIODIÉSEL DE COPAIBA
| Etapa | Masa inicial (g) | Masa final (g) | % pérdida de masa* | % rendimiento reacción |
| Secado-filtrado | 3000 | 2880 | 4 | - |
| Neutralización | 2880 | 1341 | 55.3 | 46.6 |
| Transesterificación | 1341 | 307 | 89.8 | 22.9 |
| % de Rendimiento global* | 10.2 | |||
*Respecto de la masa inicial de oleorresina
De acuerdo con los resultados obtenidos, la ruta escogida para modificar las propiedades físicas y químicas de la OC y ajustar estos parámetros a las propiedades exigibles para biocombustibles, no es apta. Se requieren estudios posteriores para establecer procesos que permitan aprovechar el potencial de la materia prima y así obtener rendimientos superiores en cuanto a la producción de biodiésel a partir de OC.
Estudio FTIR
La caracterización estructural de los diversos grupos funcionales presentes en la OC se realizó mediante espectroscopia infrarroja. En el espectro de FTIR, mostrado en la figura 2, se aprecian 17 grandes bandas de absorción en una secuencia uniforme, de modo que los espectros para la oleorresina cruda y la oleorresina filtrada y secada sólo difieren en el nivel de absorbancia de la banda correspondiente a los enlaces -OH. El uso de Na2SO4 anhidro para desecar la muestra permitió reducir en aproximadamente 53 % el contenido de humedad en la oleorresina.
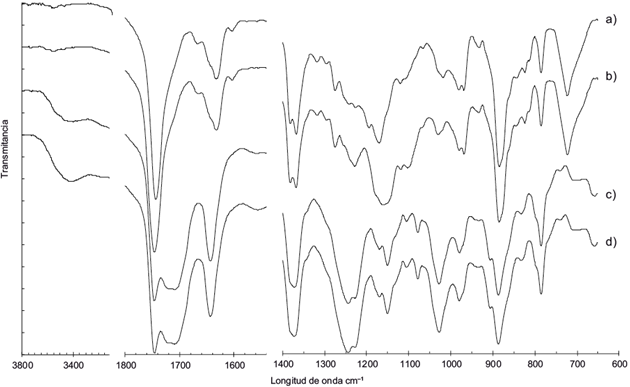
Fig. 2 Espectroscopia infrarroja por transformada de Fourier para la oleorresina de copaiba (OC) cruda y modificada, y el biodiésel de copaiba: a) biodiésel de copaiba; b) OC refinada; c) OC secada y filtrada, y d) OC cruda
En principio, en el espectro infrarrojo se observa para la OC cruda una señal correspondiente a la tensión -0H en 3399 cm-1. La banda centrada en 3077 cm-1 se asocia con la vibración del estiramiento =C-H de dobles enlaces olefínicos. Los picos en 2926 y 2869 cm-1 se relacionan con vibraciones asimétricas y simétricas de extensión -C-H del grupo metileno, respectivamente. La banda centrada en 1746 cm1 refleja la absorbancia del grupo carbonilo -C=0, característica del grupo éster en los triglicéridos (Oriani et al. 2016).
La señal originada en 1709 cm1 se atribuye al estiramiento de C=O en los ácidos carboxílicos (Marquele-Oliveira et al. 2016). El pico en 1643 cm-1 se asocia con la vibración de la deformación C=C de los dobles enlaces olefínicos. La tensión en 1557 cm-1 es atribuible a la vibración del anillo aromático (Bruni y Guglielmi 2014). Las bandas originadas en 1443 y 1372 cm-1 se asignan a la vibración de la flexión -C-H de los grupos CH2 y CH3 de los hidrocarburos alifáticos. Las bandas 1244, 1170, 1150 y 1105 cm-1 se asocian con las vibraciones del estiramiento del grupo -C-O en ácidos carboxílicos y C-O en ésteres, respectivamente. El pico en 1026 cm-1 se puede atribuir a la vibración de los enlaces -C-H en compuestos aromáticos. Finalmente, las bandas entre 980 y 785 cm-1 se explican por la vibración de la flexión fuera del plano de las olefinas.
Los espectros infrarrojos, tanto para la oleorresina modificada como para el biodiésel obtenido, difieren de la OC cruda únicamente en la intensidad de las bandas de absorción (Fig. 2). Se observa la definición de las bandas correspondientes a la vibración de compuestos del grupo carbonilo, específicamente los ésteres, así como la disminución de las bandas de absorción de los ácidos carboxílicos en cuanto resultado de la transesterificación. Adicionalmente, se evidencia la disminución en la absorbancia de compuestos aromáticos, eliminados casi en su totalidad durante las etapas de refinado y transesterificación.
Comportamiento a bajas temperaturas
Las curvas de enfriamiento-calentamiento para la OC cruda evidencian un comportamiento estable de la muestra entre -60 y 50 ºC, en la que no se aprecian procesos de cristalización o fusión (Fig. 3). Respecto de la oleorresina refinada, se aprecia cómo la modificación química dio lugar a cambios de fase, al promover reacciones exotérmicas y endotérmicas ante variaciones en el flujo de calor. Se puede observar cómo en la etapa de enfriamiento a -44.53 ºC se origina el primer cambio de fase o cristalización. Posteriormente, al aumentar su temperatura se presentan dos reacciones endotérmicas a -45.76 y -26.52 ºC, en las que se funde la muestra.
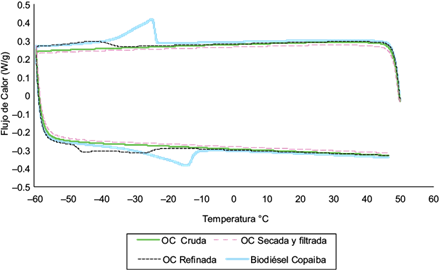
Fig. 3 Curvas de enfriamiento-calentamiento de la oleorresina de copaiba (OC) cruda, secada y filtrada, refinada, y el biodiésel de copaiba
En cuanto al biodiésel de copaiba, en la figura 3 y el cuadro IV se aprecia cómo los cambios de fase se relacionan con mayor cantidad de energía, tanto para la formación de cristales (ºΔHc) como para la fusión de la muestra (ºΔH m ), con relación a la oleorresina refinada. Se observa una exoterma en la etapa de enfriamiento que coincide con el inicio de la formación de cristales (T n ) a -23.23 ºC con cristalización a -24.68 ºC. Posteriormente, se aprecia una endoterma durante la etapa de calentamiento a -14.42 ºC que se relaciona con la fusión de la muestra. Los cambios entre los procesos de cristalización y fusión son un fenómeno conocido en ácidos grasos insaturados y ésteres alquílicos (Issariyakul et al. 2008, Yilmaz et al. 2015).
CUADRO IV ENTALPÍAS DE CRISTALIZACIÓN Y FUSIÓN EN LA OLEORRESINA REFINADA Y EL BIODIÉSEL DE COPAIBA
| Pico núm. | Oleorresina de copaiba refinada | Biodiésel de copaiba | |||||||||
| T (º C) | ºΔHc (J/g) | % CV | ºΔHm(J/g) | % CV | T(º C) | ºΔHcc (J/g) | % CV | ºΔHm (J/g) | % CV | ||
| 1 | -44.53 | 1.92 | 0.69 | - | - | - | 6.25 | 0.29 | - | - | |
| 2 | -45.76 | - | - | 0.59 | 0.21 | -24.68 | - | - | 5.44 | 1.19 | |
| 3 | -26.52 | - | - | 0.72 | 0.43 | -14.42 | - | - | - | - | |
ºΔH c : energía asociada a la formación de cristales en la muestra, ºΔH m : energía asociada a la fusión de la muestra, CV: coeficiente de variación
En el cuadro IV se presentan los calores latentes asociados a puntos de cristalización y fusión para la oleorresina refinada y el biodiésel de copaiba, con sus respectivos coeficientes de variación (CV).
Estabilidad oxidativa
La estabilidad oxidativa de la OC cruda y refinada, y el biodiésel obtenido a partir de su transesterificación fue estimada por DSC. Los termogramas correspondientes se presentan en la figura 4, en la que se aprecia que los tratamientos previos a los que fue sometida la oleorresina para reducir los niveles de acidez y viscosidad del aceite dan lugar a variaciones importantes en su comportamiento a temperaturas altas. La OC cruda presenta un par de picos endotérmicos en 161 y 173 ºC que pueden atribuirse a la volatilización de compuestos de bajo peso molecular y posterior oxidación de la muestra.
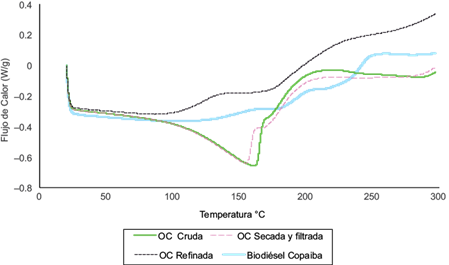
Fig. 4 Curvas de estabilidad oxidativa de la oleorresina de copaiba (OC) cruda, secada y filtrada, y refinada, así como del biodiésel de copaiba
Claramente se aprecia que los compuestos volátiles presentes en la oleorresina cruda son eliminados casi en su totalidad después de los procesos de refinado y transesterificación, resultado acorde con los perfiles de espectroscopia infrarroja en cada caso (Fig. 2). Tanto la OC refinada como el biodiésel de copaiba presentan puntos de inflexión similares, por encima y por debajo de la temperatura de inicio de oxidación de la oleorresina en su estado virgen, que pueden atribuirse a la oxidación parcial de los compuestos de cada una de las muestras (Fig. 4 y Cuadro V).
CUADRO V TEMPERATURAS DE OXIDACIÓN PARA LA OLEORRESINA DE COPAIBA (OC) CRUDA, SECADA Y FILTRADA, Y REFINADA, ASÍ COMO DEL BIODIÉSEL DE COPAIBA
| Pico núm. | OC cruda | OC secada y filtrada | OC refinada | Biodiésel de copaiba |
| Temperatura (ºC) | ||||
| 1 | 161.39 | 155.36 | 169.93 | 128.05 |
| 2 | 173.69 | 169.93 | 174.56 | 180.92 |
| 3 | - | - | - | 220.56 |
Los mecanismos de degradación de la oleorresina pueden incluir procesos de oxidación, polimerización e isomerización y reacciones de escisión en ácidos grasos, así como procesos de volatilización de sesquiterpenos, que afectan tanto su composición química, cualitativa y cuantitativa, como su respuesta ante cambios de temperatura en presencia de O2.
Como se aprecia en el cuadro V, al considerar la descomposición total de la muestra, se puede observar que la estabilidad oxidativa del biodiésel de copaiba es mayor y se incrementa en 46 y 47 ºC aproximadamente, en relación con la oleorresina cruda y la refinada, respectivamente (Scalarone et al. 2002, Cartoni et al. 2004, Fox y Stachowiak 2007). De acuerdo con los resultados obtenidos, los procesos de refinado y transesterificación favorecen la estabilidad del biocombustible ante procesos de degradación en ambiente oxidante.
Capacidad calorífica
La capacidad calorífica (Cp) de las muestras se determinó por el método calorimétrico según la norma ASTM E1269 [ASTM 2005b]. En la figura 5 se observa la variación en el valor del Cp de las muestras en el intervalo de las temperaturas de estudio (46.85-66.85 ºC). Pese a que la tendencia es la misma y los cambios en el Cp son directamente proporcionales a los cambios en la temperatura, la oleorresina en su estado crudo presenta una capacidad calorífica superior con relación a su versión modificada y al biodiésel de copaiba. Se resalta que el refinado del aceite disminuye notablemente el Cp de la muestra, que luego de la reacción de alcoholis se incrementa nuevamente, pero presenta valores inferiores respecto de la OC cruda. Los valores de capacidad calorífica encontrados guardan relación con los valores de Cp para mezclas de metil ésteres de ácidos grasos (Pauly et al. 2014).

Fig. 5 Capacidades caloríficas de la oleorresina de copaiba (OC) cruda, secada y filtrada, y refinada, así como del biodiésel de copaiba
En el cuadro VI se presentan las características físicas y químicas de la OC cruda y refinada, y el biodiésel de copaiba. En todos los casos, el punto de inflamación determinado a partir del método de copa cerrada Pensky Martens es ligeramente inferior al límite que establece la norma para el biodiésel. Esto se puede atribuir a la presencia de compuestos volátiles en la oleorresina, que afectan esta propiedad. Sin embargo, los resultados experimentales para cada muestra son superiores a los valores permitidos para el punto de inflamación del combustible diésel, según la norma ASTM D975 (ASTM 2016b) (Atabani et al. 2013, Silitonga et al. 2013).
CUADRO VI COMPARATIVO DE LAS PROPIEDADES FÍSICAS Y QUÍMICAS DE LA OLEORRESINA DE COPAIBA (OC) CRUDA, SECADA Y FILTRADA, Y REFINADA, ASÍ COMO DEL BIODIÉSEL DE COPAIBA
| Propiedad | OC cruda | OC secada y filtrada | OC refinada | Biodiésel copaiba | ASTM D6751* (ASTM 2015b) | ASTM D975** (ASTM 2016b) |
| Densidad (g/ml) | 0.966 | 0.965 | 0.911 | 0.901 | 0.880 | 0.850 |
| Viscosidad 40 ºC (mm2/s) | 53.3 | 50.1 | 19.8 | 8.5 | 1.9-6.0 | 1.9-4.1 |
| Índice de acidez (mg/g KOH) | 17.99 | - | 0.57 | - | 0.5 máx, | - |
| Punto de inflamación (ºC) | 98 | 99 | 98 | 96 | 100-170 | 60-80 |
| Punto de fluidez (ºC) | -24 | -24 | < -39 | < -39 | -15-16 | -35 |
* Especificación estándar para biocombustibles; ** especificación estándar para aceites combustibles diésel; ASTM: Sociedad Estadounidense para Pruebas y Materiales
Las temperaturas más bajas en las que la OC cruda, modificada y el biodiésel de copaiba pueden fluir superan en todos los casos los límites establecidos por la norma ASTM D97 (ASTM 2005c) para biocombustibles. En cuanto a la OC refinada y el biodiésel de copaiba, también sobrepasan el límite para combustibles de origen fósil, con un valor inferior a -39 ºC (Atabani et al. 2012, Silitonga et al. 2013).
De acuerdo con el comportamiento exhibido por las muestras y en particular el biodiésel de copaiba en condiciones extremas de temperatura, estos valores evitarían la obstrucción de los filtros y conductos del combustible, así como problemas de funcionamiento del motor, ya sea por falta de combustible, fallas de partida o lubricación inadecuada a bajas temperaturas.
CONCLUSIONES
Se concluye que los métodos empleados en esta investigación para la modificación química de la oleorresina no son eficientes, ya que se genera la pérdida de gran parte de la materia prima disponible. Sin embargo, las propiedades físicas y químicas medidas en la oleorresina cruda, modificada y el biocombustible obtenido, permiten establecer el potencial de este recurso para la formulación de biodiésel.
En todos los casos, el comportamiento a baja temperatura podría traducirse como una contribución significativa a la reducción de problemas de fluidez de combustible en condiciones extremas de temperatura. Sin embargo, propiedades como la viscosidad y la densidad, tanto de la oleorresina como del biodiésel de copaiba, condicionan su uso directo como combustible, pues debido a su alta viscosidad podría generar obstrucción tanto en filtros como en inyectores del motor. Los puntos de inflamación se encuentran por debajo del valor estándar para biocombustibles, pero superan los límites para combustibles de origen fósil, por lo que estarían en condiciones seguras de almacenamiento y transporte.
De acuerdo con los resultados obtenidos, los procesos de refinado y transesterificación influyeron positivamente en la estabilidad oxidativa de la oleorresina de copaiba cruda. Evidentemente, la estabilidad de la oleorresina refinada y el biodiésel de copaiba fue superior en 46 y 47 ºC, respectivamente.
En general, la oleorresina de copaiba constituye una alternativa ecosostenible que se podría emplear para mejorar las propiedades de flujo en frío en combustibles, tanto en su forma cruda como modificada o transesterificada. Su uso, aunque condicionado de forma directa, podría considerarse en mezclas con gasóleo y otros biocombustibles, a fin de mejorar las propiedades a bajas temperaturas. En estudios posteriores sería posible establecer otro proceso eficiente para la modificación química de la oleorresina.











 nueva página del texto (beta)
nueva página del texto (beta)





