INTRODUCCIÓN
La industria minera es una de las actividades que tiene una contribución importante en el crecimiento económico de México. En particular, esta actividad aunada al aprovechamiento forestal, contribuye con más del 80 % en la economía de la ecorregión templada del estado de Chihuahua. En general, tiene impactos políticos, económicos, sociales y ambientales a escalas global y local (Fernández-Manso et al. 2012). Además, en cuanto a la estructura del paisaje forestal tiene efectos significativos en las comunidades locales y en el ambiente (Younger 1997).
La estrecha relación entre la forma de vida y la explotación de los recursos naturales causa una grave contaminación ambiental, pérdida de recursos bióticos y abióticos, fragmentación de hábitat, erosión y contaminación por metales pesados (Hilson y Van Der Vorst 2002, Bridge 2004, Kumah 2006). La contaminación del agua es un gran problema que se relaciona con el crecimiento económico de cualquier país y región (Srinivasa y Govil 2008). El agua de manantiales y los flujos superficiales son la principal fuente para uso doméstico en áreas rurales (Ansari et al. 1999). Su calidad es de vital importancia debido a su uso en las actividades antrópicas (Torres et al. 2009).
La contaminación por metales potencialmente nocivos en sedimentos, suelo y agua es una de las amenazas más importantes para la calidad del ambiente y de la salud humana (Gómez-Álvarez et al. 2011). El agua se altera en sus propiedades biológicas, físicas y químicas, debido a varios agentes de la naturaleza y por la forma en que se utiliza (Metcalf y Eddy 1996).
Las actividades mineras están asociadas con los impactos ambientales, incluyendo la contaminación por metales de los sedimentos y de los sistemas acuáticos (Hun-Bok et al. 2005). La minería está asociada con la modificación de la superficie, lo cual afecta la cuenca y el régimen hidrológico tanto en cantidad como en calidad (Bud et al. 2007). Ejemplo de lo anterior son los metales pesados que ingresan al ambiente acuático principalmente por descargas directas de fuentes industriales (Alloway y Ayres 1993). Específicamente, los problemas ambientales relacionados con los depósitos de mineral son el drenaje ácido y las altas concentraciones de metales pesados en el agua de drenaje de los yacimientos mineros (Carrillo-Chávez et al. 2003).
El distrito de Ocampo es uno de los corredores mineros de gran importancia en actividades económicas del estado de Chihuahua. Su localización es al centro oeste del estado, el cual contempla el parque nacional de Basaseachi y el área de protección de flora y fauna Tutuaca. Los ecosistemas forestales ubicados en este distrito evidencian procesos de degradación y contaminación ambiental producidos por las actividades forestales y por la explotación minera. Además, en esta región nacen los ríos Balloreca, Concheño y Apituchi, los cuales pertenecen a la región hidrológica sur de Sonora (RH09) y drenan agua y sedimentos a las áreas de agricultura de la costa del Pacífico (Villanueva et al. 2009). La geología de la zona se encuentra formada por rocas ígneas extrusivas (85.4 % riolita-toba ácida) y sedimentarias (12 % arenisca-conglomerado) y en menor escala por rocas volcánicas del tipo riolíticas terciarias del periodo Cuaternario (CONANP 2014). La composición del suelo es de origen residual y aluvial dominado por Feozem, Regosol y Litosol. Esta área se encuentra en un intervalo de altitud de 458 a 2911 msnm y presenta un clima templado subhúmedo con lluvias de verano. El intervalo de precipitación anual en el municipio de Moris es de 600 a 1000 mm (INEGI 2005a), mientras que para el resto de la zona es de 1000 a 1200 mm (INEGI 2005b). Dada la variabilidad fisiográfica de esta región, se encuentran en ella diversos tipos de asociaciones vegetales como el bosque de pino encino y otras coníferas latifoliadas. Ejemplo de lo anterior son: los pinos (Pinus arizonica, Pinus durangensis, Pinus engelmannii, Pinus ayacahuite y Pinus leiophylla), los encinos (Quercus rugosa, Quercus crassifolia, Quercus sideroxyla y Quercus fulva), el táscate (Juniperus deppeana) y el madroño (Arbutus arizonica y Arbutus xalapensis; Azarcoya 2012). De igual manera, entre las nueve principales especies nativas de ictiofauna presentes en los cauces de la región se incluyen: el rodapiedras mexicano (Compostoma ornatum), y otras especies como Catostomus bernardini, Gila nigrescens, Gila robusta, Ictalarus melas, Ictalarus pricei, Lepomis cynaellus y Salmo sp.
Actualmente no existen estudios que permitan conocer el impacto de las actividades mineras sobre la calidad del agua. Por lo anterior, el objetivo de este trabajo fue evaluar las concentraciones de algunos elementos traza en muestras de agua de ríos y manantiales en el ambiente circundante del corredor minero de oro y plata en el distrito de Ocampo, Chihuahua. Con ello se podrá tener un análisis inicial del impacto por contaminación química hacia estos cuerpos de agua que son las principales fuentes de suministro para uso y consumo humano en dicha región.
MATERIALES Y MÉTODOS
El muestreo se llevó a cabo después de la temporada de lluvias, en el mes de octubre de 2014. Las muestras de agua fueron colectadas de manantiales y ríos que son las principales fuentes de abastecimiento de agua para consumo humano. Los ríos Balloreca, Concheño y Apituchi son permanentes y fueron muestreados en varios puntos a lo largo del flujo de agua. Asimismo, se colectaron muestras de agua de siete manantiales (Fig. 1). Los parámetros de temperatura, sólidos disueltos totales, conductividad eléctrica, turbidez y pH fueron medidos in situ, con un potenciómetro multiparamétrico (Hanna, modelo HI-98130). La georreferenciación de cada punto de muestreo fue realizada con un sistema de geoposicionamiento global GPS (Garmin, modelo GPSmap 62s). Cada muestra fue colectada en recipientes de polietileno de 1 L de capacidad, las cuales fueron preservadas adicionando HNO3 (hasta pH = 2) para ser analizadas en el laboratorio posteriormente. El pretratamiento de los recipientes de muestreo fue realizado como lo indica la norma NOM-001-ECOL -1996 (SEMARNAT 1996).
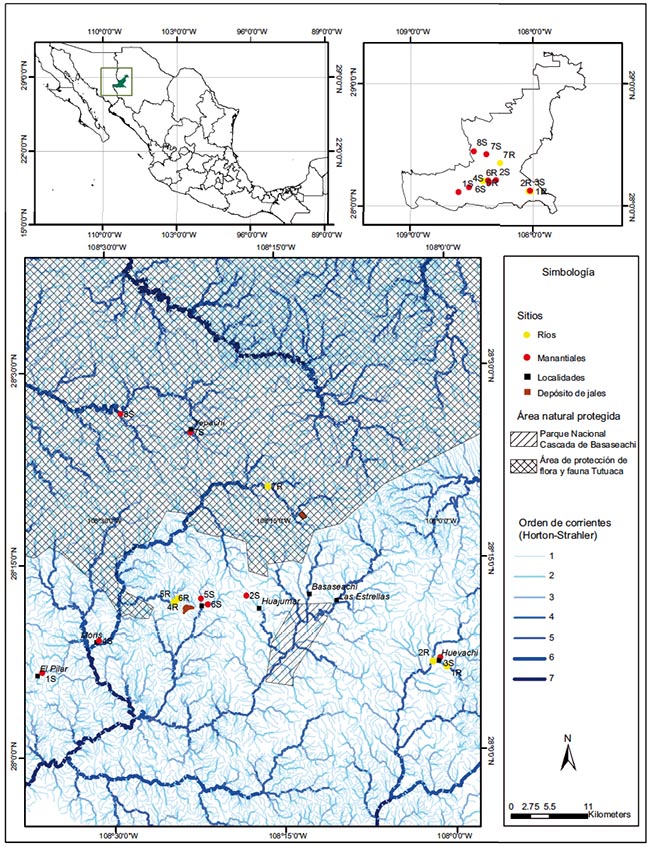
Fig. 1 Localización del área de estudio con los puntos de muestreo de agua de río (R) y manantial (S)
En el laboratorio, las muestras fueron digeridas en microondas (Anton Paar, modelo Multiwave GO) utilizando HCl y HNO3 (EPA 2007). La caracterización elemental se realizó mediante un espectrómetro ICP-OES, manufacturado por Perkin Elmer, modelo 8300. Las mediciones realizadas para cada muestra se realizaron por triplicado. Además, se midió una muestra blanco utilizando agua desionizada grado reactivo (Sumilab). Asimismo, para la calibración del equipo se utilizaron soluciones patrón de concentraciones de 1, 5 y 10 mg/L de un estándar de 21 elementos, de alta pureza (STD-As QC 21 elements, 100 mg/L de cada elemento), marca Perkin Elmer. Los elementos mayoritarios analizados fueron Ca y Mg, mientras que los elementos traza fueron As, Be, Cd, Cr, Cu, Li, Ni, Pb, Sb, Se, Sr y Zn. El límite de detección del equipo (LD) para los elementos analizados es del orden de ppb (µg/L): As (1), Be (0.08), Ca (0.58), Cd (0.05), Cr (0.15), Cu (0.69), Li (0.23), Mg (0.3), Ni (0.35), Pb (1.1), Sb (1.1), Se (1.3), Sr (0.01), Zn (0.88). A partir de los elementos mayoritarios se pudo calcular la dureza. Generalmente, la dureza se expresa en ppm de CaCO3 o meq/L, por lo que se determina utilizando la ecuación 1:
Dureza (mg/L CaCO3) = (meq Ca/L + meq Mg/L) × 50 (1)
Donde, un meq/L CaCO3 equivale a 50 ppm CaCO3.
RESULTADOS
En el cuadro I se muestran los datos de temperatura (T), pH, sólidos disueltos totales (SDT), conductividad eléctrica (CE), turbidez (TB) y las coordenadas geográficas de cada sitio de muestreo. La T del agua de manantial fue ligeramente más alta que la de las muestras de río, con valores promedio de 18.3 y 16.1 en agua de río y manantial, respectivamente. Los valores de pH en agua de río fueron de neutral a ligeramente básico, mientras que en agua de manantial el pH fue de ligeramente ácido a neutro. Los valores de los SDT determinados en muestras de río y manantial se encontraron en un intervalo de concentraciones de 23 a 334 mg/L y de 13 a 242 mg/L, respectivamente. Los valores de pH y SDT se encuentran dentro de los límites permisibles propuestos en las diferentes agencias de regulación para agua de consumo humano (EPA 2000, SSA 1994, WHO 2008).
Cuadro I resultados de los parámetros medidos in situ de las muestras de los ríos (Balloreca, Concheño y Apituchi) y manantiales, así como los límites permisibles para cada uno de ellos propuestos por las diferentes agencias reguladoras de calidad de agua
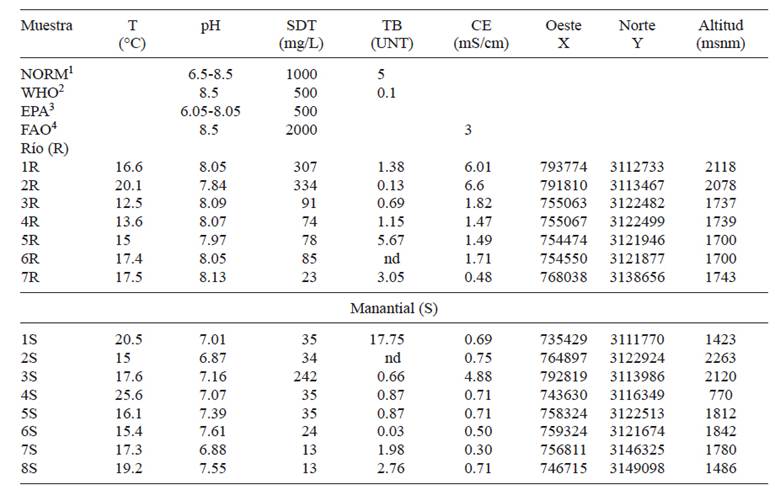
1NOM-127-SSA1-1994, (Secretaría de Salud 1994), agua de consumo humano.
2Organización Mundial de la Salud, (WHO 2008), agua de consumo humano.
3Agencia de Protección Ambiental, (EPA 2002), agua de consumo humano.
4Organización de las Naciones Unidas para la Agricultura y la Alimentación (FAO, por sus siglas en inglés), Ayers (1976), calidad del agua para agricultura.
T = temperatura, pH = potencial de hidrógeno, SDT = sólidos disueltos totales, TB = turbidez, CE = conductividad eléctrica.
Por otra parte, se encontró que los valores de TB fueron variables tanto en muestras de río como en manantiales. Así, en las muestras de agua de río el intervalo de TB en unidades nefelométricas de turbidez (UNT) fue de 0.13 a 5.67 UNT, mientras que en agua de manantial el intervalo fue entre 0.03 y 17.8 UNT. Las muestras 5R y 1S mostraron valores por encima del límite permisible para agua de consumo humano en la normatividad mexicana (SSA 1994). Es importante puntualizar que tomando en cuenta el valor del límite de calidad establecido por la Organización Mundial de la Salud (OMS) (0.1 UNT), la mayoría de las muestras se encuentran por arriba de dicho valor (WHO 2008). Sin embargo, en la muestra de agua del punto 6S se obtuvo un valor de TB por debajo de los límites establecidos por todas las agencias aquí presentadas. La CE fue mayor en muestras de agua de río que en agua de manantial, donde los valores promedio fueron de 2.8 y 1.2 mS/cm, respectivamente. Con ello, las muestras 1R, 2R y 3S mostraron valores de CE por arriba de los límites establecidos para irrigación agrícola por la Organización de las Naciones Unidas para la Alimentación y la Agricultura (FAO) (Ayers 1976).
Además, en el presente estudio se analizó el contenido de varios elementos mayoritarios y traza. Los contenidos de As, Be, Cd, Cr, Pb y Sr en las muestras colectadas se encontraron por debajo del límite de detección del equipo. Los resultados de las concentraciones de Ca, Mg, Cu, Li, Ni, Sb, Se y Zn se encuentran en el cuadro II. La concentración promedio de Ca en agua de río fue más alta que en las muestras de agua de manantial, con valores de 8.7 y 6.2 mg/L, respectivamente. Los contenidos de Mg fueron solamente detectados en muestras de agua de río en un intervalo de concentraciones de 0.7 a 1.9 mg/L. De acuerdo con la normatividad, las concentraciones de estos elementos son menores a los límites permisibles. Asimismo, la dureza fue calculada utilizando los contenidos de Ca y Mg. El intervalo determinado fue de 11.4 a 42.6 mg/L CaCO3 y de 5 a 22.5 mg/L CaCO3, en las muestras de agua colectadas en río y manantial, respectivamente.
Cuadro II Concentración de elementos traza (mg/L) en muestras de agua de río (balloreca, concheño y apituchi) y manantial
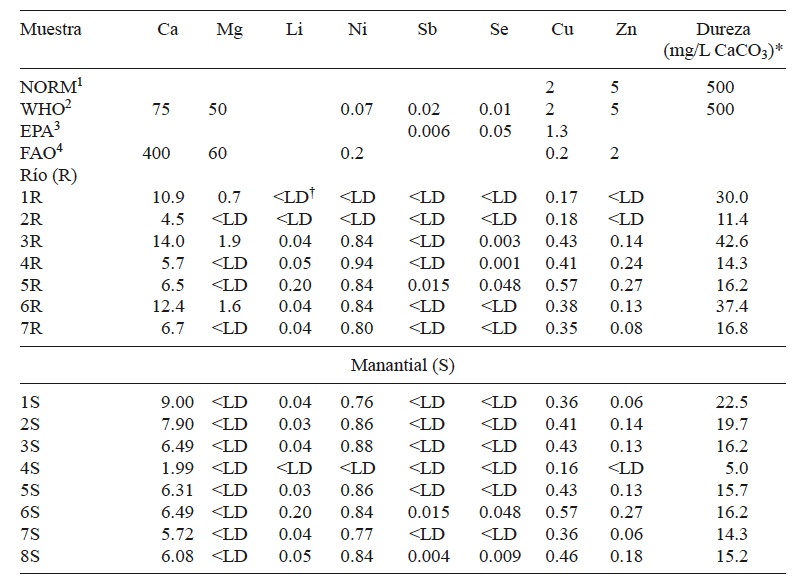
1NOM-127-SSA1-1994, (Secretaría de Salud 1994), agua de consumo humano.
2Organización Mundial de la Salud, (WHO 2008), agua de consumo humano.
3Agencia de Protección Ambiental, (EPA 2002), agua de consumo humano.
4Organización de las Naciones Unidas para la Agricultura y la Alimentación (FAO, por sus siglas en inglés), Ayers (1976), calidad del agua para agricultura.
*Calculados de las concentraciones de Ca y Mg en las muestras de agua
† Limite de detección = LDequipo< 1µg/L
DISCUSIÓN
Los valores de los parámetros fisicoquímicos obtenidos en las muestras de agua fueron bajos, excepto para la TB. La principal causa de la TB en el agua es el material particulado debido a la resuspensión de los sedimentos. El valor más alto de TB en agua de río se encontró en la muestra 5R. Asimismo, en el agua de manantial de la muestra 1S se obtuvo un valor de 17.8 UNT. Es importante mencionar que el agua de este manantial se utiliza principalmente para consumo humano en esa región. En este punto de muestreo, el agua proviene de una mezcla de flujos de dos manantiales lo cual causa resuspensión de los sedimentos del fondo en el punto de muestreo. Además, adyacentes a este punto muestreado existen jales de la minería independiente (gambusinos) los cuales, por procesos de erosión y lixiviación, contribuyen con iones disueltos y partículas sedimentables. Para el agua de consumo humano un valor de TB de 5 UNT es por lo general aceptable (SSA 1994), aunque esto puede variar de acuerdo con las características de la fuente. Sin embargo, los valores de TB recomendados deben estar por debajo de 0.1 UNT para la calidad del agua de consumo humano según la OMS (WHO 2008). Ningún efecto sobre la salud ha sido propuesto por un valor alto de TB. Sin embargo, es de gran importancia en la calidad de agua para condiciones de vida acuática (CCME 2007). Asimismo, la CE mostró valores altos en las muestras 1R, 2R y 3S. Todas ellas fueron tomadas en la cuenca del río Apituchi, lo cual concuerda con las altas concentraciones de SDT en esos puntos de muestreo. Además, los valores calculados de dureza son menores a los límites considerados en la regulación nacional e internacional, dichos valores indican que el agua de los ríos y los manantiales aquí analizados se puede catalogar como "agua blanda" (< 50 mg/L CaCO3).
Los elementos traza medidos en las muestras de agua se encontraron en la tendencia siguiente: Ni ˃ Cu ˃Zn ˃ Li > Se. La mayoría de los elementos traza fueron menores en comparación con los límites establecidos para agua de consumo humano presentados por la Agencia de Protección Ambiental de Estados Unidos de América (EPA 2000) y la normatividad mexicana (SSA 1994). Por el contrario, el Sb sí se presentó en algunas muestras en concentraciones mayores al límite permisible. Este elemento fue detectado sólo en algunas muestras, con un intervalo de concentraciones entre 0.004 y 0.015 mg/L. Además, en dos muestras de agua de río (3R y 4R) las concentraciones de Se estuvieron por encima de los límites marcados por la EPA.
De manera general, el agua continental presenta concentración baja de Ni (Ayers 1976, WHO 2008). El Ni no es tomado en cuenta por la normatividad para agua de consumo en la EPA y en la regulación mexicana. Sin embargo, las concentraciones encontradas en todas las muestras son mayores a las establecidas por la OMS. Las muestras de agua mostraron concentraciones altas de Ni tanto para ser usadas como agua de consumo o para la agricultura. Se sugiere que las concentraciones altas de Ni son debidas a las características geológicas de la región, aunque en el presente trabajo no se realizó la caracterización elemental del material rocoso.
Por otra parte, en la zona de estudio se localiza mineralización de elementos tales como Au, Ag, Cd, Cu, Pb, Sb, Zn y Hg (SGM 2010). En esta misma zona se encuentran reportados los contenidos de Cu, Sb y Zn en sedimentos de arroyos. Así, las concentraciones de Cu en sedimentos de algunos arroyos de la zona se encuentran en un intervalo de 0.9 a 22 ppm (SGM 2000a), mientras que en las muestras de agua del presente estudio fueron de 0.17 a 0.57 mg/L. Tales concentraciones se encuentran por debajo de los límites permisibles para el agua de consumo. No obstante, en la mayoría de las muestras dichas concentraciones se encuentran por encima del límite permitido por la FAO para el agua de riego (Cuadro II). Aunque en esta región no se practica ampliamente la agricultura, hay pequeñas granjas donde se tiene, a menor escala, la práctica de cultivo para el consumo familiar. De igual manera, el Servicio Geológico Mexicano reporta que en sedimentos de arroyo localizados en los alrededores del Pilar, las concentraciones de Sb fueron hasta de 396 ppm (SGM 2000b). En esa comunidad se colectó agua de manantial (punto 1S), donde la concentración de este elemento no fue detectada. De igual manera, los sedimentos de los arroyos presentes en el resto de la zona de estudio mostraron concentraciones de Sb de 2.2 a 4.7 ppm (SGM 2000b). Por otra parte, es conocido que el Se frecuentemente se encuentra en asociación con minerales que contienen azufre (ATSDR 2003) mientras que Sb se asocia a óxidos (ATSDR 1992). En el presente estudio, el agua obtenida en los puntos 5R y 6S mostraron concentraciones altas de Cu, Se y Sb en comparación con el resto de los puntos (Cuadro II). Por lo anterior, ambos elementos presentes tanto en las muestras de agua de manantial como en las de río, pueden estar siendo transportados principalmente por sedimentos y el material particulado suspendido en agua. Estas muestras de agua fueron tomadas en una zona altamente alterada por las actividades antrópicas relacionadas con la actividad minera, específicamente por el cambio de uso de suelo (incendios forestales, bancos de materiales, jales mineros, caminos, cultivos, entre otros).
Por otra parte, las concentraciones de Zn en las muestras de agua estuvieron por debajo de los límites permisibles establecidos por las diferentes instituciones tomadas en cuenta en este trabajo. Además, aunque el valor límite permisible de Zn se encuentre en 5 mg/L, la OMS recomienda que el agua que contenga 3 mg/L no es apta para consumo humano (WHO 2008). Algunos autores han reportado valores que han alcanzado concentraciones > 500 mg/L de Zn en agua superficial en estudios realizados en zonas circundantes a un distrito minero (Ramos et al. 2014). Valores de concentración que son muy altos en comparación con lo encontrado en nuestro estudio (valor máximo de concentración de 0.27 mg/L; Cuadro II). La concentración del Zn en el agua está en función del pH, potencial de reducción oxidación (Eh) y de otras especies químicas presentes (SRHNA 2004, WHO 2008). En agua superficial, el Zn comúnmente se encuentra con valencia +2 en especies químicas tales como ion libre (Zn+2) y compuestos inorgánicos como ZnSO4 y ZnCO3. Como ZnSO4, es soluble en agua y provoca un sabor astringente indeseable al agua a una concentración mayor de 4 mg/L. Como carbonato de zinc su solubilidad disminuye con el aumento de pH (WHO 2008). En la figura 2 se muestra la correlación encontrada entre las concentraciones de Zn respecto al pH. Las muestras de agua de los ríos mostraron pH en un intervalo de neutro a ligeramente básico, donde la concentración de Zn manifestó una tendencia a disminuir (R2 = 0.66 y p = 0.0002) al decrecer el valor del pH (Fig. 2a). Por el contrario, en muestras de agua tomadas en manantiales, donde los valores de pH oscilaron desde ligeramente ácido a neutro, se observó que la concentración de Zn se incrementa (R2 = 0.64 y p = 0.1) con el aumento del pH (Fig. 2b). En agua con condiciones de oxidación y pH cercanos a 7, el Zn es principalmente encontrado como ion libre y con bajas concentraciones como hidróxido o carbonato (SRHNA 2004). Con lo anterior, podemos sugerir que en agua de río de nuestra zona de estudio el Zn se encuentra asociado a carbonatos en el intervalo de pH medido. Por ello, el ZnCO3 tenderá a precipitarse sobre superficies de sedimentos debido a su baja solubilidad (0.21 g/L). Lo anterior corrobora las concentraciones de Zn en sedimentos de arroyos en la zona de estudio, con intervalo de concentraciones de 17.3 a 83 ppm (SGM 2000c). Además del pH, se observó que existe una correlación lineal de los contenidos de Zn y Cu, para el agua de río (R2 = 0.67) y de manantial (R2 = 0.77). Como resultado, el Zn y Cu presentarán sus máximas concentraciones en agua a pH alrededor de 7.98. Por lo anterior, se puede sugerir que a un mayor pH a partir de 7, estos elementos probablemente se encuentren adsorbidos a los sedimentos.
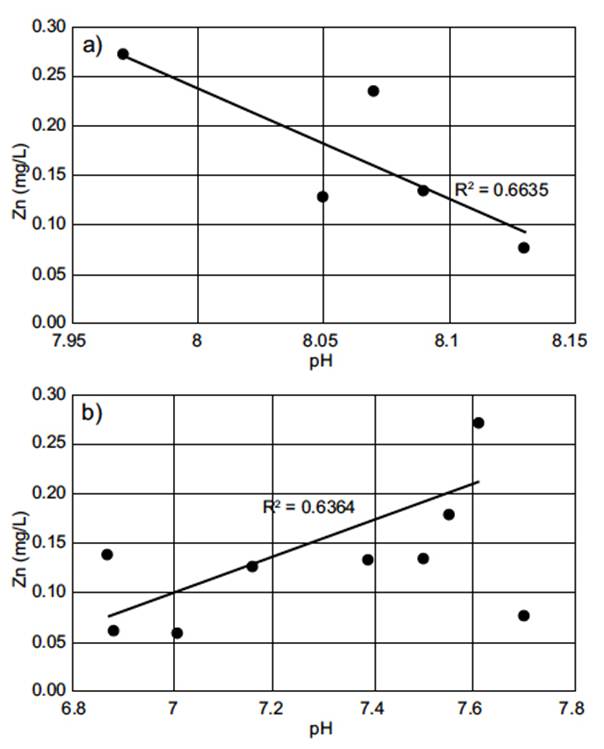
Fig. 2 Correlación lineal de pH con las concentraciones de Zn en las muestras de agua de: a) río y b) manantial
En este estudio se calcularon los elementos traza en muestras de agua. Sin embargo, la mayoría de los elementos tienen que ser evaluados en los sedimentos debido a su alta reactividad, así como a los fenómenos de adsorción, desorción, precipitación y resuspensión, para así obtener una mejor comprensión del fenómeno de interacción sólido/solución.
Tanto la evaluación de los parámetros físicos y químicos como la caracterización de los elementos pueden indicar una adecuada calidad de agua para el desarrollo de la vida acuática. En consecuencia, algunos países tienen normas bien establecidas para la protección de la vida acuática. Por ejemplo, el Consejo Canadiense de Medio Ambiente toma en cuenta los valores de 0.004, 0.025 y 0.05 mg/L, como límites permisibles para Cu, Ni y Zn, respectivamente (CCME 2007). Sin embargo, la EPA considera un valor más estricto permisible de concentración de Zn en agua de 0.012 ppm (EPA 2002) para no afectar la vida acuática. En comparación con estas regulaciones, las muestras de agua de río analizadas presentaron valores más altos de concentraciones de Cu, Ni y Zn. Por lo tanto, en las zonas donde las actividades antrópicas están involucradas deben vigilarse las concentraciones de elementos traza. Además, otros autores han mencionado que valores altos de TB en cuerpos de agua podrían afectar tanto en cantidad como en calidad la producción de pescado (Singler, et al. 1984). Es recomendable evaluar y monitorear los contenidos de elementos traza en rocas, suelos, sedimentos de los ríos, flora y fauna del distrito minero de Ocampo, con el fin de tener una mejor comprensión de la movilidad de tales elementos y su posible influencia como contaminantes.
CONCLUSIONES
Las actividades mineras están frecuentemente relacionadas con los impactos ambientales, incluyendo la contaminación por metales pesados en los sistemas acuáticos. Aunque, las concentraciones de elementos determinadas en este trabajo son menores que los límites permitidos por la EPA y por la regulación mexicana para agua de consumo humano, algunos de ellos superan los permisibles por la OMS. Lo anterior es debido en gran medida a las características geológicas de la región. Sin embargo, se determinó que el río Balloreca está siendo impactado por la actividad antrópica en la zona cercana a los jales mineros debido a la presencia de elementos tales como Cu, Li, Sb, Se y Zn. Se concluye también, que en los cuerpos de agua, el pH juega un papel importante en la presencia de especies químicas como son el Cu, el Ni y el Zn. Sin embargo, por diversos estudios se observa que son los sedimentos quienes son una fuente importante de transporte de metales pesados en la región estudiada. Debido a que el agua tiene TB alta, se plantea que las especies químicas cuantificadas se encuentran asociadas al material particulado suspendido. La realización de este tipo de estudios es importante debido a que representa una línea base de análisis que permite plantear estrategias para reducir los efectos negativos que afectan el desarrollo de la biota, principalmente en cuerpos de agua. Asimismo, se sugiere establecer medidas de remoción de elementos tóxicos en el agua, tanto de manantiales como de ríos, cuando el agua de dichas fuentes sea utilizada para consumo humano con la intención de disminuir cualquier efecto adverso a la salud de la población.











 nova página do texto(beta)
nova página do texto(beta)


