Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista internacional de contaminación ambiental
versão impressa ISSN 0188-4999
Rev. Int. Contam. Ambient vol.25 no.3 Ciudad de México Ago. 2009
Composición iónica y niveles de acidez de las lluvias en Maracaibo, Venezuela, entre 1989 y 2001
Ion composition and acidity levels of the Maracaibo rains, Venezuela, between 1989 and 2001
Ligbel SÁNCHEZ, José MORALES, Harvi VELÁSQUEZ, Dennis PORTILLO, Yulixis CANO, Brinolfo MONTILLA, Nelkis IRIARTE y Johan MESA
Laboratorio de Química Ambiental, Departamento de Química, Facultad Experimental de Ciencias, Universidad del Zulia, Maracaibo 4011, Venezuela. Fax: 058–261–7598125; e–mail: ligbels@hotmail.com
Recibido septiembre 2008
Aceptado enero 2009
RESUMEN
Los gases y aerosoles atmosféricos, desde varias fuentes de emisión naturales y antrópicas, se incorporan en las gotas de lluvia a través de varios procesos fisicoquímicos durante los eventos de precipitación. El conocimiento de la composición química de las precipitaciones es crítico para el entendimiento de la contaminación regional y local y sus efectos sobre los ecosistemas. Entre las sustancias ácidas o potencialmente ácidas envueltas en la formación de la lluvia ácida, se puede señalar los compuestos de azufre, nitrógeno y cloro. Un factor importante en las características ácido–base de la lluvia es la emisión de materiales alcalinos como carbonato de calcio, magnesio y amoniaco, que se encuentran generalmente como un vapor capaz de neutralizar los ácidos sulfúrico y nítrico. Los datos de la química de las lluvias, en este trabajo, provienen de varios sitios de la ciudad de Maracaibo, las muestras de agua de lluvia fueron recolectadas en tres períodos repartidos entre los años 1989 y 2001, con equipos de muestreo manuales y automáticos. Para los diferentes análisis realizados se utilizaron un espectrómetro de absorción atómica modalidad llama, Perkin–Elmer 3110 y un cromatógrafo iónico con detector de conductividad, marca Dionex 2000i/SP. El pH–PPV en la lluvia de Maracaibo es 4.8, indicativo de una atmósfera ligeramente ácida e influenciada por: SO4–2, Cl– y NO3– en 86 %. La especie neutralizante más importante es el NH3, aunque las concentraciones de Ca+2 y Mg+2 son aportes adicionales al proceso de neutralización atmosférica. El mayor flujo de depositación húmeda fue exhibido por: NH4+, SO4–2, Cl– y NO3– con 67.5 %. Estadísticamente, se evidenció una alta correlación entre SO4*, Cl* y NO3– con el ion H+ (p<0.05), ratificando su influencia en la acidez de las lluvias de Maracaibo. Se concluye que sólo una pequeña fracción de los iones potencialmente ácidos contribuyen a la acidez libre de las lluvias, debido a la capacidad neutralizante del NH3, Ca* y Mg*.
Palabras clave: lluvia ácida, balance iónico de lluvias, contaminación atmosférica, pH, tasa de depositación húmeda.
ABSTRACT
The atmospheric gases and aerosols coming from various natural and anthropogenic emissions are incorporated into raindrops through various physicochemical processes during rain events. Knowledge of the chemical composition of precipitation is critical to understand regional and local air pollution and its effects on the ecosystems. Sulfur, nitrogen and chlorine compounds are mainly involvedin rain acidity production as acidic or potentially acidic species. An important factor in the acid–base characteristics of rain is the emission of alkaline materials such as calcium–magnesium carbonates and ammonia, generally found as a vapour responsible to sulfuric and nitric acids neutralizing. Rain chemistry reported in this work originates from several sites of the city of Maracaibo and the rainwater samples were gathered in three periods between 1989 and 2001, using manual and automatic samplers. The different analyses were made using a flame atomic absorption spectrometer, Perkin–Elmer 3110 and an ion chromatography equipment with a conductivity detector, Dionex 2000i/SP. The pH–PPV in Maracaibo rainwater was 4.8, indicating an atmosphere lightly acid and influenced by SO4–2, Cl– and NO3– in 86 %. NH3 is the most important neutralizing species, though the concentrations of Ca+2 and Mg+2 are additional contributions to atmospheric neutralizing process. The major flow of wet deposition was exhibited by NH4+, SO4–2, Cl– and NO3– with 67.5 %. Statistically, a high correlation was found between SO4*, Cl* and NO3– ions with the H+ ion (p<0.05), ratifying its influence in the acidity of Maracaibo's rain. It is concluded that a small fraction of the acid potentially ions contributes to free acidity of the rains, due to the neutralizing capacity of NH3, Ca* and Mg*.
Key words: acid rain, atmospheric pollution, ionic balance of rains, pH, wet deposition.
INTRODUCCIÓN
Recientemente se han publicado estudios sobre precipitación química en países tropicales (Williams et al. 1997, Ayers et al. 2000, Gillent et al. 2000, Lara et al. 2001), así como estudios sobre la química del agua de lluvia para países con clima semiárido (Mamane y Gottlieb 1995, Satsangi et al. 1998, Herut et al. 2000, Norman et al. 2001, Topçu et al. 2002), y especialmente en Venezuela (Morales et al. 1990, Sanhueza et al. 1992, Morales et al. 1995, 1996, 1998, Sánchez et al. 2001). En la cuenca del Lago de Maracaibo (Venezuela) se ha demostrado que existe una amplia variación espacial y temporal en la pluviosidad, dándose eventos prolongados e intensos de lluvia y de sequía en algunas regiones. Se han estudiado períodos de sequía con lluvias ocasionales y períodos de lluvia con lapsos muy secos (varios días). Por tal razón, en la cuenca se deben tomar ambos procesos atmosféricos, depositación húmeda y seca, como importantes para la evaluación del ciclo de nutrientes (Morales et al. 1990, Sánchez et al. 2001); la depositación húmeda cumple un papel muy importante en la limpieza de la atmósfera, ya que a través de este proceso se aporta la mayor cantidad de iones desde la misma (Abdul Hameed et al. 2006).
Con frecuencia se da por sentado que el pH natural de la lluvia no contaminada, controlada por la disociación del dióxido de carbono (CO2) atmosférico disuelto, tienen un valor de 5.6; las disminuciones con respecto a este valor se deben a adición de componentes ácidos por actividades humanas (Charlson y Rodhe 1982, Ravichandran y Padmanabhamurty 1994).

Los contaminantes emitidos a la atmósfera pueden variar de alguna forma el pH de la lluvia (Charlson y Rodhe 1982, Stumm y Sigg 1987, Ravichandran y Padmanabhamurty 1994). Por ejemplo, en el oeste y mediooeste de los Estados Unidos de América, las partículas del suelo tienden a ser básicas (por su alto contenido de carbonatos) y pueden incrementar el pH de las lluvias. Por otra parte, a lo largo de la región este se forman aerosoles por interacción de los ácidos sulfúrico y nítrico gaseosos; además, las partículas del suelo son usualmente ácidas, lo cual produce una disminución en el pH de la lluvia (Babich et al. 1980). Los procesos que afectan la acidez de la precipitación son muy numerosos y complejos e incluyen transformaciones gas–partícula, reacciones fotoquímicas y catalíticas, reacciones acuosas dentro de la nube y de la lluvia y el transporte atmosférico (Stumm y Sigg 1987, Morales et al. 1990, 1995, Mphepya et al. 2004).
La precipitación ácida se atribuye en primer lugar a los ácidos fuertes sulfúrico (H2SO4) y nítrico (HNO3). Los precursores inmediatos de estos ácidos son los gases SO2 y NO2, de origen natural o antrópico. En general, las fuentes naturales de estos gases tienen una distribución global, mientras que las emisiones antrópicas tienden a concentrarse cerca de los centros poblados (complejos industriales y vehículos automotores). Estos gases son oxidados en la atmósfera durante la dispersión para producir H2SO4 y HNO3. Las principales fuentes antrópicas de SOx son los combustibles fósiles (carbón y petróleo), fertilizantes (Al–Momani et al. 1995) y los procesos industriales (Williams et al. 1997), en especial la producción primaria de metales. En adición a los combustibles fósiles, el transporte vehicular también contribuye en una proporción significativa a las emisiones totales de NOx. En algunas regiones industrializadas las emisiones de cloruro de hidrógeno gaseoso (HCl) pueden contribuir a la formación de precipitación ácida (Morales et al. 2000). El HCl es un contribuyente significativo en la acidez de la lluvia, sin embargo, las fuentes y mecanismos de su formación aún no se han establecido completamente. Las emisiones antrópicas provienen principalmente de la producción de cloro como gas y HCl (Zhu y Liu 2003).
Además de las fuentes principales de contaminación atmosférica, existen otros contribuyentes importantes en la formación de lluvias ácidas. El amoníaco (NH3, especie alcalina más importante en la atmósfera) se encuentra generalmente como un vapor alcalino capaz de neutralizar los ácidos sulfúrico y nítrico, produciendo un incremento en el pH de la precipitación (De Mello y De Almeida 2004). Sin embargo, como el amoníaco se disuelve para formar amonio (NH4+), éste puede incrementar la tasa de conversión de SO2 a H2SO4 en la atmósfera, al favorecer la formación de sulfato de amonio [(NH4)2SO4] (Erisman y Wyers 1993, Druyzer et al. 1994). La mayor parte de las emisiones de amoníaco a la atmósfera ocurren por procesos naturales y biológicos, como por ejemplo: descomposición de la materia orgánica, incendios forestales, volatilización del suelo (fertilizantes) y océano (Al–Momani et al. 1995, Krupa 2002).

Un factor importante en las características ácido–base de la lluvia es la emisión de materiales alcalinos sólidos (como carbonato u óxidos de calcio y magnesio) provenientes del suelo, los cuales pueden tener una acción significativa en la disminución de la acidez de la lluvia (Varma 1989, Al–Momani et al. 1995, Prakasa Rao et al. 1995, Teir et al. 2006).

Los ácidos orgánicos (por ejemplo, acido fórmico y acético) son constituyentes químicos importantes de la precipitación y del agua de las nubes (Aneja 1993,Williams et al. 1997); la fuente de estos compuestos no está bien establecida, aunque se asume su aparición a partir de emisiones biogénicas o quema de combustible fósil (Sanhueza et al. 2001, Kelly et al. 2002, Sanhueza et al. 2003).
El presente trabajo tiene como principal objetivo analizar el resultado de tres períodos de muestreo de aguas de lluvia en la ciudad de Maracaibo, Venezuela, entre los años 1989 y 2001, para contribuir a la evaluación y mantener una base de datos de los cambios en la depositación húmeda de esta región.
MATERIALES Y MÉTODOS
La ciudad de Maracaibo es la capital del Estado Zulia (Venezuela), con aproximadamente 2.6 millones de habitantes y está ubicada al norte: 71°56'00'' longitud oeste y 10°34'00'' latitud norte, y al sur: 71°45'00'' longitud oeste y 10°31'00'' latitud norte (Fig. 1). Con un clima semiárido, se encuentra al borde del estrecho de Maracaibo, en dirección suroeste, viento abajo del Complejo Petroquímico El Tablazo, las refinerías de Amuay y Cardón y las canteras de la Isla de Toas, fuente de materia prima para la producción de cemento. En esta ciudad se encuentran otras fuentes de emisión (industrias y un gran parque automotor), las cuales aportan gases y partículas que generan una influencia ambiental importante en la región, entre las que se pueden distinguir la Termoeléctrica Ramón Laguna y la Planta de Cemento Vencemos Mara.

El régimen estacional de precipitación en esta región de estudio es diferente al del resto del país. La época de lluvia se encuentra entre los meses de abril a noviembre, con precipitaciones esporádicas variables, observándose dos períodos de mayor lluvia: abril–junio y septiembre–noviembre. La época seca se presenta entre los meses de diciembre y marzo, sin precipitaciones significativas. El volumen promedio de precipitación anual oscila entre 300 y 500 mm (INE 2008a). La media de temperatura anual es 28 °C (con temperaturas promedio mínimas de 23 °C y máximas de 35 °C) (INE 2008b) y los vientos prevalecientes sobre la ciudad, desde el Mar Caribe, poseen una dirección NE y NNE, como puede observarse en la figura 2 (estos datos fueron suministrados por La Estación Meteorológica La Cañada, Estado Zulia).
Períodos y sitios de muestreo
Los sitios de muestreo se distribuyeron en función de los períodos muestreados entre 1989 y 2001: en 1989 el muestreo se realizó en la zona norte de la ciudad de Maracaibo (septiembre–noviembre 1989), en el sitio 1; en el período de octubre de 1995 a diciembre de 1996, se escogieron cuatro sitios de muestreo en la zona norte (sitios 1, 2, 3 y 4) y dos sitios en la zona sur de la ciudad de Maracaibo (sitios 5 y 6); en el período febrero de 2000 a mayo de 2001, el muestreo se realizó nuevamente en el sitio 1. A continuación se describe cada sitio de muestreo:
Sitio 1: Ubicado en la zona norte de la ciudad, el muestreador fue colocado en la azotea del edificio Bloque A–1 de la FEC–LUZ a una altura de 10 m, aproximadamente. Este sitio se caracteriza por estar influenciado por el tráfico automotor de avenidas y calles.
Sitio 2: Ubicado en la zona norte de la ciudad, el muestreador fue colocado a nivel del suelo en un área despejada, en la Estación de Bomberos Universitaria frente a la Facultad de Ingeniería de LUZ. Este sitio también está caracterizado por la influencia del tráfico automotor de avenidas y calles.
Sitio 3: Ubicado en la zona noroeste de la ciudad, el muestreador fue colocado a nivel del suelo en una zona residencial denominada Sector La Limpia, de alta densidad en tráfico automotor.
Sitio 4: Ubicado en la zona noroeste de la ciudad, el muestreador fue colocado a nivel del suelo en una zona residencial denominada Sector Cuatricentenario y, al igual que el sitio 3, con numeroso tráfico automotor.
Sitio 5: Ubicado en la zona sur de la ciudad, el muestreador fue colocado a nivel del suelo en una zona residencial denominada Sector Sierra Maestra, con un tráfico automotor de mediana densidad.
Sitio 6: Ubicado en la zona sur de la ciudad, el muestreador fue colocado a nivel del suelo en una zona residencial denominada Urbanización San Francisco, con un mayor tráfico automotor que el sitio 5.
Los sitios 5 y 6 se localizan en un área de influencia directa a las emisiones provenientes de la Planta Termoeléctrica Ramón Laguna y la Planta de Cemento Vencemos Mara, ubicadas aproximadamente a 8 y 10 km de distancia de los sitios mencionados, como aparecen señaladas en la figura 1.
Recolección y análisis químico de muestras
Los muestreos de los períodos 1989 y 1995–1996 fueron realizados con un equipo de diseño para recolección manual de muestras de lluvia, que consistía en un embudo de boca cuadrada conectado a un envase de polietileno soportado en una estructura metálica para darle estabilidad. El colector se abría manualmente al comenzar el evento de lluvia y al terminar de llover se cerraba para evitar la contaminación por sedimentación de especies químicas en la atmósfera. El muestreo del período 2000–2001 se realizó con un equipo automático para recolección de muestras de depositación húmeda y seca, marca Andersen, modelo APS. La ventaja de este colector automático es que dismuye la contaminación del agua de lluvia recolectada antes y después de cada evento y garantiza que todos los eventos de lluvia sean tomados sin excepción. Gracias a este equipo se recolectó una cantidad representativa de muestras del período 2000–2001, ya que hubo muy pocas precipitaciones durante este período.
Se usaron botellas de polietileno de diferentes capacidades para la recolección de las muestras; todos los envases fueron lavados con HNO3 a 10 % durante 24 horas. Después se enjuagaron con suficiente agua destilada y desionizada hasta que la conductividad del agua de lavado fuera igual a la del agua desionizada, garantizando que no existiera ningún tipo de ión contaminante en los envases. Finalmente, se secaron a baja temperatura en una estufa y se guardaron hasta su uso.
Todas las muestras de lluvia se removieron de los colectores lo más pronto posible, antes de doce horas después de cada evento. Se midió el volumen y el pH de cada muestra (potenciómetro marca Corning, modelo 125) y se filtraron; posteriormente cada muestra se dividió en dos porciones de 200 mL, las cuales fueron preservadas para su análisis correspondiente con CHCl3 (3:500) para el análisis de aniones (iones no metálicos) por cromatografía iónica, o con HNO3 (hasta un pH de 2) para la determinación de cationes (iones metálicos) por espectrometría de absorción atómica.
La concentración de NH4+ en los períodos 1989 y 1995–1996, fue evaluada por medio de un electrodo selectivo de amonio marca Orion, modelo 95–12, mientras que en el muestreo del período 2000–2001 se determinó dicha concentración a través de un cromatógrafo iónico (CI) con un detector de conductividad (Dionex, modelo 2000i/SP), usando una columna catiónica CS12A y una precolumna CG12A.
Los metales Na+, K+, Ca+2 y Mg+2 fueron analizados por la técnica de espectrometría de emisión y absorción atómica, en las muestras de los años 1989 y 1995–1996. Se usó un espectrómetro de absorción atómica Perkin–Elmer 3110 con condiciones de trabajo óptimas establecidas por la técnica utilizada (Perkin–Elmer 1984). En el período 2000–2001, el análisis de los cationes se llevó a cabo en un equipo CI DIONEX 2000i/SP, con una columna catiónica CS12A y una precolumna CG12A, usando un método isocrático con H2SO4 22 mN como eluyente (0.5 mL/min de velocidad de flujo).
El análisis de aniones (Cl–, NO3–, SO4–, PO4–3, CH3COO– y HCOO–) en el muestreo de 1995–1996, se realizó utilizando un equipo CI Dionex 2000i/SP, con una columna aniónica AS11 y una precolumna AG11. Para la separación de los aniones inorgánicos se usó NaOH 21 mM y para los aniones orgánicos NaOH 0.5 mM, como eluyente (1 mL/min de velocidad de flujo). Para el período de muestreo 2000–2001, el análisis de los aniones se realizó con el mismo equipo CI provisto de una columna aniónica AS14 y una precolumna AG14, usando una mezcla de eluyentes para la separación de los iones Na2CO3 1.8 mM – NaHCO3 1.7 mM (1 mL/min de velocidad de flujo).
Con el objeto de hacer un estimado del error experimental de las muestras de agua de lluvia, se tomaron cuatro muestras de un mismo evento escogido aleatoriamente, preservándose para el posterior análisis de aniones y cationes respectivos. El análisis de estas fracciones mostró una reproducibilidad relativamente buena, con una desviación estándar relativa (DER) menor a 10 % para los iones analizados. Los límites de detección de los metales analizados por espectrometría de absorción atómica se determinaron de tres veces la desviación estándar de diez lecturas del control (Cuadro I). En el caso de los límites de detección para los análisis por cromatografía iónica, se obtuvieron aplicando la siguiente ecuación:

donde Ybl es el corte en el eje Y cuando la concentración es cero (control), Sbl es la desviación estándar del control, b es la pendiente de la curva de calibración y n el número de medidas individuales (Long y Winefordner 1983).

Ecuaciones matemáticas para expresar los resultados
La fórmula utilizada para el cálculo de la concentración promedio ponderada en volumen (CPPV) permite homogenizar los eventos de lluvia de baja precipitación con elevadas concentraciones iónicas con los eventos de alta precipitación y concentraciones diluidas; equivale a mezclar todas las lluvias en un mismo recipiente y luego medir la concentración iónica, la cual sería equivalente a la CPPV expresada en µeq/L:

Donde Cn es la concentración del ión en cada evento de lluvia (µeq/L), Pn los mm de precipitación de cada evento y Pperíodo es la sumatoria de los mm correspondientes al período de muestreo (Fornaro y Gutz 2006, Mphepya et al. 2004).
La tasa de depositación húmeda (TDH, mg/m2 x período) representa el flujo iónico de masa hacia el ecosistema mediante la depositación por lluvia. La TDH depende directamente de dos factores: la concentración iónica en la lluvia y la cantidad de lluvia que precipita. Para el cálculo de TDH se utilizó la siguiente ecuación:

Donde PE es el peso equivalente del ión del cual se calcula la TDH (Mphepya et al. 2004).
RESULTADOS Y DISCUSIÓN
Precipitación y composición química
La composición química de las lluvias de Maracaibo presentó un pH–PPV de 4.8 para el período completo de 1989 a 2001, similar a los valores obtenidos en los períodos de muestreo individuales, como se observa en el cuadro II. Con los valores individuales de la concentración de hidrógeno se calculó su concentración promedio y con este valor se determinó el pH promedio ponderado en volumen correspondiente. Los resultados indican que la lluvia de la ciudad de Maracaibo es ligeramente ácida, influenciada mayormente por las especies inorgánicas SO4–2, NO3–, Cl– y NH4+, siendo ésta última la especie alcalina más abundante en la atmósfera de esta ciudad.
Los mayores contribuyentes a la acidez potencial en los tres períodos muestreados son las especies aniónicas inorgánicas SO4–2, NO3–, Cl–; éstas fueron neutralizadas por especies químicas alcalinas representadas por los cationes NH4+, Ca+2 y Mg+2, permitiendo sólo una acidez libre de 5 %, aproximadamente. En 1989 se encontraron las concentraciones más altas de NH4+, SO4–2, Cl– y HCOO–, mientras que NO3– y PO4–3 fueron más abundantes en 1996; en 2000 se obtuvieron altas concentraciones de Na+, K+, Ca+2, Mg+2 y CH3COO–, lo cual evidencia el exceso de cationes en el balance iónico para este período en Maracaibo.
El valor de pH–PPV calculado a partir de la CPPV de H+ para el período completo 1989–2001, fue aproximadamente de 5, lo cual indica que la lluvia de esta ciudad posee cierto carácter ácido; sin embargo. las fluctuaciones entre los valores de pH obtenidos en todos los eventos (3.6–8.0) reflejan que este valor depende de las características atmosféricas del período de muestreo. 48 % de los eventos de lluvia presentaron un pH menor a 5.6, aunque sólo 7 % estuvo por debajo de 4, mientras que 52 % fueron eventos con pH mayor a 5.6, lo que sugiere una gran influencia de especies alcalinas en estas muestras de lluvia. De estos resultados se puede inferir que las lluvias de la ciudad Maracaibo están directamente influenciadas por fuentes antrópicas como la petroquímica, la industria eléctrica, la quema de combustible fósil y el tránsito automotor.
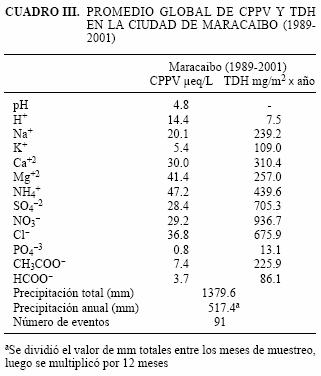
Las TDH mostradas en el cuadro III permiten conocer la cantidad de mg/m2 x año que se depositan de cada especie en el ecosistema de la región estudiada. Los iones que poseen mayor TDH en Maracaibo son NO3– > SO4–2 > Cl – > NH4+ > Ca+2 > Mg+2, los cuales influyen mayoritariamente a la química de las precipitaciones de la ciudad. Las TDH mostradas para los iones HCOO– y CH3COO– son comparables con las encontradas en algunas zonas rurales donde predominan las fuentes biogénicas (emisión natural o quema de vegetación) (Morales et al.1995).
En Maracaibo, 80 % del contenido iónico de las muestras de agua de lluvia está constituido por los siguientes iones: NO3–, Cl –, SO4–2, NH4+, Ca+2 y Mg+2, los cuales mantienen una relación significativa en cuanto a las fuentes de emisión y el origen de las especies. Existe una contribución de estos iones por la influencia de aerosoles de origen marino, la cual se puede evaluar por medio de la siguiente ecuación (Morales et al. 1996):

Las relaciones de la composición química del agua de mar para cada ión son: K+:0.021; Ca+2:0.044; Mg+2:0.25; SO4–2:0.122 y Cl–:1.17. Los resultados obtenidos de las concentraciones de los iones marinos se restaron de los totales calculados y se obtuvo la contribución de estos iones originados en la corteza terrestre, biogénicos más los antrópicos. En el cuadro IV se aprecian los porcentajes calculados para cada uno de los iones en exceso con respecto del aerosol marino y que afectan potencialmente la química de las precipitaciones.

Todos estos iones (con excepción del Cl–) tienen una importante influencia en la composición química de las precipitaciones (> 90 %) por provenir de fuentes de emisión no marinas (corteza terrestre, biogénicas y antrópicas). En el caso del Cl– se observa un aporte similar (cercano a 50 %) tanto de fuentes no marinas como de origen marino. Las emisiones de cloro provenientes de la planta de cloro–soda ubicada vientos arriba de la ciudad de Maracaibo en el complejo petroquímico El Tablazo (Fig. 1), son las que explican principalmente los altos niveles de Cl– no–marino encontrados en las lluvias de esta ciudad (Abdul Hameed et al. 2006).
La composición química de las precipitaciones fue tratada calculando coeficientes de correlación estadística, con 95 % de intervalo de confianza. En el cuadro V se muestran valores de coeficientes de correlación entre algunos iones del agua de lluvia colectada en la ciudad de Maracaibo; sólo se reflejaron los pares con una correlación mayor a 0.5. Se observa que el H+ se correlaciona con los iones SO4–2, SO4*, Cl* y NO3–, confirmando que estos iones son los que contribuyen principalmente a la acidez potencial de las lluvias. Los iones orgánicos CH3COO– y HCOO– se correlacionan entre ellos porque poseen la misma fuente de emisión (fuentes biogénicas o quemas de combustible fósil). El Na+ mantiene una correlación con el Cl– ya que ambos provienen del aerosol marino, que ejerce una gran influencia sobre la ciudad de Maracaibo. Cl– y NO3–, así como Cl*, exhiben una relación en cuanto a su fuente de origen: aerosol marino y gas–particulado atmosférico (Morales et al. 1996, Sánchez et al. 2001).

Balance iónico de las lluvias de Maracaibo
Si todos los iones SO4*, Cl*, NO3–, PO4–3, CH3COO– y HCOO– existieran en forma de acidez libre, las lluvias hubieran tenido un pH de 4.1. La diferencia indica que los ácidos presentes en las muestras de lluvia estuvieron bajo un proceso de neutralización significativo. La relación entre la sumatoria de los iones positivos y la sumatoria de los negativos es 1.65 (Abdul Hameed et al. 2006), mostrando una buena capacidad neutralizante en la atmósfera de Maracaibo, sobre todo por parte del NH3 (relativo a la concentracación de NH4+) (Fornaro y Gutz 2006). Es importante señalar que el SO4–2 y el Cl– de origen marino no están asociados a la acidez libre (H+) de la lluvia, sino que se asocian a los cationes naturales del agua de mar (principalmente Na+, K+, Ca+2, Mg+2); por esta razón, en los cálculos de la acidez libre sólo se toman en cuenta el sulfato y cloruro no–marinos (SO4* y Cl*).
CONCLUSIÓN
El valor promedio del pH de lluvia en la ciudad de Maracaibo es 4.8, lo cual indica que la atmósfera es ligeramente ácida y tiene influencia de SO4–2, NO3– y Cl– en un 86 %. La especie neutralizante más importante es el NH3 (relativo a la concentración de NH4+), conjuntamente con los aportes no marinos de Ca y Mg. El mayor flujo de depositación húmeda (TDH) es de los iones que afectan altamente el equilibrio ácido–base en la atmósfera de la ciudad: NO3–, Cl–, SO4–2 y NH4+ (67.5 %). Es importante mencionar que los iones que son removidos de la atmósfera por depositación húmeda afectan al ecosistema donde son depositados: suelos, cuerpos de agua, construcciones en general, seres vivos, etc., y que manteniendo un monitoreo de lo que se deposita se pueden controlar o minimizar las emisiones de contaminantes a la atmósfera de la ciudad. La influencia de fuentes de origen no marino es marcada en Maracaibo, ya que los valores encontrados de iones en exceso con respecto al aerosol marino son mayores a 50 %, exceptuando Cl–, cuyo mayor aporte lo ejerce el mar (64 %). La correlación estadística (p<0.05) entre los iones estudiados ratifica la influencia de las especies ácidas SO4*, Cl* y NO3– sobre el pH de las lluvias de la ciudad de Maracaibo. Debido a la alta capacidad neutralizante de la atmósfera de la ciudad (NH3, Ca, Mg), sólo una porción de los iones potencialmente ácidos contribuyen a la acidez libre de las lluvias.
AGRADECIMIENTOS
Los autores de este trabajo desean agradecer al Consejo de Desarrollo de Ciencias y Humanidades de la Universidad del Zulia (CONDES–LUZ) por proporcionar todo el soporte necesario para la realización de este trabajo.
REFERENCIAS
Abdul Hameed M., Al Obaidy J. y Joshi H. (2006). Chemical composition of rainwater in a tropical urban area of northern India. Atmos. Environ. 40, 6886–6891. [ Links ]
Al–Momani I.F., Yavuz Ataman O., Anwari M.A., Tuncel S., Kose C. y Tuncel G. (1995). Chemical composition of precipitation near an industrial area at Izmir, Turkey. Atmos. Environ. 29, 1131–1143. [ Links ]
Aneja V.P. (1993). Organic compounds in cloud water and their deposition at a remote continental site. J. Air Waste Ma. 43, 1239–1244. [ Links ]
Ayers G.P., Peng L.C., Fook L.S., Kong.C.W., Gillett R.W. y Manins P.C. (2000). Atmospheric concentrations and deposition of oxidised sulfur and nitrogen species at Petaling Jaya, Malaysia. Tellus B 52, 60–73. [ Links ]
Babich H., Davis D.L. y Stotzky G. (1980). Acid precipitation. Causes and consequences. Environment 22, 6–13. [ Links ]
Charlson R.J. y Rodhe H. (1982). Factors controlling the acidity of natural rainwater. Nature 295, 683–685. [ Links ]
De Mello W.Z. y De Almeida M.D. (2004). Rainwater chemistry at the summit and southern flank of the Itatiaia massif, Southeastern Brazil. Environ. Pollut. 129, 63–68. [ Links ]
Druyzer J.H., Verhagen H.L.M. y Weststrate J.H. (1994). The dry deposition of ammonia onto a Douglas Fir forest in the Netherlands. Atmos. Environ. 28, 1241–1253. [ Links ]
Erisman J.W. y Wyers G.P. (1993). Continous measurements of surface exchange of SO2 and NH3; implications for their possible interaction in the deposition processes. Atmos. Environ. 27A, 1937–1949. [ Links ]
Fornaro A. y Gutz I.G.R. (2006). Wet deposition and related atmospheric chemistry in the Sao Paulo metropolis, Brazil. Part 3: Trends in precipitation chemistry during 1983–2003. Atmos. Environ. 40, 5893–5901. [ Links ]
Gillentt R.W., Ayers G.P., Mhwe T., Selleck P.W. y Harjanto H. (2000). Concentration of N and sulfur species in gas and rainwater from several sites in Indonesia. Water. Air Soil Poll. 120, 205–215. [ Links ]
Herut B., Starinsky A., Katz A. y Rosenfeld D. (2000). Relationship between the acidity and chemical composition of rainwater and climatological conditions along a transition zone between large deserts and Mediterranean climate, Israel. Atmos. Environ. 34, 1281–1292. [ Links ]
INE (2008a). Instituto Nacional de Estadística. Precipitación total, según entidad federal, y estación meteorológica, 1999–2003. (en línea). http://www.ine.gov.ve/Fnaturales/CuadroNaturales.asp?Codigo=121–0222/01/2008 [ Links ]
INE (2008b). Instituto Nacional de Estadística. Temperatura promedio anual del aire, media, máxima y mínima según entidad federal, dependencia federal, estación meteorológica y año, 1999–2003. (en línea). http://www.ine.gov.ve/Fnaturales/CuadroNaturales.asp?Codigo=121–0322/01/2008 [ Links ]
Kelly V.R., Lovett G.M., Weathers K.C. y Likens G.E. (2002). Trends in atmospheric concentration and deposition compared to regional and local pollutant emissions at a rural site in southeastern New York, USA. Atmos. Environ. 36, 1569–1575. [ Links ]
Krupa S.V. (2002). Sampling and physico–chemical analysis of precipitation: a review. Environ. Pollut. 120, 565–594. [ Links ]
Lara L.B.L.S., Artaxo P., Martinelli R.L., Victoria R.L., Camargo P.B., Krusche A., Ayers G.P., Ferraz E,S.B. y Ballester M.V. (2001). Chemical composition in rainwater and anthropogenic influences in the Piracicaba River Basin. Southeast Brazil. Atmos. Environ. 35, 4937–4945. [ Links ]
Long G.L. y Winefordner J.D. (1983). Limit of detection. A closer look at the IUPAC definition. Anal. Chem. 55, 712A–724A. [ Links ]
Mamane Y. y Gottlieb J. (1995). Ten years of precipitation chemistry in Haifa, Israel. Water. Air Soil Poll. 82, 549–558. [ Links ]
Morales J.A., Hermoso M., Serrano H. y Sanhueza E. (1990). Trace elements in the Venezuelan Savannah atmosphere during dry and wet periods, with and without vegetation burning. Atmos. Environ. 24A, 407–414. [ Links ]
Morales, J.A., Bifano, C. y Escalona, A. (1995). Rainwater chemistry at the western savannah region of the Lake of Maracaibo Basin, Venezuela. Water, Air Soil Poll. 85, 2325–2330. [ Links ]
Morales J.A., Sánchez L., Albornoz A., Socorro E. y Morillo A. (1996). Concentraciones de especies antropogénicas en la lluvia de la ciudad de Maracaibo. Congreso Mundial sobre Contaminación del Aire en Países en Vías de Desarrollo. San José de Costa Rica. 21 al 26 de agosto, 1996. Vol. II, pp. 221–228. [ Links ]
Morales J.A., Sánchez de Graterol L., Velásquez H., de Nava M.G. y de Borrego B.S. (1998). Determination by ion chromatography of selected organic and inorganic acids in rainwater at Maracaibo, Venezuela. J. Chromatogr. A. 804, 289–294. [ Links ]
Morales J.A., Sánchez de Graterol L. y Mesa J. (2000). Determination of chloride, sulfate and nitrate in groundwater samples by ion chromatography. J. Chromatogr. A. 884, 185–190. [ Links ]
Mphepya J.N., Piennar J.J., Galy–Lacaux C., Held G. y Turner C.R. (2004). Precipitation chemistry in semi–arid areas of Southern Africa: a case study of a rural and an industrial site. J. Atmos. Chem. 47, 1–24. [ Links ]
Norman M., Das S.N., Pillai A.G., Granat L. y Rodhe H. (2001). Influence of air mass trajectories on the chemical composition of precipitation in India. Atmos. Environ. 35, 4223–4235. [ Links ]
Prakasa Rao P.S., Momin G.A., Safai P.D., Pillai A.G. y Khemani L.T. (1995). Rain water and throughfall chemistry in the silent valley forest in south India. Atmos. Environ. 29, 2025–2029. [ Links ]
Ravichandran C. y Padmanabhamurty B. (1994). Acid precipitation in Delhi, India. Atmos. Environ. 28, 2219–1197. [ Links ]
Sánchez L., Morales J., Barroso O., Quiva D., Mesa J., Portillo D., Cano Y. e Iriarte N. (2001). Evaluación de la composición química de muestras de lluvia en la ciudad de Maracaibo. V Congreso Venezolano de Química. Maracaibo, Venezuela. 1 al 5 de abril, 2001. pp. 701–704. [ Links ]
Sanhueza E., Arias M.C,. Donoso L., Graterol N., Hermoso M., Marti L., Romero J., Rondón A. y Santana M. (1992). Chemical composition of acid rains in the Venezuelan savanna region. Tellus B 44, 54–62. [ Links ]
Sanhueza E., Holzinger R., Donoso L., Santana M., Fernández E. y Romero J. (2001). Compuestos orgánicos volátiles en la atmósfera de la Gran Sabana. I: Concentraciones y química atmosférica. Interciencia 26, 597–605. [ Links ]
Sanhueza E., Alfonzo Y. y Santana M. (2003). Compuestos orgánicos volatiles en la atmósfera de la Gran Sabana. II: HCHO, HCOOH y CH3COOH en lluvias. Interciencia 28, 29–35. [ Links ]
Satsangi G.S. Lakhani A., Khare P., Singh S.P., Kumari K.M. y Srivastava S.S. (1998). Composition of rain water at a semi–arid rural site in India. Atmos. Environ. 32, 3783–3793. [ Links ]
Stumm W. y Sigg L. (1987). Aquatic chemistry of acid deposition. Several chemical concepts are prerequisite to understanding acid deposition genesis and properties. Environ. Sci. Technol. 21, 8–13. [ Links ]
Teir S., Eloneva S., Fogelholm C.J. y Zevenhoven R. (2006). Stability of calcium carbonate and magnesium carbonate in rainwater and nitric acid solutions. Energ. Convers. Manage. 47, 3059–3068. [ Links ]
Topçu S., Incecik S. y Atimtay A.T. (2002). Chemical composition of rainwater at EMEP station in Ankara, Turkey. Atmos. Res. 65, 77–92. [ Links ]
Varma G.S. (1989). Impact of soil–derived aerosols on precipitation acidity, in India. Atmos. Environ. 23, 2723–2728. [ Links ]
Williams M.R., Fischer T.R. y Melack J.M. (1997). Chemical composition and deposition of rain in the Central Amazon, Brazil. Atmos. Environ. 31, 207–217. [ Links ]
Zhu J. y Liu Z. (2003). Long–range persistence of acid deposition. Atmos. Environ. 37, 2605–2613. [ Links ]














