Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista mexicana de cardiología
Print version ISSN 0188-2198
Rev. Mex. Cardiol vol.24 n.3 México Jul./Sep. 2013
Caso clínico
Bloqueo AV completo congénito. Revisión y presentación de un caso
Congenital complete av block. Review and case report
Juan Manuel Cortés Ramírez,* Juan Manuel de Jesús Cortés de la Torre,** Raúl Arturo Cortés de la Torre,*** Baldomero Javier Reyes Méndez,* Alfredo Salazar de Santiago,* Sofía Isabel Carrillo Aguilar,* Noel Veyna Fajardo,* Francisco Luna Pacheco,* Javier Aguayo Pérez,* Luis Claudio Macías Islas****
* Área de la Salud UAZ.
** Residente de Medicina Interna, Hospital San José, Tec. de Monterrey.
*** Escuela de Medicina "Ignacio Morones", Tec. de Monterrey.
**** Hospital General de Zacatecas, IMSS.
Dirección para correspondencia:
Juan Manuel Cortés Ramírez
Guerrero Núm. 128,
Col: Centro, Zacatecas, Zac.
Tel: 9229225
E-mail: dr.cortesramirez@gmail.com
RESUMEN
El bloqueo auriculoventricular es un retardo o interrupción del impulso eléctrico proveniente del nodo sinusal a nivel del nódulo auriculoventricular. Es congénito en uno de cada 20,000-25,000 nacidos vivos. Secundario a desarrollo embrionario anormal del nodo auriculoventricular asociado a anomalías cardiacas estructurales o por isoinmunización materna con anticuerpos que dan daño inmunológico irreversible del tejido cardiaco del feto, por inflamación y fibrosis. Los factores de mal pronóstico son: coexistencia con malformaciones cardiovasculares, insuficiencia cardiaca, frecuencia ventricular menor de 50 por min, bradicardia durante el sueño menos de 30 por min, marcapaso bajo o cambiante, QT prolongado. En asintomáticos, se recomienda seguimiento con monitoreo y ecocardiografía. Las indicaciones de marcapasos permanente son: ritmo de escape con complejos anchos, ectopia y disfunción ventricular, QT largo, cardiomegalia y auriculomegalia derecha.
Palabras clave: Cardiopatía congénita, bloqueo auriculoventricular completo congénito, isoinmunización materna.
ABSTRACT
The atrioventricular block is a delay or interruption of the electrical impulse from the sinusal node, to level of the auriculoventricular nodule is a congenital (BAVC), in one of every 20,000-25,000 born alive. Secondary to an abnormal embryonic development of the node AV, associated with structural cardiac abnormalities or for maternal is immunization with antibodies that cause immunological irreversible damage in the fetal heart tissue, by inflammation and subsequent fibrosis. The factors of worst prognosis are: Coexistence with cardiovascular malformations, heart failure, ventricular frequency below 50 per minute, bradycardia less than 30 per minute during sleep, pacemaker under or changing, long QT. In asymptomatic patient, it is recommended monitoring and follow-up with echocardiography. Indications for permanent pacemaker are: escape rhythm with wide complex, ectopy and ventricular dysfunction, long QT, cardiomegaly and right atrial dilatation.
Key words: Congenital heart disease, congenital complete atrioventricular block, maternal isoimmunization.
INTRODUCCIÓN
El bloqueo auriculoventricular (AV) es un retardo o interrupción del impulso eléctrico proveniente del nodo sinoauricular a nivel del nodo auriculoventricular. El de tipo congénito (BAVC) se presenta en forma aislada o familiar, uno por cada 20,000 a 25,000 nacidos vivos. La primera descripción la realizó Morquio en 1901, la primera confirmación electrocardiográfica, Van den Heuvel en 1908 y el primer diagnóstico prenatal fue realizado por Yater en 1929.1-3
Una de las causas es el desarrollo embrionario anormal del nodo AV, asociado a anomalías cardiacas estructurales como: la transposición de grandes arterias, los síndromes poliesplénicos, ventrículo único, tumores del miocardio, síndrome de QT-largo y el de Kearn-Soyer (oftalmoplejía externa, retinosis pigmentaria y miopatía mitocondrial), presente en 25 a 50% de los casos.4,5
La otra forma, en 80% de los casos es sin malformaciones estructurales, afecta a recién nacidos y niños por defecto congénito secundario a isoinmunización materna anormal, con autoproducción de anticuerpos IgG antinucleares, anti-SSA/Ro y anti-SSB/La6 que se transfieren vía transplacentaria con daño inmunológico irreversible en el tejido cardiaco en forma de inflamación y posterior fibrosis que causa bloqueo auriculoventricular con ausencia del nodo auriculoventricular.6 Los anticuerpos se detectan en el suero de las madres y en el tejido cardiaco del recién nacido,7 y persisten hasta los cuatro meses de vida extrauterina. La positivización de los AC y los criterios clínicos de enfermedad autoinmune materna pueden ocurrir años después del nacimiento de un feto afectado,8 principalmente lupus eritematoso sistémico3,7,10 y raramente artritis reumatoide o dermatomiositis.4,6,9 Son factores de riesgo: diagnóstico de BAVC en miembros de la familia, títulos elevados de AC anti-Ro+ (superiores a 1:16), la presencia de AC anti-Ro+ (SS-A) acompañados de AC anti-La+ (SS-B) y ciertos haplotipos HLA (HLA DR3), insuficiencia cardiaca, frecuencia ventricular menor de 50 por min, bradicardia durante el sueño menor de 30 por min, marcapaso bajo o cambiante, QT prolongado y bloqueos de rama.
El síndrome de lupus neonatal incluye: eritemas, leucopenia, anemia y trombocitopenia y BAVC, única complicación permanente, los restantes desaparecen después de seis a ocho meses de vida extrauterina.
Se detecta por Doppler o ecocardiografía fetal entre las 16 y 30 semanas de gestación por bradicardia fetal persistente, con insuficiencia cardiaca congestiva o hidropesía fetal secundaria y mortalidad mayor del 20%, muchos de los afectados necesitarán de marcapaso en los primeros 12 meses de vida.2
En el seguimiento hasta los 30 o 40 años de edad, muestra buen pronóstico cuando no coexisten anomalías cardiacas, cursan con frecuencia cardiaca entre 50 y 70 por minuto, con desarrollo psicomotor adecuado y sin crisis de Stokes-Adams.3 En un estudio de Fernández y colaboradores, la mortalidad fue de 5.5%, siempre en lactantes. Con seguimiento mayor de 10 años en 40 pacientes no se registró mortalidad a largo plazo (dos mujeres tuvieron cinco embarazos y partos normales, con hijos normales). Se colocó marcapaso cardiaco en 9.3% de los pacientes.11
Tratamiento médico, betamiméticos, en recién nacido y lactante menor con insuficiencia cardiaca y frecuencia ventricular fija menor de 50 por min, y si fracasa, implantación de marcapasos transitorio o permanente. En niños y adolescentes asintomáticos, se recomienda seguimiento con monitoreo y ecocardiografía, ya que pudiera comenzar con síntomas a cualquier edad. Las indicaciones de marcapasos permanente son ritmo de escape con complejos anchos, ectopia y disfunción ventricular, QT largo, cardiomegalia y crecimiento de aurícula derecha.12
PRESENTACIÓN DEL CASO
Masculino de 33 años de edad, carga genética para diabetes mellitus, hipertensión arterial sistémica y cardiopatías por ambas ramas, producto de gesta III, madre de 28 años, durante la gestación, la cual se le diagnostica artritis reumatoide a los 34 años de edad, diabetes mellitus a los 40 años, carcinoma renal a los 50 años. Ocupación cajero, vida sedentaria, refiere disnea de grandes esfuerzos, edema de miembros inferiores vespertino posicional o con el calor, precordalgia punzante, con duración de tres horas, sin relación con esfuerzos y sin más datos acompañantes, motivo por el cual acudió a consulta y al realizarle electrocardiograma, se detectó bloqueo auriculoventricular completo (Figura 1). El ecocardiograma transtorácico no mostró alteraciones estructurales (Figura 2).
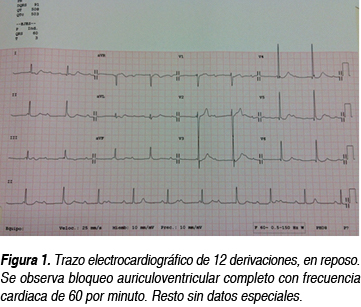
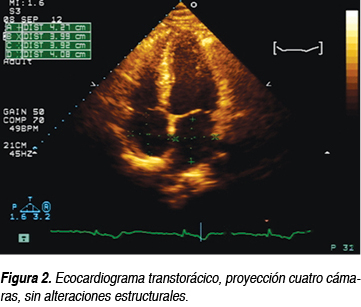
COMENTARIO
En realidad se trata de una patología rara, en un hospital general se presenta un caso aproximadamente cada cinco años. Por ello, en caso de bradicardia en paciente joven, generalmente no hacemos diagnóstico diferencial con bloqueo auriculoventricular (AV) completo congénito, de ahí que el diagnóstico se hace por exclusión. Cuando está definido, es necesario practicar monitoreo de Holter, prueba de esfuerzo y ecocardiograma para integrar lo mejor posible el diagnóstico y estar en posibilidad de ofrecer el mejor tratamiento; la indicación de marcapasos está relacionado con la clase funcional y la actividad del paciente, pero no descartamos que la colocación de marcapasos sea la opción más recomendable. El paciente motivo del reporte, está en clase funcional I, sin evidencia de afección alguna, y se mantiene con seguimiento periódico con la intención de indicar el marcapasos definitivo en el momento más oportuno.
REFERENCIAS
1. Michaëlsson M. Congenital heart block: an international study of the natural history. Cardiovasc Clin. 1972; 4: 85-101. [ Links ]
2. Yater WM. Congenital heart block. Review of the literature: report of a case with incomplete heterotaxy, the electrocardiogram in dextrocardia. Am J Dis Child. 1929; 38: 112-136. [ Links ]
3. Grolleau R, Leclerg F, Guillaumont S, Voisin M. Congenital atrioventricular block. Arch Mal Coeur Vaiss. 1999; 92: 47-55. [ Links ]
4. Bradyarrhythmias. In: Nelson: Textbook of pediatrics . WB Saunders, Philadelphia, 1992: 1197. [ Links ]
5. Chuaqui B, Farrú O. Bloqueo atrioventricular completo con doble interrupción del sistema conductor. Rev Chil Pediatr. 1986; 57: 440-444. [ Links ]
6. Bradiarritmias. En: Nelson: Tratado de pediatría . La Habana: Editorial Ciencias Médicas, 1998; 1680. [ Links ]
7. Sirén MK, Julkunen H, Kaaja R, Kurki P, Koskimies S. Role of HLA in congenital heart block: susceptibility alleles in mothers. Lupus. 1999; 8: 52-59. [ Links ]
8. Finkelstein Y, Alder Y, Harel L, Nussinovitch M, Youinou P. Anti-Ro (SSA) and anti-La (SSB) antibodies and complete congenital heart block. Ann Intern Med. 1997; 148: 205-208. [ Links ]
9. Azuafa A, Saulny de Jorgez J, Berroteran O, Moeante A, Abbruzzese C, González C et al. Diagnóstico ecográfico prenatal de bloqueo auriculoventricular congénito. Rev Obstet Ginecol Venez. 1986; 46: 145-146. [ Links ]
10. de Parseval N, Forrest G, Venables PJ, Heidmann T. ERV-3 envelope expression and congenital heart block: what does a physicological knockout teach us. Autoimmunity. 1999; 30: 81-83. [ Links ]
11. Fernández GB, Batista N, Zarlenga B, Román MI, Kreutzer EA. Bloqueo auriculoventricular completo congénito. Rev Lat Cardiol Cir Cardiovasc Infant. 1985; 1: 49-56. [ Links ]
12. Tanel R, Rhodes L. Arritmias en fetos y neonatos. Clínicas de Perinatología. Enfermedades Cardiovasculares en el Neonato. 2001; 1: 181-199. [ Links ]
Nota
Este artículo puede ser consultado en versión completa en: http://www.medigraphic.com/revmexcardiol














