Introdução
Ainteração entre os níveis e as modalidades que integram o Sistema Nacional de Educação vem sendo destacada como uma ação fundamental, tanto pelas políticas públicas quanto pelos setores da sociedade, pois vincula-se aos processos de democratização, acesso, permanência e qualidade do ensino. Trata-se de uma preocupação que tem promovido, cada vez mais, discussões em torno da efetividade e divulgação das atividades universitárias, uma vez que, dentre as importantes missões das instituições superiores, uma delas é difundir o conhecimento acumulado através do ensino. Dessa forma, se faz necessária uma maior colaboração entre os dois níveis, básico e superior, buscando dar sentido as pesquisas realizadas e associando a teoria com o cotidiano (Habermas, 2004; Tauchen e Devechi, 2016).
Exemplos de possibilidades de interação entre pesquisa e ensino são extração química, caracterização espectroscópica e utilização de indicadores naturais de pH. Dessa forma, buscou-se com esse trabalho demonstrar a interação entre o resultado obtido em pesquisa realizada durante pós-graduação em produtos naturais, e aulas teóricas e práticas desenvolvidas em turmas de ensino médio.
Fundamentação Teórica
A pesquisa é uma das atividades intrínsecas e essenciais à instituição universitária, ao lado do ensino e da extensão. Dentre as importantes missões da instituição superior, uma delas é difundir o conhecimento acumulado através do ensino, além de produzir novos conhecimentos. Essa produção deve buscar responder às necessidades e ter, como preocupação, constituir-se na expressão do real, que deve ser compreendida como característica do procedimento científico, podendo ser aplicadas na resolução de problemas das diversas áreas de atuação do homem (Pardo e Colnago, 2011).
Apesar dessa missão, ainda existem diversas discussões em torno da efetividade das atividades universitárias, sobre a qualidade do ensino universitário e básico, no que diz respeito à centralização e burocratização dos processos de gestão educacional, falta de colaboração prática entre as instituições de ensino e pesquisa, falta de retorno das pesquisas desenvolvidas pela universidade e descontinuidade das ações (Tauche e Devechi, 2016).
Dessa forma, existe uma crítica à separação entre teoria e prática, projetando a universidade como locus da primeira e a escola, da segunda. Há uma falta de sentido que acompanha os estudos universitários, em que a teoria parece descolada da relação cotidiana com o mundo, e o não reconhecimento de que a prática é sempre encharcada de saberes (Habermas, 2004).
Em muitos casos, a articulação entre universidade e escola (ensino básico) só é consolidada através da presença de um sujeito mediador que transita pelos dois contextos educativos, ou seja, que possui legitimidade junto aos pares na escola e consegue articular suas demandas com as atividades que são promovidas pela universidade (Tauchen e Devechi, 2016).
Com relação ao ensino de Química para o Ensino Médio, esse sujeito mediador precisa ter conhecimento e vivência de temas interdisciplinares, enfatizando a exploração de conceitos químicos, a partir do cotidiano dos alunos. Além disso, segundo os PCNs, através de experimentação na escola, devem ser desenvolvidas habilidades cognitivas, tais como controle de variáveis, tradução da informação de uma forma de comunicação para outra (gráficos, tabelas e equações químicas), elaboração de estratégia para resolução de problemas, tomada de decisão baseada em análises de dados e valores, respeito às ideias dos colegas e colaboração no trabalho coletivo (Brasil, 2006).
Nesta linha de pensamento, Silva, Vieira e Soares (2018), afirmam que as práticas que os alunos possam reproduzir em casa e que sejam de fácil entendimento, ou seja, que permitam colocar a mão na massa, favorecem o aprendizado com autonomia.
Diante disso, as atividades experimentais devem ser um dos ensejos para que os estudantes tenham motivação para continuarem a estudar, dando-lhes uma forma de conhecimento com base na sua desenvoltura.
A utilização de indicadores naturais de pH na aprendizagem de química, faz com que estes se revelem como um providencial recurso didático, uma vez que a interdisciplinaridade está contida, desde os procedimentos de coleta, extração, até a explicação da mudança de cor, envolvendo conceitos e procedimentos de biologia, química geral, analítica, orgânica, de produtos naturais e físico-química. A abordagem prática com indicadores naturais, oferece através destes aspectos, grande quantidade de detalhes e informações aos alunos em diferentes estágios de aprendizado. Além disso, o baixo custo dos experimentos propicia sua utilização em qualquer escola.
Indicadores Ácidos-Bases são bastante relevantes para a sociedade, meios acadêmicos, pesquisas científicas, bem como empresas. O principal objetivo é indicar se alguma substância, seja ela em estado líquido ou sólido, tem caráter alcalino ou ácido, dependendo das características físico-químicas delas. Inúmeras espécies de plantas, flores e frutas possuem substâncias em sua seiva que mudam de cor conforme o pH do meio em que estão inseridas, sugerindo que tais espécies podem atuar como indicadores ácido-base, e ser utilizadas em práticas laboratoriais nas escolas, substituindo indicadores sintéticos (Cuchinski et al., 2010; Terci e Rossi, 2001).
Diante da variedade de espécies vegetais e substâncias que apresentam essa função e da possibilidade de utilização em sala de aula, as perspectivas de trabalhos pedagógicos que podem ser desenvolvidas com a utilização de indicadores naturais em atividades didáticas representam uma importante ferramenta para fortalecer a articulação da teoria com a prática. Isso é bastante desejável por favorecer o sucesso do processo de ensino/aprendizagem, o que nem sempre é tarefa trivial, principalmente quando o tema é a Química (Terci e Rossi, 2002).
Na literatura são apresentados diversos exemplos de trabalhos que descrevem vegetais e frutas que podem ser utilizados como indicadores de pH, sendo alguns exemplos, o açaí (Damasceno et al., 2015), flores de quaresma e azaleia, casca de feijão (Soares et al., 2001), flores de hibisco (Santos et al., 2012), repolho roxo (Pereira et al., 2017) e beterraba (Cuchinski et al., 2010).
Entretanto, os estudos envolvendo pesquisas com mudanças de cores, neste caso, os indicadores, vão além da simples observação e percepção dos olhos, exigem técnicas de análises sofisticadas e de grande valor agregado, nem sempre disponível para sociedade em geral.
Desta forma, outros aspectos que são desenvolvidos nas pesquisas de pós-graduação e que também podem ser abordados no ensino médio, contemplando as orientações dos PCNs, por terem caráter interdisciplinar, são os conceitos básicos relacionados com as técnicas espectroscópicas de identificação de substâncias, como a espectroscopia de infravermelho e de ultravioleta, uma vez que estas técnicas podem ser associadas a diversos conteúdos, como por exemplo, radiação eletromagnética, ligações químicas e funções orgânicas, abrangendo química, física, biologia e matemática.
Esse tipo de abordagem permite desenvolver o enfoque em Ciência, Tecnologia e Saúde (CTS), visando a alfabetização científica e tecnológica dos cidadãos, auxiliando-os a construir conhecimentos, habilidades e valores necessários para tomar decisões responsáveis sobre questões de ciência e tecnologia (Santos & Mortimer, 2002). O enfoque CTS considera a ciência envolvida e a tecnologia aplicada concomitante com as suas implicações para a sociedade, tornando-se um importante aliado em sala de aula para a contextualização de temas científicos com os fatos do cotidiano (Lopes, 2012).
As análises instrumentais e sua interpretação em sala de aula, como por exemplo as espectroscopias, exigem uma investigação por parte do aluno, servindo como esfera de abstração para compreensão de características das moléculas e determinação de suas fórmulas estruturais (Lino & Silva, 2014).
Um exemplo de radiação que pode ser discutida no ensino médio, com enfoque CTS, é a infravermelha. Inserir o conceito de radiação infravermelha e interpretação de espectros durante as aulas de grupos funcionais orgânicos, exige do aluno imaginação, analogias, elaboração de modelos e senso investigativo, uma vez que cada molécula possui suas próprias frequências naturais de vibração, absorvendo ondas eletromagnéticas de frequências específicas e gerando um espectro de absorção característico. Além disso, segundo Leite & Prado (2012), a partir da espectroscopia de infravermelho, outros temas podem ser discutidos, como ciência forense, raios X, forças e polaridade das ligações e estrutura da matéria.
A radiação ultravioleta é outro tema que pode ser discutido no ensino médio, permitindo a realização de debates acerca de diversos eixos, como exposição à radiação e uso de protetores solares. Nesse contexto, Lopes (2012) fez um estudo através de espectroscopia de ultravioleta, abordando a discussão acerca de radiações solares e fotoprotetores em sala de aula, trazendo conceitos de radiação ultravioleta e sua subdivisão, além da existência de protetores solares sintéticos e naturais, que podem ser identificados pela presença de grupos cromóforos em sua estrutura.
Conforme o exposto, a arte de aprender e ensinar química é um processo que necessita da imaginação e da capacidade de interpretação da linguagem química, para entender os conceitos e os processos químicos. Entretanto, essas características nem sempre são atingidas durante o processo de aprendizagem, sobretudo, quando não se tem a mobilização de ambas as partes envolvidas, nem o desejo de ensinar e aprender (Francisco et al., 2020).
Diante disso, esse trabalho tem como objetivo discorrer sobre a associação entre a pós-graduação e o ensino médio, através do desenvolvimento de metodologias de ensino voltadas para aprendizagem significativa e experimentação investigativa, com enfoque CTS.
Metodologia
O método empregado nesta pesquisa foi o qualitativo, pois "a abordagem qualitativa parte do princípio de que há uma relação dinâmica entre o mundo real e o sujeito, uma interdependência viva entre o sujeito e o objeto, um vínculo indissociável entre o mundo objetivo e a subjetividade do sujeito" (Chizzotti, 1991, p. 79).
Os procedimentos de investigação que nortearam a temática da pesquisa situaram-se na metodologia do estudo de caso. Segundo André (1998), utiliza-se o estudo de caso quando se procura encontrar novas definições sobre um determinado fenômeno. Os dados da pesquisa foram coletados por meio da aplicação de questionários englobando todo o universo de estudo, ou seja, turmas do curso técnico integrado em edificações, da rede pública de ensino.
No presente estudo foram abordados aplicação da emodina como indicador ácido base, em aula prática, assim como, a utilização do espectro de ultravioleta da emodina para discussão de espectroscopia e atividade fotoprotetora, e o uso do espectro de infravermelho dessa substância, para identificação de grupos funcionais orgânicos, em sala de aula.
• Aplicação da emodina como indicador ácido base
Inicialmente, foi realizado estudo fitoquímico com Chamaecrista sp., tendo como um dos resultados, a extração da emodina, durante o curso de doutorado em farmacoquímica.
Após isolamento e caracterização da substância, percebeu-se que, por se tratar de uma antraquinona, essa substância poderia apresentar propriedades como indicador de pH (Cunha, 2009). Dessa forma, a substância foi colocada em contato com soluções de pH 1 a 14, a fim de observar a variação de coloração. Após observar a variação na coloração, esta então aplicada como indicador ácido-base em sala de aula.
Depois de ministrar aula teórica sobre funções inorgânicas (ácido e base), para 80 alunos do primeiro ano, do curso técnico integrado em Edificações, foi realizada a aula prática sobre indicadores ácido-base naturais, utilizando a solução etanólica da emodina. Para essa aula, foram utilizados copos descartáveis, vidros de penicilina e soluções encontrados no dia-a-dia, como: vinagre, ácido muriático (produto utilizado para a limpeza de superfícies duras e difíceis de limpar) e solução de soda cáustica (produto utilizado para desobstrução de encanamentos), preparada previamente pela professora. Para realização dos testes, foram misturados 5 mL de solução com 1 mL de indicador.
Além disso, por se tratar de uma turma de curso técnico integrado em Edificações, foi realizada também a identificação do caráter ácido-básico do cimento e da cal comercial. Para isso, 3 g das amostras (cimento e cal) foram misturadas a 30 mL de água destilada, separadamente, sendo retirados os sobrenadantes, com ajuda de uma pipeta, e colocados em contato com a solução de emodina (Lobato et al., 2018).
Após a realização da aula prática, foi aplicado um questionário com o objetivo de obter a opinião dos alunos acerca da metodologia utilizada. Este documento continha as seguintes perguntas:
-
Avalie a Prática de Ensino
( ) Ótima ( ) Boa ( ) Ruim
-
Ela ilustra bem a parte teórica envolvida?
( ) Sim ( ) Não
-
Você consegue relacionar o que aprendeu pela prática com o que vive em seu cotidiano
( ) Sim ( ) Não
-
Avalie a parceria entre Aula Teórica e Aula Prática
( ) Excelente ( ) Ótima ( ) Satisfatória ( ) Ruim
-
Antes da aula sobre ácidos e bases, você sabia que algumas plantas contêm indicadores naturais de acidez e basicidade?
( ) Sim ( ) Não
• Utilização da emodina para discussão de espectroscopia de ultravioleta e atividade fotoprotetora em sala de aula
Após aula sobre radiação eletromagnética, foi trabalhado o tema protetores solares, com esses mesmo alunos, temática bastante pertinente, uma vez que os alunos se encontram no sertão da Paraíba, nordeste brasileiro, região com clima muito quente e com muita exposição a raios solares.
Durante essa aula, foram discutidos espectros de ultravioleta de produtos naturais e sintéticos, que apresentam atividade fotoprotetora, mostrando as regiões do Ultravioleta (UVA, UVB ou UVC), bem como os efeitos que a exposição à radiação causa ao ser humano. Como forma de avaliação, foi utilizado o espectro de ultravioleta da substância isolada, para que os alunos identificassem as regiões em que ela absorve com maior intensidade e se ela poderia ter atividade fotoprotetora.
• Utilização da emodina para discussão de espectroscopia de infravermelho em sala de aula
Com duas turmas do terceiro ano (30 alunos, em cada turma), desse mesmo curso, foi discutido o espectro de infravermelho da substância em questão. Essa discussão foi realizada após aula teórica sobre funções orgânicas, objetivando apresentar métodos de identificação de substâncias orgânicas, mais especificamente, de grupos funcionais.
Para avaliar a assimilação do conteúdo, foi realizado um teste, no qual os alunos deviam analisar os grupos funcionais da emodina, identificar as bandas características e dizer qual dos dois espectros correspondiam a ela. Para isso, foi disponibilizado um material contendo os espectros de infravermelho, a fórmula estrutural da emodina e uma tabela com os principais grupos funcionais e suas regiões de absorção no infravermelho (Quadro 1).
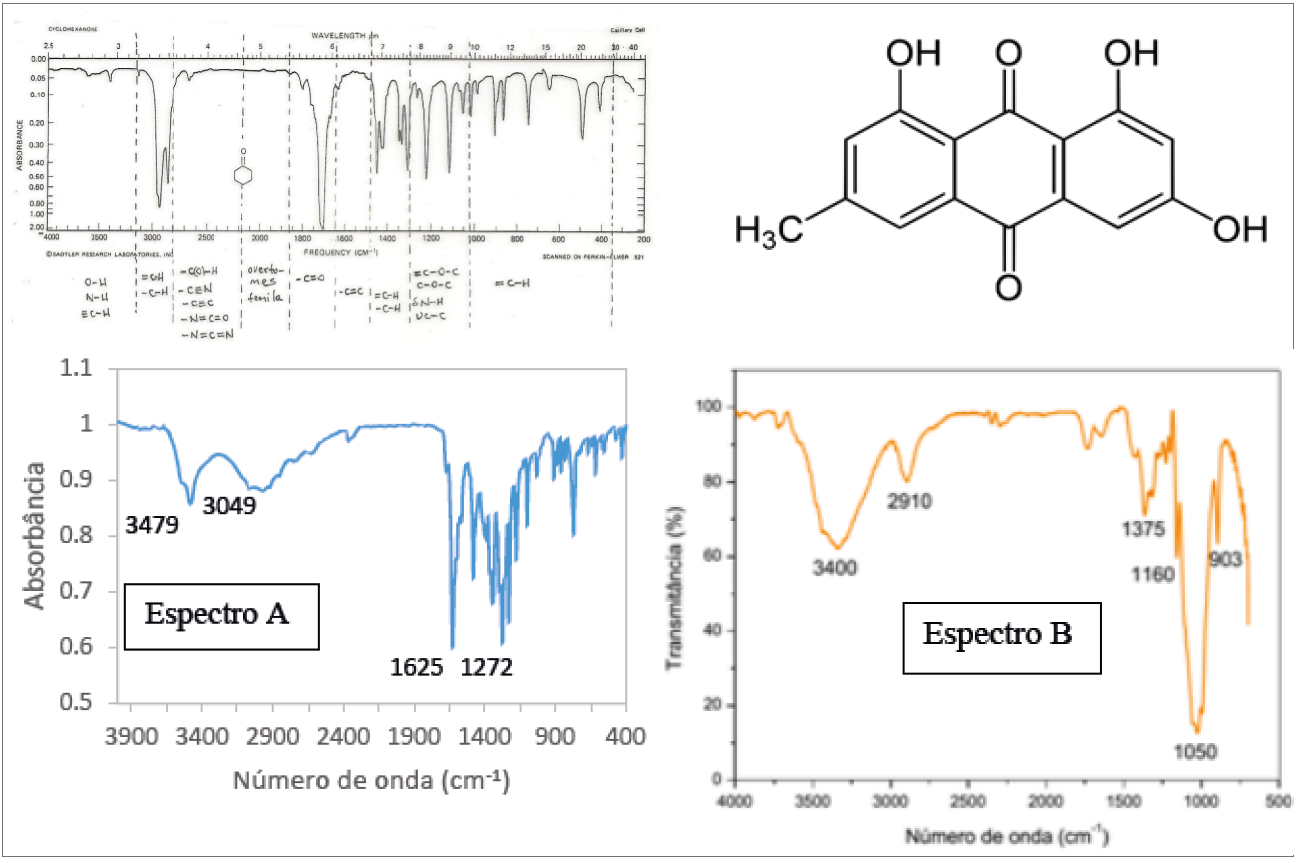
Quadro 1 Teste realizado com os alunos do terceiro ano, sobre espectroscopia de infravermelho. Espectro A: fonte: Própria. Espectro B: fonte: Andrade et al. 2014
Resultados e Discussões
• Obtenção e aplicação da emodina como indicador ácido base
Os dados de RMN 1H e 13C e de infravermelho, da substância isolada, e sua comparação com a literatura (Chu, Sun e Liu, 2005), permitiram identificá-la como sendo a l,6,8-trihidroxi-3-metil-9,10-antraquinona, mais conhecida como emodina (Figura 1), isolada pela primeira vez no gênero Chamaecrista.
Ao colocar 1 mL da emodina em contato com soluções de pH 1 a 14, foram observadas as seguintes colorações: amarelo, para pH de 1 a 9, e rosa, para pH de 10 a 14. Segundo Nguyen e colaboradores (2008), a desprotonação da emodina para sua base conjugada devido ao pH básico, causa uma mudança de coloração. Essa mesma informação é dada no trabalho de Pal et al (1993), no qual menciona-se que em pH alcalino, essa molécula é solúvel em água, apresentando uma mudança de cor de amarelo para vermelho. Apesar dos relatos sobre a mudança de cor da emodina, de acordo com o pH do meio, não há trabalhos sobre sua utilização para fins didáticos.
A Figura 2 apresenta a coloração da solução de emodina e as variação observadas ao colocá-la em contato com amostras de ácido muriático, soda cáustica e vinagre, mostrando uma coloração, amarela para o vinagre e ácido muriático, indicando caráter ácido, e coloração rosa para soda cáustica, indicando seu caráter básico. Esses resultados estão de acordo com a composição das amostras, uma vez que o ácido muriático é composto de ácido clorídrico, o vinagre é composto de ácido acético.

Figura 2 Coloração da solução concentrada de emodina (a) e as variação observadas ao colocá-la em contato com amostras de ácido muriático (b), vinagre (c) e soda cáustica (d). Fonte própria.
A figura 3 mostra os sobrenadantes da cal (a) e do cimento (c), além de mostrá-los em contato com a solução de emodina (b e d), indicando o caráter básico de ambos os materiais. Estes resultados estão de acordo com a composição desses materiais, uma vez que, e o cimento tem alcalinidade alta devida a presença de cal livre e reações de hidratação de silicatos (Senff et al., 2005), e a cal é composta de óxido de cálcio (óxido básico). A utilização desses materiais permitiu contextualizar ainda mais a prática, uma vez que estes são bastante encontrados no campo de trabalho dos futuros técnicos de edificações.

Figura 3 Sobrenadante da cal sem indicador (a) e com indicador (b); sobrenadante o cimento sem indicador (c) e com indicador (d). Fonte própria.
A realização dessa prática, utilizando indicador natural de pH e materiais encontrados no cotidiano (Figura 4), permite inferir que os professores precisam desmistificar a ideia dos alunos de que as aulas experimentais ocorrem somente em laboratórios futuristas, superequipados e de alta tecnologia, e mostrar aos pesquisadores a necessidade de buscar a aplicação de seus resultados para a sociedade, ajudando a associar teoria e prática.
Esse resultado está de acordo com Lima e Alves (2016), quando afirmam que apesar das estruturas físicas e organizacionais das instituições de ensino terem influências múltiplas no processo de ensino e aprendizagem da experimentação, o professor, mesmo sem ter o laboratório em sua escola, pode utilizar recursos que são acessíveis aos alunos para preparar aulas experimentais, com os materiais alternativos, sendo possível realizar os experimentos na própria sala de aula, envolvendo a participação efetiva dos alunos.
A aceitação da metodologia aplicada nessa aula foi observada ao analisar o questionário respondido pelos alunos, uma vez que mais de noventa por cento dos alunos avaliou a prática realizada e a parceria entre aula teórica e prática, como ótimas (Perguntas 1 e 4), considerando que esta ilustrou bem o conteúdo teórico (Pergunta 2), conseguindo relacionar o conhecimento adquirido com o cotidiano (Pergunta 3). Tais respostas também nos permite inferir que os alunos atribuem uma importância significativa à aprendizagem por aulas experimentais, principalmente, quando elas são contextualizadas, levando a uma maior compreensão de situações do cotidiano e da matéria.
Essa avaliação também foi realizada no trabalho de Silva e colaboradores (2018), que trata de atividades experimentais com indicadores no ensino da EJA, mostrando que a maior parte dos alunos classificaram as aulas práticas como interessantes e destacaram que essa é uma ferramenta que lhes auxiliam nas compreensões dos diferentes conteúdos de química trabalhados em sala. Lucas e colaboradores (2013) também realizaram trabalho com extrato de beterraba, como indicador natural de pH, utilizando-o como material instrucional para ensino de química, observando após questionário, que as aulas teórica e prática, ministradas concomitantemente, ajudam na assimilação de teoria, além de despertar a curiosidade e interesse. Sugerindo que esta metodologia de ensino deva ser aplicada sempre que possível, independentemente de ser ensino fundamental, médio ou superior, uma vez que estimula a participação mais ativa dos estudantes.
Através do questionário, também foi possível observar que apenas dezoito por cento dos alunos afirmaram que não sabiam que as plantas contêm indicadores naturais de pH, antes da realização da aula sobre ácido-base (Pergunta 4). Essa afirmativa pode estar relacionada ao fato de que o uso de corantes naturais, tanto no ensino médio como no superior, tem sido proposto frequentemente, uma vez que é considerado uma ferramenta para despertar o interesse dos estudantes para o conteúdo abordado (Lucas et al., 2013). Exemplos de alguns trabalhos nesse tema são: O uso de indicadores naturais para abordar a experimentação investigativa problematizadora em aulas de Química (Pereira et al., 2017); Coleção de propostas utilizando produtos naturais para a introdução ao tema ácido-base no Ensino Médio (Parte I) (Martins et al., 2017); e Uma Abordagem das Atividades Experimentais no Ensino de Química: Uso da Flor Ixorachinensi como Indicador Ácido-Base (Guerra et al., 2018).
Diante disso, o emprego da cor das substâncias como tema motivador proporcionou uma boa participação dos alunos durante a aula, os quais demonstraram interesse e curiosidade, corroborando com o trabalho de Leite (2018), ao afirmar que a experimentação em sala de aula pode favorecer a compreensão de um problema relacionado ao cotidiano do aluno, permitindo ao estudante se familiarizar com o processo científico, adquirindo uma percepção diferenciada do "fazer ciência". Além disso, as atividades experimentais contribuíram para problematizar entendimentos acerca da natureza da ciência, provocando reflexões e discussões a partir dos conhecimentos científicos.
• Utilização da emodina para discussão de espectroscopia de ultravioleta e atividade fotoprotetora em sala de aula
No espectro de ultravioleta da emodina é possível observar que esta apresenta grande absorção na região de UVC (100-280 nm) e UVB (280-320 nm) (Figura 5), sendo um potencial fotoprotetor de acordo com a região em que absorve. Na discussão desse espectro pelos alunos, foi observado que eles conseguiram compreender as regiões do ultravioleta e identificá-las no espectro, além de inferir que a emodina apresenta atividade fotoprotetora, como pode ser observado nas respostas abaixo.

Figura 5 Espectro de ultravioleta da emodina, identificando as regiões de UVA, UVB e UVC. Fonte própria.
Aluno 1: " A emodina pode ser utilizada como protetor solar, porque absorve radiação UVC e UVB".
Aluno 2: "A substância tem atividade fotoprotetora porque tem bandas altas na região de UVC e UVB".
Dessa forma, foi possível discutir sobre radiação solar, seus efeitos benéficos e maléficos ao corpo humano e a importância do uso de fotoprotetores, através de um enfoque CTS e seguindo as Orientações Curriculares Nacionais para o Ensino Médio (BRASIL, 2006), uma vez que o processo ocorreu de maneira interdisciplinar e contextualizada, contribuindo para formação de um cidadão mais crítico e consciente cientificamente (Santos, 2007).
• Utilização da emodina para discussão de espectroscopia de infravermelho em sala de aula
Na discussão do espectro de infravermelho, foi observado que os alunos compreenderam a técnica, conseguindo associar os grupos funcionais presentes na emodina (cetona, fenol, aromático), com as bandas de absorção do espectro (C=O, C-O, O-H, =C-H), como pode ser observado na resposta abaixo, de um aluno:
"Pode ser representada pelo espectro A, que apresenta uma banda longa por volta de 3000 cm-1 , relacionada ao OH, e também uma banda na faixa dos 1800 cm-1 , que representa C=0".
A introdução de conceitos básicos de técnicas espectroscópicas de identificação de substâncias, utilizadas em pesquisas científicas, fazendo uso de linguagem acessível ao nível dos alunos, possibilitou a revisão sobre os conceitos de radiação eletromagnética, geralmente abordados na disciplina de Física, e relacionar as funções orgânicas presentes na emodina com as frequências de vibração no infravermelho, desenvolvendo nos alunos capacidade de abstração, através de uma aprendizagem significativa, com enfoque CTS.
Lino e Silva (2014) ao utilizarem essa mesma metodologia em sala de aula, também perceberam que é possível utilizar técnicas instrumentais mais complexas como motivadoras de aprendizagem, despertando interesse e curiosidade nos alunos, afirmando que nem sempre, assuntos considerados específicos ou avançados devem ser evitados em sala de aula, uma vez que todo conhecimento é válido, não importando qual o nível de seriação dos estudantes.
Diante disso, percebe-se que é possível trabalhar algumas técnicas instrumentais mais complexas, encontradas em alguns laboratórios de química e utilizá-las como ferramentas motivadoras de aprendizagem, despertando interesse e curiosidade nos alunos.
• Normas de segurança discutidas durante a aula experimental
Tendo em vista que o ácido muriático (HCl) e a soda cáustica (NaOH) podem causar queimaduras graves na pele, nos olhos e nas mucosas, foram preparadas previamente soluções diluídas, pela professora, e os estudantes foram orientados a utilizar equipamentos de proteção adequados, como luvas, máscara, jaleco e óculos de proteção.
Conclusões
A interação entre pós-graduação e ensino básico, através de uma substancia utilizada como recurso didático, obtido durante o desenvolvimento de uma tese de doutorado, se mostrou bastante interessante e importante, pois possibilitou a realização de aulas práticas e teóricas em uma escola que ainda não contava com laboratório, reagentes e/ou vidrarias. Além disso, permitiu discutir sobre um conteúdo pouco abordado no ensino médio, como radiação de infravermelho e ultravioleta, incentivando os discentes a buscarem dominar linguagem científicas e relacionar as informações codificadas com desenhos de estruturas orgânicas.
Ao mesmo tempo, aplicação da emodina em aulas para ensino básico, abriu novas perspectivas para os cursos e alunos de graduação e pós-graduação, que trabalham com fitoquímica, uma vez que, não raramente, as substâncias isoladas durante esse período são esquecidas na bancada, por não apresentarem atividades desejadas na pesquisa inicial, podendo tais produtos somar-se como ferramentas didáticas.
Com o desenvolvimento da atividade, os alunos identificaram substâncias ácidas e básicas presentes no dia-a-dia, aprenderam que existem substâncias naturais que indicam o caráter ácido ou básico de amostras e tiveram acesso a novos conhecimentos sobre métodos de caracterização de compostos orgânicos, mais especificamente, espectroscopia de infravermelho e ultravioleta, conteúdo raramente abordado no ensino médio, sendo incentivados a desenvolver interesse pela pesquisa e criando um ciclo de ensino-aprendizagem.











 nueva página del texto (beta)
nueva página del texto (beta)