Introducción
La mineralización de la materia orgánica es un factor de suma importancia en el mantenimiento de la fertilidad de los suelos, a través de este proceso se reciclan los nutrimentos y se puede conocer la disponibilidad nutrimental en el suelo, para hacer más eficiente el uso de fertilizantes y abonos orgánicos (Havlin et al., 1999; Jarvis et al., 1996). La mayoría de los estudios de mineralización de materiales orgánicos se ha enfocado a nitrógeno, incluso se han desarrollado índices de este nutrimento de enorme utilidad para evaluar las pérdidas en sistemas intensivos para la producción de forraje en México (Figueroa et al., 2011). Estudios recientes en diferentes tipos de suelo han concluido que la textura del suelo afecta la mineralización de nitrógeno, aunque los patrones estacionales tienen mayor efecto en esta, por los cambios de temperatura (Watts et al., 2010). Las compilaciones de información reciente sobre las tasas de mineralización de materia orgánica, en zonas áridas, se han enfocado al estudio del nitrógeno (Celaya y Castellanos, 2011), así como, a los estudios de mineralización con el método de resinas sintéticas en experimentos de campo, donde a los suelos se les ha añadido estiércol bovino lechero (Flores et al., 2008) y biosólidos generados en plantas de tratamiento de aguas negras, con sistemas de tipo primario avanzado (Flores et al., 2007).
Por lo anterior, ha sido menor la atención dedicada a otros nutrimentos de importancia económica como el fósforo, principalmente en suelos agrícolas. Además, han sido escasos los estudios para sistemas de producción donde se utilizan aguas negras o residuales. Tal es el caso de las áreas agrícolas del Valle de Juárez, Chihuahua, que se han irrigado con aguas negras desde hace 30 años, donde la actividad lechera ha sido común, así como la utilización del estiércol bovino como abono orgánico, se producen 138 mil toneladas de éste al año (peso húmedo), 34 kg de estiércol producido por día (Flores, et al., 2008). El problema radica en que los productores aplican el estiércol sin conocimiento de la dosis, las características químicas y de humedad de éste, ni de las condiciones físicas y químicas del suelo, por lo que se ha incrementado la salinización de los suelos en el citado valle. También, existen otros factores, como el deficiente sistema de drenes o el uso de agua salina de pozos mezclada con aguas negras o residuales, entre otros (Flores et al., 2009; Flores et al., 2008).
La excesiva aportación de fósforo proveniente de las aguas residuales y estiércoles puede causar problemas de toxicidad y reducir la disponibilidad de otros nutrimentos para las plantas; además, el agua de drenaje de los suelos agrícolas se transfiere a los cuerpos de agua, donde puede causar eutroficación y serios problemas cuando se utiliza para la recreación, la pesca o para beber (Correll, 1998). Esto puede pasar en el Valle de Juárez porque el agua de drenaje agrícola y las aguas residuales de Ciudad Juárez llegan al Río Bravo (Olivas et al., 2011). También el exceso de fósforo puede contaminar los acuíferos a través de infiltraciones (Koopmans et al., 2007).
La textura del suelo y el tipo de drenaje influyen en las pérdidas de fósforo por lixiviación en las aguas superficiales, asimismo, la mineralización de la materia orgánica o formas minerales fácilmente solubles son posibles vías de pérdidas de fósforo de suelos agrícolas. Suelos arenosos con producción animal intensiva y alta aplicación de estiércol presentan acumulación de P en el perfil del suelo, con su subsecuente lixiviado a mantos acuíferos (Chardon y Schoumans, 2007; Salas et al., 2003). Dado que la respiración del suelo es buen indicador de la fertilidad y actividad microbiana del suelo, Haney et al. (2008) evaluaron un método basado en la liberación de CO2, concluyeron que el método con gel de solvita y análisis de CO2 podría dar buena información de la actividad microbiana y mineralización de N y P, en suelos tratados con composta de estiércol proveniente de ganado lechero. Estos autores encontraron una correlación entre el CO2 liberado y el N y el P mineralizados, después de 28 días de incubación, al utilizar dosis de 0 a 80 Mg ha-1. La mineralización de N y P varió entre 0 y 30 mg kg-1.
Las aplicaciones continuas de estiércol y fertilizante inorgánico pueden resultar en el enriquecimiento del suelo y en el riesgo ambiental asociado a las concentraciones de fósforo que pueden ser mayores a 60 mg kg-1 (Castellanos et al., 2000). Dao y Cavigelli (2003), mencionan que el fósforo tiene la particularidad de que permanece en el suelo, a diferencia del carbono, que se pierde por respiración microbiana y el nitrógeno que se volatiliza o se lixivia. Las variaciones en la composición química de fósforo y la falta de certidumbre en la predicción de liberación de nutrientes de estiércoles y compost todavía dificultan la predicción de tasas de descomposición y tamaños de reservas, sin utilizar incubaciones de laboratorio de largo plazo (Kalbasi y Karthikeyan, 2004). Dada la necesidad de realizar estudios sobre las aportaciones de fósforo al agua residual y de la eficiencia de las aplicaciones de estiércoles en suelos agrícolas con diferente textura, se llevó a cabo el presente estudio para evaluar la cantidad de fósforo mineralizado y nitrógeno total proveniente de estiércol bovino, en tres tipos de suelo y con dos calidades de agua de riego, en condiciones de campo.
Materiales y métodos
El experimento se estableció en un predio utilizado para la propagación de plantas y elaboración de compost, junto al edificio Q del Instituto de Ciencias Biomédicas (ICB) de la Universidad Autónoma de Ciudad Juárez (UACJ), localizado a 31o 44’ 45.53” N y 106o 26’ 33.24” O (www.google.earth). El estudio se realizó de marzo a septiembre de 2010, durante el ciclo agrícola primavera-verano, el de mayor actividad en el Valle de Juárez, Chihuahua. Los factores en estudio fueron 1) tres tipos de suelo Fluvisoles de las Series Caseta (arcilloso) y Juárez (franco y franco-arenoso), los cuales fueron formados por aluvión en las planicies sujetas a inundación por el río Bravo y por arroyos en terrazas bajas (CIEPS, 1970). La clasificación US-Taxonomy los indica como fine-silty, mixed, calcareous, thermic typic torrifluvents (USDA, 1980); 2) la calidad de agua de riego, con dos tipos: residual del canal de descarga en las plantas de tratamiento de aguas negras y potable de la llave, esta última para representar el riego con agua del río Bravo o de pozos que son comunes en la región; 3) el estiércol aplicado, con dos niveles: 0 y 50 Mg ha-1, con base en peso seco. El diseño experimental fue completamente al azar, factorial con 12 tratamientos (Cuadro 1). El ensayo tuvo cuatro repeticiones, lo que dio un total de 48 unidades experimentales, consistentes en cilindros de aluminio de 5 cm de diámetro y 15 cm de largo (Figura 1). Los cilindros se llenaron, conforme a cada tratamiento, con suelo, estiércol y agua de riego. En cada cilindro se agregaron entre 270 y 300 g de suelo (dependiendo de la textura), la dosis de estiércol indicada y 100 mL de agua dependiendo del tipo riego.
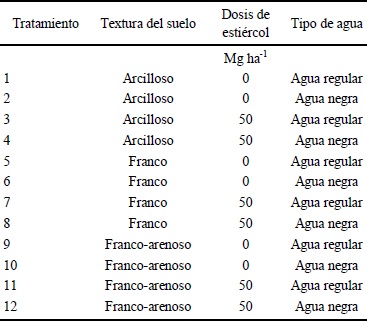
Cuadro 1 Tratamientos evaluados que incluyen el tipo de suelo, dosis de estiércol y tipo agua de riego

Figura 1 Unidades experimentales representadas por cada cilindro de aluminio de 15 cm de altura y 5 cm de diámetro.
Los cilindros se marcaron con tinta permanente y se colocaron en el suelo, en orificios separados a 10 cm. Durante el estudio se agregó agua a los cilindros, para mantener la humedad del suelo lo más cercano a la capacidad de campo y favorecer la actividad microbiana, aunque los tratamientos con textura arenosa presentaron menor humedad durante el estudio. El análisis granulométrico del suelo se realizó mediante la técnica del hidrómetro de Bouyoucos (Bouyoucos, 1962; Day, 1965). El análisis de nitrógeno inorgánico (NH4 + NO3) del suelo fue mediante extracción con KCl 2 N, óxido de magnesio para determinar el NH4 y aleación de Devarda para NO3, en ambos casos se tituló con ácido sulfúrico (Mulvaney, 1996). El nitrógeno total Kjeldahl (NTK) del suelo y del estiércol se determinaron mediante digestión ácida (Bremner, 1996) y la materia orgánica del suelo con el método de Walkley y Black (Nelson y Sommers, 1996). El pH y la conductividad eléctrica del suelo se determinaron con un electrodo Pinchale Corning 530 y un conductivímetro Orion 3 Star, respectivamente (Rhoades, 1996).
El fósforo inorgánico del suelo se determinó con el método Olsen, con un espectrofotómetro Genesys 20 (Olsen y Sommers, 1982). El análisis de estiércol consistió en preparar una pasta de saturación, de la cual se obtuvo un extracto para determinar N inorgánico (Mulvaney, 1996), fósforo soluble, con un espectrofotómetro (Olsen y Sommers, 1982), pH y conductividad eléctrica, determinados directamente en el extracto (Rhoades, 1996). A los datos generados se les realizó un análisis de varianza para un diseño completamente al azar con arreglo factorial 3 × 2 × 2, la separación de promedios se realizó mediante la técnica de comparación múltiple de la diferencia mínima significativa (DMS), así como análisis de correlación y regresión lineal simple entre fósforo Olsen, NTK, humedad del suelo y densidad aparente. Todos los análisis estadísticos se realizaron con el paquete computacional SPSS versión 17 (Acton y Miller, 2009).
Resultados y discusión
Caracterización de los Suelos, Estiércol y Agua
Los suelos analizados acorde a su pH se clasificaron como medianamente alcalinos. Los suelos arenoso y arcilloso presentaron bajos niveles de salinidad, mientras que el suelo franco presentó más de 4 dS m-1 (Cuadro 2), lo que indica que fue un suelo salino (Aceves, 2011). El N inorgánico fue muy bajo en el suelo franco-arenoso, bajo en el suelo arcilloso y medio en el suelo de textura franco (Castellanos et al., 2000) (Cuadro 2). Con respecto a P Olsen, el suelo franco-arenoso fue bajo y los otros suelos muy altos, ya que concentraciones superiores a 11 mg kg-1 son suficientes para abastecer la demanda de cultivos como trigo y algodón (Havlin et al., 1999). En cuanto a materia orgánica y nitrógeno total resultaron bajos los tres suelos (Castellanos et al., 2000), pero el franco-arenoso está cercano a la clasificación de muy bajo en estas variables. Esta información refleja que se cubrió buena parte de la variabilidad edáfica al incluir las tres series de suelo más importantes que existen en el Valle de Juárez (CIEP, 1970), lo cual conlleva a la utilidad de la información generada para los sistemas de producción regional.
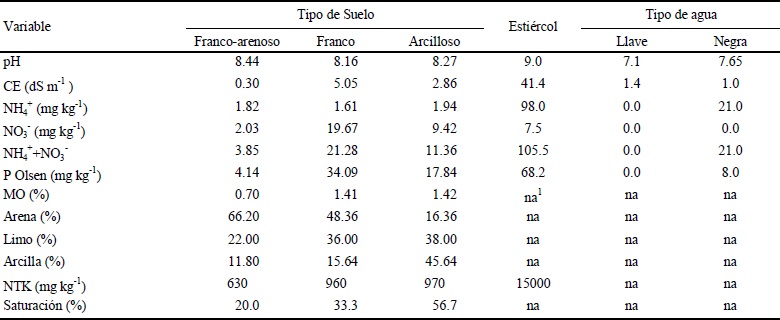
1 na = no analizado.
Cuadro 2 Características químicas y físicas de los suelos, y química del estiércol y agua de riego.
El estiércol presentó pH alcalino, conductividad eléctrica fuertemente salina, el contenido de N-NH+ 4 fue alto en comparación con N-NO-, y alto en P Olsen (Cuadro 2). El pH del agua de riego de la llave fue neutro y el del agua residual fue ligeramente alcalina, ambas fuentes de riego fueron no salinas (Aceves, 2011).
Caracterización de los Diferentes Tratamientos
La temperatura del suelo en los cilindros de incubación varió poco entre las texturas de suelo, por ello se decidió reportar solo un registro por fecha, lo cual en promedio fue 31.6 oC y un intervalo de 19.5 a 45.9 oC durante marzo a septiembre de 2010 (Figura 2). Estas temperaturas favorecen la actividad microbiana y la mineralización de materia orgánica, ya que las condiciones óptimas para una mineralización adecuada son de 30 a 35 oC de temperatura del suelo, entre -33 a -10 kPa de potencial de agua del suelo, pH entre 6 a 8 y textura de suelo franco (Cassman y Munns, 1980; Jarvis et al., 1996; Flores et al., 2008).

Figura 2 Temperatura del suelo registrada en los cilindros durante el periodo experimental de marzo a septiembre de 2010.
La aplicación de estiércol (50 Mg ha-1) causó una disminución significativa de la densidad aparente en las tres texturas de 0.06 g cm-3, después de 206 días de incubación en campo, lo cual puede atribuirse que al agregar materia orgánica al suelo aumentó el espacio poroso y, por ende, disminuyó el peso del suelo en el cilindro. El rango de densidad aparente para todas las unidades experimentales observada en este estudio fue de 1.47 g cm-3 para el tratamiento de suelo franco- arenoso sin estiércol y 1.148 g cm-3 para el suelo arcilloso con 50 Mg ha-1 de estiércol, este resultado coincide con lo indicado por Brady y Weil (1996), que afirman que la aplicación de estiércol promueve mayor porosidad del suelo y mejora la actividad microbiana al permitir mayor flujo de agua, aire y nutrientes.
El tipo de suelo causó un efecto altamente significativo en las variables fósforo, nitrógeno total, CE, pH y humedad del suelo (P < 0.01), al igual que el estiércol (con excepción del pH) el tipo de agua de riego utilizada significó diferencias altamente significativas entre tratamientos para la variable CE del suelo, mientras que la interacción agua × estiércol registró efecto significativo para el pH del suelo (Cuadro 3).
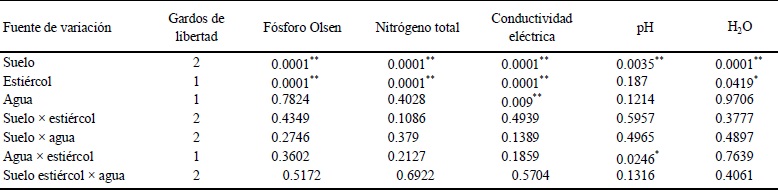
Nivel de significancia observado = Pr > F: *, **, prueba de F significativa al 0.05 y 0.01 nivel de probabilidad, respectivamente; H2O = porcentaje de humedad en el suelo al final del experimento.
Cuadro 3 Probabilidad de error (P) para las variables fósforo, nitrógeno total, conductividad eléctrica, pH y humedad del suelo.
Las variables densidad aparente, humedad del suelo final, CE, NT y P Olsen resultaron estadísticamente diferentes entre los tres tipos de suelos, como efecto fijo de este factor en estudio, a todos los niveles de los otros factores: tipo de agua y dosis de estiércol (Cuadro 4). De esta forma, la concentración promedio de P Olsen fue mayor estadísticamente para el suelo de textura franco seguido del suelo arcilloso, esto atribuido a una mayor actividad microbiana en el suelo franco, lo cual produjo mayor mineralización de fósforo, en cambio el suelo franco-arenoso fue el que menor cantidad de fósforo mineralizado presentó, ya que su textura no permitió una mayor actividad microbiana debido a la baja presencia de bacterias y retención de humedad por el menor espacio poroso que presenta este suelo (Jarvis et al., 1996).
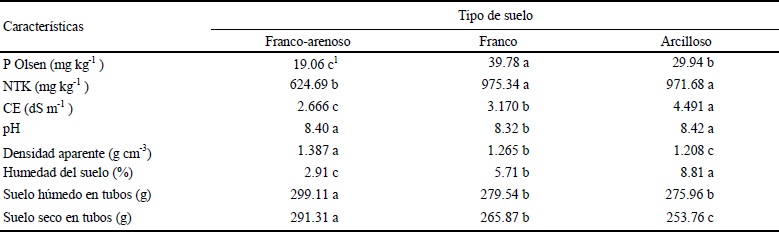
1 Medias seguidas por la misma letra son estadísticamente iguales a un nivel de significancia de 0.05. NTK = nitrógeno total Kjeldahl; CE = conductividad eléctrica.
Cuadro 4 Características físicas y químicas de los diferentes suelos al final del experimento.
El suelo franco-arenoso mostró la concentración de NT significativamente menor, mientras que entre los otros suelos no hubo diferencia significativa (Cuadro 4). El pH varió poco y fue significativamente menor en el suelo franco, mientras que la CE fue mayor en el suelo arcilloso y menor en el franco-arenoso.
La adición de estiércol y la dosis de 50 Mg ha-1, causó un aumento promedio entre suelos de 0.661 dS m-1 en la conductividad eléctrica, debido a que el estiércol contiene altos niveles de sales. Así también, la humedad del suelo, al final del experimento, aumentó con la aplicación de estiércol (Cuadro 5), es decir, el estiércol conserva el agua del suelo, lo cual es benéfico para las plantas y los microorganismos del suelo, ya que necesitan humedad para realizar sus funciones metabólicas y transpiración, y a su vez puedan absorber agua y nutrientes del suelo (Jarvis et al., 1996). La concentración de fósforo aumentó 24 mg kg-1, en promedio, con la aplicación de 50 Mg ha-1 de estiércol bovino, mientras que el NTK aumentó 248 mg kg-1 en promedio con dicha dosis. En el Cuadro 5 se muestran los promedios para el efecto fijo de la dosis de estiércol para las combinaciones de niveles de tipo de agua de riego utilizado y en los tres niveles referidos como tipos de suelo en conjunto, es decir, no es un promedio directo, sino que se obtuvo del análisis del promedio de la DMS para las combinaciones con y sin estiércol.
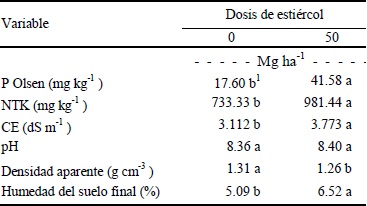
1 Medias seguidas por la misma letra son estadísticamente iguales a un nivel de significancia de 0.05. NTK = nitrógeno total Kjeldahl; CE = conductividad eléctrica.
Cuadro 5 Comparación de promedios para el factor dosis de estiércol a todos los niveles de los otros dos factores en estudio (texturas de suelo y tipo de agua) en las variables evaluadas, al final del experimento.
El tipo de agua de riego utilizada tuvo efecto significativo en la CE, al aumentar en promedio 0.41dS m-1 cuando se utilizó agua negra o residual proveniente de las plantas de tratamiento. Los promedios de las demás variables evaluadas resultaron estadísticamente iguales, es decir, que el tipo de agua de riego no afectó las concentraciones de P y NTK en los tres tipos de suelo evaluados, ya que la densidad aparente y el contenido de humedad del suelo son variables muy poco influenciadas por el tipo de agua utilizado.
El Tratamiento 8 presentó, en promedio, la mayor concentración de P Olsen, corresponde a suelo franco con estiércol (50 mg kg-1) y agua negra. Por lo que el aumento coincide con las características del suelo franco, la adición de estiércol y el tipo de agua. Mientras que el tratamiento que mostró la menor concentración fue el 10, con la combinación de suelo franco-arenoso, sin estiércol y agua negra. Los tratamientos donde se registró mayor concentración de NTK fueron el 4 y el 5, que corresponden al tipo de suelo arcilloso, con estiércol y agua de la llave y agua negra, respectivamente; mientras que el Tratamiento 9, con suelo franco-arenoso, sin estiércol y agua de la llave, fue el más bajo. El pH más alto registrado fue para los suelos arcillosos y franco-arenosos, mientras que en el que se encontró con menor pH fue el Tratamiento 5, con suelo franco, sin estiércol y agua de llave (Cuadro 6).
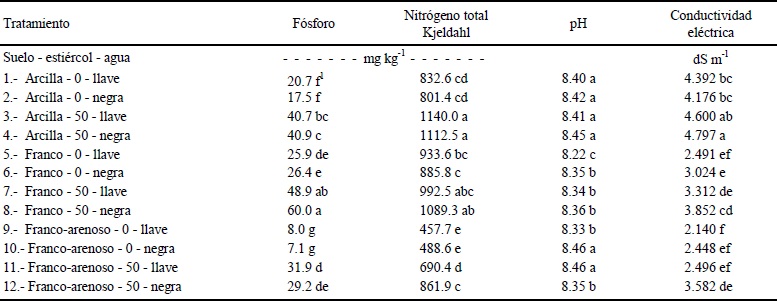
1 Medias seguidas por la misma letra son estadísticamente iguales a un nivel de significancia de 0.05.
Cuadro 6 Contenido de fósforo, nitrógeno total, pH y conductividad eléctrica de los suelos con diferente tratamiento.
La CE fue más alta en el Tratamiento 3 y 4, mientras que la más baja se presentó en el Tratamiento 9, franco- arenoso, sin estiércol y agua de llave. Las diferencias entre los suelos con y sin estiércol, en cuanto a la concentración de P Olsen, variaron de 20 a 33.6 mg kg-1, al aplicarse 50 Mg ha-1 de estiércol. El suelo arcilloso presentó una diferencia de 20 a 23.4 mg kg-1 de P, quizás la aplicación del agua negra permitió agregar P a la solución del suelo. El suelo franco mostró una diferencia mayor, de 23.1 a 33.6 mg kg-1 entre agua de la llave y agua negra, mientras que en el suelo franco-arenoso las diferencias entre el tratamiento sin estiércol y aquel con 50 Mg ha-1 fueron de 23.9 y 22.1 mg kg-1, cuando se irrigó con agua de la llave y agua residual, respectivamente. Estas concentraciones de P están en el rango de 0 a 30 mg kg-1 de P para varios suelos reportados por Haney et al. (2008). La mayor retención de humedad y capacidad de intercambio iónico en los suelos arcilloso y franco puede explicar el aumento de P Olsen mineralizado, lo cual coincide con Watts et al. (2010) quienes indican que la textura y temperatura del suelo afectan la mineralización.
Aunque el coeficiente de correlación es relativamente bajo (r2 = 0.48), en la Figura 3 se muestra que existe una tendencia de aumento en la concentración de P Olsen, a medida que se incrementa la concentración de NTK en las 48 unidades experimentales evaluadas en este estudio. Esto indica que las aportaciones de materia orgánica, a través del estiércol, en suelos de texturas extremas (arenoso a arcilloso) y manejados con calidades de agua desde de la llave a residual, reflejan un aumento notable de la fertilidad de los suelos. La Figura 4 muestra una tendencia de disminución en el contenido de humedad en el suelo, a medida que aumenta la densidad aparente de los suelos. Esto es explicable por la naturaleza de los suelos franco-arenosos que se caracterizan por retener menor humedad y presentar densidades aparentes altas (1.4 a 1.5 g cm-1). Por el contrario, los suelos arcillosos retienen mucho la humedad al tener mayor porosidad, pesan menos y tienen densidades aparentes menores (1.1 a 1.2 g cm-1), de tal manera que los suelos francos quedan intermedios en estas características físicas (Brady y Weil, 1996).

Figura 4 Correlación entre el contenido de nitrógeno total Kjeldahl y fósforo del suelo de los diferentes tratamientos.

Figura 5 Correlación entre la densidad aparente y la humedad del suelo de los diferentes tratamientos.
La cantidad de P mineralizado del estiércol fue similar entre los tipos de suelo (Cuadro 7). La adición de estiércol (50 Mg ha-1) en los tres tipos de suelo estudiados (franco-arenoso, franco y-arcilloso) causó un aumento del fósforo mineralizado en los 206 días de incubación, en condiciones de campo, en comparación con los tratamientos en los que no se agregó estiércol. El estiércol utilizado en este estudio tuvo 68.2 mg kg-1 de P Olsen. Es decir, se aplicaron 1.16 mg P por cilindro (270 g suelo en promedio) o bien, 4.29 mg kg-1, lo que correspondería (4.29 × 100 / 26.9 del suelo arcilloso) a 15.95% del fósforo inorgánico aplicado en el estiércol, el restante 84.05% fue fósforo orgánico del estiércol que se mineralizó, es decir 21.7 -4.29 = 17.41 mg P kg-1 suelo es la cantidad neta de P mineralizado.
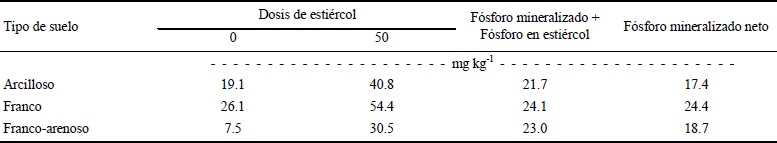
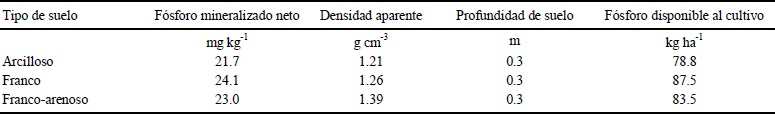
Cuadro 7 Contenido de fósforo del estiércol mineralizado en el suelo durante 206 días de incubación en campo.
A partir del P mineralizado neto que se indica en el Cuadro 7 y con el uso de la densidad aparente de cada tipo de suelo se calculó la cantidad de fósforo disponible para el cultivo (Cuadro 8). Por ejemplo, los cultivos de algodón y sorgo forrajero requieren 67 y 90 kg P ha-1 (Havlin et al., 1999) por lo que con la aplicación de 50 Mg ha-1 de estiércol se podría satisfacer la demanda de esos cultivos para los suelos del Valle de Juárez, Chihuahua. Flores et al. (2008) obtuvieron promedios de P Olsen que van desde 2.9 mg kg -1, como mínimo, hasta 60.9 mg kg-1; mientras que en la presente investigación se obtuvieron promedios de P mineralizado disponible para cultivo que van desde 78.8 mg kg-1 hasta 87.5 mg kg-1 que, de acuerdo con las demandas nutricionales de varios cultivos, se pueden considerar suelos con alto contenido en fósforo.
Conclusiones
Los resultados del estudio muestran que la aplicación de estiércol y el tipo de suelo afectan la disponibilidad de P Olsen, pero no el tipo de agua, por lo que deben considerarse en los planes de manejo de los suelos para evitar excesos de este nutriente y problemas de salinidad. Los suelos analizados en el estudio fueron de textura franco-arenoso, franco y arcillosa; medianamente alcalinos, bajos en materia orgánica y en nitrógeno total Kjeldahl y medios en N inorgánico. Los suelos franco- arenoso y arcilloso fueron bajos en salinidad, mientras que el de textura franco fue salino. La conductividad eléctrica de los suelos aumentó con la aplicación de estiércol, en promedio, de 3.11 dS m-1 a 3.77dS m-1; la humedad en el suelo mostró un aumento al final del experimento al agregar la dosis de estiércol de 50 Mg ha-1, este fue de 5.09 a 6.52% en promedio. La mayor densidad aparente fue de 1.452 g cm-3 en el suelo arenoso sin estiércol e irrigado con agua de la llave. Los niveles de P Olsen detectados en el suelo al final del experimento (206 días de incubación) fueron de 40.8, 54.4 y 30.5 mg kg-1 para los suelos arcilloso, franco y arenoso. Mientras que las concentraciones estimadas de P Olsen mineralizado neto fueron de 17.4, 24.4 y 18.7 mg kg-1 para los mismos suelos. La estimación de P disponible a las plantas fue de 78.8, 87.5 y 84.5 kg ha-1, para los suelos arcilloso, franco y arenoso.











 nueva página del texto (beta)
nueva página del texto (beta)