Introducción
La eficiencia de uso de los fertilizantes se mide por el método del balance de masas, en el cual el porcentaje de recuperación del P aplicado, se calcula por el cociente de la remoción de P por el cultivo entre el P aplicado en la fertilización (Syers et al., 2008, Fixen, 2009). Las mejores prácticas de manejo (MPM), referidas a la agricultura, son aquellas acciones aplicadas con recursos que han sido probadas con investigación con el objeto de lograr el mejor desempeño combinado de aspectos económicos, sociales y ambientales (IFA, 2009). En el caso particular de la frecuente baja o falta de respuesta de los cultivos a la aplicación de los fertilizantes fosfatados se ha tratado de resolverse por medio de tecnología agrícola e industrial. Las alternativas para resolver la falta de respuesta de los cultivos a la aplicación de P son: a) evitar en lo posible, una rápida precipitación de los fosfatos al aplicarlos por separado o combinado en complejos órgano-minerales para adecuar el pH del suelo; b) situar los fertilizantes cerca de las raíces; c) incorporar abonos verdes o estiércoles (Mansell et al., 1985, Grant y Heaney, 1997); d) favorecer una mayor tasa de su movimiento en el suelo por difusión (Cho, 1991) a través del manejo del riego y mejoramiento de la estructura del suelo con prácticas de labranza (Enfield et al., 1981a y b, Eghball et al., 1990, Rehm et al., 1995) con el propósito de abastecer la zona de baja concentración de P en la rizosfera (Barber, 1995); e) con el uso de micorrizas o la selección de biotipos de cultivos con mayor capacidad de exudación de ácidos orgánicos para disolver y absorber P inmóvil del suelo (Li et al., 1997; Zhang et al., 1997); y f) con la práctica de rotar cultivos con baja demanda de P o con la habilidad de movilizar y reciclar el P (Schachtman et al., 1998). Desde el punto de vista tecnológico, las opciones para aumentar la eficiencia del uso de los fertilizantes fosfóricos son: a) producción de gránulos para reducir la superficie de contacto con el suelo; b) formulación con NH4 + en fertilizantes líquidos con o sin sustancias orgánicas; y c) uso directo de ácido fosfórico en el agua de riego para reducir el pH y así evitar la formación de incrustaciones de precipitados de CaCO3 y MgCO3 en los emisores de riego (Sample et al., 1979, Engelstad; 1985, Linquist et al., 1997).
La movilidad del fósforo en suelos de zonas áridas del norte de México donde se cultiva la vid está relacionada con la cantidad de materia orgánica, la presencia de CaCO3 sólido en la matriz del suelo y la calidad de agua de riego. En estos suelos, los valores de pH son alcalinos con valores frecuentes de 7.5 a 8.5. Al comparar las constantes de disociación del H3PO4, cuyos valores de pH son de 2.1 para H2PO4 - y de 7.2 para HPO4 2-. La mayor proporción de P inorgánico como H2PO4 - en la solución del suelo ocurre con pH < 6.0. El radical H2 PO4 - es absorbido preferencialmente por las plantas en condiciones del medio del suelo con pH entre 5 y 6 unidades (Akinremi y Cho, 1991; Indiati, 2000).
Ante la evidencia de la baja disponibilidad de P en los suelos cultivados con vid en el estado de Sonora, se planteó la interrogante ¿existen condiciones que favorezcan la movilidad y disponibilidad del P en el espacio de raíces, por medio de la aplicación de fuentes de Penelagua de riego por goteo con el uso de mejoradores? Para dar una respuesta a esa interrogante, en el presente estudio se caracterizaron las curvas de distribución del P en perfiles de suelos arenosos calcáreos, bajo tratamiento con cinco fuentes fertilizantes en agua de riego alcalina y con yeso más H2SO4 (aguayeso) suministrados en riego por goteo.
Materiales y métodos
Preparación de los Medios Porosos
Se colectaron muestras de perfiles aluviales de suelo (S) de 0 a 0.60m y subsuelo (Sb) de 0.60 a 1.20m en terrenos cultivados con vid en la región de Pesqueira, en Hermosillo, Sonora, México. Las características físico-químicas del suelo y subsuelo fueron: saturación de humedad de 21 y 19% respectivamente; pH en extracto suelo:agua 1:2 de 8.5 para suelo y 7.26 para subsuelo; materia orgánica de 0.9% en suelo y 0.4% en subsuelo; textura (método de Bouyoucos) del suelo con 21.96% de arcilla, 15.72% de limo y 62.32% de arena. El subsuelo mostró valores similares a los del suelo, pero la fracción de arena fue ligeramente más gruesa con un porcentaje mayor de gravilla. Los cationes extraíbles con acetato de amonio 1 N pH 7 en el suelo fueron (mg kg-1 suelo): 1158 Ca, 322 Mg, 176 Na y 320 K; y valores similares para subsuelo en un orden de ± 5%, pero con una alta reacción de efervescencia al aplicar HCl 10%. Los valores de P fueron 13.6 y 7.2 mg kg-1 en suelo y subsuelo respectivamente extraído con H2 SO4 0.25 M y medido con el método del azul de molibdeno (Jackson, 1976). De acuerdo a la cartografía de DEGETENAL- INEGI (1982) y con base en la Referencia Mundial del Recurso Suelo (FAO, 1998), los suelos se clasifican como Calcisoles háplicos y Fluvisoles cálcicos con profundidades mayores que 1.5 m.
Se empacaron 36 columnas con suelo y 36 columnas con subsuelo en tubos de vidrio de 10 cm2 de sección transversal y 1 m de longitud con 1000 g de suelo y subsuelo (medios porosos). La densidad aparente del empacado fue de 1.43 g cm-3 y la profundidad (Z) fue 0.7 m. El coeficiente de variación de la densidad aparente de los medios porosos en las columnas a cada 0.05 m fue menor a 4%.
Fuentes de Fósforo, Riegos y Mejoradores
Se probaron cinco fertilizantes, dos con 100% de orto fosfatos (H2PO4 -): ácido fosfórico (H3PO4 -, 72% de P2O5) y fosfato mono-amónico (MAP; NH4H2PO4, 11 y 52% de N y P2O5, respectivamente); dos fertilizantes con mayor proporción de poli fosfatos (> 75%): poli fosfato de amonio líquido o 10-34-0 y Poly- Feed® (15-31-15); y finalmente un producto fosfórico líquido mezclado con sustancias húmicas Fertigro®. Los tratamientos y sus contenidos de N-P2O5-K2O y de P elemental, así como el cálculo de los gramos de fertilizante utilizados para preparar 2 L de solución a 50 mg L-1 de P, se presentan en Cuadro 1.
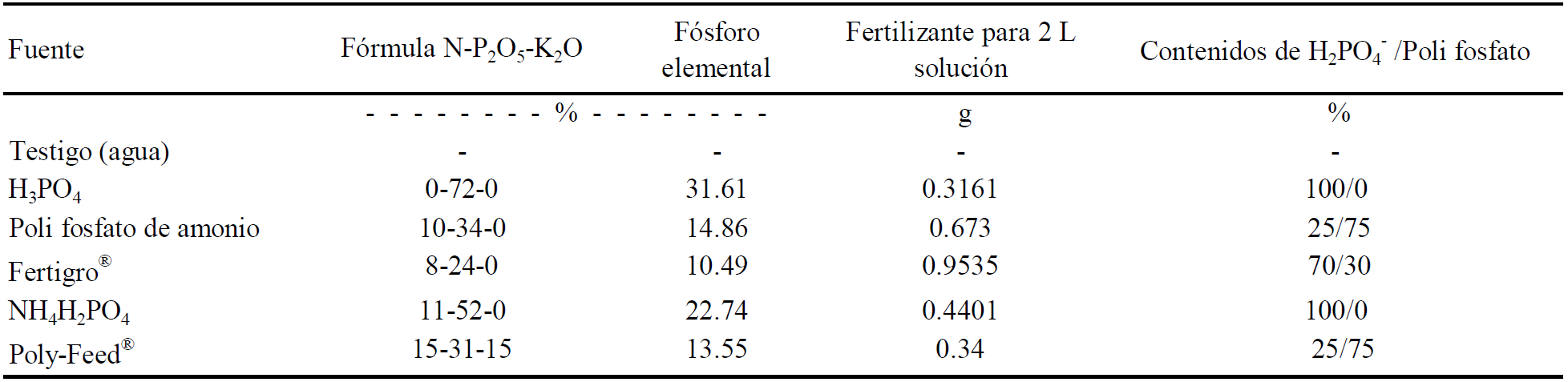
Cuadro 1 Fuentes fertilizantes, formulaciones comerciales y equivalencia de fósforo (P), cantidades de producto en 2 L de solución con 50 mg L-1 de P y proporción de H2PO4 (Orto fosfato)/poli fosfato.
Se probaron dos tipos de agua: A = agua de pozo (naturalmente alcalina) y Am = el agua de pozo tratada con mejoradores aquí nombrada aguayeso. Las características del agua de pozo fueron: pH de 7.16, conductividad eléctrica (CE) = 0.522 dS m-1; y los siguientes iones en me L-1; Ca2+ = 1.56, Mg2+ = 0.84, Na+ =2.40, HCO3 - =3.36, Cl- =0.78ySO4 2- =0.70. El aguayeso (Am) se preparó a partir del agua de pozo (A) más H2SO4 grado reactivo y yeso Sonora micronizado (grado talco, esto es más de un 90% pasa por tamiz de 250 mallas) con 96.18% de pureza (22.48% Ca). Las cantidades de H2SO4 añadido fueron de 1.68 me L-1 (para neutralizar 50% de los me L-1 de HCO3 -), y de yeso agrícola para añadir 3.24 me L-1 de Ca para dar la relación de Ca2+: Na+ de 2:1. Los valores finales del agua con mejoradores (Am) para el pH fue 5.5 y para la CE fue de 0.857 dS m-1. Los reactivos utilizados para preparar el agua tipo Pesqueira se mencionan en el Cuadro 2.
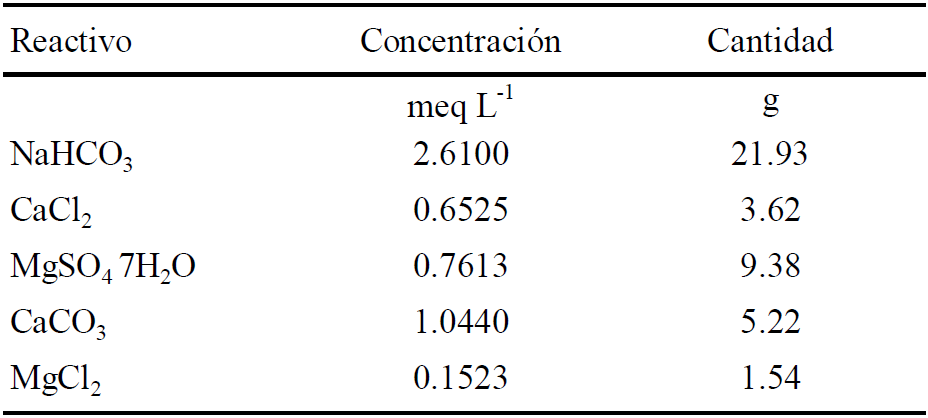
A = agua de pozo naturalmente alcalina, ajustada a CE = 0.522 dS m-1.
Cuadro 2 Reactivos para preparar 100 L de agua tipo Pesqueira (A).
Se aplicaron 11 riegos (ri), los cuales se asociaron fracciones de drenaje o lixiviación denominadas fi. El primer riego (r1) fue de 0.30 m de lámina de agua de riego por inundación con el propósito de humedecer el suelo y subsuelo empacados en columnas y definir el equivalente de un volumen poroso. Para r1 se colectó una f1 0.028 m en promedio del total de las 72 columnas del ensayo. Por lo tanto, el volumen poroso medido (f) fue 0.272 m (calculado al aplicar 0.30 m de lámina de riego por inundación para humedecer columnas de suelo y subsuelo - 0.028 m drenados en promedio). Después se aplicaron cuatro láminas (r2-5) de 0.04 m por inundación para lavar sales y medir los cambios del pH en los lixiviados (f2-5). Finalmente, en la modalidad de fertirriego por goteo con P en dosis de 50 mg L-1, se aplicaron seis láminas (r6-11) de 0.04 m, asociadas a la colecta de fracciones de lixiviación (f6-11). Así, se calcula del primer drenado d1 = 0.028 m, es equivalente a una fracción poroso de lavado (f1 = 0.028 m/0.272 m = 0.103). Para el segundo lavado, el cálculo del considera lo acumulado del drenaje o lixiviados de láminas subsiguientes con la fórmula fi = (di+di+1)/0.272, donde di+1 = d2 es el segundo drenado y así sucesivamente. Las fracciones porosas acumuladas de cinco efluentes del proceso de drenaje para lavar sales fueron: f1 = 0.10, f2 =0.27, f3 =0.44, f4 =0.59 y f5 =0.72.Yparalos efluentes de seis lixiviados de P fueron: f6 = 0.86, f7 = 1.01, f8 = 1.16, f9 = 1.31, f10 = 1.45 y f11 = 1.60. Esto es, tanto las fracciones porosas de lavado como las fracciones de los lixiviados fueron del orden de 15% del volumen poroso, similar a la práctica agrícola para mantener las sales en exceso fuera del bulbo de humedecimiento de las raíces.
Diseño y Variables Medidas
El diseño fue un factorial completo de dos medios porosos o suelos (S y Sb) × dos tipos de agua (A y Am) × seis fuentes de P (incluye testigo sin fertilizar) × tres repeticiones. Los procesos de infiltración y lavado por inundación se evaluaron con 18 repeticiones, para suelo con agua alcalina (S × A), suelo con aguayeso (S × Am), subsuelo con agua alcalina (Sb × A) y subsuelo con aguayeso (Sb × Am). El proceso de fertirriego de cinco fuentes de P más el testigo absoluto, sin P, se evaluaron con tres repeticiones. La concentración de P soluble asociada con los fertirriegos se midió en seis lixiviados por el método del molivdovanadato y con el espectrofotómetro Hach modelo DR2000. Las columnas de suelos se seccionaron a cada 0.10 m. Dentro de cada sección de suelo se extrajo el P con H2SO4 0.25 M y se cuantificó con el método del azul de molibdeno (Jackson, 1976). A cada drenado y lixiviado se le determinó el pH y la CE (dS m-1) con una precisión 0.01 y 0.001 respectivamente, con el medidor de doble función Corning M90. Los datos de la variación de los drenados en cuanto la acidez, contenidos de sales solubles y lixiviados de P fueron analizados con el programa Statistical Analysis System (SAS, 1999) y las medias se diferenciaron con la prueba de Tukey a 5%. Las distribuciones de P en el eje vertical de los medios porosos fueron graficadas y por balance de masas se calculó el desplazamiento en profundidad de la disponibilidad de P por fuente probada.
Resultados y discusión
Cambios de pH y CE
El efecto de las fuentes de P en el fertirriego con agua (A) y aguayeso (Am) sobre el pH y la CE se presentan en Cuadro 3. El valor promedio de pH de los lixiviados más bajo fue 8.2 y se midió con Poly-Feed® al regar con agua alcalina. El valor más alto de pH fue con Fertigro® producto combinado con sustancias orgánicas con el agua con mejoradores (únicamente H2SO4). La reducción del pH la explica Cho (1991), quien establece que el transporte difusivo de orto fosfatos en un medio con Ca2+ intercambiable es retardado porque el ion acompañante de los fosfatos reemplaza al Ca2+ de los sitios de intercambio catiónico y el mismo amonio libera H+. En cambio, el aumento del pH con Fertigro® se explica porque está elaborado a partir de sustancias húmicas extractadas del mineral de la leonardita o la turba con NaOH y Na4P2O7 (Francioso et al., 1998).
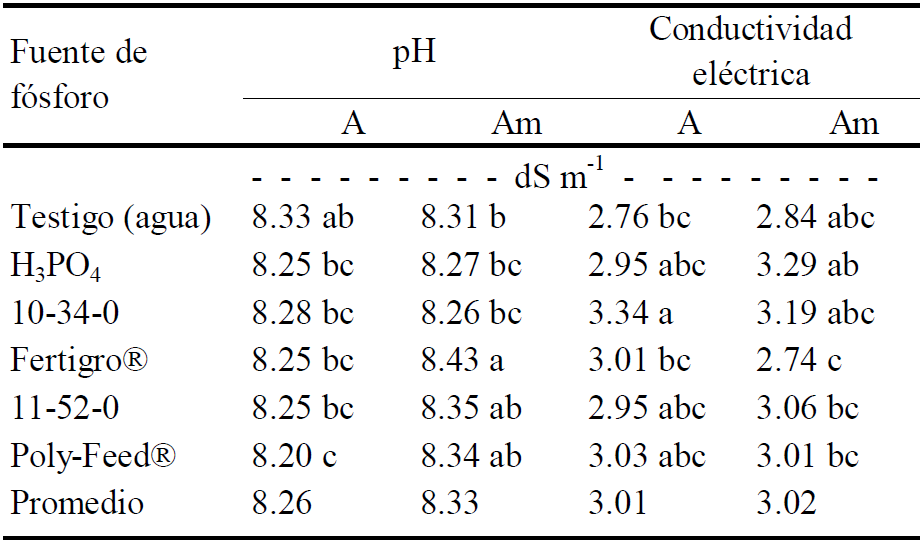
Medias con letras distintas en columna son estadísticamente diferentes (Tukey, P ≤ 0.05).
Cuadro 3 Comparación de medias por efecto de cinco fuentes de fósforo sobre el promedio de seis valores de pH y conductividad eléctrica (dS m-1) en lixiviados de agua (A) y aguayeso (Am).
Las fuentes de P en agua alcalina (A) causaron aumentos en el contenido de sales en los lixiviados respecto al testigo. Hubo diferencia estadística en la CE con la aplicación con poli fosfato de amonio o 10-34-0 (3.34 dS m-1) cuando se le comparó contra el testigo sin fertilizante (2.76 dS m-1). En cambio los fertirriegos de P con agua tratada (Am), no modificaron la salinidad de los lixiviados cuando se comparan con el testigo. Se reitera el conflicto de mezclar fertilizantes fosfóricos con sustancias húmicas en el agua con mejoradores, por lo cual se omitió el yeso (Ca2+) y sólo se añadió H2SO4 para evitar turbidez y precipitaciones.
Los altos valores de pH y de CE resultantes en las muestras del proceso de lavados de sales a través del riego por inundación (f1 = 0.10 a f5 = 0.72) y de los lixiviados con riego por goteo con las fuentes de P (de f6 = 0.86 a f11 = 1.60); condicionan a una baja distribución vertical y disponibilidad del P en estos medios porosos.
Lixiviación y Distribución Vertical de P en Suelo
No se encontraron diferencias estadísticas en las concentraciones de P en los seis lixiviados por calidad de agua de riego, ni por tipo de medio poroso de suelo y subsuelo o fuente fertilizante. Así, para ilustrar las diferencias de la concentración de P en los lixiviados en ambos medios porosos entre el ácido fosfórico y el testigo sin fertilizar con riego de agua alcalina (A) fue de 7.34 mg L-1 (H3PO4) - 6.81 mg L-1 (Testigo) = 0.53 mg L-1; y para aguayeso (Am) fue de 8.16 mg L-1 (H3PO4) - 7.61 mg L-1 (Testigo) = 0.55 mg L-1. En sentido práctico y de diagnóstico, la diferencia medida en los lixiviados de 0.5 mg L-1 de P entre el ácido fosfórico y el testigo, luce despreciable contra el valor de 50 mg L-1 de la concentración de la fuentes fosfóricas aplicadas en el fertirriego. Por ello, se procedió por medio del método de balance de masas a medir la distribución vertical del P proveniente de cada fertilizante en las columnas de ambos medios porosos mediante su extracción del suelo con H2SO4 0.25 M (Cuadro 4).
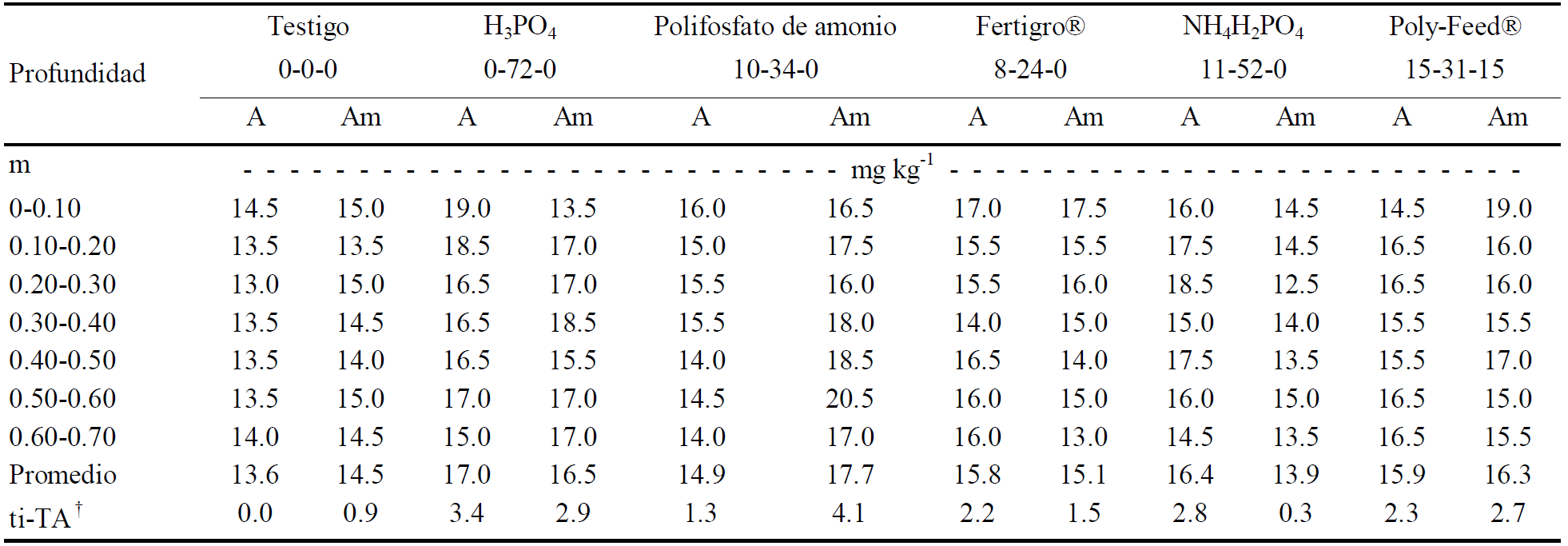
† ti-TA = diferencia del promedio de P de las siete profundidades por los tratamientos “ti” con P en la columna menos el correspondiente promedio sin P del testigo (T) con agua alcalina (A). CME (cuadrado medio del error) = 1.47; CV (coeficiente de variación) = 9.42; DMS (diferencia media significativa) para fuentes de P = 0.924; para tipos de agua la DMS = 0.365 y para profundidad del suelo la DMS = 1.033.
Cuadro 4 Concentraciones de fósforo por fuentes y profundidad en columnas de suelo regadas con agua (A) y aguayeso (Am).
El hecho de regar el suelo con aguayeso (Am) provocó un aumento del P en la columna testigo sin fertilizar con un promedio de 0.86 mg kg-1. Con poli fosfato de amonio (10-34-0) aplicado con aguayeso Am, el P en la columna de suelo se incrementó en 4.07 mg kg-1; seguido por el tratamiento con H3PO4 con solo agua (A) con valor de 3.36 mg kg-1. La mayor disponibilidad de P con H3PO4 se explica por la liberación de iones H+ y los orto fosfatos (H2 PO4 - y HPO4 2-), pero estos radicales de carga negativa en un medio muy alcalino están sujetos a una pronta reacción con cationes para formar compuestos de baja solubilidad. En contraste, con las fuentes con poli fosfatos como el 10-34-0 (75% poli fosfatos y 25% de orto fosfatos), requieren del proceso de hidrólisis para separar la cadena de poli fosfatos, y este fenómeno retarda la precipitación de las 3/4 partes del componente de este fertilizante (Mansell et al., 1985; Grant y Heaney, 1997).
A fin de valorar el P real retenido en cada una de las siete profundidades por efecto de la aplicación de las cinco fuentes fertilizantes con P, se hizo el cálculo al sustraer de las medias de concentración de P de cada tratamiento ti menos el valor del testigo respectivo con A y Am. Todas las fuentes de P incrementaron la concentración de P en las distintas profundidades del suelo con excepción para el fertirriego con MAP 11-52-0 (100% orto fosfatos con amonio) con agua tratada con mejoradores (Am), con el cual incluso el valor promedio en la columna fue negativo de 0.5 mg kg-1 de P; Cuadro 5. De igual modo, todas las fuentes fertilizantes combinadas con aguayeso (Am) se encontraron valores en la columna de suelo menores de P en promedio contra las columnas regadas con sólo agua (A), con la excepción del tratamiento con el fertilizante fluido con poli fosfatos de amonio 10-34-0 (75% de poli fosfatos). Estos dos casos de baja disponibilidad neta de P en la columna de suelo confirma la teoría las fuentes con P deben de aplicarse preferentemente solas en el fertirriego por interacciones químicas de precipitación.
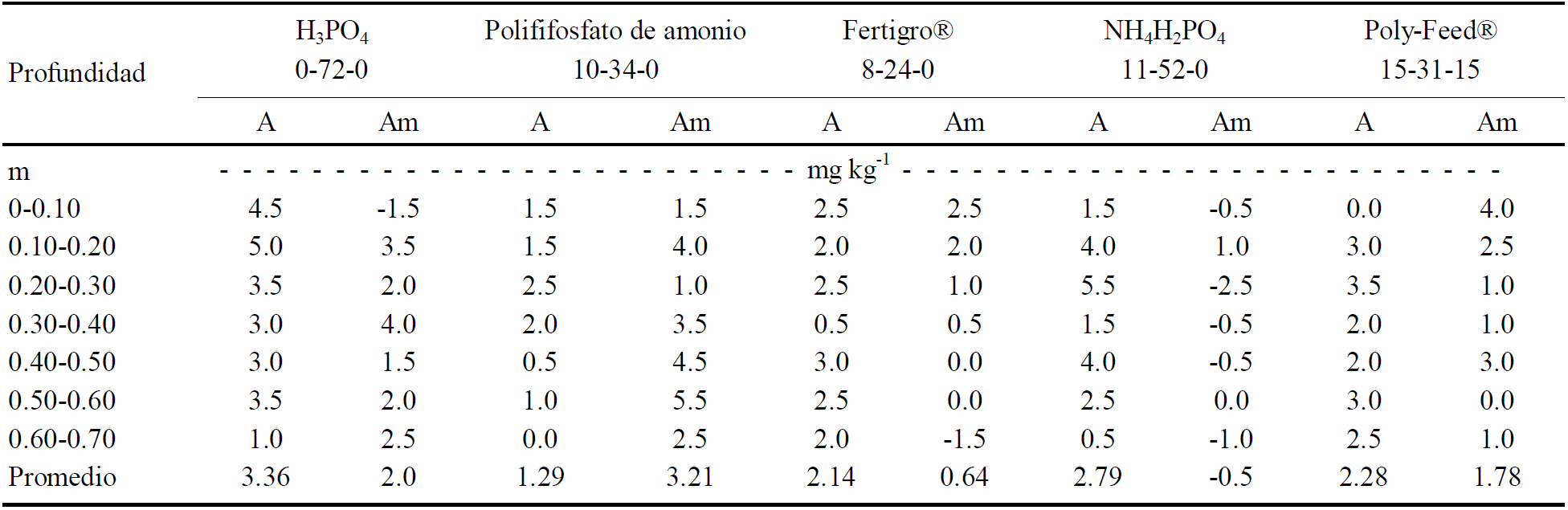
Cuadro 5 Concentración de fósforo por fuentes y profundidad en las columnas al restar los respectivos valores del testigo con agua (A) y agua con mejoradores (Am) en suelo.
Por otra parte, las fuentes con ion acompañante amonio favorecen el intercambio con el Ca2+ y el Na+ ubicados en los sitios de carga negativa de las arcillas (Sample et al., 1979, Akinremi y Cho, 1991, Yibirin et al., 1996, Gale et al., 2000) y, según Sharpley et al. (1988), en un medio rico en sodio se libera más P. Con base en el análisis del Cuadro 5 se aprecia la disponibilidad de P en promedio en la columna de suelo fue mayor cuando se aplicó H3PO4 en agua alcalina (A) con 3.36 mg kg-1 de P, seguido por el tratamiento con poli fosfato de amonio 10-34-0 con aguayeso (Am) con 3.21 mg kg-1 de P, y en tercer lugar con MAP 11-52-0 en aguayeso (Am) con 2.79 mg kg-1 de P. Por ello, durante el tiempo que requieren estos procesos y con la intermitencia del flujo del agua del riego por goteo, se favoreció una mayor distribución vertical del P pero con valores fluctuantes a lo largo de la columna de suelo (Khasawneh et al., 1974). Sin embargo, es cuestionable la distribución del P medida en secciones de 0.10 m de suelo, en lugar de hacerlo como frecuentemente se reporta en milímetros por el proceso de difusión (Barber, 1995; Cho, 1991). Sin embargo, la información obtenida en el presente estudio está acorde con Engelstad (1985), quien indica que hay significativo movimiento de P en suelos de textura ligera.
En la Figura 1 se destacan las curvas de la distribución de P en las columnas de suelo de las dos fuentes fosforadas con mayor desplazamiento con el fertirriego con agua de riego alcalina sin tratar (A), estas fueron: el ácido fosfórico (H3PO4 y el fosfato mono-amónico MAP (11-52-0) en comparación contra el Testigo sin fertilizante.
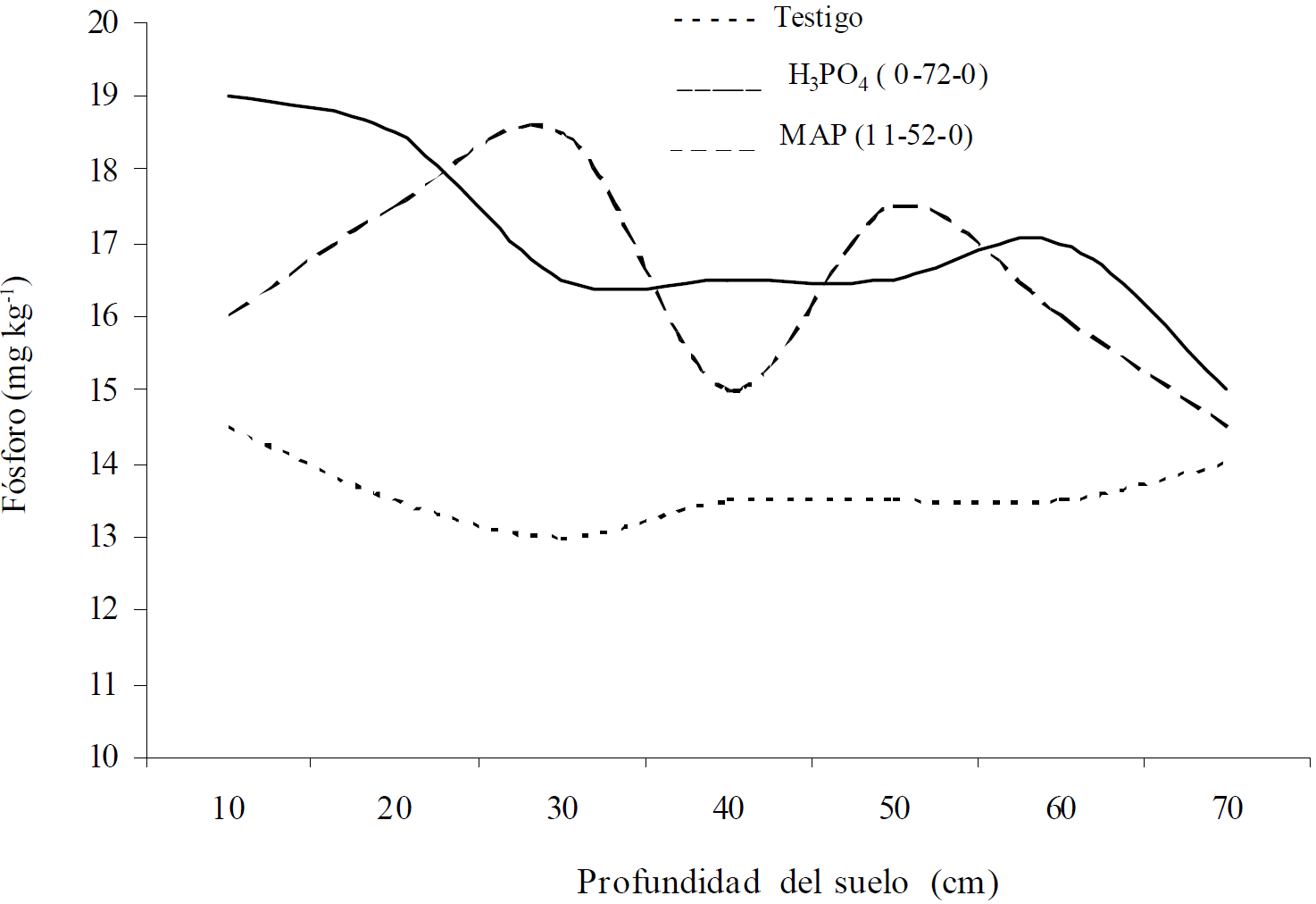
Figura 1 Distribución vertical del fósforo en suelo al aplicar H3PO4 y fosfato mono-amónico(MAP) contra testigo con agua de pozo.
Se observa con la línea continua la concentración de P del H3PO4 baja en forma continua de 19 mg kg-1 en 34 la superficie a 15 mg kg-1 en la sección más baja de la columna de suelo de 60 a 70 cm. En cambio, la línea de la concentración de P del MAP 11-52-0 tiene dos picos o fluctuaciones de valores mayores en los tramos de 20 a 30 cm (18.5 mg kg-1) y otro segundo menos pronunciado en el intervalo de 40 a 50 cm (17.5 mg kg-1). Estos incrementos de P por la fertilización de estas dos fuentes fosfóricas al compararlas contra la curva sin pendiente de la concentración del testigo de 13.6 mg kg-1; dan crédito al concepto la posible movilidad significativa del fosforo en suelos de textura ligera según Engelstad (1985).
Distribución Vertical de P en el Subsuelo con Presencia de CaCO 3
Los valores de la concentración de P en los extractos obtenidos en subsuelo con presencia de CaCO3, y para cada tratamiento se presentan en el Cuadro 6.
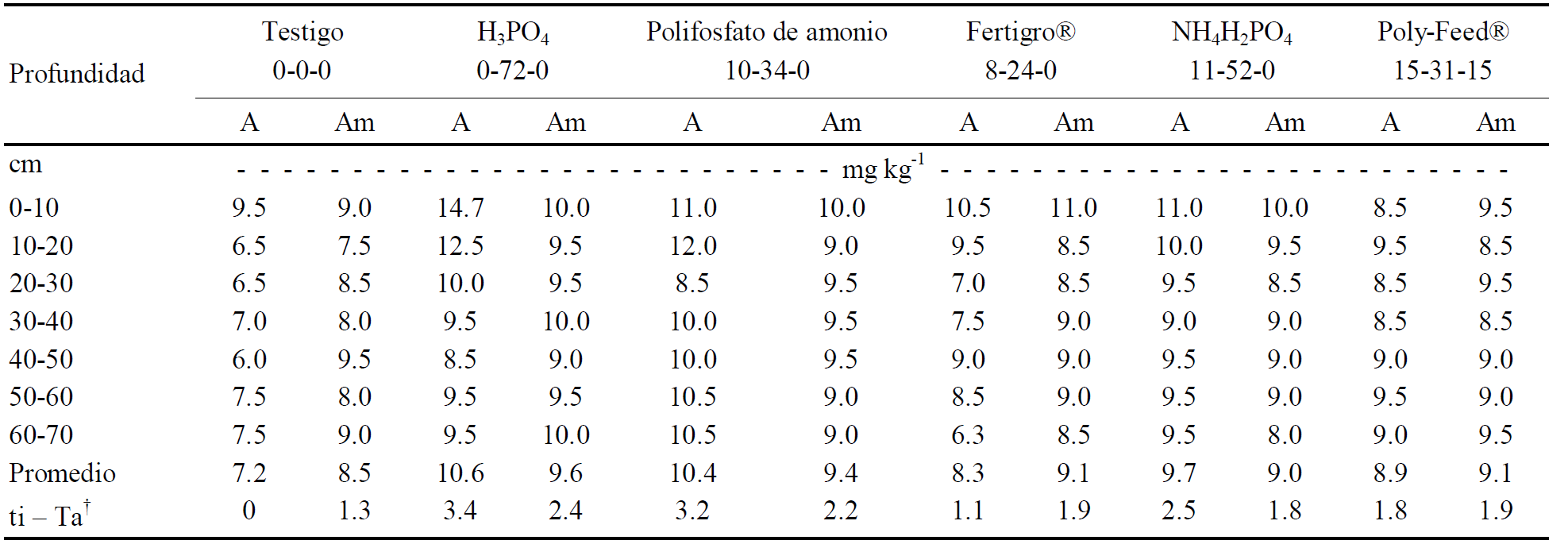
† ti-TA = diferencia del promedio de P en siete profundidades por los tratamientos “ti” con el promedio de P en la columna del testigo (T) con agua alcalina (A). CME (cuadrado medio del error) = 1.083; CV (coeficiente de variación) = 11.86; DMS (diferencia media significativa) para fuentes de P = 0.679; para tipos de agua la DMS = 0.268 y para profundidad del suelo la DMS = 0.759.
Cuadro 6 Concentraciones de fósforo por fuentes y profundidad en columnas de subsuelo con presencia de CaCO3, regados con agua (A) y aguayeso (Am).
En el subsuelo el valor promedio de P en la columna aumentó para las cinco fuentes fosfóricas aplicadas en el fertirriego tanto con agua sola (A) o con aguayeso (Am). Incluso el riego con aguayeso en el testigo sin fertilizante se cuantificó un aumento de 1.3 mg kg-1 de P en promedio en comparación con el regado con agua sola o alcalina (A). Esta disponibilidad de 1.3 mg kg-1 P en el testigo resultó de la diferencia de 8.5 menos los 7.2 mg kg-1 de Am y A, respectivamente. En contraste, en suelo la diferencia fue menor de 0.9 mg kg-1, resultado de 14.5 - 13.6 mg kg-1 de Am y A, respectivamente. Es decir, los registros de la concentración del P en los testigos sin P en el suelo casi duplicaron a los tratamientos homólogos del subsuelo. Los valores más altos de P en suelo son lógicos debido a su incorporación en la superficie por la acción de las raíces y la descomposición de los residuos orgánicos; así como por la práctica de abonado del agricultor y la mayor retención de P en las fracciones coloidales.
En el subsuelo, al comparar los valores del P por el fertirriego con fósforo aplicados con agua alcalina (A) en comparación con aguayeso (Am), se observó en todas las fuentes al añadir mejoradores al agua se provocó una disminución en la concentración de P.
La fuente menos eficiente, con relación al contenido del P en el subsuelo, fue con Fertigro®, producto con sustancias húmicas, tanto con A como con Am. Esto se debe a grupos orgánicos ligados al P, los cuales interfieren en la medición de P con el método de ácido ascórbico- azul de molivanadato (He et al., 1998).
Los valores reales añadidos por las fuentes fertilizantes de P extraíble para cada profundidad en subsuelo se calcularon al descontar los valores de los respectivos testigos con A y Am (Cuadro 7).
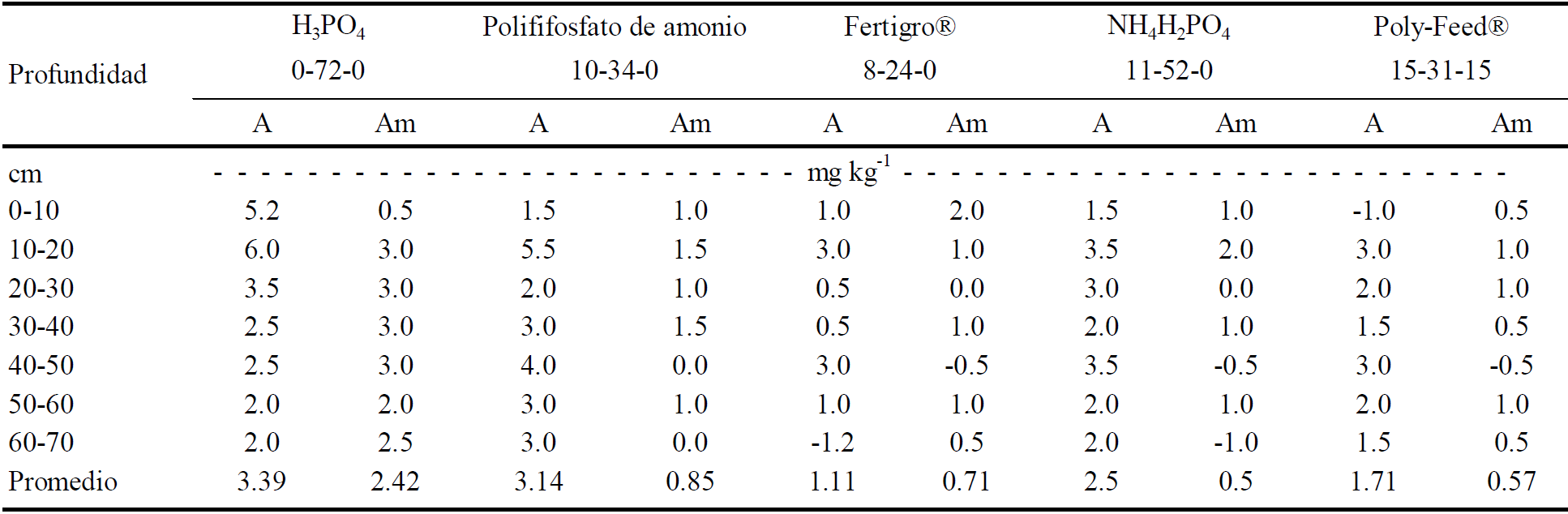
Cuadro 7 Concentraciones de fósforo por fuentes y profundidad al descontar respectivos valores del testigo con agua (A) y aguayeso (Am) en subsuelo con presencia de CaCO3.
La mayor disponibilidad de P en el subsuelo se midió en todos los casos con el riego con agua alcalina (A). El aumento de la concentración de P en la columna de subsuelo con H3PO4 aplicado con en agua alcalina fue de 3.39 mg kg-1 de P, seguida por poli fosfato de amonio 10-34-0 (3.14 mg kg-1 de P) y en tercer lugar por MAP u 11-52-0 (2.5 mg kg-1 de P).
En la Figura 2, se destacan las dos fuentes con la mayor profundidad del P alcanzada en subsuelo al aplicarlos con agua alcalina (A). Estas fuentes fueron el ácido fosfórico y el fosfato mono-amónico u (11-52-0), ambas comparadas contra el testigo sin fertilizar.
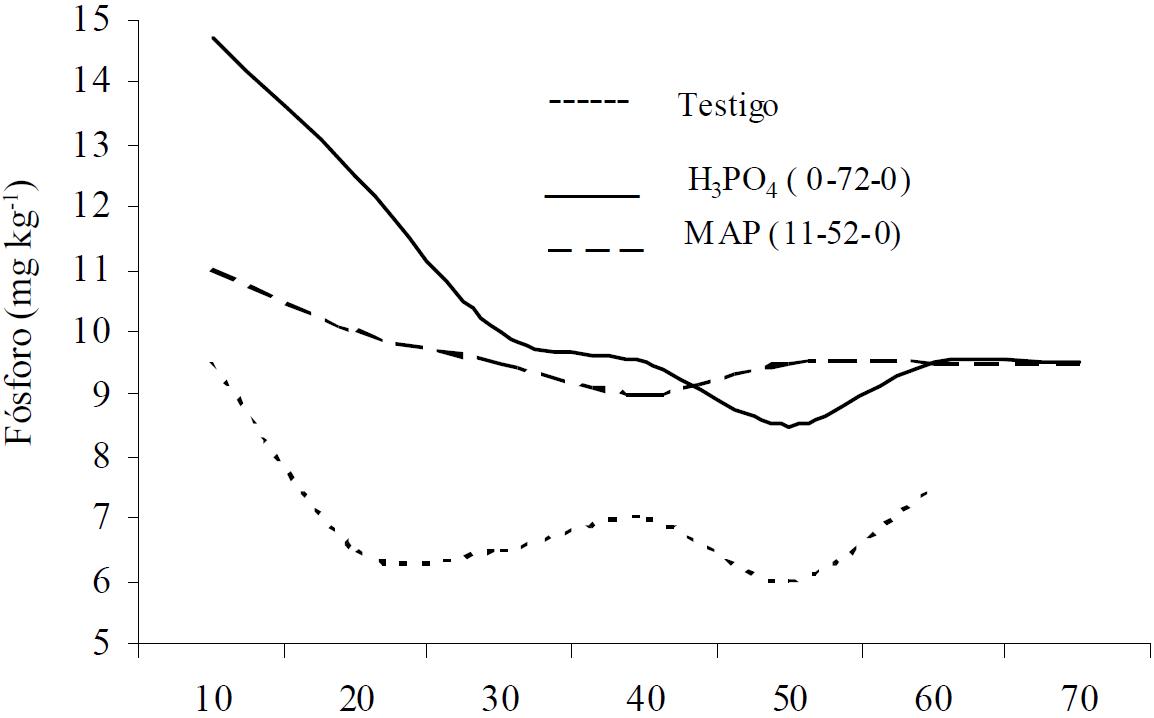
Figura 2 Distribución del fósforo en subsuelo al aplicar H3PO4 y fosfato amónico (MAP) en agua alcalina (A) contra testigo sin fósforo.
Al regar con agua alcalina el subsuelo, se observa con la línea continua baja la concentración de P del H3PO4 de 14.7 mg kg-1 en los primeros 10 cm 34 a 12.5 mg kg-1 en la sección de 10 a 20 cm, y después se mantiene hasta el fondo de la columna con valores del orden de 10 mg kg-1 de P. En cambio, la línea de la concentración de P del MAP 11-52-0, guarda un valor casi constante de 10 mg kg-1 en toda la profundidad de la columna de subsuelo. Estos incrementos de P por la fertilización de estas dos fuentes fosfóricas al compararlas contra la curva fluctuante a la baja del testigo sin fertilizar con un valor promedio de 7.2 mg kg-1 confirma la posibilidad de aportar P a las raíces profundas de la vid al momento de la floración en un medio de subsuelo de textura arenosa con presencia de carbonato de calcio.
La comparación de la disponibilidad de P por efecto de fuentes de fertilizante en suelo y subsuelo y por calidad del agua se resume en el Cuadro 8.
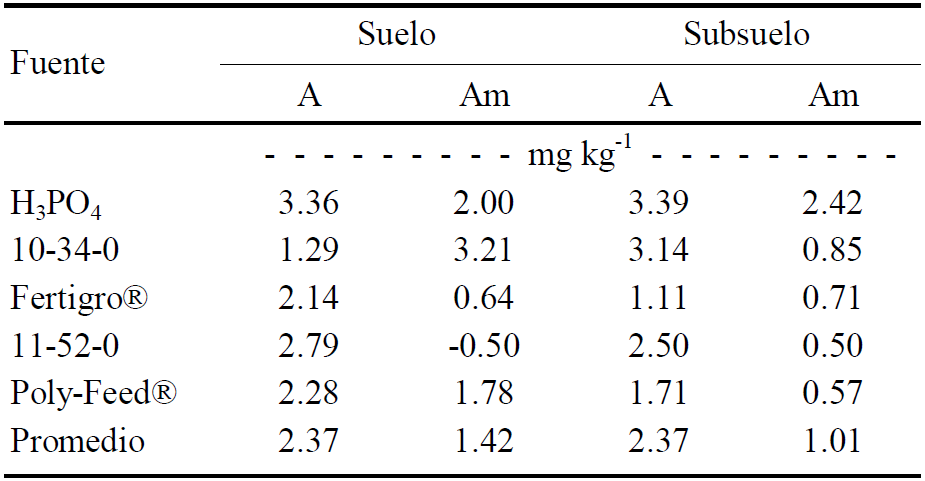
Cuadro 8 Comparación de la disponibilidad promedio de fósforo (P) en columnas con suelo contra subsuelo para cinco fertilizantes fosfóricos en agua alcalina (A) y aguayeso (Am).
La disponibilidad promedio del P fue similar para los dos medios porosos e incluso fueron de igual valor con riego de agua alcalina (2.37 mg kg-1 de P). Los mejoradores añadidos al agua de riego redujeron en 40% y 57%, la disponibilidad del P en el suelo y el subsuelo respectivamente. Al referirse al uso de fertilizantes fosfóricos en el agua de riego sin tratar o alcalina, el H3PO4 permitió la más alta concentración de P en ambos medios porosos con valores de 3.36 y 3.39 mg kg-1 de P disponible en la columna, seguido por el MAP 11-52-0 en suelo y el poli fosfato de amonio 10-34-0 en subsuelo. Los altos valores de pH mayores de 8.3 unidades registrados en los lixiviados presuponen condiciones de alta probabilidad para la formación de Ca3 (PO4)2, fenómeno que afectó en menor proporción al fertirriego con poli fosfato de amonio 10-34-0 en el suelo con Am en el cual se encontró 3.21 mg kg-1 de P disponible en la columna, así como en el subsuelo con A con un valor de 3.14 mg kg-1 de P.
Conclusiones
Con el análisis de los resultados se concluye: a) debe evitarse el mezclado de fertilizantes fosfóricos y mejoradores en el agua de riego como H2SO4 y yeso micronizado, porque no sólo se reduce su disponibilidad para los cultivos, sino que incluso provoca precipitaciones insolubles de P; b) la mayor disponibilidad del P en las columnas regadas con agua alcalina (A) en suelo y subsuelo se obtuvo con H3PO4, fosfato mono amónico 11-52-0 y poli fosfato de amonio 10-34-0; c) el fertilizante 11-52-0 resultó con mayor distribución del P en el suelo con agua; d) los fosfatos asociados a los humatos presentaron los valores más bajos de la concentración de P en suelo y subsuelo irrigados con A y Am y e) la cantidad de P encontrada a mayor profundidad en suelos arenosos por efecto de la aplicación de H3PO4, fosfato mono amónico y poli fosfatos de amonio, confirma la posibilidad de aportar P a las raíces profundas de la vid al momento de la floración en un medios porosos de suelo y subsuelo alcalino de textura arenosa.











 nueva página del texto (beta)
nueva página del texto (beta)


