ANTECEDENTES
La insuficiencia renal aguda se define como la disminución de la capacidad renal para llevar a cabo sus funciones, que puede tener aparición rápida. Esta disfunción ocasiona que se acumule agua, solutos y metabolitos tóxicos en el organismo. Esta alteración en el funcionamiento renal puede ocurrir con o sin lesión renal evidente o puede manifestarse como exacerbación en un paciente con una lesión previa.1,2
La incidencia de insuficiencia renal aguda en los pacientes críticos varía entre 35 y 50%, los cuadros de sepsis son la principal causa de insuficiencia renal aguda en terapia intensiva), otras enfermedades pueden desencadenar un cuadro de insuficiencia renal aguda, como traumatismo, cirugías, cirugía cardiaca, insuficiencia cardiaca, enfermedades autoinmunitarias, la ingesta de fármacos, etc.1,3,4
La insuficiencia renal aguda se vincula con mayor mortalidad en terapia intensiva. En nuestro país encontramos los siguientes resultados publicados: en 2006 el trabajo de Moreno y colaboradores reportó mortalidad cercana a 50% cuando es concomitante con sepsis y Chávez en 2010, en un trabajo multicéntrico, reportó 72% de pacientes en terapia intensiva con insuficiencia renal aguda y su causa más frecuente fue la disfunción multiorgánica con 35%.2,5
Los grupos de investigación de ADQUI (Acute Dialysis Quality Initiative) y AKIN (Acute Kidney Injury Network) trabajaron para obtener una clasificación y propusieron las escalas RIFLE y AKIN (Cuadros 1 y2). Ambas clasificaciones se han comparado y los resultados en cuanto a mortalidad son similares entre ambos métodos y tienden a aumentar a medida que avanza la gravedad de la insuficiencia renal aguda. AKIN, a diferencia de RIFLE, requiere dos mediciones de creatinina en un lapso de 48 horas para establecer el diagnóstico de insuficiencia renal aguda.3,6
Cuadro 1 Escala RIFLE
| RIFLE | Creatinina sérica (CR) | Diuresis |
|---|---|---|
| R (riesgo) | Incremento 1.5 veces la CR basal. FG disminuida > 25% | < 0.5 mL/kg/h por 6 horas |
| I (daño) | Incremento 2 veces la CR basal. FG disminuido > 50% | < 0.5 mL/kg/h por 12 horas |
| F (insuficiencia) | Incremento 3 veces la CR basal o CR > 4 mg/dL IRA sobre IRC. FG disminuido > 75% | < 0.3 mL/kg/h por 24 horas o anuria por 12 horas |
| L (pérdida) | Pérdida de la función renal > 4 semanas | |
| E (final) | Insuficiencia renal estadio terminal (> 3 meses). |
IRC: insuficiencia renal aguda; FG: filtrado glomerular.
Cuadro 2 Escala AKIN
| AKIN | Creatinina sérica (CR) | Flujo urinario (FU) |
|---|---|---|
| 1 | Aumento de CR > 0.3 mg/dL o 1.5 a 2 veces de la concentración basal | < 0.5 mL/kg/h más de 6 horas |
| 2 | Aumento de CR > 2 a 3 veces de la concentración basal | < 0.5 mL/kg/h más de 2 horas |
| 3 | Aumento de CR > 3 veces de la concentración basal o CR ≥ 4 mg/dL | < 0.3 mL/gk/h más de 24 horas o anuria de 12 horas. |
Sólo debe tomarse un criterio (flujo urinario o creatinina sérica) para clasificar. Los pacientes que reciben terapia de reemplazo renal se consideran categoría 3 independientemente de la etapa en que se inicie. Las etapas 1, 2 y 3 corresponden a las etapas R, I y F de RIFLE, respectivamente. Esta clasificación exige dos mediciones de creatinina separadas de 48 horas, el primer valor es el basal.
El tratamiento de la insuficiencia renal aguda varía desde la protección renal hasta la terapia de reemplazo renal, actualmente en terapia intensiva se cuenta con la herramienta de terapia de reemplazo renal continua, el objetivo de esta revisión fue reunir los conceptos, terminología, modalidades, sus principales indicaciones, así como aspectos básicos de su programación, para tratar de comprender y facilitar la prescripción de esta terapia.
Terapia de reemplazo renal continua: modalidades, conceptos y terminología
El término terapia de reemplazo renal continua se refiere a las terapias que purifican la sangre en forma extracorpórea, sustituyendo la función renal en forma continua durante las 24 horas del día, esta modalidad tuvo su inicio en 1977 por Kramer.7
A continuación mencionaremos algunos conceptos para entender con más facilidad la terapia de reemplazo renal continua.
Ultrafiltrado. Se llama así al fluido recogido en la bolsa distal al hemofiltro (Figura 1), es decir, la cantidad de agua eliminada del plasma circulante de la sangre; ésta forma parte del volumen de efluente. En algunos sitios se le conoce como extracción.

Figura 1 Equipo de terapia de reemplazo renal continua. La flecha amarilla muestra el hemofiltro, la flecha azul, el líquido de reinyección o de sustitución, la flecha verde, dónde se recoge el total de líquido efluente, la flecha negra, el líquido de diálisis.
Líquido de diálisis o dializante. Fluido que se instala en contracorriente del filtro de la sangre.
Líquido efluente. Es la suma del líquido dializante más el ultrafiltrado (líquido que se colecta en bolsa distal o final).
Líquido de sustitución o de reinyección. Es el fluido que se instala antes del filtro o después de éste para reemplazar el volumen de ultrafiltrado.8
La terapia de reemplazo renal continua tiene cuatro modalidades que pueden usarse en diversas enfermedades y diversos escenarios clínicos: 1)ultrafiltración lenta continua, 2)hemofiltración venovenosa continua, 3)hemodiálisis venovenosa continua, 4)hemodiafiltración venovenosa continua.
Ultrafiltración lenta continua. En esta modalidad la principal utilidad reside en poder controlar el balance hídrico de los pacientes, como en la sobrecarga hídrica (insuficiencia cardiaca congestiva). En esta técnica no hay líquido de sustitución ni reemplazo porque el objetivo primordial es retirar el exceso de volumen (Figura 2).9
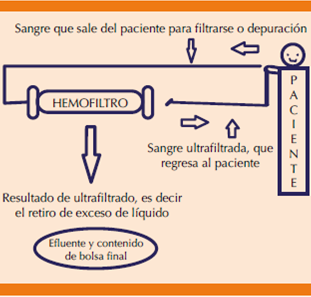
Figura 2 Ejemplo de funcionamiento de ultrafiltración lenta continua. El contenido a filtrar es la cantidad de sangre que comenzará a ser manejada para extraer líquido programado.
Hemofiltración venovenosa continua. Esta modalidad consiste en hacer pasar el flujo de sangre a través de un filtro de alta permeabilidad hidráulica. El mecanismo que se utiliza es el convectivo. Es decir, se transporta agua y solutos a través de un filtro al ejercer una presión, que está dada por bomba de rodillos (circuito venovenoso). En esta variante de terapia el ultrafiltrado es mayor a las pérdidas del paciente, por tanto, se necesitará líquido de sustitución (Figura 3).9
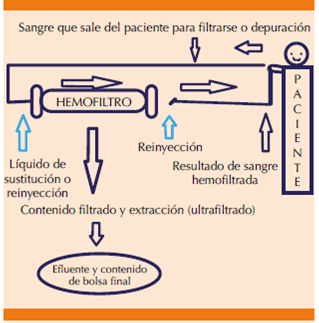
Figura 3 Ejemplo de funcionamiento de hemofiltración venovenosa continua. El líquido de sustitución o reinyección (flechas azules) pude usarse antes o después de filtro, lo que dependerá del equipo con el que se cuente, en este caso el efluente o líquido final será el ultrafiltrado.
Hemodiálisis venovenosa continua. En esta modalidad se usa la difusión como principal fuente de mejora del fluido tratado, éste consiste en hacer pasar un flujo lento del dializante a contracorriente del flujo sanguíneo, consiguiendo así la difusión de moléculas de pequeño tamaño. En este método no se necesita de líquido de reinyección (Figura 4).9

Figura 4 Ejemplo de hemodiálisis venovenosa continua. La flecha verde es el flujo del líquido dializante en contracorriente que permite la difusión de las moléculas, el efluente consiste en el líquido dializado y puede agregarse extracción o ultrafiltrado.
Hemodiafiltración venovenosa continua. Esta modalidad combina los beneficios de hemodiálisis venovenosa continua + hemofiltración venovenosa continua, es decir, se utilizan dos métodos de reemplazo renal, la convección y la difusión. Con esta combinación pueden eliminarse partículas de mayor peso molecular (> 1000 Da), como es el caso de insuficiencia renal inducida por trauma (rabdomiólisis). Al utilizar esta modalidad es necesaria la reinyección para conseguir el adecuado equilibrio de fluidos (Figura 5).9,10
Indicaciones
La indicación del inicio de terapia de reemplazo renal continua no está del todo clara; la indicación precisa de este método es ante una situación clínica que requiere que se corrija el funcionamiento renal, por tanto, la decisión de en qué momento se iniciará será tomada por los médicos de terapia intensiva. Sin embargo, en el trabajo que realizó Jung y colaboradores, donde se analizó el inicio temprano de la terapia de reemplazo renal continua, se encontró mayor beneficio al iniciar el procedimiento de manera temprana. Las indicaciones absolutas son: acidosis metabólica severa, sobrecarga hídrica resistente a diuréticos, intoxicaciones susceptibles de curarse, las alteraciones electrolíticas graves y que el paciente se encuentre hemodinámicamente inestable. Al tomar en cuenta las escalas AKIN Y RIFLE, Canseco y su grupo, en 2010, iniciaron la terapia en estadio I y F de RIFLE, equivalente a los estadios 2 y 3 de la escala AKIN, se observó respuesta adecuada a la depuración y estabilidad clínica.6,8,11,12 En el Cuadro 3 se muestran las indicaciones de la terapia de reemplazo renal continua.
Cuadro 3 Indicaciones de terapia de reemplazo renal continua
| Indicaciones | Comentario |
|---|---|
| Acidosis grave | Típicamente pH < 7.0 |
| Uremia severa | Asociada con neuropatía, miopatía, encefalopatía o pericarditis |
| Hipervolemia | Edema pulmonar por congestión, edema abdominal asociado con oliguria o anuria |
| Hipercalemia y otros electrólitos | Generalmente potasio > 6.5 mmol/L, hipernatremia severa |
| Intoxicaciones | Procainamida, litio, fenformina, salicilatos, medio de contraste y resto de compuestos dializables |
| Rabdomiólisis | En pacientes con lesiones de aplastamiento, para prevenir complicaciones. Se puede barrer mioglobina |
| Sepsis | Mediadores inflamatorios |
Los beneficios adicionales que esta terapia ofrece es la posibilidad de mantener la eliminación de volumen y personalizar los líquidos de sustitución de acuerdo con el estado clínico del paciente y combinar los métodos de depuración, así como mantener mayor estabilidad hemodinámica por efectos clínicos y bioquímicos.6,8,13
Accesos vasculares
El éxito de una buena terapia de reemplazo renal continua depende del éxito del funcionamiento del acceso venoso y del catéter que se elija, en los adultos se prefiere un catéter de doble lumen que mida 11-12 Fr para cada lumen. En nuestro centro de trabajo el más usado es el catéter Mahurkar. A diferencia de lo que se cree en algunos centros, de que el uso de un acceso subclavio es más seguro para canalizar un vaso donde se llevará a cabo una terapia de sustitución, debido a menos eventos de infecciones, alguna evidencia científica muestra que esta vía puede acarrear mayores complicaciones al momento de someter a un paciente a terapia de reemplazo renal continua, porque las complicaciones pueden ser trombosis y estenosis de ese vaso, además, las tasas de infecciones por accesos femorales se reportan bajas con cuidados de rutina de terapia intensiva, con aumento del riesgo en pacientes obesos. El acceso subclavio queda como última opción al momento de usar una vía. Las vías más recomendadas para acceso es la vía venosa femoral y la vena yugular derecha (la principal) seguida de la vena yugular izquierda. Algunos recomiendan la vía de acceso femoral como primera opción porque el sitio de acceso es fácil y se evitan problemas con el circuito del aparato.8,9,14
Anticoagulación
La anticoagulación del circuito del equipo para terapia de reemplazo renal continua es necesaria porque la trombosis del filtro ocasiona el funcionamiento inadecuado y más costos para la terapia sustitutiva. Una vez que la sangre entra en contacto con el circuito se activan los sistemas de coagulación de la sangre de manera que debe acompañarse de un método que evite que esto suceda.8
Las alternativas son administrar heparina no fraccionada a dosis de 40 UI/kg en bolo seguida de una infusión de 5-15 UI/kg/h, tomando como control TTPA con intervalo 1.5-2 veces del valor normal (35-45 seg).
También puede administrarse enoxaparina a dosis de carga de 0.15 mg/kg e infusión de 0.05 mg/kg/h utilizando control de factor anti-Xa 0.25-0.35 UI/mL, esta medida es más costosa. En los pacientes que padezcan trombocitopenia secundaria a heparina una opción es argatroban a dosis de 30 mg/kg/h y vigilar TTp cada 12 horas. Existen otras alternativas, como citrato y prostaglandinas que en nuestro medio no es de prescripción frecuente; sin embrago, el citrato cuenta con un grado fuerte de recomendación.8
Algunos pacientes tienen riesgo de sangrado debido a su estado clínico. Los pacientes que cumplan los siguientes criterios pueden no requerir terapia de anticoagulación: 1)plaquetas < 70,000, 2) TTPA > 65 seg, 3)INR > 2, 4)coagulación intravascular diseminada, 5)hemorragia espontánea mayor.9
Fluidos de reemplazo y diálisis
Existe una variada cantidad de líquidos de sustitución que están disponibles para usarse en las modalidades en que se utilice la hemofiltración, la elección dependerá de las características del paciente y los objetivos metabólicos de cada uno. Los preparados de Gambro (prisma set) o de Baxter (plasma lyte) son de primera línea. Las recomendaciones actuales no concluyen cuál debe utilizarse; sin embargo, al momento de elegir líquidos de diálisis en un paciente con hipercalemia se prefiere utilizar bolsas sin aporte de potasio y cuando no tenga alteraciones electrolíticas, con preparados convencionales. Se agregará bicarbonato de acuerdo con el estado metabólico del paciente (acidosis metabólica), se programará a velocidad de 1000 cc/h y se podría aumentar hasta 4500 mL/h. Debe recordarse que al aumentar el líquido de reinyección pude aumentar la depuración de solutos.8
En el Cuadro 4 se indican líquidos de sustitución y líquidos de diálisis.
Cuadro 4 Líquidos y contenidos de sustitución
| Electrólitos | Plasma (mEq/L) | Fisiológico 0.9% | Solución a 0.45% con 75 mEq NaHCO3 | Solución inyectable con 150 mEq NaHCO3 | Prismasate 4 K+ | Prismasate 0 K+ | Plasma-lyte |
|---|---|---|---|---|---|---|---|
| Sodio | 135-145 | 154 | 152 | 150 | 140 | 140 | 140 |
| Cloro | 100-108 | 154 | 77 | 0 | 113 | 109.5 | 98 |
| Potasio | 3.5-5.0 | 0 | 0 | 0 | 5 | 0 | 5 |
| Magnesio | 1.5-2.0 | 0 | 0 | 0 | 1.5 | 1 | 3 |
| Lactato | 0.5-2.0 | 0 | 0 | 0 | 3 | 3 | 0 |
| Bicarbonato | 22-26 | 0 | 75 | 150 | 32 | 32 | 0 |
| Glucosa | 70-110 | 0 | 0 | 0 | 110 | 0 | 0 |
| Acetato | 0 | 0 | 0 | 0 | 0 | 0 | 27 |
| Calcio | 2.3-2.6 | 0 | 0 | 0 | 2.5 | 3.5 | 0 |
| Osmolaridad | 280-296 | 308 | 304 | 0 | 300 | 287 | 294 |
| Gluconato | 0 | 0 | 0 | 0 | 0 | 0 | 23 |
Programación de terapia de reemplazo renal continua y situaciones especiales
La dosis óptima de terapia de reemplazo renal continua dependerá de las características patológicas que acompañen a un paciente, es decir, su equilibrio hídrico, su estado de nutrición, etc. La dosis que debe administrarse aún sigue en controversia, la dosis que recomienda Ronco puede ser aceptada, dosis más altas, de más de 40 mL/kg/h de efluente no han demostrado mejor efecto en la mortalidad, por tanto, podría administrarse una dosis de 25-35 mL/kg/h (efluente). Sin embargo, en la última revisión en este año el grupo de trabajo de Bagshaw recomienda una dosis mínima de 20-25 mL/kg/h.15 En una revisión sistemática y metanálisis realizados por Zhang y su grupo, donde buscaron la efectividad de manejo intensivo de terapia de reemplazo renal continua con dosis más altas y de mayor flujo en una población de 1803 pacientes con terapia de reemplazo renal continua, sus resultados fueron que la mortalidad no se ve afectada a pesar del aumento de la dosis.16
En otro estudio realizado por Zhang y su grupo, en el que administraron dosis de 50 a 85 mL/kg/h en 280 pacientes, no se encontraron efectos en la mortalidad a 90 días.17
En otro estudio Navas y colaboradores encontraron beneficio adicional con la terapia de reemplazo renal continua con dosis de 35 mL/kg/h.18 El mejor indicador de qué dosis administrar hasta este momento es seguir las condiciones clínicas del paciente y los resultados bioquímicos y metabólicos.8
Una vez que el paciente está en terapia intensiva y requiere terapia de reemplazo renal continua comenzaremos con los pasos básicos de su programación:
Determinar la modalidad que vamos a utilizar de acuerdo con la enfermedad.
Calcular la anticoagulación si es necesario.
Preparar la máquina con solución fisiológica 0.9% 1000 cc, si es autorizado se cebará con 5000 UI de heparina no fraccionada.
Ajustar el flujo de bomba sanguíneo, que puede iniciarse en 100 mL/min y puede incrementarse a 200 mL/min o más si se utiliza modalidad de hemofiltración venovenosa continua para poder aumentar el aclarado de la sangre o barrido de partículas que se deseen depurar. La fracción de filtración (UF/flujo sangre) debe ser menor de 25%. Por ejemplo, una cantidad de efluente de 3750 mL requerirá un flujo sangre de 250 mL/min. De manera que 250 mL/min x una hora = 15 L/h de flujo sangre, 15 L/4 = 3.75 L = 25% de flujo sangre, donde 4 representa 25% de un entero.
Elegir el líquido de sustitución, puede iniciarse con un volumen de 1000 mL/h y puede incrementarse de 500 mL/hora y aumentar hasta 4500 mL, lo que dependerá de los resultados de laboratorio de electrólitos séricos, creatinina y BUN. Este líquido depende de la modalidad a elegir o administrar una dosis de convección de 15 mL/kg/h.
Elegir el líquido de diálisis de acuerdo con las características del paciente y de acuerdo con la modalidad. Puede iniciar 0-4500 mL/h, por lo general, iniciando a 1000 mL/h o dosis de 10 mL/kg/h, de manera que al sumar la dosis de convección y dializante obtendremos 25 mL/kg/h (15 mL/kg/h + 10 mL/kg/h).
La extracción dependerá del paciente y modalidad, comenzando con 50 a 100 mL/h y utilizando hasta 2000 mL/h de ultrafiltrado.
Se recomienda solicitar estudios de laboratorio cada 6-8 horas, que incluya biometría hemática, química sanguínea, electrólitos completos, gasometrías, TTP e INR (Cuadros 5y6).8
Cuadro 5 Selección de la modalidad de acuerdo con la enfermedad a tratar
| Enfermedad | Modalidad | Programación |
|---|---|---|
| Manejo de líquidos. Oliguria. Rabdomiólisis. Eliminación de moléculas de mediano tamaño. | Hemofiltración venovenosa continua | Flujo de bomba sangre Reinyección o líquido de sustitución Ultrafiltrado Anticoagulación |
| Uremia. Solutos. | Hemodiálisis venovenosa continua | Flujo de bomba sangre Líquido de diálisis Ultrafiltrado Anticoagulación |
| Manejo de líquidos. Sepsis. Eliminación de moléculas de bajo peso molecular. Eliminación de solutos. | Hemodiafiltración venovenosa continua | Flujo de bomba sangre Líquido de sustitución o reinyección Líquido dializante o de diálisis Ultrafiltrado Anticoagulación |
| Manejo de sobrecarga hídrica, equilibrio de volumen (insuficiencia cardiaca congestiva) | Ultrafiltración lenta continua | Flujo de bomba sangre Ultrafiltrado Anticoagulación |
Cuadro 6 Principales modalidades de terapia de reemplazo renal continua y valores de programación
| Modalidad | Aclarado de urea (g/d) | Líquido de reemplazo | Dializante | Eliminación de solutos | Ultrafiltrado (mL/h) | Líquido de diálisis (mL/h) |
|---|---|---|---|---|---|---|
| Ultrafiltración lenta continua | 1-4 | No | No | Convección | 100-400 | 0 |
| Hemofiltración venovenosa continua | 22-24 | Sí | No | Convección | 500-4000 | 0 |
| Hemodiálisis venovenosa continua | 24-30 | No | Sí | Difusión | 0-350 | 500-4000 |
| Hemodiafiltración venovenosa continua | 36-38 | Sí | Sí | Convección y difusión | 500-4000 | 500-4000 |
En todos los pacientes que reciban terapia de reemplazo renal continua deben tomarse en cuenta varias situaciones especiales que son importantes para su estado durante el tiempo en que será hospitalizado en terapia intensiva, una de las situaciones debe ser la nutrición porque someterse a esta terapia puede ocasionar ciertos desequilibrios metabólicos y puede ocasionar eventos negativos en el paciente. Se recomienda que el aporte de nutrientes sea de 25-35 kcal/kg/d con 60-70% de carbohidratos y 30-40% de lípidos. Las proteínas se recomiendan a razón de 1.5-2.0 g/kg/d. Los electrólitos, como K, P y Mg requieren vigilancia; debe mantenerse a los pacientes sobre todo con concentraciones de K > 4 mEq/L (Cuadro 7), además, aportar P al líquido de sustitución, en el caso del Mg, pueden requerirse bolos intravenosos para su corrección. También debe tomarse en cuenta el aporte de vitaminas hidrosolubles, como las vitaminas del complejo B, la vitamina C y las liposolubles, como las vitaminas E, K, A y los oligoelementos.19
Cuadro 7 Recomendaciones para tratamiento de hipocalemia en terapia de reemplazo renal continua
| Concentraciones de potasio sérico (mEq/L) | Potasio a añadir (mEq/L) | mL a añadir por cada litro de líquido de sustitución | mL a añadir a cada 5 litros de líquido de sustitución |
|---|---|---|---|
| 5.5 o más | 0 | No | No |
| 4.5-5.5 | 3 | 7.5 | 37.5 |
| < 4.5 | 4 | 10 | 50 |
Las alteraciones electrolíticas tienen especial atención, así como la azoemia, que se aliviará al incrementar el flujo de reinyección y de diálisis, en cuanto a la hiponatremia, pueden añadirse soluciones de NaCl a 3%, 70 mL por bolsa de 5 L. En hipernatremia pueden administrarse soluciones glucosadas a 5% en infusión o soluciones al ½ osmolar, así como calcular la pérdida de agua. En hipocalcemia puede reponerse en forma parenteral, en hipercalcemia se cambiará el líquido de diálisis a uno libre de calcio y se deberá aumentar el dializante con bicarbonato de sodio o el líquido de sustitución.
En la hipomagnesemia deberá reponerse en forma parenteral y los valores altos de este electrólito se manejarán con incremento de bicarbonato de sodio al líquido de diálisis o aumento de la reinyección. En cuanto al fósforo, las medidas serán similares.8,20 Otra situación importante que debemos tener en cuenta en los pacientes con terapia de reemplazo renal continua es la dosificación de antimicrobianos porque durante esta terapia éstos pueden estar con dosis bajas y ocasionar fracaso en los pacientes con infección. Algunos autores recomiendan vigilar los valores de antimicrobianos en suero cuando se cuente con este método.21
Retiro de la terapia de reemplazo renal continua
Una vez que la función renal se ha recuperado, es un criterio absoluto para separar al paciente de la terapia de reemplazo renal continua, si el paciente está estable pero aún requiere sesiones de hemodiálisis para equilibrio hídrico o de solutos, se recomienda cambiar a terapia de hemodiálisis intermitente, sobre todo para disminuir costos.
Otros criterios para el retiro de la terapia de reemplazo renal continua son: 1)diuresis de 400 mL o más al día, 2)trastornos metabólicos curados, 3)no se requiere para eliminar solutos, 4)equilibrio hídrico adecuado.8,22
Terapia de reemplazo renal continua vs hemodiálisis intermitente
La terapia de reemplazo renal continua se ha convertido en una modalidad de soporte renal común en los pacientes con insuficiencia renal aguda en terapia intensiva; sin embargo, no en todos los centros hospitalarios se cuenta con esta modalidad y, por el contrario, cuentan con máquinas para hemodiálisis intermitente. No se ha encontrado diferencia de mortalidad cuando se usa terapia de reemplazo renal continua vs hemodiálisis intermitente, sólo se ha documentado mayor beneficio en pacientes inestables donde se mantiene mejor al enfermo en términos hemodinámicos, a diferencia de cuando se emplea hemodiálisis intermitente.
En el estudio de Vinsonneau y colaboradores, compararon la terapia de reemplazo renal continua vs hemodiálisis intermitente para el tratamiento de la insuficiencia renal aguda, encontraron que no existe diferencia en cuanto a una modalidad u otra, y concluyeron que la decisión de prescribir terapia de reemplazo renal continua o hemodiálisis intermitente dependerá de los recursos del centro hospitalario.23,24
Ejemplo de programación
Paciente masculino de 50 años de edad con diagnóstico de choque séptico, con peso de 80 kg con presión arterial de 90/50 mmHg, frecuencia cardiaca 100/minuto, frecuencia respiratoria 18/minuto, temperatura 37.8ºC, flujos urinarios 0.1 mL/kg/h en las últimas 8 h, con Cr de 3.0 mg/dL, presión capilar pulmonar 20 mmHg con acidosis metabólica, con equilibrio hídrico global de + 9500 mL en las últimas 48 h.
Estamos ante un paciente con una lesión renal aguda, con equilibrio positivo que se sabe condiciona mayor riesgo de mortalidad, sin poder mantener adecuados flujos urinarios y que se beneficiará de la depuración de mediadores inflamatorios por la sepsis, así como de la adecuada extracción de líquido y depuración de solutos por insuficiencia renal. De manera que elegiríamos la modalidad de hemodiafiltración venovenosa continua, que ayudará a remover moléculas de mayor tamaño, en control de líquidos y solutos a extraer. Iniciaremos con la dosis de 30 mL/kg/h, lo que da un volumen de 2400 mL, de esos 2400 mL tomaremos como ultrafiltrado o extracción la cantidad de 100 mL/h, es decir, contribuiremos al retiro de 100 mL/h para iniciar el camino hacia un equilibrio de líquidos neutro a negativo. Un líquido de diálisis de 1000 mL/h y un líquido de reinyección o reinyección de 1300 mL/h, lo que nos da como volumen final los 2400 mL calculados. El flujo se iniciará a 150 mL/min. Asimismo, se otorgará heparina para anticoagulación. Debemos recordar que este manejo es dinámico de acuerdo con las necesidades del paciente.
CONCLUSIONES
La terapia de reemplazo renal continua parece ser un procedimiento seguro y eficaz en pacientes críticamente enfermos y con inestabilidad hemodinámica que requieren hemodiálisis para mantener el equilibrio hidroelectrolítico y de sustancias que pudieran perjudicar la evolución del paciente. Esta terapia permite en forma dinámica modificar, de acuerdo con el estado clínico y bioquímico del paciente, los parámetros del equipo para obtener los resultados deseados. A pesar de que la evidencia científica no muestra resultados en la mortalidad vs la hemodiálisis convencional, sí ofrece beneficio en cuanto a la estabilidad clínica, que la convierte en una opción atractiva para este tipo de pacientes. Esta revisión incluye aspectos básicos, esteremos trabajando en una versión con conceptos y programación avanzada.











 text new page (beta)
text new page (beta)



