ANTECEDENTES
El ácido láctico constituye el producto final del metabolismo anaerobio de la glucosa y se obtiene de la reducción del ácido pirúvico en una reacción catalizada por la enzima deshidrogenasa láctica en tejidos con alta actividad glucolítica, como intestinos, músculo estriado, cerebro, piel y eritrocitos. En condiciones normales, las concentraciones de ácido láctico se mantienen bajas (menores a 2 mEq/L) debido a su metabolismo constante a través de la gluconeogénesis o su oxidación por el ciclo de Krebs en órganos como el hígado y los riñones.1 La acidosis láctica es una acidosis metabólica debida a la acumulación de ácido láctico, caracterizada por un pH menor de 7.35, anión gap elevado y lactato en sangre mayor de 4 mEq/L. Las causas pueden estar relacionadas con la sobreproducción de ácido láctico (acidosis láctica tipo A) o disminución en su metabolismo (acidosis láctica tipo B). Es una de las principales causas de acidosis metabólica en pacientes hospitalizados y, por otro lado, el lactato constituye un biomarcador específico para estratificar y predecir el riesgo de muerte en pacientes en estado crítico, ya que traduce el grado de disfunción orgánica en estos pacientes.1,2 Comunicamos un caso raro de acidosis láctica mixta persistente secundaria a choque séptico, metformina y múltiples infartos hepáticos debido a trombosis espontánea de la arteria hepática.
CASO CLÍNICO
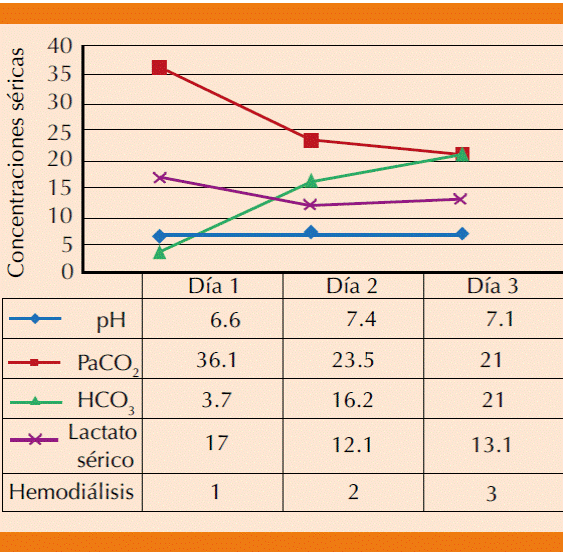
Paciente femenina de 72 de edad con antecedentes heredofamiliares de diabetes mellitus 2. Diagnóstico de diabetes mellitus 2 de 17 años de evolución con tratamiento regular con metformina 850 mg cada 12 horas, glibenclamida 5 mg cada 12 horas y con aparentemente buen control metabólico. Ingresó al servicio de Urgencias por dolor abdominal tipo cólico, evacuaciones diarreicas sin moco ni sangre, fiebre no cuantificada, ataque al estado general y somnolencia de tres días de evolución. A la exploración física se encontró confusa y somnolienta, con signos clínicos de deshidratación, taquicárdica, taquipneica, con hipotensión arterial y oliguria. El abdomen se encontraba globoso, con peristalsis presente, doloroso a la palpación en forma generalizada y sin datos de irritación peritoneal. En los exámenes de laboratorio de ingreso se documentó leucocitosis con neutrofilia y ban-demia, además de cifras elevadas de creatinina sérica y urea, hipercalemia, acidosis metabólica de anión gap elevado e hiperlactatemia (Cuadro 1). El abordaje diagnóstico se complementó con una tomografía axial de abdomen, en la que no se evidenció una causa orgánica del dolor abdominal y tampoco se observaron datos de isquemia intestinal (Figura 1). Se integraron los diagnósticos de sepsis grave con foco infeccioso gastrointestinal, daño renal agudo AKIN 3 secundario a necrosis tubular aguda con criterios dialíticos de urgencia, además de acidosis láctica grave secundaria a choque séptico y metformina. A su ingreso la paciente tuvo insuficiencia respiratoria que requirió ventilación mecánica y recibió tratamiento temprano basado en metas para pacientes con sepsis y choque séptico con soluciones cristaloides intravenosas, antibiótico intravenoso con piperacilina/tazobactam ajustados a la función renal, bicarbonato intravenoso, infusión de norepinefrina a dosis elevadas y tratamiento hemodialítico con sesiones de hemodiálisis intermitentes prolongadas. La evolución clínica durante las primeras 48 horas de tratamiento fue satisfactoria; con mejoría del estado ácido-base y de la cifra de presión arterial media que permitió la disminución progresiva hasta dosis mínimas del vasopresor, así como disminución en los marcadores inflamatorios procalcitonina y proteína C reactiva. Sin embargo, posterior a 48 horas de tratamiento la paciente persistió con concentraciones elevadas de lactato en sangre a pesar de tres sesiones de hemodiálisis, cifras de presión arterial media por arriba de 65 mmHg con dosis mínima de vasopresor y pruebas de funcionamiento hepático dentro de límites normales (Figura 2). Se agregó dobutamina al tratamiento y como parte del reabordaje diagnóstico de la hiperlactate-mia persistente se realizó una TAC de tórax y abdomen que documentó múltiples y extensos infartos hepáticos secundarios a trombosis de la arteria hepática (Figura 3). La paciente tuvo disfunción orgánica múltiple resistente a tratamiento médico y finalmente falleció al cuarto día de hospitalización.
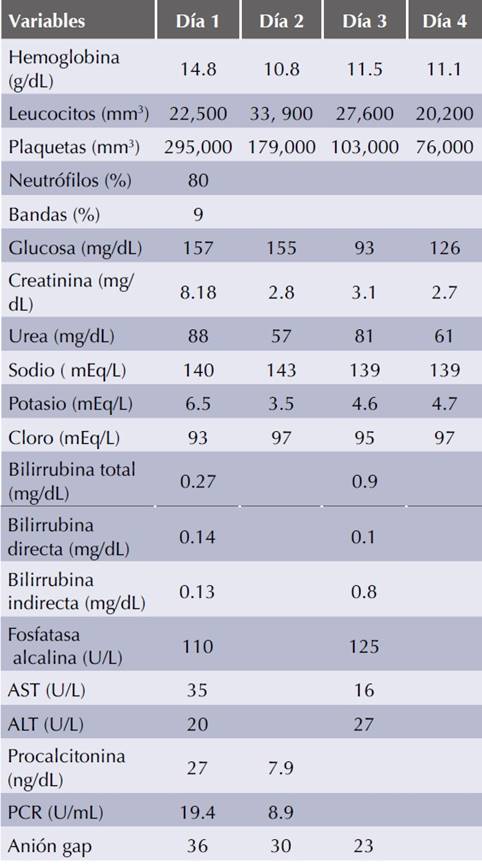
AST: aspartatoaminotransferasa; ALT: alaninoaminotransfe-rasa; PCR: proteína C reactiva.
Cuadro 1 Evolución de los parámetros de laboratorio
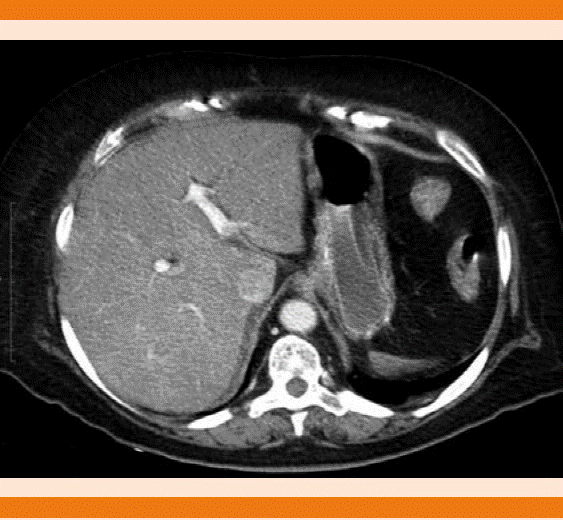
Figura 1 Imagen axial de tomografia computada con contraste en fase venosa portal que demuestra la adecuada perfusión hepática sin evidencia de zonas de isquemia o infartos hepáticos.
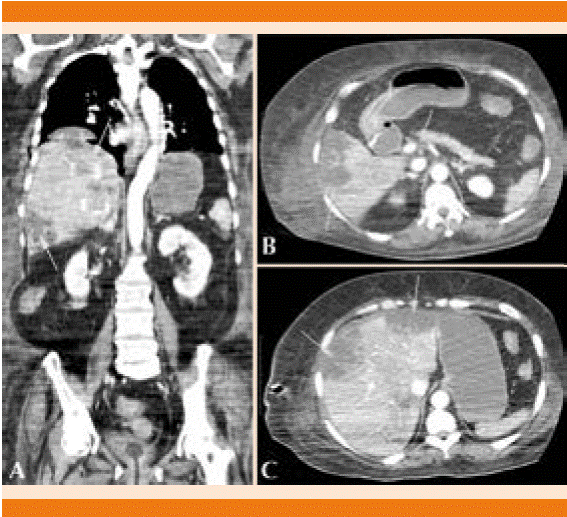
Figura 3 Imágenes de tomografía computada con contraste. A. Múltiples zonas hipoatenuantes que no realzan con el material de contraste. B. Imagen axial en fase arterial que muestra oclusión parcial del tronco celiaco que se extiende hacia la arteria hepática, además de múltiples zonas hepáticas hipocaptantes a nivel periférico con realce ausente. C. Parénquima hepático con múltiples zonas hipoatenuantes, en regiones periféricas, con realce ausente.
DISCUSIÓN
La acidosis láctica es una acidosis de anión gap elevado debida a la acumulación de lactato y protones en el líquido corporal. Esta acumulación puede ser el resultado del incremento en la producción (acidosis láctica tipo A) de lactato, la disminución en su metabolismo (acidosis láctica tipo B) o la combinación de ambos mecanismos, como en el caso que comunicamos. La acidosis láctica típicamente afecta a pacientes con estado de choque, que se caracteriza por el aporte de oxígeno a los tejidos de manera insuficiente para cubrir sus demandas metabólicas. En estas condiciones de hipoxia tisular global o localizada, el flujo metabólico de la vía glucolítica se incrementa y ocasiona acumulación del piruvato. Sin embargo, éste no es incorporado al ciclo aerobio de Krebs en las mitocondrias, desviando su metabolismo hacia la conversión en ácido láctico, aumentando el lactato intracelular y su liberación hacia la sangre.1,2
El tratamiento de la acidosis láctica tipo A va encaminado a restablecer y mantener la estabilidad hemodinámica, mejorar la oxigenación tisular y el estado ácido base, acompañado del tratamiento específico de la causa. Las metas de la reanimación inicial son: mantener la presión arterial media entre 65 y 70 mmHg, mantener la presión venosa central entre 8 y 12 mmHg y diuresis >0.5 mL/kg/h. Para alcanzar estas metas de reanimación en la mayoría de los casos es necesario administrar vasopresores, inotrópicos o ambos. Sin embargo, la administración de dosis elevadas de catecolaminas puede agravar la hiperlactatemia debido a la reducción en la perfusión tisular y la sobreestimulación del receptor β2 adrenérgico. Asimismo, estas medidas deberán acompañarse de acciones que garanticen el aporte adecuado de oxígeno a nivel tisular, como son: mantener una cifra de hemoglobina >7 g/dL, mantener saturación venosa de oxígeno de la vena cava superior de 70% o saturación de oxígeno venosa mixta de oxígeno de 65% mediante transfusiones sanguíneas, el aporte de oxígeno suplementario y, en caso necesario, con apoyo ventilatorio.1-3
El mejoramiento del estado ácido-base constituye una parte fundamental en los pacientes con acidosis láctica. En este sentido, la administración de bicarbonato en pacientes con acidosis es controvertida, porque algunos modelos experimentales y observaciones clínicas sugieren que la administración de bicarbonato puede deprimir la función cardiaca debido a la disminución del calcio y puede exacerbar la acidosis a nivel intracelular debido a la acumulación de dióxido de carbono.4,5 Asimismo, en el contexto de acidosis metabólica y daño renal, la terapia con bicarbonato intravenoso puede verse complicada con sobrecarga de volumen, hipernatremia y alcalosis de rebote una vez que la acidosis se ha resuelto.2 En el caso específico de acidosis láctica, se ha demostrado que la administración de bicarbonato aumenta la producción neta de lactato.6 Sin embargo, en casos de acidemia grave (pH<7.2), como en el caso de nuestra paciente, se recomienda la administración de bicarbonato intravenoso para mejorar el estado ácido-base, debido a los efectos sistémicos nocivos de la acidemia grave, aunque el beneficio en la mortalidad y parámetros hemodinámicos de esta medida no se ha demostrado.7
La hemodiálisis constituye otra medida terapéutica para pacientes con acidosis láctica, debido a su capacidad de depuración de lactato y la posibilidad de aportar bicarbonato lentamente, sin el riesgo de disminuir la concentración del calcio ionizado. Esta ventaja de la hemodiálisis previene la depresión miocárdica durante la corrección de la acidosis, además de prevenir la sobrecarga hídrica e hiperosmolaridad que frecuentemente ocurren en pacientes con acidosis tratados con bicarbonato intravenoso. La hemofiltración y la terapia de reemplazo renal continua constituyen en la actualidad las modalidades dialíticas recomendadas para el tratamiento de pacientes con acidosis láctica, ya que la tasa de aporte de bicarbonato en estas modalidades es más lenta en comparación con las modalidades intermitentes y son mejor toleradas por los pacientes con inestabilidad hemodinámica.2,8 Sin embargo, se ha demostrado que la tasa de depuración de lactato alcanzada con estas modalidades dialíticas es menor a la tasa de generación de lactato en pacientes críticamente enfermos. Asimismo, la hemodiálisis en el caso específico de acidosis láctica secundaria a la administración de metformina, como en nuestra paciente, tiene utilidad terapéutica adicional porque permite la eliminación de la metformina de manera efectiva.9,10
La metformina es una biguanida prescrita para el tratamiento de la diabetes mellitus tipo 2 debido a su bajo costo, perfil de seguridad y beneficio cardiovascular. Tiene biodisponibilidad de 50 a 60% en el intestino, no se une a proteínas plasmáticas, con vida media de 6 horas y 90% se elimina sin metabolizar por vía renal en 24 horas. La metformina altera la depuración del lactato a nivel hepático por inhibición del complejo I de la cadena respiratoria mitocondrial. Disminuye la actividad de la piruvato deshidrogenasa y el transporte mitocondrial de electrones, lo que condiciona la activación del metabolismo anaerobio y el paso de piruvato a lactato.11 Su administración está contraindicada en situaciones clínicas que predisponen la aparición de acidosis láctica como: alcoholismo, insuficiencia cardiaca, insuficiencia respiratoria, hepatopatía y daño renal. Sin embargo, la verdadera incidencia de acidosis láctica secundaria a la administración de metformina se desconoce. Los autores de dos excelentes revisiones sistemáticas recientemente publicadas respecto al tema concluyeron que hasta la fecha no existen datos consistentes de la asociación entre la administración de metformina y la acidosis láctica. Los autores revisaron más de 347 estudios que incluyeron 70,490 pacientes-años tratados con hipoglucemiantes. No encontraron diferencias en el riesgo de acidosis láctica, la incidencia fue de 4 casos por 100,000 pacientes-años en pacientes tratados con metformina y de 5 casos por 100,000 pacientes-años en pacientes tratados con otros hipoglucemiantes. La evidencia actual de asociación entre la administración de metformina y el riesgo de acidosis láctica proviene de más de 300 casos de acidosis láctica. Sin embargo, como en el caso que comunicamos, todos estos casos reportados han sido pacientes con alguna afección médica aguda y grave concurrente, como sepsis, choque, insuficiencia cardiaca congestiva, insuficiencia hepática y daño renal, que enmascaran la asociación fisiopatológica entre metformina y acidosis láctica en estos contextos clínicos.12,13
La concentración inicial de lactato y su depuración durante el curso del proceso patológico ha demostrado ser un biomarcador específico para la estratificación y predicción del riesgo de muerte en pacientes críticamente enfermos. Estudios clínicos han demostrado de manera consistente que incluso una medición elevada de lactato en sangre en forma aislada se asocia con resultados adversos y que la hiperlactatemia persistente se asocia con aumento significativo en la mortalidad, sobre todo con concentraciones de lactato >4 mmol/L; independientemente del estado del paciente en relación con choque o hipotensión arterial.1,14
El tratamiento de la acidosis láctica de tipo B está dirigido a la corrección de la causa específica que condiciona la acidosis. En el caso que comunicamos, las medidas terapéuticas consistieron en la suspensión de la metformina y su eliminación con el tratamiento hemodialítico. Sin embargo, la hiperlactatemia persistente a pesar del tratamiento dialítico y la corrección del estado de choque nos obligó a descartar otras causas de acidosis láctica; en la tomografía computada abdominal de control se evidenciaron múltiples y extensos infartos hepáticos secundarios a trombosis de la arteria hepática no observados en la tomografía de ingreso. La trombosis de la arteria hepática constituye una complicación frecuente en pacientes con trasplante hepático y sobreviene como una complicación poco frecuente en pacientes sometidos a procedimientos intraabdominales invasivos. Sin embargo, la trombosis espontánea de la arteria hepática en pacientes sin estos antecedentes constituye una complicación extremadamente rara, con pocos casos reportados en la bibliografía médica. En este contexto clínico, las principales causas reportadas han sido la existencia de un estado procoagulante primario, cáncer y sepsis. En nuestro caso, consideramos que el origen de esta complicación fue multifactorial, como las potenciales causas destacan la sepsis, deshidratación, síndrome urémico, choque, hipoperfusión tisular y la administración de dosis elevadas de vasopresores. Asimismo, los infartos hepáticos múltiples constituyen una manifestación clínica rara de la trombosis de la arteria hepática debido al doble sistema de irrigación del hígado.15-17
CONCLUSIONES
La acidosis láctica es una acidosis de anión gap elevado debida a la acumulación de lactato y generalmente asociada con mal pronóstico desde el punto de vista clínico. Los infartos hepáticos múltiples y extensos debidos a trombosis espontánea de la arteria hepática constituyen una causa rara de acidosis láctica persistente y una complicación poco frecuente en pacientes críticamente enfermos.











 nueva página del texto (beta)
nueva página del texto (beta)