Introducción
Existen muchas causas por las que un recién nacido o un lactante pueden requerir una ileostomía de forma temporal.1,2,3Después de controlar el cuadro agudo o descartar ciertas afecciones puede plantearse la restitución del tránsito intestinal.
En general, los niños con ileostomía crecen más lentamente4,5 y, con frecuencia, la diferencia de calibre entre los cabos proximal y distal demanda una cirugía con mayores dificultades técnicas, por la atrofia del segmento disfuncional, lo que puede tener mayor morbilidad en el posoperatorio.5
Objetivo
Exponer y describir una técnica de realimentación en niños con ileostomía que permite aumentar la curva de crecimiento y disminuir las dehiscencias anastomóticas y dermatitis posoperatoria.
Material y métodos
Estudio retrospectivo de serie de casos de pacientes con ileostomía tratados con la técnica de realimentación de estoma distal, previa a la restitución del tránsito intestinal, atendidos durante el año 2014. El protocolo se inició con un ileograma que descartó cualquier tipo de obstrucción mecánica desde el estoma disfuncional hasta el ano (Figura 1). En los niños con derivación, pero sin una causa de obstrucción anatómica clara, también se tomó una biopsia rectal incisional para descartar enfermedad de Hirschsprung. Después del alta hospitalaria, y en las primeras consultas posoperatorias, se inició la capacitación a los familiares en la técnica. La descripción es la siguiente: el familiar que cuida al paciente debe tomar la materia fecal de la bolsa del estoma proximal, mezclarla con 50 mililitros de solución salina al 0.9% y colar la mezcla. El líquido obtenido se introduce a través de una sonda Foley (16 French) que se coloca en el estoma distal, con el globo mínimamente inflado. Con una jeringa de 20 mL a infusión lenta, a razón de 3 mL por minuto, este procedimiento debe efectuarse tres veces al día (Figura 2). Como parte del protocolo de la realimentación se les indica que para la dilución de la fórmula láctea debe utilizarse solución salina al 0.9% y loperamida a dosis inicial de 0.5 hasta 4 mg cada 6 horas.
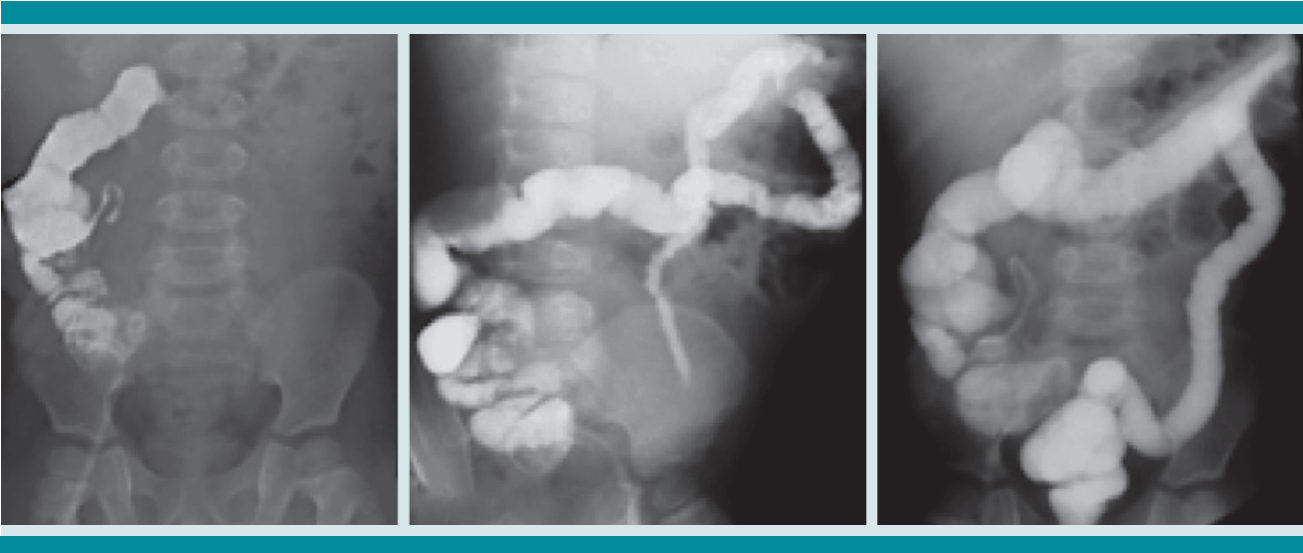
Figura 1 Imágenes de ileograma distal previas al inicio de la realimentación para demostrar la permeabilidad del intestino.

Figura 2 Pasos de la realimentación. A) Colocación de la materia fecal mezclada con suero salino fisiológico y colada en un recipiente. B) Lubricación de la sonda Foley. C) Colocación de la sonda Foley en el estoma distal e inflación del globo. D) Infusión lenta de la mezcla a través de la sonda.
Se revisó el padecimiento que condicionó la derivación en los pacientes; edad y peso al inicio de la realimentación, curva de ganancia ponderal, duración de la realimentación, hallazgos macroscópicos de la cirugía del cierre de la ileostomía y las repercusiones posoperatorias.
Resultados
De los 7 pacientes estudiados, 4 tuvieron atresias intestinales (uno de los casos asociada con gastrosquisis); 1 sospecha de enfermedad de Hirschsprung que se descartó; otro enterocolitis y el restante sufrimiento intestinal posinvaginación. La media de edad gestacional al nacimiento fue de 35 semanas (rango 28-39) y una mediana de peso al nacimiento de 2 kg (rango 1.9-3.5). La cirugía que motivó la derivación se efectuó a una mediana de 3 días de vida (rango 1 día-6 meses de vida). Esto debido a que los pacientes con obstrucción intestinal neonatal (atresia intestinal, gastrosquisis, enterocolitis necrotizante) se operaron en los primeros días de vida, mientras que el paciente con sospecha de enfermedad de Hirschsprung y el paciente con invaginación intestinal se operaron a edades más tardías (2 meses y 6 meses, respectivamente). Los niños iniciaron la realimentación a una edad media de 5 meses de vida (rango 2 a 7 meses), 4 meses en promedio después del procedimiento quirúrgico inicial (rango 2 a 6 meses). Al inicio de la realimentación el peso medio fue de 4.4 kg (rango 1.7-7.7 kg). La ganancia ponderal fue de 0.7 kg al mes, en promedio, con un rango de 0.36 hasta 1.4 kg al mes. La realimentación permaneció entre 1 y 6 meses, con una media de entre 3 y 4 meses.
No hubo complicaciones relacionadas con el procedimiento de realimentación por el estoma distal. La cirugía de restitución del tránsito intestinal se efectuó en todos los casos mediante una incisión en huso periestomal, previo cierre de los estomas con seda 3/0. No se encontró desproporción entre los cabos intestinales a anastomosar. En todos los casos se realizó una anastomosis término-terminal manual en dos planos (primer plano, cara posterior, puntos simples totales vicryl 5/0 y cara anterior puntos simples totales invertidos vicryl 5/0; segundo plano, puntos simples seromusculares seda 5/0) y cierre de brecha de meso con surgete vicryl 5/0. Se llevaron a cabo cinco anastomosis ileoileales y dos anastomosis ileocólicas. En todos los pacientes se dejó un drenaje intraabdominal (penrose o blacke).
Cinco de los pacientes iniciaron con tránsito intestinal a las 48-72 horas de la cirugía, con alimentación al cuarto día posoperatorio. Una de las pacientes (la niña con diagnóstico de gastrosquisis) tuvo clínica de obstrucción intestinal y se volvió a operar al sexto día posoperatorio: la anastomosis estaba íntegra, pero con bridas firmes, quizá por su enfermedad de base, y se realizó bridolisis. Otro de los pacientes tuvo tránsito al tercer día posoperatorio, con inicio de la alimentación, pero con fiebre y salida de material purulento por el drenaje intraabdominal; después inició con un cuadro de obstrucción intestinal. Se decidió reoperar y el hallazgo transoperatorio fue un absceso intraabdominal que condicionaba la adherencia de un asa. La anastomosis intestinal estaba íntegra. Se realizó bridolisis y drenaje del absceso. A las 48 horas el paciente tuvo tránsito intestinal y se reanudó la tolerancia enteral a los 4 días posoperatorios.
Ninguno de los pacientes tuvo dermatitis perianal posoperatoria. Luego de un tiempo de seguimiento medio de dos años (rango 21 a 29 meses), una paciente falleció debido a una complicación de su prematuridad. El resto de los pacientes sigue con una curva de ganancia ponderal y de talla normal para su edad, comiendo y evacuando adecuadamente.
Discusión
La derivación intestinal es una operación que puede ser necesaria en casos de obstrucción intestinal anatómica o funcional.1,2,3 En nuestros pacientes, la causa más frecuente fue la atresia intestinal; no se consideró apropiada la anastomosis primaria y el cirujano optó por una derivación de dos cabos, lo que nos parece una opción adecuada. La derivación intestinal ideal debe efectuarse con un estoma proximal maduro (aproximadamente 1 cm de altura), en un lugar amplio de piel donde la bolsa pegue adecuada mente y con una fístula mucosa distal para evitar el prolapso, permitir mejor adherencia de las bolsas y la realización de estudios o realimentación por la misma, separada unos 3-4 cm del estoma proximal.6 En nuestros pacientes con atresia intestinal el grupo del Centro Colorrectal para Niños siempre efectúa como primera opción una ileostomía tipo Santulli.7 Consideramos que esta opción quirúrgica es la mejor para los pacientes, porque el proceso de realimentación se lleva a cabo de manera fisiológica; por lo tanto, los padres no tienen que realizarlo.
En 2014 se efectuaron cinco ileostomías tipo Santulli, todas con evacuaciones por el ano al tercer día posoperatorio, que se cerraron en un procedimiento quirúrgico de 1 hora de duración, con tránsito a las 48 horas de la cirugía, con estancia hospitalaria media de 4 días y sin complicaciones posoperatorias ni dermatitis perianal.
Se recomienda no realizar derivaciones intestinales tipo Hartmann, porque esta derivación no permite irrigar o realimentar el cabo distal ni efectuar estudios distales para comprobar la permeabilidad.6 En 2014 hicimos un cierre de ileostomía, tipo Hartmann, en un paciente con obstrucción intestinal funcional, en el que se descartó enfermedad de Hirschsprung y la desproporción entre cabos fue de 3:1, con colon distal desfuncionalizado. La anastomosis fue de mayor riesgo, con una importante dermatitis perianal durante varias semanas después de la cirugía.
Otras situaciones en las que fue necesaria la ileostomía en nuestros pacientes fue la enterocolitis necrotizante, invaginación intestinal y sospecha de enfermedad de Hirschsprung. En los dos primeros casos los hallazgos intraoperatorios de la primera cirugía justificaban una ileostomía, uno por perforación en un paciente prematuro y otro por importante sufrimiento intestinal del íleon terminal luego de la desinvaginación por taxis. En el tercer caso, ante la ausencia de un padecimiento anatómico que explicara la obstrucción intestinal, se recomendó la toma de biopsia rectal incisional para descartar enfermedad de Hirschsprung. Preferimos la biopsia incisional a la biopsia con pistola de succión, porque en lactantes esta última puede aportar poco material, insuficiente para el diagnóstico.8
A todos los pacientes, previo inicio de la realimentación, se efectuó un estudio contrastado a través del estoma distal, al igual que todos los grupos que optan por la realimentación.
Debe comprobarse la permeabilidad desde el estoma hasta el ano, descartando obstrucciones y estenosis. En caso de una posible zona de transición compatible con enfermedad de Hirschsprung, también se recomienda la toma de biopsia rectal incisional.
La realimentación se utilizó por primera vez en 198312 y sus ventajas son amplias:13 previene la atrofia del intestino distal y aumenta la capacidad de absorción, lo que permite mayor ganancia ponderal, y el tamaño del intestino.9,10,14 Ambos procesos facilitan la anastomosis que se realizará al cerrar la derivación.5,9,10,13
Algunos grupos han utilizado la técnica en el posoperatorio inmediato, porque está descrito que, con frecuencia, los neonatos con enterostomías tienen síndrome de intestino corto y alto riesgo de pérdida de electrólitos y de líquidos con escasa ganancia ponderal.10 Está demostrado que al aumentar la capacidad de absorción del segmento distal de intestino, mediante la realimentación, se reducen los requerimientos de nutrición parenteral total,9,11 es posible eliminar la colestasis estimulando la circulación entero-hepática,9,13 controlar la pérdida de líquidos, corregir el desequilibrio electrolítico y aumentar la ganancia ponderal.5 Nuestros pacientes no requirieron ser realimentados durante el internamiento, quizá porque sus ileostomías eran muy distales. Pensamos que la realimentación temprana puede ser muy útil en pacientes con derivaciones altas donde estos problemas se agravan. Otra ventaja es que se evita la colitis por derivación:14 la estasis fecal o de moco en el intestino distal aislado promueve la proliferación bacteriana, lo que provoca absorción de toxinas, colitis y ulceración y condiciona de manera refleja una diarrea secretora en la ileostomía, lo que resulta en mayor pérdida de líquidos y mayor desequilibrio electrolítico.15 La realimentación evita la proliferación bacteriana porque mantiene el tránsito intestinal con una digestión y absorción fisiológica hasta llegar a la defecación.10
Existen muchas técnicas descritas para la realimentación5,9,10,11,12,13,14,16, pero, en general, son complejas, con introducción de múltiples sondas y, en ocasiones, con materiales de infusión o protectores para la piel costosos. Nuestro protocolo es sencillo, barato y fácilmente reproducible por los padres. No utilizamos sonda para extraer la materia fecal, si no que ésta se toma de la bolsa de ileostomía tres veces al día.
Pataki y col17 reportan la posibilidad de complicaciones sépticas al realimentar con el contenido de la bolsa de colostomía, debido al hallazgo de mayor proporción de colonias bacterianas en los cultivos de muestras fecales cuanto mayor es el tiempo de estasis. En nuestros pacientes no hubo complicaciones. Por el contrario, observamos que la realimentación promueve evacuaciones más espesas por el estoma proximal y menores alteraciones hidroelectrolíticas, debido a la prevención de la colitis por derivación.14 La materia fecal se mezcla con solución salina fisiológica, se cuela, y éste es el material con el que se efectúa la realimentación. Los pacientes con ileostomía tienen riesgo de pérdida total del sodio corporal, lo que se asocia con falla en el crecimiento.4 En la preparación de material con solución salina fisiológica se aportan suplementos de sodio, lo que se ha correlacionado con aumento de peso en los pacientes con ileostomía.4 El hecho de realimentar con la materia fecal colada evita que se obstruya la luz de la sonda. El material de realimentación se introduce por el estoma distal con una sonda Foley 16 Fr. La colocación inicial de la sonda debe efectuarla el cirujano; posteriormente se le enseña al familiar cómo inflar el balón de la sonda Foley con la cantidad precisa de agua, que impida fugas de la materia fecal, que no provoque sufrimiento del estoma, porque podría ocasionarle perforaciones.18 Ni en nuestro grupo ni en revisiones de otros grupos se ha observado esta complicación.13,19 Después de inflar el globo de la sonda Foley ésta se tracciona ligeramente para que el globo haga un tapón y evite la salida del material. La infusión debe hacerse lentamente, el material de realimentación debe tardar en pasar alrededor de 10 minutos. Todos nuestros pacientes tuvieron evacuaciones formadas por el ano en las primeras 48-72 horas posoperatorias.
En nuestro protocolo asociamos otras dos medidas: recomendamos la preparación de la fórmula en solución salina fisiológica, para aumentar el aporte de sodio en estos pacientes4 y, la segunda, agregamos la administración de loperamida para conseguir evacuaciones más formadas por la ileostomía, sin haber encontrado ningún efecto adverso.20
Con todas estas medidas hemos obtenido ganancias ponderales previas al cierre de entre 0.36 hasta 1.4 kg al mes (promedio 0.7 kg al mes), mejores que las de otras series9,11,14, lo que ha permitido operar niños más grandes, con mayor peso y mejor perfil nutricional. El cabo distal creció considerablemente, pasando de ser un segmento disfuncionalizado, en los casos de atresia intestinal, a tener un calibre similar al del intestino funcional. No tuvimos ninguna dehiscencia de anastomosis. Pensamos que la similitud de calibre de los cabos disminuyó la posibilidad de que el edema característico de la anastomosis obstruyera la luz del segmento distal y condicionara aumento retrógrado de la presión, lo que podría provocar dehiscencias anastomóticas. Dos pacientes necesitaron reoperación por obstrucción intestinal, ninguna de ellas secundaria a complicación de la anastomosis intestinal ni a la técnica de la realimentación.
Ninguno de nuestros pacientes tuvo dermatitis perianal. Después de una anastomosis intestinal, con un segmento distal disfuncionalizado, hasta que éste recupere su capacidad de absorción, el número de movimientos intestinales a lo largo de un día será alto y de características muy líquidas.15 Esta dermatitis es dolorosa, tanto como una quemadura de segundo grado, difícil de tratar y con gran afectación de la calidad de vida del paciente,15 hasta que el colon recupere su función de absorber agua y electrólitos11 y esta condición mejore.15 La realimentación previene la atrofia del intestino distal y aumenta su capacidad de absorción,9,10,14, lo que permite evacuaciones pastosas y formadas en una piel perineal ya preparada para el contacto con las heces.
Conclusión
La realimentación es una técnica fácil, segura y barata para recuperar la capacidad de absorción del segmento intestinal aislado en niños con ileostomía. La realimentación permite aumentar la ganancia ponderal del paciente, evitar la atrofia del segmento intestinal, disminuir la pérdida de líquidos y electrólitos y preparar el intestino distal para la futura anastomosis. El protocolo de realimentación intestinal aquí expuesto es reproducible y hemos conseguido buenos resultados pre, trans y posoperatorios. Consideramos que todo paciente con dos estomas e intestino distal residual disfuncional puede beneficiarse con esta técnica. El estudio efectuado tiene limitaciones porque es retrospectivo y no contó con casos controles, ni con poder estadístico; a pesar de ello, y con base en nuestra experiencia, la técnica es útil, con ventajas en la preparación de los pacientes con ileostomía que serán operados para restitución del tránsito intestinal.











 nueva página del texto (beta)
nueva página del texto (beta)


