INTRODUCCIÓN
En América Latina, en el 2010, la incidencia de enfermedad renal fue de 2.6 a 15.8 casos por cada millón de habitantes en menores de 15 años. En el 2012, en México, la incidencia fue de 3.5 por cada millón de habitantes menores de 15 años1 y cada año se diagnostican 100 mil casos de insuficiencia renal, donde 12 mil de los detectados están en etapa terminal y sólo un 30% son candidatos a trasplante renal.1
Una vez que el paciente inicia una terapia de sustitución (diálisis o hemodiálisis) se inicia también un deterioro nutricio con una pérdida de nutrimentos, principalmente aminoácidos, albúmina, vitaminas hidrosolubles y carnitina.2 El desarrollo de anemia normocítica y normocrómica es una complicación en los pacientes con insuficiencia renal crónica,3 que se trata con eritropoyetina humana recombinante;4 sin embargo, muchos pacientes siguen presentando baja respuesta a pesar del tratamiento adecuado con hierro.3,4 Varios estudios han demostrado que la suplementación con carnitina en pacientes con insuficiencia renal crónica evita las complicaciones cardiológicas, mejora la sintomatología muscular, la hipotensión intradialítica y la frecuencia de anemia que no mejora con la eritropoyetina humana recombinante.5 En 1999, la Food and Drug Administration aprobó el empleo de L-carnitina en pacientes con desordenes dialíticos y para mejorar la respuesta a la administración con eritropoyetina humana recombinante.6 En 2011 México la autorizó ante la Comisión Federal para la Protección contra Riesgos Sanitarios.7
La carnitina es una amina cuaternaria, soluble en agua, no unida a albúmina, la isoforma levo es biológicamente activa, mejor conocida como Lcarnitina, cuya importancia radica en su función principal en el metabolismo de los ácidos grasos y en la producción de energía.8 El mecanismo es que la L-carnitina transporta los ácidos grasos que se encuentra en el citosol de la célula, para que puedan entrar a la matriz mitocondrial y así comenzar el proceso de β oxidación de los ácidos grasos y obtener acetilcoenzima (CoA) y producir energía a través del ciclo de krebs.9 La principal función de la L-carnitina es la producción de energía, principalmente en riñón, hígado, cerebro y músculo esquelético, así como la de actuar como antioxidante, al reducir la peroxidación lipídica y, por ende, reduce el daño potencial a la membrana celular durante el estrés oxidativo.8
La L-carnitina se filtra libremente por la membrana glomerular y se reabsorbe por el túbulo proximal a través de un catión orgánico, con un aclaramiento renal de 1-3 mL/min. En contraste, durante la hemodiálisis (100 mL/min), la L-carnitina se disminuye en el plasma aproximadamente en un 80% al final de cada sesión.10 Esta reducción en el plasma se debe a que la síntesis endógena se ve alterada durante la hemodiálisis, así como a la deficiencia de algunos cofactores (vitamina B6, niacina, vitamina C y hierro) que son necesarios en la ruta enzimática encargada de sintetizar carnitina.10
La L-carnitina podrían influir en la respuesta a la eritropoyetina humana recombinante, al participar en los procesos de desacilación y reacilación que permiten remodelar membranas de fosfolípidos en los eritrocitos, por ende, la estimulación de la eritropoyesis en altas concentraciones (>200 mmol/L) genera un incremento en la sobrevida de los eritrocitos al reducir el estrés oxidativo.11
Hurot JM y sus colaboradores, en una revisión sistemática sobre la utilidad de la L-carnitina en pacientes con insuficiencia renal crónica con hemodiálisis, no encontraron un beneficio con la suplementación de L-carnitina sobre los niveles de triglicéridos y colesterol, pero sí observaron una mejora en los niveles de hemoglobina y una menor dosis de eritropoyetina humana recombinante.8
Otros estudios demostraron que la suplementación con L-carnitina en adultos, durante seis meses, mejoró la osmosis de la membrana celular de los eritrocitos.9 Se conoce que la L-carnitina tiene una función importante en el tratamiento de pacientes con insuficiencia renal crónica, para disminuir la anemia, ya que la hemólisis ocurre exclusivamente en pacientes con bajos niveles séricos de carnitina.10 En el estudio realizado por Aoun y su grupo a seis pacientes pediátricos con hemodiálisis, les fue administrada L-carnitina intravenosa (2.5 g por sesión para los pacientes de más de 30 kg y un 1 g para los que presentaron un peso menor a 30 kg) durante 9 meses. Al finalizar los estudios los niveles de hemoglobina aumentaron y disminuyeron los requerimientos de eritropoyetina humana recombinante, sin efectos secundarios.11
OBJETIVO
Por la evidencia ya mencionada y a la necesidad de contar con esquemas y opciones de tratamiento que mejoren y optimicen el estado nutricio y el pronóstico de la insuficiencia renal crónica en el paciente pediátrico, se realizó este estudio en un hospital público de León, Guanajuato, donde se buscó probar la hipótesis de que la suplementación con L-carnitina en pacientes pediátricos hemodializados lograba una mejoría en los marcadores bioquímicos (hemoglobina, albúmina, colesterol, triglicéridos, creatinina) y antropométricos (peso seco e índice de masa corporal).
MATERIAL Y MÉTODOS
Se realizó un estudio de reporte de casos, analítico y longitudinal, durante tres meses, en el área de hemodiálisis pediátrica de la unidad médica de alta especialidad de Gineco/Pediatra del IMSS, número 48, de la ciudad de León, Gto. Se incluyeron a 25 pacientes (casos) por simple disponibilidad, cuyos criterios de inclusión fueron: pacientes pediátricos entre 3 y 16 años de edad, ambos sexos, con diagnóstico de insuficiencia renal crónica, en tratamiento con hemodiálisis. No se incluyeron a pacientes con sepsis, candidatos a trasplante o que estuvieran recibiendo L-carnitina al momento o dos meses previos al estudio. Se excluyeron a los participantes que fallecieran o que presentaran en el transcurso alguna complicación grave relacionada a su padecimiento, así como el desarrollo de sepsis y hemorragias.
Una vez que los padres aceptaron y firmaron el consentimiento informado de sus hijos, se procedió a evaluar el estado nutricio, con lo que se obtuvieron los indicadores antropométricos, al inicio y a los tres meses, de la suplementación con L-carnitina; las mediciones se realizaban al término de las sesiones de hemodiálisis. Se obtuvo el peso seco, utilizando una báscula de marca Torino®, con precisión de 100 g. Para la estatura se utilizó un infantómetro marca Seca®, precisión 0.1 cm, para los niños que tuvieran menos de un metro; mientras que para los mayores de un metro la medición se realizó por medio de un estadímetro de la marca Seca®, con una precisión 0.1 cm.12 Con el peso y talla se obtuvo el índice de masa corporal y los valores se interpretaron con las tablas de percentiles para niñas y niños, así como las de referencia para adolescentes de 2 a 20 años, de los Centers for Disease Control and Prevention. Para el pliegue cutáneo tricipital (PCT) la medición se realizó por duplicado utilizando el plicómetro Lange®, con una precisión de 1 mm. Se midió la circunferencia del brazo (CB) con una cinta métrica de fibra de vidrio, marca Seca 201®, precisión 0.5 mm (25). Con el pliegue cutáneo tricipital y la circunferencia del brazo se obtuvo el área muscular de brazo (AMB) con la siguiente fórmula: AMB=[PB - (π* PCT)]2/4π. Posteriormente, se calculó el área adiposa del brazo (AAB) con la siguiente fórmula: AAB=AMB - ATB; para obtener el área total del brazo (ATB) se utilizó (CB mm/6.2832)2 *π. Los resultados se analizaron en base a la tabla de percentiles del área muscular de brazo para edad y sexo (mm2) de los Centers for Disease Control and Prevention. Las técnicas de medición fueron acorde las estipuladas.12
Respecto a la suplementación con L-carnitina, se aplicó Cardispan I.V., que es L-carnitina 50 mg/ kg/sesión y se preparó en un mililitro de solución salina, en una jeringa de 20 mL, 30 minutos antes de terminar cada sesión de hemodiálisis y se aplicó sobre la línea venosa.11 El cardispan fue proporcionado por la Unidad Médica de Alta Especialidad, UMAE Hospital Gineco/pediatría 48 (UMAE 48) y fue aplicado por las enfermeras del área de hemodiálisis pediátrica.
Los indicadores bioquímicos se obtuvieron del expediente médico, donde se registraron los niveles de hemoglobina durante tres meses del estudio, así como la cantidad de eritropoyetina administrada y los indicadores metabólicos (bioquímicos) como la biometría hemática para la medición de hemoglobina, albúmina sérica, colesterol, triglicéridos, sodio, potasio, calcio, fósforo, urea y creatinina; todos se registraron al inicio y al final del estudio (tres meses). Los análisis fueron realizados por personal capacitado del laboratorio de análisis clínicos de la UMAE 48.
Análisis estadístico y aspectos de ética
Para el análisis estadístico se utilizó el programa estadístico SPSS 15® (2012). Se aplicó estadística descriptiva para las variables antropométricas y bioquímicas, excepto para la interpretación del índice de masa corporal; la distribución por sexo se hizo por porcentajes. Para la comparación de los indicadores antropométricos y bioquímicos pre y post de la aplicación con L-carnitina IV se utilizó una prueba de t de student, así como una correlación de Pearson para las variables antropométricas y bioquímicas. Se procedió a una prueba de Rangos de Wilcoxon, para la comparación de la eritropoyetina y el paquete globular, pre y post la suplementación con Lcarnitina. Finalmente, se realizó un cálculo de la reducción del riesgo atribuible (siendo cada caso el mismo control, pre y post de la maniobra con L-carnitina) y una comparación por proporciones (con el paquete estadístico ®PRIMER McGrawHill Interamericana, 1998) para: peso seco, índice de masa corporal, hemoglobina, albúmina, colesterol y triglicéridos. Se consideró mejoría cuando hubo un incremento en los valores de las variables de relevancia, a los tres meses de la suplementación: para peso seco un incremento con un valor ≥ a 0.5 kg); para la hemoglobina ≥ a 1 g/dL; para el índice de masa corporal y albúmina que modificaran los valores; para colesterol y triglicéridos que se mostrara una reducción de las cifras iniciales, p<0.05 y un β del 80%. El proyecto fue aprobado por el Comité de Investigación y Ética del IMSS (Folio local: F-2012-1002-58 y Folio nacional: R-2012-1002-55). Los procedimientos de esta investigación fueron de acuerdo a los lineamientos estipulados por la ley general de la salud en materia de investigación en seres humanos, donde se aplicó el consentimiento informado. La L-carnitina ha sido utilizada previamente en este tipo de pacientes, por lo que se cuidó no poner en riesgo a los participantes.
RESULTADOS
De los 25 casos estudiados con insuficiencia renal crónica en hemodiálisis 11 fueron del sexo femenino y 14 del sexo masculino, con un promedio de edad de 12.4 años (3 a 16 años) (Cuadro 1). Al realizar la comparación con los indicadores antropométricos pre y post de la aplicación con L-carnitina IV (T de Student), se encontró una diferencia significativa para peso seco e índice de masa corporal (p=0.04) (Cuadro 2). Respecto a la comparación para los indicadores bioquímicos se observó una diferencia significativa para todos los marcadores bioquímicos (albúmina, colesterol, triglicéridos, fósforo y creatinina) excepto para la hemoglobina. Para el caso de la albúmina esta diferencia detectada se debió porque al final disminuyó sus valores; para el caso del colesterol y triglicéridos esta diferencia fue por un incremento al final de la maniobra (Cuadro 3).
Cuadro 1 Características basales de los participantes

CB: pliegue cutáneo tricipital; IMC: índice de masa corporal; AMB: área muscular de brazo; AAB: área adiposa de brazo; HB: hemoglobina; HTO: hematocrito; TGC: triglicéridos; Na: sodio; K: potasio; Ca: calcio; P: fósforo.
Cuadro 2 Comparación en los indicadores antropométricos pre y post de la aplicación con L-carnitina IV en los participantes (n=25)
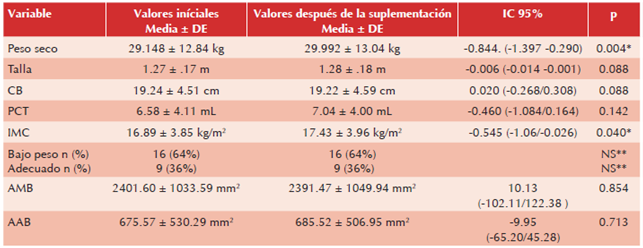
*T de student: nivel de significancia; ** Cálculo por proporciones. CB: pliegue cutáneo tricipital; IMC: índice de masa corporal; AMB: área muscular de brazo; AAB: área adiposa de brazo.
Cuadro 3 Comparación en los indicadores bioquímicos pre y post de la aplicación con L-carnitina intravenosa en los participantes (n=25)
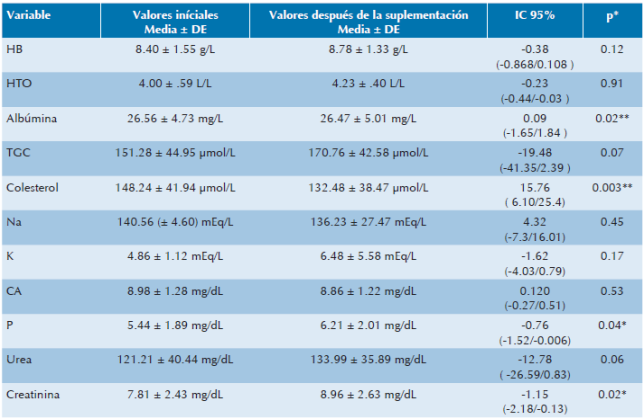
*T de student= nivel de significancia**, HB=hemoglobina, HTO= hematocrito, TGC= triglicéridos, Na= sodio, K= potasio, Ca= calcio, P= potasio.
Respecto a la comparación con las dosis del paquete globular y la aplicación de eritropoyetina humana recombinante pre y postmaniobra, sólo se observó una diferencia significativa para el paquete globular (p=0.003) (Cuadro 4).
Cuadro 4 Comparación de la eritropoyetina y el paquete globular, pre y post la suplementación con L-carnitina
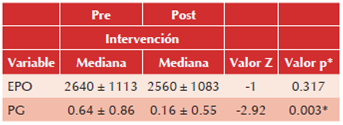
*Con prueba de rangos de Wilcoxon = valor de significancia; EPO: eritropoyetina; PG: paquete globular.
Respecto al análisis de correlación hubo una relación positiva para las variables antropométricas de peso seco, talla y área muscular de brazo con la creatinina final; el resto de las variables se muestra en el Cuadro 5.
Cuadro 5 Resultados de la correlación entre variables antropométricas con variables bioquímicas
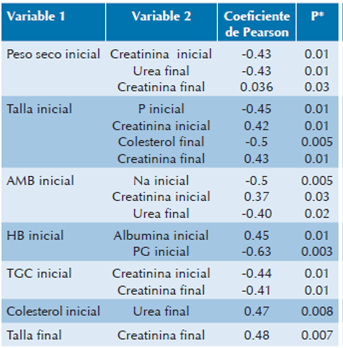
*p= análisis por correlación de Pearson.
CB: pliegue cutáneo tricipital; IMC: índice de masa corporal; AMB: área muscular de brazo; AAB: área adiposa de brazo; HB: hemoglobina; HTO: hematocrito; TGC: triglicéridos; Na: sodio; K: potasio; Ca: calcio; P: potasio; PG: paquete globular.
Al analizar el porcentaje de casos que se vieron beneficiados con la mejora en los indicadores antropométricos y bioquímicos, después de la suplementación con L-carnitina y que fueran de interés clínico de acuerdo a los expuesto en la evidencia científica, se pudo observar un cambió para la hemoglobina, el peso seco, albúmina de los casos que mejoraron sus cifras después de la maniobra; para el caso de la albúmina se observó un incremento en 17 de los casos (68%), se observó un incremento de las cifras de albúmina de 0.1 a 2 g/dL, y se mantuvo el valor dentro de lo adecuado en el 96% de los casos (Cuadro 5). Las cifras de hemoglobina en 15 de los casos presentaron un incremento al final de la maniobra de 0.1 a 2.9 g/dL, pero sólo en diez casos se observó un incremento de 1 g/dL.
Para los triglicéridos, en siete casos se observó una disminución después de la maniobra de 15 a 81 mg/dL. Para los valores de colesterol, en 15 (60%) de los casos se detectó una reducción de los valores de 6 a 54 mg/dL, pero los casos que se mantuvieron con reducciones acorde a las recomendaciones se presentan en el Cuadro 6, donde la reducción en el riesgo en cualquiera de los marcadores antropométricos y bioquímicos mencionados fue del 12 al 68% (Cuadro 6).
Cuadro 6 Comparación de los principales indicadores que mejoraron a los tres meses de la suplementación con Lcarnitina y la reducción del riesgo atribuible (N=25)

p¥: comparación por proporciones con el paquete estadístico ®PRIMER McGrawHill Interamericana (1998), entre los valores iniciales y a los tres meses de la suplementación. RRA: la reducción del riesgo atribuible.
*Aumento o mejora considerada cuando se presentó un incremento igual o mayor a 0.5 kg.
**Mejoría considerada cuando hubo un incremento en los valores de hemoglobina a los tres meses de la suplementación ≥ a 1 g/dL.
***Aunque con la intervención siguieron con cifras por arriba de lo recomendado, en un 76% hubo disminución de las cifras en un rango de 12-54 mg/dL.
Aportaciones complementarias
Aunque no fue el objetivo principal, los familiares manifestaron una mejora en los síntomas relacionados con la insuficiencia renal crónica, por ejemplo, que mejoró la adinamia, el estado anímico, la coloración cutánea. Respecto a los eventos adversos, náusea y vómito, sólo se presentó un caso, registrando que, para este caso, la L-carnitina se aplicó en bolo.
DISCUSIÓN
El deterioro nutricional en los niños con insuficiencia renal crónica es prevalente y tiene un mayor impacto de acuerdo al grupo de edad y las demandas energéticas que conlleva de acuerdo a la edad de cada paciente, por lo que las alternativas para mejorar el estado nutricio se vuelven imprescindibles.5
Acorde a los resultados observados, los valores de hemoglobina no presentaron una mejoría a diferencia de los estudios por Aoun y sus colegas,13 lo cual se puede explicar por el tamaño de muestra y por la duración de la suplementación que fue de 6 meses. Al realizar la comparación por proporciones y la medición de la reducción en el riesgo hubo una significancia clínica para la hemoglobina, lo cual es importante considerar, para ajustar los tiempos y un tamaño de muestra adecuado con estos hallazgos.
Una fortaleza de nuestro estudio comparado con el de Aoun y sus colaboradores es que se consideró desde un inicio que los participantes no estuvieran recibiendo tratamiento con hierro, lo cual pudo explicar la mejora observada en estos autores. Por otro lado, aunque una limitante fue el no contar con un tamaño de muestra adecuado, vale la pena mencionar que ésta en nuestro estudio sigue siendo mayor a la observada en la mayoría de los estudios (menor a 15 participantes) y donde tampoco hacen mención a un cálculo de tamaño de la muestra.
Por otro lado, Lilien y su equipo14 tampoco encontraron una diferencia significativa en los niveles de hemoglobina ni una reducción en la dosis de eritropoyetina, lo cual coincide en este estudio; sin embargo, es pertinente mencionar que se pensó que se podrían obtener resultados favorables, ya que la vía de suplementación de la L-carnitina en el estudio de Lilien y su grupo14 fue vía oral, y en nuestro estudio fue vía intravenosa, cuya farmacocinética es mejor acorde a la biodisponibilidad y estabilidad en la absorción,15 lo cual se pudo comprobar al hacer el cálculo por proporciones para los casos y se pudieron detectar mejorías para hemoglobina después de la maniobra con incremento de 0.1 a 2.9 g/dL, lo cual refleja un beneficio con la suplementación.
A pesar de la evidencia científica, de la falta de efectos de la suplementación con L-carnitina sobre el estado nutricio de los pacientes, puede explicarse porque se consideran sólo los parámetros de peso para la talla, talla para la edad y peso para la edad,16 y nuestro estudio analizó un conjunto de variables que se correlacionaron con el estado nutricio, encontrando diferencia significativa para el peso seco, índice de masa corporal y niveles de albúmina, creatinina y colesterol. Las variables en conjunto permiten observar un probable efecto benéfico sobre la mejoría al estado nutricio, con la suplementación de L-carnitina con un corto tiempo de intervención (3 meses). El resto de las variables antropométricas como el área muscular de brazo y el área adiposa del brazo no mostraron una mejora significativa, pero se sugiere seguir estudiando en el seguimiento a largo plazo, y un indicador de efectos a corto plazo, pudieran ser a través de los niveles de creatinina, que para este estudio tuvieron un incremento, sobre todo al hacer a correlación, posterior a la intervención con el peso, talla e índice de masa corporal, lo cual pudiera ser un marcador indirecto del aumento de la masa muscular.16
Para los valores de colesterol y triglicéridos, nuestros hallazgos no concuerdan con lo reportado por Gunes y sus colegas en el 2005.17 Para los triglicéridos no se encontró una reducción significativa en sus valores al final de la maniobra, a diferencia de los valores de colesterol que sí se observó una reducción significancia; esto se puede deber a que los pacientes con insuficiencia renal crónica presentan una deficiencia de carnitina y al ser hemodializados, ésta traspasa el filtro, lo cual explica esta falta de reducción en los niveles de triglicéridos, y al no haber una deficiencia de la carnitina, la función de facilitar la entrada a los triglicéridos de cadena media a la matriz mitocondrial y que comience el proceso de beta oxidación,5 se encuentra alterada, por lo que al ser suplementada se evitan estas dificultades facilitando el proceso y reduciendo los niveles de colesterol. Al hacer la comparación y análisis por la cantidad (porcentaje) de casos que mostraron disminución después de la maniobra, se observaron reducciones de 15 a 81 mg/dL en siete casos para los triglicéridos y, de 15 casos (60%) para el colesterol de 6 a 54 mg/dL, lo cual es un hallazgo clínico.
Otros de los bioquímicos fue el fosforo, el cual presentó un incremento en sus cifras, una razón se explica a que dicho elemento presenta variabilidad en su ingestión dietética y una limitante del estudio, fue el no contar con un registro del consumo dietético de este elemento y otros nutrimentos, por lo que sugerimos que este hallazgo se pudo deber a la ingestión de alimentos ricos en fosforo un día previo a la sesión de hemodiálisis. Por lo que esto se podría controlar en otros diseños al registrar y analizar el consumo real de alimentos en los participantes.17
Los indicadores que se esperaba contar con una diferencia significativa no se lograron con la estadística utilizada (t de student) por el pequeño tamaño de los casos de estudio, por lo que al mejorar la comparación por proporciones de los diferentes marcadores bioquímicos y antropométricos antes y después de la maniobra, se pudo detectar que hubo mejoría en la mayoría de los casos de estudio para la hemoglobina, albúmina, peso seco, colesterol y triglicéridos, con una disminución de reducción en el riesgo del 12 al 68% de los casos de estudio.
Los estudios sobre la seguridad a la administración L-carnitina, indican que los efectos adversos son bajos, para este estudio solo se presentó un evento adverso relacionado con la L-carnitina y fue la presencia de náusea y vómito. Este evento adverso no serio, que la literatura ha registrado, se debe a la técnica de aplicación de la Lcarnitina, en la que se suele usar bolo en lugar de la infusión.11
Finalmente, aunque no fue uno de los objetivos principales, los familiares mencionaron una mejora en los síntomas relacionados con la insuficiencia renal crónica, por ejemplo que mejoró la adinamia, el estado anímico, la coloración cutánea y diminución en la anorexia. Por lo que sería interesante que se puedan medir a largo plazo la mejora en la calidad de vida, al generar un impacto al estado nutricio y otros marcadores metabólicos como el equilibrio en lípidos, la glucosa y la anemia.
CONCLUSIONES
La suplementación con L-carnitina intravenosa de 50 mg/kg/sesión, 30 minutos antes de terminar cada sesión de hemodiálisis, durante tres meses, permitió una mejora en el porcentaje de los casos para peso seco, índice de masa corporal, albúmina, hemoglobina y una reducción para los casos de colesterol y triglicéridos; con una reducción del riesgo atribuible del 12 al 68% de los casos (pre y post maniobra).











 nova página do texto(beta)
nova página do texto(beta)


