Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Acta pediátrica de México
versión On-line ISSN 2395-8235versión impresa ISSN 0186-2391
Acta pediatr. Méx vol.35 no.5 México sep./oct. 2014
Artículo original
Cuantificación sanguínea de metformina y glibenclamida para endocrinología pediátrica
Quantification of metformin and glyburide in blood for paediatric endocrinology
Radamés Alemón-Medina, Juan Luis Chávez-Pacheco, Blanca Ramírez-Mendiola, Liliana Rivera-Espinosa, Raquel García-Álvarez
Laboratorio de Farmacología, Instituto Nacional de Pediatría, México.
Correspondencia:
Dr. Radamés Alemón-Medina
Laboratorio de Farmacología,
Torre de Investigación,
Instituto Nacional de Pediatría.
Avenida Imán No.1, Piso 3, CP. 04530,
México D.F., México.
Tel/Fax: 52 55 10 84 38 80
ranapez@hotmail.com
Recibido: 9 de abril 2014
Aceptado: 6 de junio 2014
RESUMEN
Antecedentes: el empleo de fármacos antidiabéticos, como la metformina y la glibenclamida, para el tratamiento y control de obesidad infantil, resistencia a insulina y diabetes mellitus tipo II en niños y adolescentes, ha obligado a determinar las concentraciones plasmáticas de dichos fármacos para ajustar correctamente las dosis.
Objetivo: establecer y validar un método de cromatografía líquida de alto desempeño con espectrofotómetro (UPLC-UV) para cuantificar metformina y glibenclamida en sangre total.
Materiales y métodos: se emplearon únicamente 0.1 mL de sangre y ambos fármacos se extrajeron por precipitación con metanol. La cuantificación se llevó a cabo con fase móvil de fosfato de potasio monobásico (KH2PO4) 0.1 M, pH = 6.5, dodecilsulfato sódico (SDS) 4.6 mM y acetonitrilo (63:7:30) a 0.8 mL/min en una columna VARIAN Pursuit® C8 150 x 3.9 mm a 40°C, a 236 nm.
Resultados: el método permitió medir de 20 a 600 nanogramos de metformina y de 100 a 2 000 nanogramos de glibenclamida por mililitro de sangre. Ambos fármacos son fisicoquímicamente estables en las muestras sanguíneas hasta por 30 días a 4°C.
Conclusión: el método propuesto permite cuantificar metformina y glibenclamida en muestras de pacientes pediátricos como apoyo al clínico para vigilar el apego al tratamiento, la biodisponibilidad y los perfiles farmacocinéticos.
Palabras clave: metformina, glibenclamida, UPLC-UV, sangre total, pediatría, endocrinología.
ABSTRACT
Background: The recent use of antidiabetic drugs such as metformin and glyburide for the treatment and control of childhood obesity, insulin resistance and type II diabetes mellitus in children and adolescents, has encouraged physicians to determine plasma levels of these drugs for the right dose adjustment.
Objective: To implement and validate a UPLC-UV method to quantify metformin and glyburide in blood samples.
Materials and methods: Only a 0.1 mL-volume blood sample was used. Both drugs are removed by precipitation with methanol. Quantitation was carried out with mobile phase of 4.6 mM potassium phosphate monobasic (KH2PO4) 0.1 M pH = 6.5, sodium dodecyl sulphate (SDS) and acetonitrile (63:7:30), at 0.8 mL/min through a VARIAN Pursuit® C8 150 x 3.9 mm column at 40°C, 236 nm.
Results: The method allows the measurement of 20 to 600 nanograms of metformin and from 100 to 2 000 nanograms of glyburide per milliliter of blood. Both drugs are physicochemically stable in blood samples for up to 30 days at 4°C.
Conclusion: Our method allows quantification of metformin and glyburide in paediatric blood samples, to support the clinicians to monitor treatment compliance, bioavailability and pharmacokinetic profiles.
Key words: Metformin, glyburide, UPLC-UV, whole blood, paediatrics, endocrinology
INTRODUCCIÓN
Recientemente se ha registrado aumento en la frecuencia de la obesidad infantil, lo que ha contribuido al incremento de niños y adolescentes con trastornos endocrinos, sobre todo de vías anabólicas.1 Estos problemas clínicos afectan tanto a países desarrollados como en vías de desarrollo, de todos los grupos socioeconómicos e independientemente de la edad, el género o grupo étnico, por lo que más de 22 millones de niños menores de 5 años son obesos y uno de cada 10 tiene sobrepeso.2,3
Con el objetivo de prevenir el desarrollo de trastornos endocrinos irreversibles, como la diabetes mellitus tipo II, y ofrecer una mejor calidad de vida a los niños con obesidad, se ha instaurado un tratamiento farmacológico como apoyo a las medidas higienicodietéticas y físicas.4-6
La metformina es el fármaco más utilizado debido a su acción antihiperglucemiante7 y a que restablece los valores normales de lípidos en la sangre; es también un auxiliar para el control del peso.8 Por otro lado, la glibenclamida es una sulfonilurea que se utiliza con frecuencia en combinación con metformina para el tratamiento de la diabetes mellitus tipo II en pacientes adultos y, aunque su uso pediátrico es limitado debido a su acción directa sobre el páncreas,9 en últimas fechas se ha tenido que emplear en endocrinología pediátrica para lograr el mejor control de la glucemia.
La aparición de los trastornos metabólicos derivados de la obesidad a edades cada vez más tempranas ha obligado a los clínicos a emplear estos fármacos antidiabéticos que, hasta hace algunos años, sólo se usaban en adultos. Es por ello que en México aún no existen presentaciones pediátricas comerciales de metformina, glibenclamida o su combinación, por lo que dichos fármacos se prescriben a menudo en dosis individualizadas ajustadas mediante la fragmentación o disolución de los comprimidos comercializados para pacientes adultos.
Esta situación motivó a los endocrinólogos del Instituto Nacional de Pediatría a buscar una manera de contar con evidencia objetiva de que las dosis ajustadas para los pacientes pediátricos originan concentraciones plasmáticas adecuadas de metformina, glibenclamida, o de ambas. El objetivo de este estudio fue adaptar y validar científicamente un procedimiento químico analítico por cromatografía líquida de alto desempeño con espectrofotómetro (UPLC-UV, por sus siglas en inglés) para cuantificar metformina y glibenclamida, simultáneamente, en una misma muestra de sangre heparinizada. Se empleó un volumen muy pequeño de sangre total como herramienta de apoyo al clínico para determinar las concentraciones sanguíneas de ambos fármacos y para confirmar que se alcanzan concentraciones terapéuticas, de tal manera que el clínico sea capaz de ajustar las dosis de tales fármacos de forma personalizada.
MATERIAL Y MÉTODOS
Reactivos
Los estándares de metformina, glibenclamida, ranitidina, salicilamida, dextrometorfano, nimesulida, ácido acetilsalicílico, paracetamol, mebendazol, metronidazol, naproxeno, propafenona, verapamilo, captopril y ciclofosfamida fueron de grado ultrapuro, siguiendo la recomendación de la Farmacopea de Estados Unidos (USP). El acetonitrilo, grado HPLC y el metanol grado reactivo, fueron adquiridos de JT Baker® (Xalostoc, México). Fosfato de potasio monobásico de Merck® (Naucalpan, México) y dodecilsulfato sódico (SDS) de Amresco® (Solon, Ohio). El agua bidestilada para elaborar las soluciones y reactivos se obtuvo de un sistema Milli-Q (Millipore, Molsheim, Francia).
Se elaboró una solución inicial de clorhidrato de metformina 1 mg/mL en agua bidestilada, a partir de la cual se hicieron diluciones subsecuentes a 20, 40, 100, 200, 400 y 600 ng/mL, que fueron las concentraciones de la curva patrón para cuantificar ese fármaco. Las concentraciones problema (concentraciones control) baja, media y alta, fueron 30, 150 y 500 ng/mL, respectivamente, que corresponden a 3 puntos intermedios de la curva patrón que se emplean en la validación del método porque permiten evaluar la exactitud y precisión del mismo. Para cuantificar la glibenclamida se preparó una solución inicial de 1 mg/mL y la curva de calibración tuvo los siguientes puntos: 100, 200, 400, 600, 1 000 y 2 000 ng/mL, así como los puntos de control 300, 900 y 1400 ng/mL; el estándar externo fue ranitidina (5 mg/mL). La curva de calibración de ambos fármacos se preparó con 80 µL de sangre total heparinizada, 5 µL de metformina y 5 µL de glibenclamida.
Para la construcción de las curvas de calibración se tuvieron en cuenta los valores de concentración plasmática de 1 800 ng/mL para metformina a 2 550 mg por vía oral y 100 ng/mL para glibenclamida, a dosis de 5 mg por la misma vía. Las curvas de ambos fármacos se calcularon para dosis hasta cinco veces menores a las empleadas en adultos para que fueran de utilidad en pediatría.
Extracción de metformina y glibenclamida a partir de sangre total
Para este proceso se empleó un volumen de sólo 0.1 mL de sangre total que se colocó en un tubo de microcentrífuga de 1.5 mL y se añadieron 50 µL de acetonitrilo. Se mezclaron en agitador de toque (vórtex) durante 1 minuto; se añadió 1 mL de metanol y se volvió a mezclar en vórtex por 1 minuto. La mezcla se centrifugó 10.000 rpm durante 5 minutos. La fase orgánica se transfirió a otro tubo y se evaporó a sequedad a 40°C bajo corriente de aire. El residuo se reconstituyó con 50 µL de fase móvil, se añadieron 10 µL del estándar externo (ranitidina 5 mg/mL) y se mezcló en vórtex por 30 segundos. De esta mezcla se inyectaron 10 µL al sistema de cromatografía líquida de alto desempeño con espectrofotómetro.
Condiciones cromatográficas
Se empleó un equipo de cromatografía líquida de alto desempeño con espectrofotómetro (UPLC-UV) marca Acquity® (Waters Co., Milford MA, EE.UU). La separación se llevó a cabo en una columna VARIAN Pursuit® C8 150 x 3.9 mm. La velocidad de flujo fue 0.8 mL/min. La columna y el inyector automático se mantuvieron a 40°C. En estas condiciones, los tiempos de retención para metformina, ranitidina y glibenclamida fueron 2, 2.4 y 6.7 minutos, respectivamente (Figura 1).
La fase móvil fue KH2PO4, 0.1 M, pH = 6.5, dodecilsulfato sódico (SDS) 4.6 mM y acetonitrilo en proporción 63:7:30, recién elaborada para cada sesión analítica. La detección se realizó a 236 nm. Los datos fueron analizados utilizando el software Empower® 2.0 (Waters, Inc.).
Validación del método
Se llevó a cabo de acuerdo con los criterios de las directrices nacionales oficiales mexicanas, que están en conformidad con las internacionales (NOM 177-SSA1-2013, FDA y EMEA). La linealidad del método, dada por la repetibilidad y reproducibilidad, se determinó por r2 ≥ 0.9, del promedio de 6 curvas de calibración y comparación de las desviaciones estándar, como lo establece la Norma Oficial.
Las variabilidades intradía e interdía se determinaron cuantificando las concentraciones control a partir de la curva de metformina y glibenclamida. La selectividad, estabilidad, límite de cuantificación y límite de detección del método también se evaluaron, así como la recuperación absoluta de ambos fármacos.
RESULTADOS
Para cuantificar metformina y glibenclamida simultáneamente en una muestra muy pequeña de sangre (microvolumen) se ha establecido y validado un método de cromatografía líquida de alto desempeño con espectrofotómetro sensible, preciso y exacto que demostró ser adecuado para analizar las concentraciones de sangre de ambos fármacos. Se pusieron a prueba diferentes disolventes, proporciones y mezclas para lograr la mejor extracción a partir de la sangre total y, finalmente, el procedimiento más adecuado fue la precipitación de los fármacos con acetonitrilo y metanol.
Los datos de exactitud y precisión (variaciones intra- e interdía, respectivamente) se muestran en el Cuadro 1. La variabilidad intradía se obtuvo mediante el análisis de cinco series de control de calidad para ambos fármacos probados y la variabilidad interdía se evaluó a las seis series de cada control de calidad durante tres días consecutivos. En ambos ensayos no se observaron diferencias significativas entre los valores nominales de ambos fármacos en las tres concentraciones, calculados a partir de la curva de calibración. Por norma oficial se aceptaron determinaciones con un coeficiente de variación menor o igual a 15%.
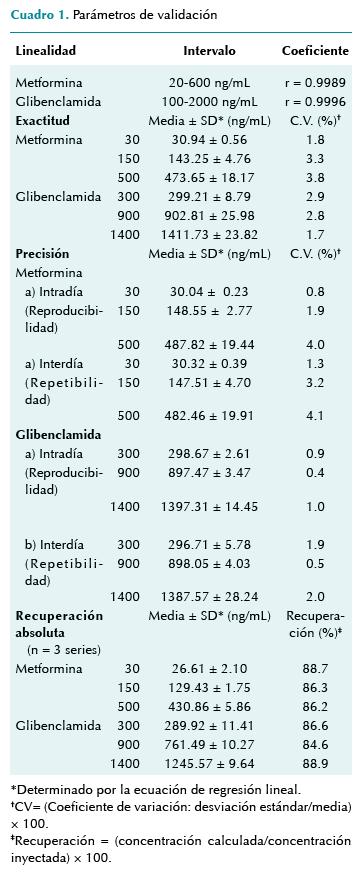
El método analítico fue lineal en un intervalo de 20 a 600 ng/mL para metformina y de 100 a 2 000 ng/mL para glibenclamida, con coeficientes de correlación r = 0.9989 y r = 0.9996, respectivamente (Cuadro 1). Para destacar que nuestro método es selectivo para los tres fármacos probados (metformina, glibenclamida y ranitidina) y que no interfieren otros fármacos en su evaluación se inyectaron distintos fármacos de prescripción común en pediatría y a las concentraciones esperadas: salicilamida, dextrometorfano, nimesulida, ácido acetil salicílico, paracetamol, mebendazol, metronidazol, naproxeno, propafenona, verapamilo, captopril, ciclofosfamida. Únicamente la salicilamida interfirió con la metformina (datos no mostrados).
La recuperación absoluta se determinó mediante el porcentaje de fármaco recuperado después del procedimiento de extracción, comparando la concentración del fármaco extraído con las mismas concentraciones del fármaco en solución. La recuperación fue de cerca de 86% para ambos fármacos (Cuadro 1).
El límite de cuantificación para la metformina fue de 20 ng/mL y de 100 ng/mL para la glibenclamida. El límite de detección para la metformina fue de 5 ng/mL (proporción señal-ruido ≥ 3) mientras que para la glibenclamida fue de 25 ng/mL. Las muestras sanguíneas se pueden congelar y descongelar hasta tres veces, con recuperación media de 89% de metformina y 90% de glibenclamida, con un coeficiente de variación < 5% (datos no mostrados).
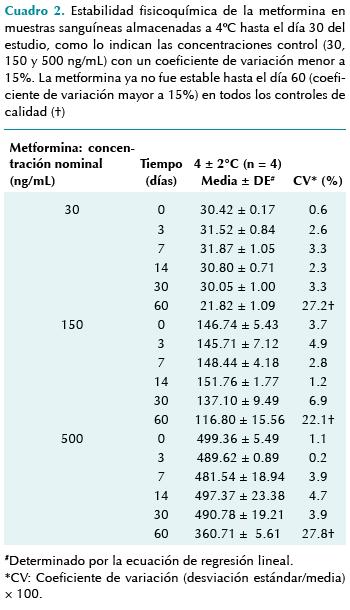
Las muestras fueron estables hasta por 30 días a 4°C (Cuadros 2 y 3). No obstante que falta confrontar los parámetros evaluados en muestras de pacientes que hayan tomado uno u otro fármaco, o ambos.

Nuestro método es la primera técnica reportada para medir simultáneamente metformina y glibenclamida, con la ventaja de utilizar un microvolumen de matriz biológica. Las muestras de los pacientes pueden tomarse a partir de los primeros 15 minutos de haber tomado el medicamento por vía oral ya que, aunque la concentración plasmática máxima se obtiene entre una y tres horas después de tomar ambos fármacos, a ese tiempo ya se tienen concentraciones detectables, pues ya se ha iniciado la absorción.
DISCUSIÓN
La prescripción de medicamentos antidiabéticos se basa en las concentraciones de biomarcadores metabólicos como la glucemia en ayuno y posprandial, insulina y el modelo de evaluación de la homeostasis (HOMA). Asimismo, se toma en cuenta el mecanismo de acción de cada fármaco individual.9 La metformina se prefiere como fármaco de primera elección en niños debido a que puede contribuir a disminuir el peso corporal y no induce hipoglucemia inmediata ni acidosis láctica.10 El uso de glibenclamida en pacientes pediátricos es limitado por ser un fármaco que induce la liberación de insulina desde el páncreas, efecto que no es deseable a menos que el control de la glucemia no pueda lograrse con metformina y dieta.11 Sin embargo, últimamente se ha tenido que emplear glibenclamida en pediatría debido a la frecuencia de obesidad infantil y a las alteraciones en la regulación de la glucemia derivadas de ésta. En estas circunstancias, es necesario detectar los niveles plasmáticos de glibenclamida y metformina, por ser fármacos de reciente incorporación en pacientes pediátricos y porque todavía no hay suficientes estudios de eficacia y seguridad de estos fármacos en niños y adolescentes;11 para ello será muy importante correlacionar las concentraciones plasmáticas de metformina o glibenclamida con los marcadores metabólicos relacionados (glucosa, insulina, HOMA) ya que, si dichos marcadores llegan a valores normales al cabo de administrar los fármacos, el clínico puede estar seguro del éxito terapéutico con las dosis que está empleando, e inclusive extrapolarlas a otros pacientes. Asimismo, en pacientes pediátricos se busca extraer muestras sanguíneas del menor volumen posible, involucrando un método rápido y confiable para la detección de fármacos.
Ya se han desarrollado y validado algunos métodos analíticos para determinar esta combinación de fármacos, incluso en presencia de otros antidiabéticos.12 Estos procedimientos han sido con base en cromatografía líquida de alta resolución (HPLC) que incluyen la extracción de los fármacos en fase sólida y el uso de determinaciones espectrofotométricas con transformaciones combinadas discretas y continuas. La exactitud, precisión y robustez de recuperación de estos métodos, reportados por otros autores, se han realizado con estricto apego a las normas internacionales.12-14 Sin embargo, esos procedimientos se han llevado a cabo utilizando las mezclas y soluciones de fármacos pero no se han extraído a partir de una matriz biológica como son la sangre o el plasma humanos. Otros métodos han incluido la extracción de los fármacos pero emplean volúmenes muy altos de plasma humano: hasta 1 mL.
En este trabajo hemos desarrollado y validado un método para determinar metformina y glibenclamida extraídos de un fluido biológico: 0.1 mL de sangre total heparinizada; compensando la falta de estudios de extracción de estos fármacos de forma simultánea y en un volumen pequeño de sangre.
En relación con los alcances de este método cabe reconocer que nuestros desarrollo y validación corresponden a la etapa preclínica, por lo que sus alcances tendrán lugar en actividades como los estudios pediátricos de vigilancia del apego al tratamiento o en pacientes con diabetes mellitus tipo 2 de edad avanzada, en donde se requieren pequeños volúmenes de sangre debido a deshidratación, pérdida de sangre o después de un análisis múltiple. En etapas ulteriores se requerirá confrontar los parámetros evaluados a partir de muestras de pacientes que se encuentren tomando cualquiera de estos fármacos.
CONCLUSIÓN
El método desarrollado en este trabajo permite describir los parámetros farmacocinéticos de la combinación de metformina-glibenclamida, o por separado, en sangre humana; por lo que al aplicarse en muestras de pacientes que tomen dichos fármacos permitirá evaluar el apego al tratamiento farmacológico y también será útil para definir las dosis exactas de estos medicamentos; aquellas que permitan alcanzar las concentraciones terapéuticas en la sangre de estos pacientes. Este método también podrá emplearse para estudios posteriores de biodisponibilidad comparada, eficacia y seguridad de los fármacos en población pediátrica con sobrepeso, obesidad o con resistencia a insulina.
REFERENCIAS
1. Ventura EE, Davis JN, Alexander KE, Shaibi GQ, Lee W, Byrd-Williams CE, et al. Dietary intake and the metabolic syndrome in overweight latino children. J Am Diet Assoc 2008;108(8):1355-9. doi: 10.1016/j.jada.2008.05.006. [ Links ]
2. Raj M. & RK. Kumar Obesity in children & adolescents. Indian J Med Res 2010;132:598-607. [ Links ]
3. Encuesta Nacional de Salud y Nutrición, 2012. Secretaría de Salud, México. ENSANUT, 2012. [ Links ]
4. Loannides-Demos LL, Proietto J, McNeil JJ. Pharmacotherapy for obesity. Drugs 2005;65(10):1391-1418. [ Links ]
5. Kanekara A, Sharma M. Pharmacological Approaches for Management of Child and Adolescent Obesity. J Clin Med Res 2010;2(3):105-11. doi: 10.4021/jocmr2010.05.288w. [ Links ]
6. De Silva-Sanigorski A, L. Prosser, L. Carpenter, S. Honisett, L. Gibbs, M. Moodie, et al. Evaluation of the childhood obesity prevention program Kids - 'Go for your life'. BMC Public Health 2010;10:288. [ Links ]
7. Lenzen S, Lortz S, Tiedge M. Effect of metformin on SGLT1, GLUT2, and GLUT5 hexose transporter gene expression in small intestine from rats. Biochem Pharmacol 1996;51:893-896. [ Links ]
8. Fulgencio JP, Kohl C, Girard J, Pegorier JP. Effect of metformin on fatty acid and glucose metabolism in freshly isolated hepatocytes and on specific gene expression in cultured hepatocytes. Biochem. Pharmacol 2001;62:439-446. [ Links ]
9. Masharani U., Karam JH. & German MS. Hormonas pancreáticas y diabetes mellitus. En: Endocrinología básica y clínica de Greenspan. Ciudad de México: El Manual Moderno, 2008; pp. 693-786. [ Links ]
10. Kendall DL, Amin R & Clayton PE. Metformin in the treatment of obese children and adolescents at risk of type 2 diabetes. Pediatr Drugs 2014;16:13-20. [ Links ]
11. American Diabetes Association. Type 2 diabetes in children and adolescents. Pediatrics 2014;105:671-680. [ Links ]
12. Sohrabi MR, N. Kamali & M. Khakpour. Simultaneous spectrophotometric determination of metformin hydrochloride and glibenclamide in binary mixtures using combined discrete and continuous wavelet transforms. Analytical Sciences 2011:27:1037-1041. [ Links ]
13. Abu Ruz S, J. Millership, J. McElnay J. The development and validation of liquid chromatography method for the simultaneous determination of metformin and glipizide, gliclazide, glibenclamide or glimperide in plasma. Chromatography B 2005;817:277-286. [ Links ]
14. Malleswararao CSN., M.V. Suryanarayana & K. Mukkanti. Scientia Pharmaceutica 2002;80:139-152. [ Links ]














