Servicios Personalizados
Revista
Articulo
Indicadores
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Ciencias marinas
versión impresa ISSN 0185-3880
Cienc. mar vol.35 no.4 Ensenada dic. 2009
Artículos de investigación
In vitro cytotoxic and antiproliferative activities of marine macroalgae from Yucatán, Mexico*
Actividad citotóxica y antiproliferativa in vitro de macroalgas marinas de Yucatán, México
R Moo–Puc1, 2, D Robledo1, Y Freile–Pelegrín1*
1 Departamento de Recursos del Mar; Cinvestav, Km 6 Carretera Antigua a Progreso, Cordemex, 97310, A.P. 73, Mérida, Yucatán, México. * E–mail: freile@mda.cinvestav.mx
2 Unidad de Investigación Médica Yucatán, Unidad Médica de Alta Especialidad, Centro Médico Ignacio García Téllez, Instituto Mexicano del Seguro Social 41 No 439 x 32 y 34, Col. Industrial, CP 97150, Mérida, Yucatán, México.
Recibido en mayo de 2009.
Aceptado en octubre de 2009.
Abstract
Extracts from 27 marine algal species (14 Rhodophyta, 5 Phaeophyta, and 8 Chlorophyta) from the Yucatán Peninsula (Mexico) were evaluated for cytotoxic and antiproliferative activity by 3(4,5–dimethylthiazole–2–yl)–2,5–diphenyltetrazolium bromide (MTT) and sulforhodamine B (SRB) assays, respectively. To determine the specificity of cytotoxic activity against tumor cells, the selective index (SI) was also calculated. The following cancer cell lines were employed: normal canine kidney (MDCK) cells, human laryngeal carcinoma (Hep–2) cells, human cervical adenocarcinoma (HeLa) cells, and human nasopharyngeal carcinoma (KB) cells. The results indicated that 44% and 51% of the algal species tested showed cytotoxic and antiproliferative activity, respectively. Most of the cytotoxic extracts were from species of Chlorophyta, with Udotea flabellum and U. conglutinate showing the highest cytotoxic activity against all the cancer cell lines. For Rhodophyta, the Bryothamnion triquetrum extract showed outstanding selective cytotoxicity against Hep–2 cells (CC50 8.29 µg mL–1, SI = 12.04). Two of the five species of Phaeophyta tested (Lobophora variegata and Dictyota caribaea) showed high cytotoxicity activity against the KB cell line. The data show that these species are a potential source of compounds for the treatment of certain cancer diseases.
Key words: antiproliferative, cytotoxicity, seaweeds, Yucatán.
Resumen
Los extractos de 27 especies de algas marinas (14 Rhodophyta, 5 Phaeophyta y 8 Chlorophyta) recolectadas en la península de Yucatán (México) fueron evaluados para probar su actividad citotóxica y antiproliferativa usando los ensayos de 3[4,5–dimetiltiazol–2–il]–2,5–bromuro de difeniltetrazolio (MTT) y sulforodamina B (SRB), respectivamente. Para determinar la especificidad de la actividad citotóxica en las células tumorales, el índice de selectividad (IS) fue también calculado. Para lo anterior fueron empleadas las siguientes líneas celulares: células normales de riñón caninino (MDCK), células de carcinoma humano laríngeo (Hep–2), células de adenocarcinoma humano de la cervix (HeLa) y células de carcinoma humano nasoafaríngeo (KB). Los resultados indicaron que 44% y 51% de las especies exhibieron actividad citotóxica y antiproliferativa, respectivamente. La mayoría de los extractos citotoxicos fueron de las especies pertenecientes a la división Chlorophyta, siendo Udotea flabellum y U. conglutinata las especies que mostraron la mayor actividad citotóxica selectiva sobre todas las líneas celulares tumorales. Para la división Rhodophyta, el extracto de Bryothamnion triquetrum tuvo una destacable citotoxicidad selectiva contra las células Hep–2 (CC50 8.29 µg mL–1 con SI = 12.04). Dos de las cinco especies de Phaeophyta probadas (Lobophora variegata y Dictyota caribaea) mostraron alta actividad citotóxica sobre la línea celular KB. Los resultados muestran que estos extractos son una fuente prometedora de compuestos para el tratamiento de algunos tipos de cáncer.
Palabras clave: algas marinas, antiproliferativo, citotóxico, Yucatán.
Introducción
El cáncer es una de las principales causas de muerte en México entre la población de 30 a 64 años (INEGI 2006). La incidencia de esta enfermedad aumenta constantemente constituyendo un desafío enorme para las instituciones de salud, en donde las demandas para su atención médica se están incrementando considerablemente, con importantes repercusiones económicas. La quimioterapia del cáncer ha sido socavada por el hecho de que los fármacos usados actualmente son relativamente tóxicos o, hasta cierto punto ineficaces, por un incremento de la resistencia. Los mecanismos moleculares de la resistencia a la droga pueden implicar una variedad de factores tales como mutación de los genes blancos y la disminucion de las concentraciones de los fármacos en las células debido a la toxicidad renal (Gottesman y Pastan 1993, Smith et al. 1998, Isnard–Bagnis et al. 2005). Por todo lo anterior, existe una urgente necesidad de descubrir nuevos agentes terapéuticos para esta enfermedad. Los recursos naturales han jugado un papel importante en la obtención de fármacos tales como el taxol, la camptotecina, la vincristina y la vinblastina (Cragg y Newman 1999), principalmente a partir de plantas superiores debido a su accesibilidad. Sin embargo, actualmente algunos fármacos obtenidos de organismos marinos han mostrado resultados prometedores en diversas fases de esta enfermedad.
Las capacidades metabólicas y fisiológicas de los organismos marinos que les permiten sobrevivir en un hábitat complejo les confieren un enorme potencial para la producción de metabolitos únicos que no se encuentran en ambientes terrestres. Así, los organismos marinos y particularmente los invertebrados sésiles han sido reconocidos como una fuente atractiva de potenciales compuestos farmacéuticos (Faulkner 2002). Entre estos organismos, las algas se reconocen también como una de las fuentes más ricas en nuevos compuestos bioactivos de las cuales se han publicado recientemente revisiones sobre la actividad biológica de sus compuestos derivados (Blunt et al. 2006). Con relación a su prometedora actividad para el tratamiento para el cáncer, Yuan y Walsh (2006) obtuvieron actividad antiproliferativa de extractos de Palmaria palmata, Laminaria setchellii, Macrocystis integrifoli y Nereocystis luetkeana sobre la línea celular de aenocarcinoma de cérvix humano (HeLa). El extracto de Stypopodium zonale demostró también gran actividad citotóxica contra la línea celular de melanoma humano (Rocha et al. 2007). Por otro lado, se ha encontrado que varias especies de algas marinas producen metabolitos secundarios con actividad antitumoral (Blunt et al. 2006). Los polisacáridos extraídos de Sargassum stenophyllum y de Capsosiphon fulvescens inhibieron la migración y la viabilidad de las células de melanoma humano in vitro e in vivo (Días et al. 2005) y la inducción de apoptosis en células gástricas humanas (Kwon y Nam 2007), respectivamente. Los fucanos de bajo peso molecular extraídos de Ascophyllum nodosum mostraron actividad antiproliferativa contra el adeno–carcinoma de colon humano (Ellouali et al. 1993) y la línea celular de carcinoma broncopulmonar (Riou et al. 1996). Por otro lado, los esteroles aislados de Galaxaura marginata y de Galaxaura oblongata han demostrado ser citotóxicos a varios tipos de células de cáncer (Sheu et al. 1996, 1997a; Huang et al. 2005). Además, el incremento de los estudios en modelos con roedores han mostrado una prometedora actividad en especies de algas rojas y verdes contra la carcinogénesis de mama (Maruyama et al. 1991, Funahashi et al. 2001), intestinal (Yamamoto y Maruyama 1985) y de la piel (Higashi–Okai et al. 1999). De hecho, el consumo de algas se ha sugerido como agente quimiopreventivo contra el cáncer de mama (Aceves et al. 2005)
Las macroalgas marinas tropicales que crecen en la costa de la Península de Yucatán representan un recurso natural importante poco estudiado. Como parte de la búsqueda de compuestos biológicamente activos nuevos, hemos iniciado el estudio de algas marinas de la costa de la Península de Yucatán. Para ello utilizamos dos análisis para determinar el efecto de extractos acuosos y orgánicos de 27 especies de algas sobre tres líneas celulares humanas de cáncer y en una línea de células normales. El primero fue el ensayo de viabilidad por MTT, el cual determina la actividad mitocondrial en células vivas y ha sido usado para medir la citotoxicidad (Mosmann 1983); el segundo fue el ensayo de sulforodamian B, un colorante que se une a aminoácidos básicos de macromoléculas y ha sido usado para medir la actividad antiproliferativa (Skehan et al. 1990).
Materiales y métodos
Recolecta y preparación de extractos algales
Las algas marinas fueron recolectadas en cuatro lugares en el Golfo de México y la costa del Caribe de la Península de Yucatán entre enero de 2005 y mayo de 2006. Una vez cosechadas, las algas fueron almacenadas en bolsas plásticas y enfriadas en hielo durante su transporte al laboratorio. Se identificaron ejemplares de todas las especies de acuerdo con Littler y Littler (2000) y fueron depositados en el Herbario de Algas Marinas del Cinvestav.
Las muestras recogidas fueron lavadas cuidadosamente con agua dulce para quitar sales, arena y epífitos y fueron almacenadas a –20°C. Se liofilizaron plantas enteras de cada especie y se molieron antes de la extracción. La extracción se realizó de las muestras secas (15 g) con 100 mL de diclorometano:metanol (7:3) durante 24 h. Los extractos fueron denominados orgánicos, fueron filtrados y concentrados hasta secarlos en vacío a 40°C y almacenados a –20°C hasta su utilización. Para preparar los extractos acuosos, semaceraron 10 g del material liofilizado durante 12 h con 100 mL de agua destilada con agitación constante. Posteriormente fueron liofilizados y almacenados como se describió anteriormente.
Líneas celulares y medio de cultivo
Las líneas celulares utilizadas para este estudio fueron: células normales de riñón canino (MDCK), células de carcinoma laríngeo humano (Hep–2), células de adenocarcinoma de cervix humano (HeLa) y células de carcinoma nasoafaríngeo humano (KB). Las células fueron cultivadas en medio de DMEM (Gibco) suplementado con 10% (v/v) de suero fetal bovino (SFB, Gibco), 100 U mL–1 de penicilina y 100 mg mL–1 de estreptomicina. Todas las líneas celulares se mantuvieron a 37°C en una atmósfera de CO2 al 5%, con una humedad del 95%. El medio de cultivo fue cambiado dos veces por semana.
Ensayo de citotoxicidad
Este análisis fue realizado de acuerdo con Rahman et al. (2001), sembrando 1.5 x 104 células viables de cada línea celular en una placa de 96 pozos (Costar) e incubándolas de 24 a 48 h. Cuando las células alcanzaron más del 80% de confluencia, se cambió el medio y las células se trataron con los extractos crudos a 6.25, 12.5, 25 y 50 µg mL–1, disueltos en dimetil sulfóxido (DMSO) a una concentración máxima de 0.05%. Después de 72 h de incubación, se agregaron 10 de una solucion de 5 mg mL–1 de 3[4,5–dimetiltiazol–2–yl]–2,5–bromuro de difeniltetrazolio (MTT, Sigma) a cada uno de los pozos y se incubó a 37°C durante 4 h. Se eliminó el medio y el formazán, un producto generado por la actividad de la deshidrogenasa en las células, fue disuelto en isopropanol acidificado (HCl 0.4 N). La cantidad de MTT–formazán, que es directamente proporcional al número de células vivas, fue determinada midiendo la densidad óptica (DO) a 540 nm usando un lector de prueba biológica (BioRad, USA). Se usó docetaxel (Sigma), un fármaco antitumoral, como control positivo, mientras que las células sin tratar (0.05% DMSO) se usaron como control negativo. Se calculó la concentración del extracto crudo que mató el 50% de las células (CC50). Todas las cocentraciones fueron evaluadas por duplicado y cada experimento fue realizado por triplicado.
Ensayo antiproliferativo
Se realizó un ensayo de la sulforodamina B (SRB) para determinar la inhibición del crecimiento mediante análisis colorimétrico, que estima indirectamente el número de células tiñendo la proteína celular total con el colorante SRB (Rahman et al. 2001). El método se aplicó bajo las mismas condiciones que los análisis citotóxicos, salvo que el medio fue substituído por DMEM al 10% de SFB para inducir la proliferación celular. Después de una incubación de 48 h, se desecho el medio y las células fueron fijadas con 100 µL de ácido tricloroacético frío al 40% (TCA, Aldrich). Después se incubaron las células a 4°C durante 1 h y las placas se lavaron cinco veces con agua fría. Se drenó el exceso de agua y las placas se dejaron secar. Posteriormente, se agregaron 50 µL de SRB (10 mg de ácido acético al 1%, Sigma) y se dejóreposar durante 30 min. Finalmente, las placas se lavaron con 50 mL de ácido acético al 1% y se aclararon cuatro veces hasta que fue posible observar el tinte adherido a las células. Se midió la DO a 540 nm usando un lector ELISA (Bio–Rad modelo 450). Se utilizó docetaxel (Sigma), un fármaco antitumoral, como control positivo, mientras que las células sin tratar fueron utilizadas como controles negativos. Se calculó el valor de IG50, definido como la concentración del extracto que inhibe el 50% del crecimiento celular. Todas las determinaciones se realizaron por triplicado.
Índice de selectividad
Para determinar la especificidad de la actividad citotóxica en las líneas célulares tumorales fue necesario obtener información sobre su citotoxidad en células normales. Por lo tanto, los extractos fueron probados contra una línea de MDCK. El índice de selectividad (SI) fue calculado usando la siguiente ecuación:

Análisis de datos
La actividad citotóxica y antiproliferativa fue determinada como el porcentaje de inhibición de la proliferación celular:

La CC50, IG50 y el 95% del límite de confianza fueron calculados por análisis de Probit.
Resultados
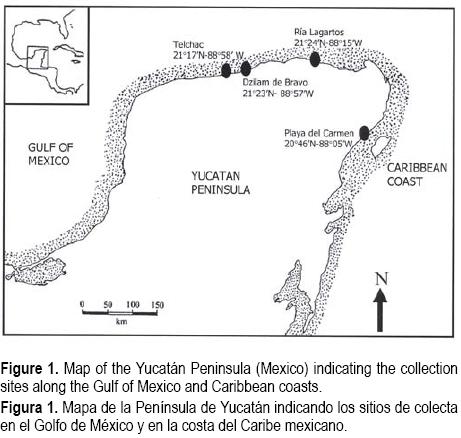
Se recolectaron veintisiete especies de macroalgas pertenecientes a las tres divisiones, en cuatro lugares de la costa (fig. 1). El material algal consistió en catorce especies de algas rojas (Rhodophyta), cinco especies de algas cafés (Phaeophyta) y ocho especies de algas verdes (Chlorophyta). En la tabla 1 se muestra el origen y la información taxonómica de cada especie, así como el rendimiento de sus extractos orgánicos y acuosos (% de peso seco).
Se evaluaron las actividades citotóxicas y antiproliferativas para aclarar si el efecto de los extractos se correlaciona directamente con la inducción de la muerte o sobre la supresión de la proliferación celular. De acuerdo a los criterios del Instituto Nacional del Cáncer de los EUA, un extracto es considerado activo si tiene una CC50 < 30 µg mL1 sobre células tumorales (Suffness y Pezzuto 1990). En este trabajo, la actividad de los extractos se consideró alta si era <30 µg mL–1, media si era de 31–60 µg mL–1 y baja si era de 61–99 µg mL–1.
Es importante señalar que los extractos acuosos no tuvieron una actividad citotoxica y antiproliferativa significativa (datos no mostrados), por lo que en las tablas 2 y 3 solamente se resumen los resultados de la actividad de los extractos orgánicos. Doce de los veintisiete extractos probados mostraron actividad citotóxica alta en algunas líneas celulares. Ninguno de los extractos probados fue más activo que el control positivo. Sin embargo, es necesario considerar que el docetaxel es un compuesto puro, un fármaco usado en el tratamiento del cáncer con una gran actividad citotoxica y antiproliferativa.
Rhodophyta
Dos de las catorce especies de Rhodophyta probadas (Bryothamnion triquetrum y Gracilaria cervicornis) resultaron citotóxicas contra las células de cáncer (tabla 2). Bryothamnion triquetrum mostró una actividad citotóxica alta y selectiva contra las células Hep–2 (CC50 = 8.29 µg mL–1 y SI = 12.04), así como una actividad media contra las células KB y HeLa (CC50= 32.57 y 48.45 µg mL–1, respectivamente). Sin embargo, el extracto mostró una actividad antiproliferativa baja en las células KB (IG50 62.98 µg mL1) (tabla 3).
Por otra parte, Gracilaria cervicornis mostró una actividad citotóxica alta contra las células KB (CC50= 19.23 µg mL–1); sin embargo, mostró actividad citotoxica en las células normales (CC50 = 48.64 µg mL1). Su actividad antiproliferativa contra células KB y HeLa fue baja (IG50= 68.28 y 75.56 µg mL–1 , respectivamente).
Phaeophyta
Tres de las cinco especies probadas de Phaeophyta (Turbinaria turbinata, Lobophora variegata y Dictyota caribaea) mostraron una cierta actividad en la línea celular KB. El extracto de T. turbinata mostró las actividades citotóxica y antiproliferativa más altas contra células KB (CC50= 23.94 µg mL–1 e IG50= 29.84 µg mL–1, respectivamente); sin embargo, también mostró actividad citotóxica contra las células normales (tabla 2).
Chlorophyta
Excluyendo la especie Halimeda tuna, los extractos de todas las Chlorophyta probadas mostraron alguna actividad citotóxica y antiproliferativa contra las células tumorales (tablas 2, 3). Las propiedades citotóxicas (CC50≤ 30 µg mL–1) obtenidas fueron altas y como sigue: P. dumetosus > U. conglutinata > U. flabellum, sobre las células Hep–2; U. flabellum > U. conglutinata > P. lamourouxii > H. incrassata, sobre las células HeLa; y U. flabellum > U. conglutinata > A. digitata > P. lamourouxii > P. dumetosus > R. phoenix, sobre las células KB.
Discusión
En este estudio se muestra la primera investigación sobre la potencial actividad citotóxica y antiproliferativa de extractos crudos de macroalgas marinas de la Península de Yucatán sobre diferentes líneas celulares de cáncer. Los resultados indicaron que 44% y 51% de las especies exhibieron actividad citotóxica y antiproliferativa, respectivamente, proporcionando evidencia de que estos recursos son una fuente potencial de drogas para ser usadas contra algunos tipos de cáncer. La mayoría de las especies que mostraron actividad citotóxica pertenecen a la división Chlorophyta, mientras que el extracto de la especie Bryothamnion triquetrum (Rhodophyta) tuvo una destacada actividad citotóxica selectiva contra las células Hep–2.
En relación con los extractos acuosos, que no mostraron ninguna importante actividad, se considera que los extractos orgánicos poseen diferentes constituyentes en comparación con los extractos hidrofílicos que pueden ser importantes por los efectos citotoxicos y antiproliferativos sobre líneas celulares de cáncer. El factor más importante es la permeación a la membrana: los compuestos lipofílicos son permeables a la membrana en tanto que los hidrofílicos no. Esto puede explicar al menos en parte el poco efecto de los extractos hidrofílicos sobre las líneas celulares.
Rhodophyta
Bryothamnion triquetrum contiene lectina como componente principal en sus células con estructuras primarias que difieren de las procedentes de plantas o animales, por lo que esta proteína puede ser el paradigma de una nueva familia de lectina (Calvete et al. 2000). Las lectinas interactúan con estructuras específicas de glicanos unidas a glicoconjugados solubles de la membrana. Estas interacciones entre proteína y carbohidrato desempeñan un papel relevante en algunos procesos biológicos tales como la comunicación entre las células, las infecciones patógenas y la defensa del huésped, fertilización, desarrollo, diferenciación de la célula, cáncer y metástasis (Damme et al. 1998, Beisel et al. 1999). Existen evidencias que demuestran que las lectinas de plantas terrestres tienen actividad antitumoral (Dalla Pellegrina et al. 2004, Park et al. 2004, Chauhan et al. 2005, Khil et al. 2007). Sin embargo, en este estudio el extracto acuoso que contiene compuestos hidrofílicos como la lectina, no registró actividad importante, lo que sugiere que las lectinas no podrían ser las responsables de la actividad citotóxica y antiproliferativa de B. triquetum sobre las células tumorales. Son necesarios más estudios para aislar e identificar los compuestos activos de B. triquetum responsables de tales efectos.
Con relación a la alta actividad citotóxica mostrada por Gracilaria cervicornis sobre las células de KB, es de destacar que se han aislado ácidos grasos clorados (Shoeb y Jaspars 2003), lecitinas con actividad acaricida (Leite et al. 2005), policavernósidos tóxicos (Yotsu–Yamashita et al. 2004) y ciclopropano con cerebrosidos, con citotoxicidad débil sobre la línea celular de melanoma (Ito y Nagai 1998, Sun et al. 2006). Sin embargo, aunque no existen otros trabajos en los que se haya reportado actividad citotoxica para esta especie en particular, los resultados obtenidos en el presente estudio hacen de G. cervicornis una candidata para futuras investigaciones.
Phaeophyta
Los bromofenoles y fenoles son una de las principales moléculas bioactivas de las Phaeophyta y recientemente han recibido gran atención debido a sus efectos terapéuticos (Kolodziej et al. 2001, Paul y Puglisi 2004, Tasdemir et al. 2006). Los florotaninos o polifenoles de algas cafés poseen un papel defensivo contra herbívoros principalmente en especies algales tropicales. Son polímeros derivados del acetato–malonato de floroglucinol y se encuentran en concentraciones altas de 25% a 40% del peso seco (Ragan y Glombitza 1986). Los florotaninos son importantes en el género Lobophora, en cuyas especies se encuentran en concentraciones de 13.9% a 29.2% de peso seco (Targett et al. 1992, Zubia et al. 2007). De hecho, se ha reportado una notable producción de florotaninos de 330 µg g–1 día–1 y una alta tasa metabólica para las especies de este género (Arnold y Targett 1998, Arnold y Targett 2000). Recientemente Zubia et al. (2007) reportaron que el extracto orgánico de L. variegata de Yucatán mostró una alta actividad antioxidante atribuíble a su alto contenido fenólico. Los compuestos fenólicos son generalmente conocidos por mostrar no sólo actividad antioxidante sino también pro–oxidante. Por ejemplo, el 4–metilcatecol ejerce una acción oxidante en las células en cultivo a través de la generación de peróxido de hidrógeno. Este efecto también puede ser observado incluso incubando el compuesto en el medio sin las células (Morita et al. 2003). La quercetina y los compuestos fenolicos relacionados que contienen una forma del catecol en sus estructuras químicas, han mostrado que son fácilmente oxidados, dando por resultado la peroxidación de lípidos bajo ciertas condiciones en ensayos in vitro (Laughton et al. 1989, Yamanaka et al. 1997, Galati et al. 1999). Otros estudios recientes también han mostrado que estos compuestos se pueden oxidar y pueden generar rápidamente el peróxido de hidrógeno en medios de cultivo celulares de uso general (Long et al. 2000). De acuerdo con estos resultados, parecería razonable considerar que los compuestos fenólicos que son completamente solubles en solventes orgánicos pueden ejercer daño oxidativo en las células como resultado de la generación de peróxido de hidrógeno en el medio de cultivo. Sin embargo, esta inferencia es poco probable debido a que L. variegata mostró una selectividad alta sobre células tumorales (SI de 6 a 17), implicando un selectivo mecanismo de acción sobre las celulas de cáncer. Además de lo anterior, la actividad antiproliferativa de L. variegata fue baja en las células KB (IG50= 68.48 µg mL–1). Un trabajo reciente mostró una débil inhibición del crecimiento de L.variegata a concentraciones <100 µg mL–1 contra células de melanoma, aunque fracciones semipurificadas mostraron un incremento del efecto con una IG50 < 18 µg mL–1 (Rocha et al. 2007), lo que sugiere la existencia de metabolitos secundarios específicos que podrían interferir con la mitosis celular. Algunas evidencias han propuesto que los compuestos fenólicos inhiben la actividad de la telomerasa en las células tumorales (Naasani et al. 1998, Mizushina et al. 2005, Chakraborty et al. 2006). La telomerasa es una transcriptasa reversa especializada, tiene un importate papel en el proceso de inmortalización y tumorogénesis. En la mayoría de los tumores, el mantenimiento de los telómeros se alcanza con la expresión de la telomerasa (Akiyama et al. 2002). El alto contenido fenólico de L. variegata puede ser la causa del efecto selectivo sobre las células tumorales, probablemente como resultado de la inhibición sobre la actividad de la telomerasa. En este sentido, es necesario realizar estudios más profundos para sustentar esta implicación. Por otro lado, el loboforólido, un macrólido policíclico estructuralmente sin precedente en algas marinas ha sido recientemente aislado de esta especie mostrando actividad antineoplásica contra la línea celular del tumor de colon HCT–116 (Kubanek et al. 2003). Por todo lo anterior, L. variegata de Yucatán se perfila como una especie prometedora y de interés para continuar con futuras investigaciones en este campo.
Por otro lado, la actividad citotóxica mostrada por Dictyota caribaea puede ser debida a la presencia de diterpenos puesto que ha sido reportado que la familia Dictyotaceae produce una serie de diterpenos únicos con actividad contra las células tumorales (Gedara et al. 2003). En cuanto a la actividad mostrada por Turbinaria turbinata, se han aislado compuestos citotóxicos y antitumorales de esta especie tales como el ácido turbinárico (Asari et al. 1989), esteroles (Sheu et al. 1997b) y fucosteroles oxigenados (Sheu et al. 1999), que podrían ser los responsables del efecto tanto citocidal como citoestático que provocan daño tanto a las células tumorales como a las normales.
Chlorophyta
La familia Udoteaceae (Halimeda, Penicillus y Udotea) mostró un cierto patrón citotóxico en relación con el análisis taxonómico a nivel de género. Esta familia es conocida por la producción de terpenos (Fenical y Paul 1984, Paul y Fenical 1987) y, aunque no es posible excluir que una o varias moléculas contribuyan a esta capacidad, la presencia de terpenos en Chlorophyta puede estar relacionada con la actividad citotóxica mostrada, puesto que se ha demostrado que este tipo de metabolitos, aislados de fuentes terrestres, son responsables de actividad citotóxica (Kintzios 2006). Los extractos de U. flabellum y de U. conglutinata mostraron la actividad citotóxica selectiva más alta contra todas las variedades de células de cáncer. El diterpenoide hidrato de udoteatrial ha sido aislado de la especie U. flabellum (Nakatsu et al. 1981), y sus análogos sintéticos han mostrado una significativa citotoxicidad in vitro contra el carcinoma humano KB y A–549 (Yu–Ting et al. 1993). Basado en lo anterior, las especies de Udotea se perfilan como fuentes potenciales para el desarrollo de nuevos agentes quimioterapéuticos.
Por otro lado, A. cf digitata mostró también una alta actividad citotóxica y antiproliferativa sobre células KB. Este resultado es similar al obtenido en estudios previos donde diferentes especies de Avrainvillea han mostrado que producen isorawsonol, un derivado brominado del difenilmetano que se relaciona con la inhibición de la proliferación celular (Chen et al. 1994). Adicionalmente, los antimitóticos glicoglicerolípidos, que juegan un papel importante en el retraso del ciclo celular en células de cáncer humano, han sido aislados de especies de este genero (Williams et al. 2007), lo que suigiere que Avrainvillea podría ser usada para el aislamiento de compuestos antiproliferativos.
En cuanto a la alta citotoxicidad mostrada por las dos especies de Penicillus de Yucatán, no existe a la fecha ningún otro estudio donde se reporten actividades similares a las encontradas en el presente estudio.
Agradecimientos
Esta investigación fue financiada por SEP–CONACYT 053687 e IMSS–FOFOI (contrato 2005/1/I/051). Los autores desean agradecer el Cinvestav por la beca postdoctoral de R Moo–Puc.
Referencias
Aceves C, Anguiano B, Delgado G. 2005. Is iodine a gatekeeper of the integrity of the mammary gland? J. Mammary Gland Biol. Neoplasia 10: 189–196. [ Links ]
Akiyama M, Hideshima T, Munshi NC, Anderson KC. 2002. Telomerase inhibitors as anticancer therapy. Curr. Med. Chem. Anticancer Agents 2: 567–575. [ Links ]
Arnold TM, Targett NM. 1998. Quantifying in situ rates of phlorotannin synthesis and polymerization in marine brown algae. J. Chem. Ecol. 24: 577–595. [ Links ]
Arnold TM, Targett NM. 2000. Evidence for metabolic turnover of polyphenolics in tropical brown algae. J. Chem. Ecol. 26: 1393–1410. [ Links ]
Asari F, Kusumi T, Kakisawa H. 1989.Turbinaric acid, a cytotoxic secosqualene carboxylic acid from the brown alga Turbinaria ornata. J. Nat. Prod. 52: 1167–1169. [ Links ]
Beisel H, Kawabata S, Iwanaga S, Huber R, Bode W. 1999. Tachylectin–2: Crystal structure of a specific GlcNAc:GalNAc–binding lectin involved in the innate immunity host defense of the Japanese horseshoe crab Tachypleus tridentatus. EMBO J 18: 2313–2322. [ Links ]
Blunt JW, Copp BR, Munro MHG, Northcote PT, Prinsep MR. 2006. Marine natural products. Nat. Prod. Rep. 23: 26–78. [ Links ]
Calvete JJ, Costa FH, Saker–Sampaio S, Murciano MP, Nagano CS, Cavada BS, Grangeiro TB, Ramos MV, Bloch C Jr, Silveira SB, Freitas BT, Sampaio AH. 2000. The amino acid sequence of the agglutinin isolated from the red marine alga Bryothamnion triquetrum defines a novel lectin structure. Cell Mol. Life Sci. 57: 343–50. [ Links ]
Chakraborty S, Ghosh U, Bhattacharyya NP, Bhattacharya RK, Roy M. 2006. Inhibition of telomerase activity and induction of apoptosis by curcumin in K–562 cells. Asian Pac. J. Cancer Prev. 7: 201–207. [ Links ]
Chauhan D, Li G, Podar K, Hideshima T, Neri P, He D, Mitsiades N, Richardson P, Chang Y, Schindler J, Carver B, Anderson KC. 2005. A novel carbohydrate–based therapeutic GCS–100 overcomes bortezomib resistance and enhances dexamethasone–induced apoptosis in multiple myeloma cells. Cancer Res. 65: 8350–8358. [ Links ]
Chen JL, Gerwick WH, Schatzman R, Laney M. 1994. Isorawsonol and related IMP dehydrogenase inhibitors from the tropical green alga Avrainvillea rawsonii. J. Nat. Prod. 57: 947–952. [ Links ]
Cragg GM, Newman DJ. 1999. Discovery and development of antineoplastic agents from natural sources. Cancer Invest. 17: 153–163. [ Links ]
Dalla Pellegrina C, Matucci A, Zoccatelli G, Rizzi C, Vincenzi S, Veneri G, Andrighetto G, Peruffo AD, Chignola R, 2004. Studies on the joint cytotoxicity of wheat germ agglutinin and monensin. Toxicol. in Vitro 18: 821–827. [ Links ]
Damme EJM, Van–Peumans WJ, Barre A, Rouge P. 1998. Plant lectins: A composite of several distinct families of structurally and evolutionary related proteins with diverse biological roles. Crit. Rev. Plant Sci. 17: 575–692. [ Links ]
Días PF, Siqueira JM, Vendruscolo LF, de Jesus Neiva T, Gagliardi AR, Maraschin M, Ribeiro–do–Valle RM. 2005. Antiangiogenic and antitumoral properties of a polysaccharide isolated from the seaweed Sargassum stenophyllum. Cancer Chemother. Pharmacol. 56: 436–446. [ Links ]
Ellouali M, Boisson–Vidal C, Durand P, Jozefonvicz J. 1993. Antitumor activity of low molecular weight fucans extracted from brown seaweed Ascophyllum nodosum. Anticancer Res. 13: 2011–2019. [ Links ]
Faulkner DJ. 2002. Marine natural products. Nat. Prod. Rep. 19: 1–48. [ Links ]
Fenical W, Paul VJ. 1984. Antimicrobial and cytotoxic terpenoids from tropical green algae of the family Udoteaceae. Hydrobiologia 116/117: 135–170. [ Links ]
Funahashi H, Imai T, Mase T, Sekiya M, Yokoi K, Hayashi H, Shibata A, Hayashi T, Nishikawa M, Suda N, Hibi Y, Mizuno Y, Tsukamura K, Hayakawa A, Tanuma S. 2001. Seaweed prevents breast cancer? Jpn. J. Cancer Res. 92: 483–487. [ Links ]
Galati G, Chan T, Wu B, O'Brien PJ. 1999. Glutathione–dependent generation of reactive oxygen species by the peroxidase–catalyzed redox cycling of flavonoids. Chem. Res. Toxicol. 12: 521–525. [ Links ]
Gedara R, Zubía E, Ortega M, el–Sharkavy S, Salama O, Shier T, Halim A. 2003. Cytotoxic hydroazulenne diterpenes from the brown alga Dictyota dichotoma. Z. Naturforsch. 58: 17–22. [ Links ]
Gottesman MM, Pastan I, 1993. Biochemistry of multidrug resistance mediated by the multidrug transporter. Annu. Rev. Biochem. 62: 385–427. [ Links ]
Higashi–Okai K, Otani S, Okai Y. 1999. Potent suppressive effect of a Japanese edible seaweed, Enteromorpha prolifera (Sujiao–nori) on initiation and promotion phases of chemically induced mouse skin tumorigenesis. Cancer Lett. 1: 21–25. [ Links ]
Huang HL, Wu SL, Liao HF, Jiang CM, Huang RL, Chen YY, Yang YC, Chen YJ. 2005. Induction of apoptosis by three marine algae through generation of reactive oxygen species in human leukemic cell lines. J Agric. Food Chem. 53: 1776–1781. [ Links ]
INEGI (Instituto Nacional de Geografía e Informática). 2006. Mortalidad general por edad y causas detalladas. Sistemas Nacionales Estadístico y de Información Geográfica, México. [ Links ]
Isnard–Bagnis C, Moulin B, Launay–Vacher V, Izzedine H, Tostivint I, Deray G. 2005. Anticancer drug–induced nephrotoxicity. Nephrol. Ther. 1: 101–114. [ Links ]
Ito E, Nagai H. 1998. Morphological observations of diarrhea in mice caused by aplysiatoxin, the causative agent of the red alga Gracilaria coronofolia poisoning in Hawaii. Toxicon 36: 1913–1920. [ Links ]
Khil LY, Kim W, Lyu S, Park WB, Yoon JW, Jun HS. 2007. Mechanisms involved in Korean mistletoe lectin–induced apoptosis of cancer cells. World J. Gastroenterol. 13: 2811–2818. [ Links ]
Kintzios SE. 2006. Terrestrial plant–derived anticancer agents and plant species used in anticancer research. Crit. Rev. Plant Sci. 25: 79–113. [ Links ]
Kolodziej H, Kayser O, Kiderlen AF, Ito H, Hatano T, Yoshida T, Foo LY. 2001. Antileishmanial activity of hydrolyzable tannins and their modulatory effects on nitric oxide and tumor necrosis factor–alpha release in macrophages in vitro. Planta Med. 67: 825–832. [ Links ]
Kubanek J, Jensen PR, Keifer PA, Sullards MC, Collins DO, Fenical W. 2003. Seaweed resistance to microbial attack: A targeted chemical defense against marine fungi. Proc. Natl. Acad. Sci. USA 100: 6916–6921. [ Links ]
Kwon MJ, Nam TJ. 2007. A polysaccharide of the marine alga Capsosiphon fulvescens induces apoptosis in AGS gastric cancer cells via an IGF–IR–mediated PI3K/Akt pathway. Cell Biol. Int. 31: 768–775. [ Links ]
Laughton MJ, Halliwell B, Evans PJ, Hoult JR. 1989. Antioxidant and pro–oxidant actions of the plant phenolics quercetin, gossypol and myricetin. Effects on lipid peroxidation, hydroxyl radical generation and bleomycin–dependent damage to DNA. Biochem. Pharmacol. 38: 2859–2865. [ Links ]
Leite YF, Silva LM, Amorim RC, Freire EA, de Melo JDM, Grangeiro TB, Benevides NM. 2005. Purification of a lectin from the marine red alga Gracilaria ornata and its effect on the development of the cowpea weevil Callosobruchus maculatus (Coleoptera: Bruchidae). Biochim. Biophys. Acta 1724: 137–145. [ Links ]
Littler DS, Littler MM. 2000. Caribbean Reef Plants. 2nd ed. Offshore Graphics, USA, 300 pp. [ Links ]
Long LH, Clement MV, Halliwell B. 2000. Artifacts in cell culture: Rapid generation of hydrogen peroxide on addition of (–)–epigallocatechin, (–)–epigallocatechin gallate, (+)–catechin and quercetin to commonly used cell culture media. Biochem. Biophys. Res. Commun. 273: 50–53. [ Links ]
Maruyama H, Watanabe K, Yamamoto I. 1991. Effect of dietary kelp on lipid peroxidation and glutathione peroxidase activity in livers of rats given breast carcinogen DMBA. Nutr. Cancer 15: 221–228. [ Links ]
Mizushina Y, Ishidoh T, Takeuchi T, Shimazaki N, Koiwai O, Kuramochi K, Kobayashi S, Sugawara F, Sakaguchi K, Yoshida H. 2005. Monoacetylcurcumin: A new inhibitor of eukaryotic DNA polymerase lambda and a new ligand for inhibitor–affinity chromatography. Biochem. Biophys. Res. Commun. 337: 1288–1295. [ Links ]
Morita K, Arimochi H, Ohnishi Y. 2003. In vitro cytotoxicity of 4–methylcatechol in murine tumor cells: Induction of apoptotic cell death by extracellular pro–oxidant action. Pharmacol. Exp. Ther. 306: 317–323. [ Links ]
Mosmann T. 1983. Rapid colorimetric assay for cellular growth and survival: Application to proliferation and cytotoxicity assays. J. Immunol. Methods 16: 55–63. [ Links ]
Naasani I, Seimiya H, Tsuruo T. 1998. Telomerase inhibition, telomere shortening, and senescence of cancer cells by tea catechins. Biochem. Biophys. Res. Commun. 249: 391–396. [ Links ]
Nakatsu T, Ravi BN, Faulkner DJ. 1981. Antimicrobial constituents of Udotea flabellum. J. Org. Chem. 46: 2435–2438. [ Links ]
Park JH, Ryu CS, Kim HN, Na YJ, Park HJ, Kim H. 2004. A sialic acid–specific lectin from the mushroom Paecilomyces japonica that exhibits hemagglutination activity and cytotoxicity. Protein Pept. Lett. 11: 563–569. [ Links ]
Paul VJ, Fenical W. 1987. Natural products chemistry and chemical defense in tropical marine algae of the phylum Chlorophyta. Bioorg. Mar. Chem. 1: 1–29. [ Links ]
Paul VJ, Puglisi MP. 2004. Chemical mediation of interactions among marine organisms. Nat. Prod. Rep. 21: 189–209. [ Links ]
Ragan MA, Glombitza KW. 1986. Plorotannins, brown algal polyphenols. Prog. Phycol. Res. 4: 130–230. [ Links ]
Rahman A, Choudhary MI, Thomsen WJ. 2001. Bioassay Techniques for Drug Development. In: Manual of Bioassay Techniques for Natural Products Research, Harwood Academic Publishers, Netherlands, pp. 34–35. [ Links ]
Riou D, Colliec–Jouault S, Pinczon du Sel D, Bosch S, Siavoshian S, De Bert V, Tomasoni C, Sinquin C, Durand P, Roussakis C. 1996. Antitumor and antiproliferative effects of a fucan extracted from Ascophyllum nodosum against a non–small–cell broncho–pulmonary carcinoma line. Anticancer Res. 16: 1213–1218. [ Links ]
Rocha FD, Soares AR, Houghton PJ, Pereira RC, Kaplan MA, Teixeira VL. 2007. Potential cytotoxic activity of some Brazilian seaweeds on human melanoma cells. Phytother. Res. 21: 170–175. [ Links ]
Sheu JH, Huang SY, Duh CY. 1996. Cytotoxic oxygenated desmosterols of the red alga Galaxaura marginata. J. Nat. Prod. 59: 23–26. [ Links ]
Sheu JH, Huang SY, Wang GH, Duh CY. 1997a. Study on cytotoxic oxygenated desmosterols isolated from the red alga Galaxaura marginata. J. Nat. Prod. 60: 900–903. [ Links ]
Sheu JH, Wang GH, Sung PJ, Chiu YH, Duh CY. 1997b. Cytotoxic sterols from the Formosan brown alga Turbinaria ornata. Planta Med. 63: 571–572. [ Links ]
Sheu JH, Wang GH, Sung PJ, Duh CY. 1999. New cytotoxic oxygenated fucosterols from the brown alga Turbinaria conoides. J. Nat. Prod. 62: 224–227. [ Links ]
Shoeb M, Jaspars M. 2003. Chlorinated C12 fatty acid metabolites from the red alga Gracilaria verrucosa. J. Nat. Prod. 66: 1509–1511. [ Links ]
Skehan P, Storeng R, Scudiero D, Monks A, McMahon J, Vistica D, Warren JT, Bokesch H, Kenney S, Boyd MR. 1990. New colorimetric cytotoxicity assay for anticancer–drug screening. J. Natl. Cancer Inst. 4: 1107–1112. [ Links ]
Smith BD, Bambach BJ, Vala MS, Barber JP, Enger C, Brodsky RA, Burke PJ, Gore SD, Jones RJ. 1998. Inhibited apoptosis and drug resistance in acute myeloid leukaemia. Br. J. Haematol. 102: 1042–1049. [ Links ]
Suffness M, Pezzuto JM. 1990. Assays related to cancer drug discovery. In: Hostettmann K (ed.), Methods in Plant Biochemistry: Assays for Bioactivity. Vol. 6. Academic Press, London, pp. 71–133. [ Links ]
Sun Y, Xu K, Liu K, Hua H, Zhu H, Pei Y. 2006. Gracilarioside and gracilamides from the red alga Gracilaria asiatica. J. Nat. Prod. 69: 1488–1491. [ Links ]
Targett NM, Coen LC, Boettcher AA, Tanner CE. 1992. Biogeographic comparisons of marine algal polyphenolics evidence against a latitudinal trend. Oecologia 89: 464–470. [ Links ]
Tasdemir D, Kaiser M, Brun R, Yardley V, Schmidt TJ, Tosun F, Rüedi P. 2006. Antitrypanosomal and antileishmanial activities of flavonoids and their analogues: in vitro, in vivo, structure–activity relationship and quantitative structure–activity relationship studies. Antimicrob. Agents Chemother. 50: 1352–1364. [ Links ]
Williams DE, Sturgeon CM, Roberge M, Andersen RJ. 2007. Nigricanosides A and B, antimitotic glycolipids isolated from the green alga Avrainvillea nigricans collected in Dominica. J. Am. Chem. Soc. 129: 5822–5823. [ Links ]
Yamamoto I, Maruyama H. 1985. Effect of dietary seaweed preparations on 1,2–dimethylhydrazine–induced intestinal carcinogenesis in rats. Cancer Lett. 26: 241–51. [ Links ]
Yamanaka N, Oda O, Nagao S. 1997. Green tea catechins such as (–)–epicatechin and (–)–epigallocatechin accelerate Cu2+–induced low density lipoprotein oxidation in propagation phase. FEBS Lett. 401: 230–234. [ Links ]
Yotsu–Yamashita M, Yasumoto T, Yamada S, Bajarias FF, Formeloza MA, Romero ML, Fukuyo Y. 2004. Identification of polycavernoside A as the causative agent of the fatal food poisoning resulting from ingestion of the red alga Gracilaria edulis in the Philippines. Chem. Res. Toxicol. 17: 1265–71. [ Links ]
Yuan YV, Walsh NA. 2006. Antioxidant and antiproliferative activities of extracts from a variety of edible seaweeds. Food Chem. Toxicol. 44: 1144–1150. [ Links ]
Yu–Ting GE, Kondo S, Katsumura S, Nakatani K, Isoe S. 1993. Absolute configuration of novel marine diterpenoid udoteatrial hydrate synthesis and cytotoxicities of ent–udoteatrial hydrate and its analogues. Tetrahedron 49: 10555–10576. [ Links ]
Zubia M, Robledo D, Freile–Pelegrin Y. 2007. Antioxidant activities in tropical marine macroalgae from the Yucatán Peninsula, Mexico. J. Appl. Phycol. 19: 449–458. [ Links ]
* DESCARGAR VERSIÓN BILINGÜE (INGLÉS–ESPAÑOL) EN FORMATO PDF














