Introducción
La farmacopea clásica empleada para atenuar y/o abolir la dependencia a drogas de abuso ilegal, con alta potencia adictiva como la cocaína, ha demostrado una eficacia terapéutica limitada, tanto al corto como al largo plazo.1,2 Basado en este desalentador panorama clínico-terapéutico, desde hace más de una década diversos investigadores han desarrollado nuevas estrategias terapéuticas contra la adicción a drogas como la cocaína.3,4
Algunos grupos de investigación han desarrollado terapias farmacológicas mediante el uso de nuevos fármacos,5,6 otros han validado métodos de inmunoterapia basados en procedimientos de vacunación activa y pasiva7,8 y unos más han explorado el uso de proteínas que involucran la destrucción de la molécula de cocaína, antes de que tenga la oportunidad de cruzar la barrera hemato-encefálica y penetrar en el tejido nervioso (Figura 1-B), como es el aumento en la actividad catalítica de enzimas como la butiril-colinesterasa (BChE)9,10,11 y la carboxilo-esterasas hepáticas (hCE-1 y hCE-2).
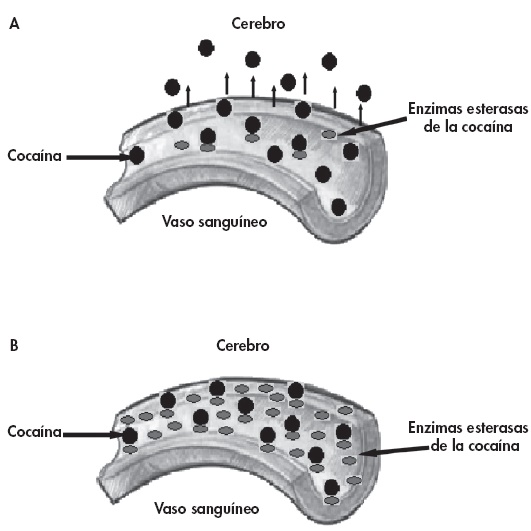
Figura 1 (A) La cocaína rápidamente se localiza dentro de los vasos sanguíneos, cruza la barrera hemato-encefálica y alcanza a su sitio blanco dentro del cerebro. Dentro de los vasos sanguíneos se localizan enzimas que hidrolizan a la cocaína (BChE, CocE), pero son pocas y su capacidad hidrolítica es limitada, por lo que son poco eficientes. (B) Cuando se administran enzimas puras o modificadas genéticamente (incrementa su capacidad de hidrólisis y su vida media) capturan rápidamente a la cocaína dentro del vaso, la hidrolizan en sus metabólitos inactivos e impiden que se lleven a cabo sus efectos reforzantes o tóxicos.
Diversos estudios epidemiológicos han reportado que un gran porcentaje de las muertes relacionadas al abuso de cocaína están generalmente relacionadas a una intoxicación por una sobredosis, debido principalmente a que se carece de una terapia eficaz.12 Desde hace varios años diversos grupos de investigación han realizado estudios encaminados a desarrollar y validar algunas estrategias terapéuticas con relativo éxito. Como se mencionó anteriormente, una de estas estrategias ha sido el aumento en la actividad catalítica de las enzimas encargadas de metabolizar a la molécula de la cocaína. Se han reportado diversos estudios describiendo cómo, mediante técnicas de biología molecular, se ha logrado potenciar la actividad de esta(s) enzima(s); otros estudios han descrito el efecto del tratamiento con estas enzimas en roedores y en humanos. Sin embargo, se carece de una revisión que describa los beneficios, ventajas, desventajas y el potencial uso futuro del aumento de la actividad catalítica de las enzimas encargadas de metabolizar a la cocaína, la BChE y las hC. El objetivo de esta revisión fue analizar los avances científicos relacionados con el aumento en la actividad catalítica de las enzimas BChE y las hCE, con el fin de describir sus principales efectos biológicos y su posible uso para el tratamiento de pacientes en condiciones de toxicidad por sobredosis de cocaína.
Método
La búsqueda bibliográfica se realizó usando el motor de búsqueda "Entrez PubMed"; en la búsqueda se utilizaron las siguientes palabras clave: Cocaine, butyrylcholinesterase, hydrolase y esterase. La búsqueda se realizó abarcando un periodo de enero de 1970 a diciembre de 2015. El algoritmo de búsqueda fue: ("cocaine"[MeSH Terms] OR "cocaine"[All Fields]) AND ("hydrolases"[MeSH Terms] OR "hydrolases"[All Fields] OR "hydrolase"[All Fields]) AND ("esterases"[MeSH Terms] OR "esterases"[All Fields] OR "esterase"[All Fields]) AND ("cholinesterases"[MeSH Terms] OR "cholinesterases"[All Fields] OR "butyrylcholinesterase"[All Fields] OR "butyrylcholinesterase"[MeSH Terms]).
Los criterios de inclusión fueron: 1) Estudios publicados en revistas internacionales indexadas, 2) artículos de investigación básica, preclínica, clínica y de revisión que 3) describan la estructura, bioquímica y cinética de las enzimas BChE y hCE, así como la caracterización del efecto biológico-terapéutico y de seguridad biológica, 4) en animales (roedores, conejos y primates) y humanos adultos, 5) estudios que se realizaron en Estados Unidos, Canadá y la Comunidad Europea y 6) que fueron publicados en idiomas inglés, francés y español.
Los criterios de exclusión fueron: que los artículos fueran 1) editoriales, opiniones de expertos o comunicaciones a congresos, 2) que los artículos, en su contenido, no incluyeran información acerca del objetivo del estudio, 3) su contenido se encontrara repetido en el contenido de otro artículo.
El análisis de los resultados indicó que la búsqueda bibliográfica arrojó un total de 220 artículos, de los cuales sólo 126 fueron considerados para la inclusión en esta revisión. De estos 126 artículos, 97 son artículos de investigación, nueve de investigación clínica, un meta-análisis y 19 artículos de revisión (Figura 2).
Resultados
Butiril-colinesterasa
La cocaína, una vez ingerida, es metabolizada casi en su totalidad. La principal vía de transformación es la hidrólisis enzimática, siendo las esterasas plasmáticas (BChE) y hepáticas (hCE-1) las principales enzimas responsables de la formación de sus metabólitos: éster de metilo-ecgonina, ecgonina y benzoil-ecgonina (Figura 1-A).
La BChE es la principal enzima que metaboliza a la cocaína en el plasma, tanto en humanos como en otras especies.13,14,15,16
La vida media de la BChE en el plasma de los animales es de aproximadamente 21.6 horas17,18,19 y metaboliza rápidamente a la molécula de cocaína20,21,22,23 en el metabolito éster de metilo-ecgonina; en cambio, las enzimas hepáticas transforman a la cocaína en los metabólitos norcocaina y benzoílo-ecgonina.20,24,25,26,27,28 Este cambio en el perfil metabólico de la cocaína tiene importantes implicaciones fisiológicas. Algunos estudios han demostrado que la benzoil-ecgonina es un potente vaso-constrictor29,30 y genera crisis convulsivas;31 por su lado, la norcocaína es un metabolito muy hepatotóxico y un poderoso anestésico local.32,33 En cambio, el éster de metilo-ecgonina no genera ningún efecto fisiológico adverso y es rápidamente eliminado por el riñón, por lo que el incremento en la concentración de este metabolito no genera efectos tóxicos en el sujeto.34
Diversa evidencia clínica sugiere que la actividad de la BChE endógena está inversamente correlacionada con la severidad de la toxicidad que la cocaína puede generar en humanos.35,36 Los niveles normales de BChE varían entre los individuos y son dependientes de la edad, el estado de salud, la exposición a toxinas ambientales y a factores genéticos.37,38,39
Algunos reportes clínicos indican que los individuos que sufren de graves problemas médicos después del uso de la cocaína, tienden a mostrar una menor actividad en la BChE plasmática que aquellos que experimentan problemas menos severos.40,41,42 Adicionalmente, algunos estudios genéticos han reportado que en casos extremos de intoxicación con cocaína, los pacientes homocigotos muestran, o bien una variante "silente" de la BChE, la cual no expresa actividad catalítica detectable,43,44 o bien niveles bajos de expresión de la BChE, o incluso muestran variantes defectuosas o "atípicas" de la enzima. Estos pacientes experimentan respuestas prolongadas a la cocaína. Estudios in vitro demostraron que la BChe proveniente de sueros de pacientes atípicos, muestran una disminución del 50% en la capacidad para hidrolizar a la cocaína en el plasma,45,46 lo cual sustenta la importante labor que lleva a cabo la BChE en el suero de sujetos dependientes a la droga.
Algunos estudios pioneros han reportado que pacientes dependientes a la cocaína que han recibido BChE humana purificada (obtenida de suero de donantes), no han presentado eventos clínicos adversos hasta por dos días,47,48 lo cual sugiere que la administración de BChE podría ser una terapia útil para tratar a pacientes dependientes a la cocaína.
En modelos animales, la administración diaria por siete días de cocaína (20 mg/kg ip.), a ratones knockout de BChE, el cual expresa una baja o nula actividad para catalizarla, generó rápidamente cardiomiopatías, depresión respiratoria (aproximadamente por 12 horas), patrones respiratorios anormales (apneusis) y, a nivel histológico, hepatotoxicidad significativa y fibrosis peri-vascular cardiaca.48 En cambio, ratones con una expresión de BChE normal recuperaron el ritmo respiratorio a valores normales 30 minutos después de la dosificación y no mostraron apneusis ni hepatotoxicidad.49,50,51
Recientemente se reportó el desarrollo de un ratón mutante-doble, el cual mostraba una expresión nula de la carboxyl-esterasa y de la BChE. Cuando se administró una dosis letal de cocaína (100 mg/kg), los ratones doble knockout mostraron un incremento (2.5 veces) en la duración de los signos tóxicos (hipotermia, hiperactividad, conductas estereotipadas, efectos oculares y flexión dorsal de la cola) en comparación con la duración mostrada por el ratón BChE naive.50
Diversas evaluaciones han reportado que la administración de BChE (15 000 o 5000 IU, iv.), derivada de suero de caballo, disminuyó la vida media de la cocaína de 26.2 minutos a 16.4 minutos en el plasma de roedores, gatos y primates.26,52,53 Además, in vitro, la BChE de roedores, primates y humanos, también incrementó el metabolismo de la cocaína.54,55,56
Con respecto a los niveles de cocaína en el cerebro, la administración de BChE (7.8 mg/kg, iv.) a ratas, redujo la concentración de cocaína en un 80% a los cuatro minutos, un 30% a los 45 minutos y un 25% a los 52 minutos posteriores a la administración de cocaína (30 mg/kg, ip.).26,57,58,59
En ratas se ha reportado que la administración intravenosa de 5000 IU, de BChE derivada de suero de caballo seguido de la administración intraperitoneal de 17 mg/kg de cocaína produjo una atenuación significativa de la actividad locomotora inducida por su administración, en sesiones de 120 minutos.56,60 También disminuyó de manera temporal el restablecimiento de su auto-administración.61,62,63,64
En roedores y primates la toxicidad aguda inducida por una sobredosis de cocaína estuvo marcada por un incremento en la presión sanguínea, una disminución en el ritmo cardíaco, hipertensión, bradicardia, supresión respiratoria y convulsiones tónico-clónicas, estas últimas están asociadas con crisis epilépticas y son los mecanismos primarios, responsables de la letalidad inducida por la sobredosis de cocaína.65,66,67
La administración de una dosis de BChE de 7.8 mg/kg, iv. incrementó los niveles plasmáticos de la enzima a más de 800 veces de lo normal, lo cual evitó la hipertensión y las arritmias cardiacas inducidas por una sobredosis de cocaína, en ratas (Lynch 1997). Dosis más altas (13.7 o 27.4 mg/kg) disminuyeron la incidencia de crisis convulsivas y muerte producidas por dosis de hasta 80 mg/kg, ip., en el ratón.68
Sin embargo, a pesar de su disposición estratégica en la circulación, la eficiencia catalítica de la BChE humana es muy baja y depende de muchos factores. En situaciones de exposición aguda a concentraciones toxicas de cocaína, la BChE es fácilmente superada.69,70
Con el objetivo de aumentar la capacidad catalítica de la BChE humana, diversos grupos de investigación realizaron mutaciones sucesivas a la hBChE.71,72,73 Al introducir una simple mutación, alanina 328-tirosina, en células transfectadas de ovario de hámster, algunos grupos de investigación lograron incrementar la velocidad de hidrólisis de la cocaína por un factor de 4;74 en cambio, si la mutación era una tirosina 332-alanina, la velocidad de reacción aumentaba 40 veces. En ratas, la administración de la BChE mutante bloqueó las crisis convulsivas y la letalidad inducida por una sobredosis de cocaína (100 mg/kg, ip).75
Hidrolasa de la cocaína
Posteriormente, mediante estudios de diseño molecular por computadora y de ingeniería genética,76,77,78,79,80 se generaron diversas enzimas capaces de hidrolizar a la cocaína a partir de la BChE humana, a las que se les denominó hidrolasas de la cocaína (hCocE). Después se diseñó un doble mutante llamado "hCocH", un mutante cuádruple denominado "AME-359",81,82 y recientemente se reportó una hBChE con cinco mutaciones simultáneas: "hCocH2".83
In vitro, la hidrolasa "hCocE" (A328W/Y332A-BChE) tuvo la capacidad de aumentar hasta por 1500 veces la eficiencia catalítica mostrada por la BChE.84,85,86 Sin embargo, a pesar del incremento en la eficiencia en la hidrólisis de la cocaína, la enzima no fue capaz de hidrolizar a la acetilcolina.
Cuando se administró la hCocE (3 mg/kg iv.) a ratas, ésta fue capaz de remover rápidamente la cocaína de los vasos sanguíneos, reduciendo la vida media de la cocaína de 52 a 18 minutos, disminuyó la concentración de cocaína en el plasma, reduciendo así su acumulación en el SNC, e incrementó los niveles plasmáticos de ácido benzoico, un producto no tóxico de la hidrólisis de la cocaína.87,88
In vivo, la hCocE disminuyó la actividad locomotora y atenuó la respuesta cardiovascular (presión sanguínea) inducida por la droga.89,90,91,92,93
En estudios de sobredosis de cocaína, en ratas, la hCocE ha demostrado una eficiencia catalítica y selectividad superior, comparada con la hBChE. La hCocE bloqueó eficientemente los efectos cardiovasculares y neurológicos inducidos por dosis letales (180 mg/kg ip.) en rata y primate.65 Así, 1 mg/kg de hCocE protegió al 100% de los animales que recibieron una dosis tóxica de cocaína (180 mg/kg), en cambio, la administración de 13 mg de BChE falló en proteger a ratas de la letalidad inducida por una dosis similar. Además, la hCocE dada a ratas después de la aparición de las crisis convulsivas no sólo acortó la duración de éstas sino que también salvó al sujeto de la muerte.94
Sin embargo, a pesar de estos resultados, una gran desventaja de la hCocE es que tiene una vida media muy corta (< 10 minutos) en el plasma, lo cual no le permite ejercer su protección a largo plazo.
Esterasa bacteriana de la cocaína
La bacteria rhodococcus sp., MB1, es capaz de producir una esterasa, la bCocE, capaz de hidrolizar a la cocaína tanto in vitro como in vivo.95 La actividad enzimática de esta esterasa se logró incrementar hasta x1000 veces más en comparación con la mostrada por la hBChE humana, 105-106 veces más rápida que un anticuerpo monoclonal.96
La administración de bCocE atenuó el restablecimiento de la conducta de búsqueda de la droga en animales entrenados previamente a auto-administrarse la cocaína y bloqueó el incremento en la actividad locomotora, inducido por ella.97
Además, la bCocE, en dosis de 28 mg/kg, restauró rápidamente (tres minutos) la presión sanguínea, disminuyó la hipertensión, la arritmia cardiaca y redujo la toxicidad inducida por una sobredosis (100 mg/kg, ip.), previniendo la muerte por crisis convulsivas, en ratas y en el ratón.98
Sin embargo, a pesar de su eficiencia las enzimas de mamíferos son más estables in vivo que las bacterianas. La esterasa bacteriana de cocaína inyectada a ratas tuvo una vida media de sólo 15 minutos, comparada con ocho horas para la CocH-albúmina humana.66
Los factores que intervienen en la duración de la vida media de la bCocE son múltiples, pero los más relevantes son la respuesta inmune generada por el huésped en contra de la enzima y la temperatura. Brim et al. reportaron que el proceso de eliminación de la bCocE bacteriana fue dependiente de la temperatura (termolábil). La bCocE tiene una vida media de sólo 11 minutos a 37°C.99
Por su lado, Ko et al. demostraron que a pesar de que la bCocE es una proteína de bacterias muy grande, por lo que es probable que pueda generar una respuesta inmune potente, la bCocE retiene su efectividad después de una o múltiples exposiciones, lo cual sugiere que la CocE es un antígeno débil y no es capaz de generar una respuesta inmune robusta.100 Esto sugiere que la temperatura endógena humana es el principal obstáculo para su uso, como agente terapéutico eficaz.
Esterasas mutantes
Dado que la esterasa bacteriana es inestable a temperaturas fisiológicas, diversos grupos de investigación realizaron una serie de mutaciones encaminadas a mejorar la estabilidad de la proteína a diferentes temperaturas. Los mutantes, denominados T172R, G173Q y L196K mostraron una estabilidad significativa in vitro, a 37°C. Cuando se evaluó, in vivo, el mutante T172R mostró una vida media de 78 minutos, mientras que los mutantes G173Q y L196K tuvieron una vida media de 75 y 403 minutos, respectivamente, a 37°C. Con respecto a su actividad hidrolítica, el mutante G173Q no mostró ninguna alteración en su actividad catalítica; en cambio, el mutante T172R y el doble mutante T172R-G173Q mostraron un incremento (de tres veces) en la capacidad para hidrolizar a la cocaína. En cambio, el mutante L196K mostró un incremento (de ocho veces) en su eficiencia catalítica.101,102
De manera paralela, Gao et al., con el afán de aumentar la actividad hidrolítica de la BChE, generaron un mutante denominado AME-359.103 Esta enzima demostró una capacidad impresionante para hidrolizar a la cocaína en el plasma.104,105 Su eficiencia catalítica se incrementó x100 veces más que la actividad catalítica mostrada por la BChE nativa humana y fue 450 veces más alta que la reportada para la CocE y la bCocE.66,98
Cuando se administró la AME-359 en una dosis de 0.5 mg/kg disminuyó de manera más eficiente, en comparación con el tratamiento con 3 mg/kg de CocE, la toxicidad cardiovascular inducida por una sobredosis de cocaína.106
Recientemente se ha descrito la producción de mutantes de la BChE humana en plantas transgénicas (Nicotinia benthamiana). El primer mutante que se desarrolló utilizando esta aproximación fue un doble mutante de la BChE, el A328W/Y332A. Este mutante mostró un aumento significativo en su actividad hidrolítica contra la cocaína.107
Las propiedades catalíticas de este mutante (llamado variante 1) fueron subsecuentemente mejoradas al introducir mutaciones adicionales en diferentes sitios de la BHcE humana para crear las llamadas: variante 2 (F227A/S287G/A328W/Y332A), variante 3 (A199S/S287G/A328W/Y332G), variante 4 (A199S/F227A/S287G/A328W/Y332G) y 5 (F227A/S287G/A328W/Y332G), siendo la variante 4 de la BChE humana la más eficiente en hidrolizar a la cocaína.107,108
Recientemente, Hou et al. evaluaron la capacidad catalítica de dos mutantes de la BChE humana, el E14-3 y el E12-7, para hidrolizar a la cocaína-etileno, un producto toxico de la cocaína. In vitro, la enzima E12-7 mejoró hasta por 817 veces la eficiencia catalítica de la BChE humana; in vivo, la E12-7 fue capaz de hidrolizar eficientemente en ratas a la cocaína-etileno, a la cocaína y a la norcocaina.109
Terapia génica
Otros grupos de investigación desarrollaron y validaron otros protocolos de transferencia genómica, donde se transfirió el gen de la CocH humana a un huésped, por medio de un vector adenoviral, con el fin de generar altos y sostenidos (por algunos meses) niveles plasmáticos de la hidrolasa de cocaína. Para ello, el DNAc de la CocE humana fue incorporada dentro de un vector adenoviral tipo 5 con un promotor de citomegalovirus (hdAD),110 el cual podía traducir el gen de la CocE humana por algunos días o semanas, en ratas, generando notorias y sostenidas cantidades de la hidrolasa en el hígado,111 incrementando la eficiencia catalítica de la proteína traducida, hdAD-CocH, comparada con la BChE de rata, hasta por un factor de 50 000 veces más.106
Otros estudios reportaron que la administración de dosis altas del vector, elevaron la actividad catalítica de la CocH hasta por 1 000 000 veces, sin reacciones secundarias aparentes.112,113,114 De hecho, Murthy et al. reportaron que la terapia de transferencia del vector hdAD-mCocH no generó efectos adversos secundarios sobre el funcionamiento del sistema colinérgico; los sujetos mostraron funciones cognitivas y motoras inalteradas.115
La administración del vector hdAD-CocH (3mg/kg) a ratas o ratones disminuyó la vida media de la cocaína y atenuó los efectos cardiovasculares inducidos por diferentes dosis.111 Además, disminuyó dramáticamente el restablecimiento de la búsqueda de la droga en el modelo de auto-administración (0.4 mg/kg) hasta por seis meses,111 pero no alteró la conducta de ingestión de agua o alimento, tampoco modificó la auto-administración de anfetaminas (0.05 mg/kg) ni disminuyó la actividad locomotora.116
Esto sugiere que el vector hdAD-mCocH no alteró la eficiencia motora o la motivación relacionada a la búsqueda de la droga, al contrario, su efecto es específico para el reforzamiento producido por la cocaína.64
Recientemente se reportó la transferencia de la mutante de la CocH humana, AME359, a ratas, mediante el vector hdAD-hCocH. La administración de este vector disminuyó la concentración de cocaína en el plasma, previno la actividad locomotora inducida por ella, el restablecimiento de la conducta de búsqueda de la droga hasta por seis meses y disminuyó la letalidad después de una sobredosis, en ratas (120 mg/kg).114
Otros estudios han reportado la transferencia de la CocH bacteriana mediante el uso de bacteriófagos. Los bacteriófagos son virus que tienen la capacidad de entrar al torrente sanguíneo y cruzar la barrera hemato-encefálica con facilidad; son capaces de tolerar una variedad de condiciones adversas como Ph extremos y tratamientos con nucleasas y enzimas proteolíticas,117 lo que hace al bacteriófago un buen medio a través del cual se puede transferir al Sistema Nervioso Central moléculas exógenas, que por su tamaño el sistema inmune o enzimático del huésped las pueden retirar rápidamente de la circulación, como la CocH.
Howell et al. reportaron que la transferencia de la CocH bacteriana, mediante un bacteriófago, a Macacos Rhesus, eliminó a la cocaína del cerebro tres veces más rápido que cuando se administró de manera sistémica. Esta ruta de administración atenuó los efectos reforzantes de la cocaína118 y evitó el incremento en la presión sanguínea y en la frecuencia cardiaca después de la administración de una sobredosis.105
Rogers et al. lograron la expresión de la CocE humana usando la proteína III (pIII) y la proteína IX (pIX) de la cubierta de un bacteriófago. Ambas preparaciones, CocE-pIII y -pIX, fueron reproducibles y generaron una alta actividad catalítica.15
Recientemente, Murthy et al. lograron transferir una BChE mutada a ratones. La transferencia mediante un vector viral elevó los niveles de la enzima 1000 veces, en comparación con los niveles normales, incrementando la capacidad catalítica de la enzima por meses, siendo capaz de eliminar a la cocaína en cuestión de segundos después de aparecer en el torrente sanguíneo. Adicionalmente, la BChE mutada fue capaz de atenuar la preferencia de lugar y disminuir la presión sanguínea y la letalidad inducida por una sobredosis (80 mg/kg).119
Terapia dual
Uno de los principales efectos de la administración de sobredosis de cocaína (100-120 mg/kg, ip.) es el daño permanente a los músculos y al hígado.112 Las terapias individuales como la administración de CocE humana (0.3 o 1 mg/kg) o de anticuerpos monoclonales (10 o 20 mg/kg), o la inmunización con un conjugado inmunogénico capaz de producir anticuerpos contra la cocaína, no han sido capaces de evitar estas alteraciones. Recientemente se ha reportado que el tratamiento con una combinación de estos agentes terapéuticos (enzima, 1 mg/kg-anticuerpo, 8 mg/kg, enzima, 1 mg/kg-100 μg KLH-Norcocaína) proporcionó una completa protección al hígado y a los músculos.112,113 Además bloqueó completamente la estimulación locomotora inducida por 10 mg/kg de cocaína,21 lo cual sugiere que la combinación de diferentes terapias podría incrementar la protección contra las acciones psicoestimulantes de la cocaína y sustentan su uso en humanos como terapias de apoyo para lograr mantener la abstinencia.120
Discusión y conclusión
Como se mencionó anteriormente, a la fecha actual se carece de una terapia farmacológica eficaz en contra de los efectos inducidos por la cocaína,1,2 sobre todo en situaciones de intoxicación por sobredosis. Una opción terapéutica es el uso y validación de nuevas terapias alternativas.3,4
En un gran porcentaje, los adictos a la cocaína fallecen cuando consumen sobredosis, lo que provoca alteraciones de tipo cardiovascular, cerebro-vascular, convulsiones y/o la muerte. De tal forma, basados en la necesidad urgente de contar con una estrategia terapéutica alternativa, la validación del uso de enzimas (BChE, COCH y CoCe bacteriana) capaces de disminuir significativamente los niveles de dosis, aun en rangos letales de cocaína, tanto en la sangre como en el cerebro,9,10 le proporcionaría a los servicios de emergencia una herramienta terapéutica única que les permitiría disminuir eficazmente los efectos letales de una sobredosis.121 Adicionalmente a su uso en situaciones de intoxicación por sobredosis, estudios en animales permiten sustentar el potencial terapéutico del uso de estas enzimas en humanos para inactivar rápidamente a la cocaína y desarrollar tratamientos para evitar las recaídas y mantener la abstinencia.122,123
Estudios clínicos de fase I han mostrado que la transferencia de la BChE humana pura o recombinante (TV-138) a sujetos sanos fue una terapia bien tolerada y segura.124 El tratamiento con diferentes dosis (50, 100 y 300 mg) de la BChE-TV-138 facilitó la abstinencia en pacientes dependientes a la cocaína, disminuyó su uso y atenuó los efectos reforzantes subjetivos generados por la droga.125,126
Aunque estos estudios sugieren que una terapia basada en el uso de una BChE humana es segura y podría ser útil en mantener la abstinencia en sujetos dependientes; como sucede con otras terapias como la vacunación activa o pasiva, esta terapia tiene ciertas limitaciones: 1) su eficiencia depende de la permanencia de la enzima en el torrente sanguíneo, 2) es una terapia que sólo podrá evitar que la droga cruce la barrera hemato-encefálica de manera temporal, no por periodos prolongados de tiempo; por lo tanto, 3) su uso está restringido a ciertas poblaciones de sujetos, sobre todo aquellos que se encuentren en una situación de intoxicación por una sobredosis.
En este sentido, se requiere de estudios futuros en los que se evalúe la eficacia y la seguridad biológica del uso de esta terapia, junto con terapias farmacológicas, inmuno-farmacológicas o psicológicas.
Por otro lado, esta revisión bibliográfica tiene una serie de limitaciones: a) la búsqueda bibliográfica no se amplió a otros motores de búsqueda como Biological abstracts, Google Schoolar, Live Search Academic, etc., b) no se realizó el truncamiento de los descriptores utilizados, c) no se llevó a cabo la revisión de las referencias bibliográficas de los artículos incluidos en la revisión y d) el poco número de trabajos encaminados a describir el uso de esta estrategia terapéutica en humanos en situaciones de intoxicación por sobredosis de cocaína, limita las conclusiones.
Estos estudios, sugieren que el aumento en la actividad catalítica de las enzimas BChE y las hCE, podría ser una estrategia útil para desarrollar una terapia alternativa para el tratamiento de pacientes en condiciones de toxicidad por sobredosis de cocaína.











 nueva página del texto (beta)
nueva página del texto (beta)



