El tomate (Solanum lycopersicum) se cultiva por excelencia en agricultura protegida en México, consolidando al país como el exportador número uno a Estados Unidos y Canadá (Atlas Agroalimentario, 2016). Entre los principales problemas que enfrenta el cultivo, se encuentra la aparición de enfermedades de origen fúngico, como la pudrición de la corona del tomate (PCT) cuyo agente causal es el hongo saprófito Fusarium oxysporum f. sp. radicis-lycopersici (Forl). La PCT es una de las enfermedades más destructivas, ya que ocasiona pérdidas en el rendimiento de sistemas de producción de invernadero y campo abierto (Szczechura et al., 2013). Entre los daños que causan a las plantas destacan el retraso en el crecimiento, la pudrición radical y lesiones necróticas extensas en el cuello y base del tallo y por consiguiente la senescencia (McGovern, 2015). La presencia de Forl ha sido reportada en los estados de Morelos (Domínguez, 2012) y Sinaloa, donde su presencia causó hasta un 50 % de reducción de la cosecha del tomate (Apodaca et al., 2004). Las estrategias convencionales de control están basadas en el uso de injertos, solarización, rotación de cultivos y principalmente en el uso de productos químicos sintéticos, de los cuales son conocidos los riesgos a la salud humana, el impacto negativo en el medio ambiente y el aumento considerable de los costos de producción (Cordero-Ramírez et al., 2013). Dadas las implicaciones negativas del uso inadecuado de fungicidas químicos, es primordial el desarrollo de nuevas formas de control para reducir la dependencia a dichos productos (Villa-Martínez et al., 2014). Dentro de las alternativas al control químico en un manejo integrado de plagas y enfermedades, se encuentra el uso de extractos vegetales con propiedades fungicidas, como Larrea tridentata. Comúnmente conocida como “gobernadora” es el arbusto dominante del desierto Sonorense y una fuente notable de compuestos naturales con aproximadamente el 50% de las hojas (en peso seco) como materia extraíble (Arteaga et al., 2005). Entre los compuestos fenólicos bioactivos más estudiados destaca el ácido nordihidroguaiarético (ANDG) (Martins et al., 2013) antioxidante que se encuentra en la resina de las células cercanas a las capas epidérmicas de las hojas y tallos. Dicho biocompuesto se encuentra presente en todas las especies del género, además, estudios interpoblacionales de L. tridentata realizados en el desierto Sonorense revelaron que las concentraciones de ANDG encontradas en la resina de sus hojas variaron en función de la latitud y de la época del año. Las flores, las hojas, los tallos verdes y algunos leñosos (<5 mm de diámetro) contienen ANDG, la concentración más alta se observó en las hojas con 38.3 mg g-1 y tallos verdes con 32.5 mg g-1 (Hyder, et al., 2002; Lira-Saldivar, 2003). Por lo que, conocer el contenido de ANDG en los extractos de L. tridentata brindará información sobre su efecto en el control de hongos fitopatógenos. Las propiedades antifúngicas de L. tridentata han sido corroboradas con trabajos desde hace aproximadamente 40 años mediante ensayos in vitro con al menos 17 hongos fitopatógenos de importancia en el área agrícola (López et al., 2005; Lira-Saldivar et al., 2006); sin embargo, son escasos los estudios in vitro contra Forl y realizar un ensayo bajo estas condiciones, marcaría la pauta para probar los extractos en condiciones in vivo, ya que a pesar de los resultados prometedores que se han publicado, la evidencia que se tiene de ensayos en invernadero o campo es insuficiente. El objetivo del presente estudio fue cuantificar el contenido de NDGA en extractos de L. tridentata para evaluar su efectividad in vitro y bajo condiciones de invernadero para establecer su potencial como biofungicida en el control de Forl.
MATERIALES Y MÉTODOS
La presente investigación se realizó en el año de 2014 en el laboratorio de Biotecnología Vegetal y el Centro Experimental de Transferencia y Tecnología 910 del Instituto Tecnológico de Sonora (ITSON) en Ciudad Obregón, Sonora, así como en el laboratorio de Ecología Química del Centro de Investigación en Alimentación y Desarrollo (CIAD) A.C. en Hermosillo, Sonora.
Obtención de la cepa de Forl
La cepa de Forl, se aisló previamente de la rizósfera de plantas de tomate cultivadas en un invernadero comercial del Valle del Yaqui, Sonora. El hongo se caracterizó por comparación de sus características coloniales y morfológicas mediante el uso de literatura especializada (Leslie and Summerell, 2016; Nelson et al., 1983) el cual se identificó molecularmente con primers específicos según Hirano y Arie (2006) (datos no publicados). Una copia del aislado se encuentra resguardada como Forlmx-19 en el banco de microorganismos del laboratorio de Ecología Química del CIAD A.C. Hermosillo, Sonora.
Obtención de extractos de L. tridentata y contenido de ácido nordihidroguayarético (ANDG)
Preparación de los extractos. Se elaboraron extractos con cuatro disolventes: diclorometano (DCM), metanol (MeOH), etanol (EtOH) y agua (H2O) a partir de muestras de hojas y tallos jóvenes de L. tridentata del desierto Sonorense (Peñuelas et al., 2015). Para los extractos de DCM y MeOH, se partió de 90 g de hojas secas y pulverizadas de L. tridentata, se extrajo por separado, con cada disolvente en sistema Soxhlet a 39 y 64.7 °C, respectivamente, durante 15 h de reflujo, seguida de una evaporación rotatoria. Para el extracto EtOH y acuoso, se maceró 1 kg de material fresco en 10 L de solución etanol:agua 7:3 (v/v) durante 8 días a temperatura ambiente (25 °C) y en la obscuridad. Transcurrido este tiempo, se filtró con gasa y posteriormente en papel (Whatman #5). El filtrado se sometió a evaporación rotatoria, la fase sólida se consideró como extracto EtOH y el sobrenadante se congeló a -45 °C y liofilizó para considerarse como extracto acuoso. Se cuantificó el contenido de ANDG en los cuatro extractos obtenidos, mediante cromatografía líquida de alta resolución fase reversa (RP-HPLC), en un sistema HPLC (Hewlett Packard series 1100, Alemania) acoplado a un detector de arreglo de diodos (DAD) en el Laboratorio de Ecología Química de CIAD A.C. Hermosillo, Sonora. Se siguió la metodología propuesta por Hyder et al. (2002) con el uso de una columna hypersil ODS C-18 y como fase móvil: A: H3PO4 1 % y B: 85 % acetonitrilo-14 % H2O-1 % H3PO4 en proporción 60/40, con elución isocrática, flujo de 1 mL min-1. La detección se realizó a una longitud de onda de 283 nm. Para la cuantificación se realizó una curva de calibración con el estándar de ANDG (pureza ≥ 90 %, Sigma Aldrich, Estados Unidos). El volumen de inyección del estándar de ANDG y las muestras fue de 25 μL., los datos se analizaron en el software Chemstation (Hewlett Packard, Alemania).
Determinación del porcentaje de inhibición de Forl por efecto de la aplicación de extractos de L. tridentata
Se utilizó el método de medio envenenado (Guerrero-Rodríguez et al., 2007) que consiste en vertir los extractos al medio de cultivo papa dextrosa agar (ADP) en cajas petri estériles de 5 cm; posterior a la solidificación del medio, se sembró por picadura central una muestra del margen de crecimiento vigoroso de la cepa aislada de 12 días de edad. El periodo de incubación fue de 7 días a 28 °C.
Variables evaluadas. Se registró diariamente el crecimiento micelial a partir del tercer día de incubación, midiendo en mm en dos diámetros cruzados, el monitoreo se detuvo al alcanzar el testigo el 100 % de la caja. La inhibición se determinó con la fórmula del porcentaje de inhibición=(dc-dt/dt)x100, donde dc es el diámetro promedio del crecimiento micelial del control y dt es el diámetro del crecimiento micelial con los diferentes extractos (Lira-Saldivar et al. 2003).
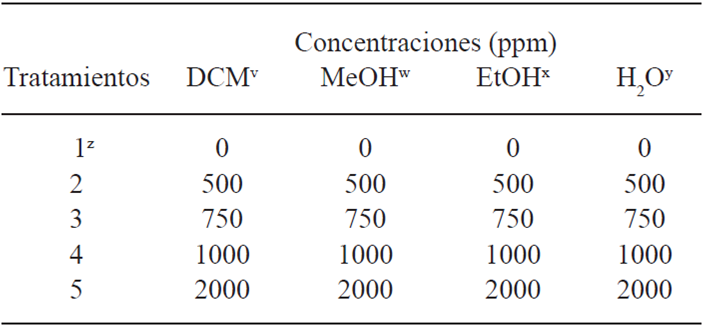
Diseño experimental. Se empleó un análisis factorial 4x5, donde el factor A fueron los extractos y B las concentraciones (Cuadro 1). El diseño experimental fue completamente al azar y se empleó un ANOVA y comparación de medias por Tukey (p<0.05) en el software Statgraphics 5.1.
Bioensayo in vivo
Se realizó en condiciones de invernadero en el Centro Experimental y Transferencia de Tecnología 910 (CETT-910) del Instituto Tecnológico de Sonora (ITSON) en el Valle del Yaqui, Sonora. Se emplearon 100 plántulas comerciales de tomate tipo cocktail var. F1 Prolyco2 con 35 días de crecimiento. El manejo agronómico del cultivo (fertilización, riegos y manejo cultural) se realizó de acuerdo a la Agenda Técnica Agrícola de Sonora (SAGARPA, 2015).
Inoculación de Forl. Se sembró por estría la cepa aislada de Forl, en botellas Roux con 250 ml de ADP adicionado con 3.5 ml de ácido tartárico al 10 %, previamente esterilizadas y gelificadas según la NOM-111-SSA1-1994 y Camacho et al. (2009). Se incubaron a 28 °C por 7 días hasta obtener desarrollo del micelio. Se colocaron sobre el agar, perlas de vidrio y tween 20 al 0.02 %, mediante movimientos suaves se recuperaron los conidios en un matraz estéril. Se realizó un conteo en la cámara de Neubauer y se ajustó a una concentración de 107 conidios mL-1 con agua destilada. En esta solución inoculante se sumergieron por 30 min las raíces de las plántulas, previamente heridas con bisturí en las raíces secundarias, posteriormente, se trasplantaron en macetas de 9 L que contenían suelo tipo franco arcilloso del Valle del Yaqui, Sonora.
Aplicación de tratamientos. Para lograr la adhesión de las diferentes concentraciones de los extractos evaluados, se utilizó el adherente agrícola Gardytec® (Técnica Mineral S.A. de C.V) a razón de 1 L ha-1. Se reactivaron los extractos en acetona a razón de 100 ml ml-1 (extracto DCM y EtOH) y acetona:agua (extracto MeOH y H2O), se agregó el adherente agrícola y se mezcló hasta obtener una suspensión. Cada 7 días después del transplante, descubriendo la parte superior de la raíz se aplicó el extracto correspondiente alrededor de esta.
Variables evaluadas
Se efectuaron las siguientes mediciones a los 49 días después de la inoculación (ddi): índice de clorofila con SPAD 502 de Minolta (entre las 11:00 y 14:00 h) en unidades clorofila (UC), altura de la planta con un flexómetro (desde la base del tallo hasta el ápice) y el número de hojas. Posterior a la aparición de la 5a hoja verdadera se evaluó cada planta en una escala del 1 al 5 (Cuadro 2) según la intensidad de la enfermedad (Marlatt et al. 1996). Una vez clasificadas, se calculó el índice de severidad con la fórmula de Towsend y Heuberguer (1943): Severidad= (∑nv/ 5N) x 100, donde n= plantas por cada categoría; v= valor de cada categoría; N= plantas en unidad experimental. Los datos se normalizaron con logaritmo natural antes del ANOVA. La incidencia se calculó por el porcentaje de plantas que presentaron algún síntoma de infección de Forl. Se consideran sobrevivientes las plantas que al término del experimento permanecieron vivas.
Diseño experimental
Se aplicó un arreglo completamente al azar con 10 tratamientos y 10 repeticiones (Cuadro 3). Las concentraciones de los tratamientos se definieron de acuerdo a los resultados de la CMI previamente realizado. Se realizó un ANOVA y prueba de rangos múltiples con el software Statgraphics plus versión 5.1.
RESULTADOS Y DISCUSIÓN
Determinación del porcentaje de inhibición de Forl por efecto de la aplicación de extractos de L. tridentata
En el Cuadro 4 se muestra la actividad de los extractos evaluados sobre el crecimiento micelial de Forl. El extracto de L. tridentata con DCM presentó inhibición de 98 % a 750 ppm, 94 % el MeOH a 2000 ppm y 97 % el EtOH a 500 ppm, lo que significa que los compuestos extraídos con EtOH tuvieron mayor poder fungicida sobre Forl in vitro. Estos resultados sirvieron de base para determinar las dosis para los tratamientos in vivo, considerando la concentración de cada extracto (p≤0.05) que inhibió completamente el crecimiento micelial del hongo. Se decidió aumentar la concentración a 3000 y 6000 ppm del extracto H2O, por presentar poco efecto sobre la inhibición del crecimiento de Forl.
Cuadro 4 Efecto de los extractos de L. tridentata sobre el crecimiento micelial de Forl

v diclorometano, w metanol, x etanol, y agua
Letras diferentes representan diferencias significativas entre tratamientos (Tukey p≤0.05)
La máxima inhibición del extracto hidroalcohólico de L. tridentata se ha reportado en 7000 y 5000 ppm para Aspergillus flavus y Penicillium sp., respectivamente (Moreno-Limón et al., 2011). El efecto antifúngico de L. tridentata se atribuye a los compuestos fenólicos, debido a que extractos polifenólicos inhibieron al máximo con 0.7 ppm en Pythium sp., Colletotrichum truncatum, C. coccodes, Alternaria alternata, F. verticillioides, F. solani, F. sambucinum y Rhizoctonia solani (Osorio et al., 2010).
Entre los compuestos fenólicos de L. tridentata destaca el ANDG, compuesto que se extrae de la resina en hojas y tallos (Lira et al., 2003). La cantidad que se extrajo de éste compuesto está directamente relacionado al grado de polaridad del disolvente (Moreno-Limón et al., 2011). De éste modo, en el presente ensayo se cuantificaron 68, 64, 6.07 y 2.8 mg g-1 de ANDG en los extractos de DCM, EtOH, MeOH y H2O, respectivamente, correlacionando las concentraciones cuantificadas en los extractos con el efecto sobre el crecimiento micelial que se presenta en el Cuadro 4.
Es sumamente complejo estandarizar una recomendación para el uso de extractos en el control de microorganismos fitopatógenos, ya que además del triángulo básico hospedero-patógeno-clima, influyen gran cantidad de factores como: disolvente y condiciones de extracción, latitud y altitud de la zona de muestreo de L. tridentata (Lira-Saldivar et al., 2003), variabilidad en razas y patogenicidad entre las formas especiales de F. oxysporum Fol y Forl; más aún, in vivo debe considerarse el efecto de la biodiversidad de organismos en el suelo y ambiente.
Bioensayo in vivo
Índice de clorofila. El contenido de clorofila en las hojas se muestra en el Cuadro 5. Todos los extractos presentaron niveles superiores (p<0.05) en comparación con el testigo absoluto y el fungicida comercial. Destacan los tratamientos con H2O 6000, DCM 3000 y MeOH 4000 ppm con 49, 48 y 45 unidades de clorofila, respectivamente, los cuales son valores superiores a los reportados para plantas de tomate sanas (35 y 37 UC) (Mercado-Luna et al., 2010). Los demás tratamientos presentaron valores dentro de este rango, a excepción del testigo y el control positivo donde se observó el daño causado por Forl.
Las UC proveen una medida indirecta y cuantitativa de la cantidad de N en la planta, además del efecto de variables climáticas (Rincón-Castillo y Ligarreto, 2010; Vázquez et al., 2012). Las plantas tratadas con extractos de L. tridentata mantuvieron un estado general de bienestar, aun cuando fueron infectadas con Forl.
Altura de planta. En el Cuadro 5, se observan los valores de la altura de las plantas en cada tratamiento, todos los extractos fueron estadísticamente superiores (p≤0.05) al testigo absoluto y fungicida comercial, desde la primera semana hasta el término del experimento. Los tratamientos H2O 4000, MeOH 4000 y DCM 3000 ppm, presentaron plantas con 49, 48, 42 % mayor altura, respecto a las plantas que recibieron el fungicida comercial. Se reportaron incrementos en altura de plantas de tomate (144 y 148 %) por Díaz-Díaz et al. (2013) con extractos de L. tridentata en concentraciones de 3000 y 2000 ppm con el uso de MeOH y acetona como disolventes. En el testigo absoluto (0 ppm) se observó retraso en el crecimiento general, a consecuencia de la sintomatología característica de Forl: invasión de raíz, pérdida prematura de hojas inferiores y pudrición de la radícula. Los extractos de Neem (Azardiachta indica) al igual que L. tridentata favorecen la altura (hasta en un 35 % comparado con el testigo) de plantas de tomate cuando han sido infectadas con F. oxysporum (Hadian et al., 2011).
Cuadro 5 Desarrollo vegetativo de plantas de tomate inoculadas con Forl y tratadas con extractos de L. tridentata a los 49 ddi
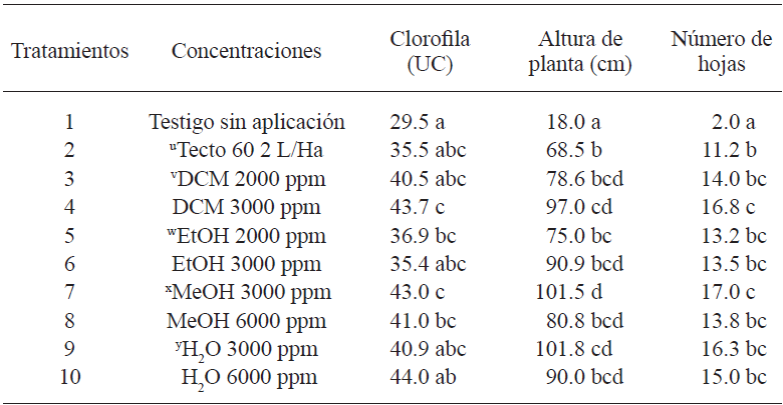
u fungicida comercial, v diclorometano, w etanol, x metanol, y agua. Letras diferentes representan diferencias significativas entre tratamientos (p≤0.05)
Número de hojas. Todos los tratamientos presentaron mayor número de hojas (p≤0.05) que el testigo absoluto, sobresaliendo los tratamientos MeOH 4000, DCM 3000, H2O 4000 ppm, con 52, 50 y 45 % más hojas que el fungicida comercial, respectivamente (Cuadro 5). Díaz-Díaz et al. (2013) registraron un incremento de 25 % en el peso seco al aplicar extractos de L. tridentata a 3000 y 2000 ppm en plantas de tomate inoculadas con P. capsici lo que da cuenta de una mayor desarrollo vegetativo al igual que los resultados aquí presentados; se reporta también el uso de infusión de L. tridentata como estimulante del desarrollo vegetal en tomate, en combinación con lanolina y manteca de cacao, al aumentar el peso seco (77 %) y fresco (100 %) (Recinos, 2010). No se observaron signos de toxicidad en las dosis utilizadas, al igual que os extractos acuosos de L. tridentata al 30 % y después de 5 días de aplicación (Rojob, 2008). La infestación de Forl, implica marchitez de las hojas inferiores hacia la parte superior (Fernández-Herrera et al., 2013) por lo que los bajos niveles de infestación permitió a las plantas generar y conservaron mayor número de hojas que el testigo absoluto y fungicida comercial.
Severidad. Se encontraron diferencias significativas (p≤0.05) entre los tratamientos MeOH a 4000 y DCM a 3000 ppm, los cuales presentaron índices de severidad de 55 y 57 % (respectivamente) en comparación con el 94 % del testigo absoluto y H2O 6000 ppm. Díaz-Díaz et al. (2013) reportaron hasta 83 % de disminución en la severidad al evaluar plantas de tomate infectadas con P. capsici y tratadas con extractos de L. tridentata y acetona a concentraciones de 2000 ppm. Los resultados mostrados (Figura 1-A) señalan un 45 % de disminución de la severidad en MeOH 4000ppm y se establece la relación entre las variables del desarrollo vegetativo y la PCT. Existe un comportamiento similar entre los tratamientos DCM 3000, MeOH 4000 y H2O 4000 ppm, con los cuales se obtuvieron menores índices de severidad y valores superiores de clorofila, altura y número de hojas respecto al fungicida comercial, considerándose el primer reporte sobre la severidad que presenta Forl sobre plantas de tomate que han sido tratadas con extractos de L. tridentata.
El extracto DCM 3000 ppm, presentó el mínimo índice de severidad y un desarrollo vegetativo superior respecto al fungicida comercial, así como una inhibición del 100% a 1000 ppm en el bioensayo in vitro de Forl y mayor contenido de ANDG. En relación con lo anterior, Martins et al. (2012) plantearon que la actividad antifúngica de L. tridentata se atribuye a tres compuestos: ANDG, kaempferol y quercetina, los cuales son sumamente compatibles con el disolvente diclorometano encontrándose en mayor disponibilidad por la polaridad que estos poseen. Hanaa et al. (2011) y Villa-Martínez (2015) emplearon extractos acuosos de neem y sauce (Salix babylonica) en plántulas de tomate, los cuales redujeron la incidencia de la enfermedad de la marchitez por F. oxysporum en plántulas de tomate hasta casi un 30%, mediante el aumento de las actividades de las enzimas defensivas antioxidantes secretadas por la planta de tomate, como la peroxidasa, la catalasa y la superóxido dismutasa.
Incidencia. Se obtuvieron diferencias estadísticamente significativas (p≤0.05); el 100 % de las plantas tratadas con los tratamientos testigo y H2O 6000 ppm registraron síntomas de infección de Forl (Figura 1-B); sin embargo, al aplicar los extractos DCM 3000 y MeOH 4000 ppm la incidencia alcanzó apenas 40 y 50 %, respectivamente. No encontramos reportes de ensayos in vivo para control de Forl con extractos de L. Tridentata; sin embargo, en plantas de zanahoria se reportó 5 % de incidencia de tizón de la hoja causado por A. dauci al aplicar un extracto hidrosoluble de L. tridentata, mezclado con quitosano (Hernández-Castillo et al. 2006).
Sobrevivencia. A los 49 ddi sobrevivió una de cada diez plantas tratadas con el testigo y H2O a 6000 ppm mientras que con los extractos DCM 3000 y MeOH 4000 ppm favorecieron la sobreviviencia del 60 % de las plantas. Con los tratamientos EtOH 2000 y MeOH 6000 ppm 50 % y con el fungicida comercial 40 % (Figura 1-C). Estos resultados demuestran una disminución de la agresividad de Forl por efecto de los extractos vegetales de L. tridentata, lo cual puede atribuirse a que las sustancias fenólicas presentes en los extractos reaccionan químicamente con los sistemas sensitivos de las enzimas volviéndolas catalíticamente inactivas ante este patógeno, favoreciendo por lo tanto la sobrevivencia de las plantas (Tappel y Marr, 1954).
CONCLUSIONES
Los resultados que se obtuvieron permiten concluir que los extractos de L. tridentata pueden ser utilizados como parte de un manejo integrado de la pudrición de la corona del tomate causada por F. oxysporum radicis-lycopersici en condiciones in vivo. Destaca la consistencia de los extractos de DCM a 3000 ppm y MeOH a 4000 ppm en la incidencia y severidad de Forl y la sobrevivencia en plantas de tomate. Es importante hacer mención que es el primer reporte in vivo donde se evalúe la capacidad antifúngica de los extractos de L. tridentata sobre Forl en plantas de tomate en el Valle del Yaqui, aunque es recomendable llevar la investigación a nivel de invernadero comercial enfocándose en disolventes más amigables con el medioambiente.











 texto en
texto en