Botrytis cinerea (Teleomorfo: Botryotinia fuckeliana), agente causal de la pudrición gris, ataca un amplio rango de plantas en todo el mundo (Piesik et al., 2015). Este hongo ha desarrollado resistencia a algunos fungicidas convencionales, particularmente benzimidazoles y dicarboximidas (Panebianco et al., 2015). Múltiples aplicaciones de los diferentes tratamientos de control químico en frutas y hortalizas pueden generar problemas a la salud del personal de campo agrícola y al consumidor, detención de exportaciones por residuos de plaguicidas, daños al ambiente y efectos perjudiciales a organismos benéficos para la agricultura (Yadav et al., 2015). Por consiguiente, es necesario reemplazar el uso de sustancias tóxicas por alternativas naturales amigables con el ambiente y la salud humana (Enríquez-Guevara et al., 2010).
Una alternativa en el manejo integrado de enfermedades es el uso de compuestos naturales producidos por algunas plantas, a los cuales se les atribuye propiedades antifúngicas (Compean y Ynalvez, 2014). Entre estos compuestos se encuentran los isoflavonoides, diterpenoides, alcaloides, aceites esenciales, estilbenos y polipéptidos (Soylu et al., 2010). Particularmente, se ha reportado que Vitis vinifera posee diversos compuestos con actividad antimicrobiana y antifúngica como miricetina, ácido elágico, kaempferol, quercitina, ácido gálico, entre otros (Schnee et al., 2013). Entre los compuestos fenólicos presentes en extractos de cáscara de una mezcla de tres cultivares chilenos de V. vinifera se reportó la mayor actividad antifúngica de ácido p-coumarico (98.5 μg/mL) y kaempferol (100.9 μg/mL); el extracto fenólico fue reportado con potencial contra B. cinerea (Mendoza et al., 2013).
De la misma manera, el resveratrol (RVS), compuesto aislado por primera vez de eléboro blanco (Veratrum album) y perteneciente al grupo de los estilbenos, ha sido reportado como compuesto activo contra diferentes hongos fitopatógenos en el cultivo de la vid, i. e. Erysiphe necator, Plasmopara viticola y B. cinerea (Alonso-Villaverde et al., 2011; Wu et al., 2013). Adrian y Jeandet (2012) indicaron que RVS, a 60 μg/mL, ocasionó disrupción de la membrana de los conidios de B. cinerea. Por otra parte, el crecimiento micelial de B. cinerea in vitro se inhibió entre 50 y 70 % por acción de RVS (Salgado et al., 2015). Además, al evaluar la efectividad, de manera separada, de RVS y tres compuestos relacionados con éste, (E)-3,4,5-trimethoxy-β-(2-furyl)-estireno, (E)-4-methoxy-β-(2-furyl)-estireno y (E)-3,5-dimethoxy-β-(2-furyl)-estireno a 100 μg/mL, se logró inhibir 70 % de la germinación de conidios de B. cinerea (Caruso et al., 2011).
En el territorio de México se reporta la presencia de más de 16 especies silvestres del género Vitis (Cruz, 2007). Actualmente, en la localidad de Santa Cruz, Municipio de Zumpahuacán, Estado de México, México, se tiene una colección de plantas de este género; a las cuales se les estudia sistemáticamente para incrementar su aprovechamiento. Particularmente, la hoja de las especies silvestres de vid del centro de México (Vitis spp.), al igual que la hojas de V. vinifera, presenta cantidades importantes de compuestos fenólicos (Franco et al., 2012). Tobar-Reyes et al. (2009) mencionan que de RVS se pueden encontrar de 0.04 a 39.5 μg/g de peso fresco; además, determinaron la existencia de ácido gálico, rutín y ácido caféico. Debido a que la presencia de compuestos fenólicos en hojas de vid silvestre indica su potencial como agente de control natural de enfermedades en vegetales, en el presente trabajo se evaluó in vitro la actividad antifúngica contra B. cinerea de extractos de hojas frescas de las accesiones de vid silvestre P-178, E-200 y TN-4.
Materiales y métodos
Cepa fúngica
Se colectaron frutos de pimiento morrón (Capsicum annuum) con síntomas de pudrición gris, en el Centro de Investigación y Transferencia de Tecnología (CITT) “Rancho El Islote”, del Instituto de Investigación y Capacitación Agropecuaria, Acuícola y Forestal del Estado de México (ICAMEX), localizado en Villa Guerrero, Estado de México a 18° 58’ 04’’ latitud norte y 99° 39’ 21’’ longitud oeste. Posteriormente, en el Laboratorio de Fitopatología del ICAMEX se tomaron fragmentos de aproximadamente 5 × 5 mm de tejido de los frutos enfermos, los cuales se desinfestaron con hipoclorito de sodio al 1 % (v/v) por 3 min, se enjuagaron con agua destilada estéril tres veces y se transfirieron a cajas de Petri con medio de cultivo avena-agar (MCAvA) acidificado, con ácido láctico al 25 % (v/v), a pH 4.5 y se incubaron a 26±2 °C durante 8 días. Posteriormente, usando la técnica de punta de hifa, una porción de tejido micelial se transfirió a otra caja de Petri con MCAvA, con la finalidad de obtener una cepa pura del hongo. Para comprobar la patogenicidad de los aislamientos se inocularon frutos sanos de fresa (Fragaria × ananassa) cv. Festival, previamente desinfestados como se describió anteriormente. A los frutos se les ocasionaron tres heridas, de aproximadamente 2 mm de diámetro por 2 mm de profundidad, con agujas de disección previamente esterilizadas. En dichas heridas se depositaron 20 μL de una suspensión de 1×106 conidios por mililitro. Una vez que se observaron los síntomas típicos de pudrición gris, se procedió a la identificación del hongo comparando las estructuras morfológicas observadas (tipo y color de micelio, septación, conidióforos, ramificación de conidióforos, largo y ancho de conidios) con las claves de Barnett y Hunter (1998); mientras que para la determinación de la especie se emplearon las descripciones especializadas de Ellis (1971) y Crous et al. (2007).
Adicionalmente, se enviaron muestras del hongo al Laboratorio de Diagnostico Fitosanitario del Colegio de Postgraduados, Montecillo, México, en donde se analizaron molecularmente. La secuencia ITS obtenida del hongo se comparó con secuencias de organismos referencia con mayor similitud, por medio de una búsqueda en la base de datos BLAST del GenBank® (National Institutes of Health (NIH), Bethesda, MD, USA). Una vez comprobada la especie, el hongo fue cultivado para realizar las pruebas del presente experimento.
Obtención de extractos vegetales
Se obtuvieron hojas sanas y uniformes en tamaño y color (Franco et al., 2012) de tres accesiones de vid silvestre: (1) E-200, originaria de Tejupilco, Estado de México, (2) TN-4, originaria de Tenancingo, Estado de México y (3) P-178, originaria de Hueytamalco, Puebla; todas ellas establecidas en el banco de germoplasma de vid silvestre de Zumpahuacán, México. El tejido vegetal se trasladó al Laboratorio de Horticultura de la Universidad Autónoma del Estado de México, Toluca, México; en donde se maceraron 200 g de hojas por accesión en 250 mL de metanol al 99 %; esta mezcla se dejó en reposo en oscuridad durante una semana. Posteriormente, el extracto se filtró y se concentró en un rotavapor, hasta tener 50 mL de la solución madre libre del solvente de extracción. Los extractos se envasaron en un frasco ámbar y se colocaron en refrigeración (4 °C) para su conservación.
Identificación de polifenóles
Empleando como estándar ácido gálico, se determinó el contenido de fenoles totales en los extractos de hoja de vid silvestre (EHVS) con el método Folin-Ciocalteu (Mora et al., 2009), a 760 nm en un espectrofotómetro; se expresó el resultado en equivalentes de ácido gálico (EAG). La identificación de algunos compuestos polifenólicos de los EHVS de cada accesión se realizó con un HPLC Shimadzu bomba isocrática (serie 42205), empleando una columna Spherisorb fase reversa C18 1 μm × 250 mm × 4.6 mm (Waters, USA). Como fase móvil se usó agua: acetonitrilo: ácido acético (70:29.9:0.1). El nivel de flujo fue 1 mL min-1 permitiendo cinco minutos de estabilización entre cada muestra. La señal fue monitoreada a 270 nm (Lorrain et al., 2013). Las muestras fueron inyectadas por triplicado en el sistema cromatográfico; cuantificando los compuestos detectados por el método de estándar interno.
Actividad antifúngica
En matraces con MCAvA a pH 4.5, sin solidificar, se vertieron las cantidades correspondientes (Cuadro 1) de los EHVS de cada una de las tres accesiones, resveratrol (RVS) (Sigma), extracto de cítricos (EC) (Tecnosafe), cyprodinil+ fludioxonil (funguicida Switch® 62.5 WG) (SW), además como testigo absoluto (TA) se tuvo MCAvA sin ningún ingrediente adicional.
Cuadro 1. Concentración de compuestos fenólicos en medio de cultivo avena agar adicionado con extractos de hoja de vid silvestre (Vitis spp.).

EAG: Equivalentes de ácido gálico. Los datos son la media de tres repeticiones; valores con letra diferente presentan diferencia estadística a P≤0.05.
De cada EHVS se tomaron 6, 8 y 12 mL para aforar a 100 mL de MCAvA a pH 4.5. Cada solución se vació en cajas de Petri debidamente etiquetadas y se dejó solidificar. Los tratamientos con RVS (60, 90 y 120 μg/mL), EC (3, 5 y 8 % (v/v)) y SW (500, 800 y 1000 μg/mL) se prepararon de la misma manera, empleando RVS disuelto en agua: metanol 1:1, SW en agua destilada, mientras que EC se empleó en su forma comercial líquida. Para cada uno de los 19 tratamientos se realizaron cuatro repeticiones, con tres cajas de Petri por repetición, siendo cada caja de Petri una unidad experimental. El experimento se realizó por duplicado, debido a la similitud de ambos resultados, el análisis estadístico presentado en este reporte corresponde a uno solo de los experimentos.
Posteriormente, se colocó, en el centro de cada una de las cajas de Petri con MCAvA y su respectivo tratamiento, un disco de 5 mm de diámetro de MCAvA con micelio activo de B. cinerea de 5 días de edad. Las cajas se incubaron a 26±2 °C y el diámetro de la colonia de B. cinerea se midió cada 48 h con ayuda de un vernier digital. Para cada repetición, las mediciones concluyeron cuando la superficie del MCAvA en todas las cajas del TA fue cubierta totalmente por el micelio. Los valores medios del crecimiento micelial fueron transformados a porcentaje de inhibición del crecimiento micelial (ICM) en relación con el TA utilizando la fórmula: ICM (%) = [(dTa − dt)/dTa (ICM)] × 100, donde dTa y dt representan el diámetro del crecimiento micelial del TA y de cada uno del resto de los tratamientos, respectivamente (Soylu et al., 2010). La disposición de las cajas de Petri en la incubadora permitió tener un diseño experimental completamente al azar.
Al final del experimento, de cada tratamiento se obtuvieron esporas del MCAvA con ayuda de una varilla de vidrio y agua destilada estéril. Por cada unidad experimental previamente descrita, se tomó una alícuota de la suspensión con conidios y fue transferida a una cámara de Neubauer para realizar el conteo de los conidios de acuerdo con la metodología de Moo-Koh et al. (2014). Los datos se convirtieron a porcentajes y los resultados se reportaron como inhibición de la esporulación (IE) siguiendo la fórmula: IE (%) = [(ETa − Et)/ETa] × 100, donde ETa y Et representan el número de conidios en el TA y en cada uno de los tratamientos restantes, respectivamente (Soylu et al., 2010).
Por otro lado, a partir de un cultivo esporulado (8 días de edad), se preparó una suspensión de 1 × 106 conidios por mililitro en agua destilada estéril. Se colocaron 200 μL de esta suspensión en cajas de Petri con MCAvA suplementadas con las diferentes dosis de cada uno de los 19 tratamientos. Al final de un periodo de 48 h de incubación a 22±2 °C, se evaluó la germinación de 100 conidios ubicados de manera aleatoria. Se consideró germinado cuando el largo del tubo germinativo fue igual o mayor al tamaño del diámetro del conidio. El porcentaje de inhibición de la germinación (IGC) se determinó mediante la fórmula empleada por Soylu et al. (2010): IGC (%) = [(GTa − Gt)/GTa] × 100, donde GTa y Gt representan el número de conidios germinados en el TA y en cada uno del resto de los tratamientos, respectivamente. El diseño experimental y el número de repeticiones por tratamiento fue el mismo del trabajo de crecimiento micelial.
Análisis estadístico
Los datos de porcentajes de ICM, IE e IGC se transformaron a y = arsin (sqrt (y/100)). Los datos fueron procesados mediante análisis de varianza de bloques completamente al azar con un factor y en caso de significancia se procedió a la comparación de medias con la prueba de Tukey (P ≤ 0.05) con el programa estadístico SAS® (SAS Institute, 2002).
Resultados
Identificación morfológico-molecular
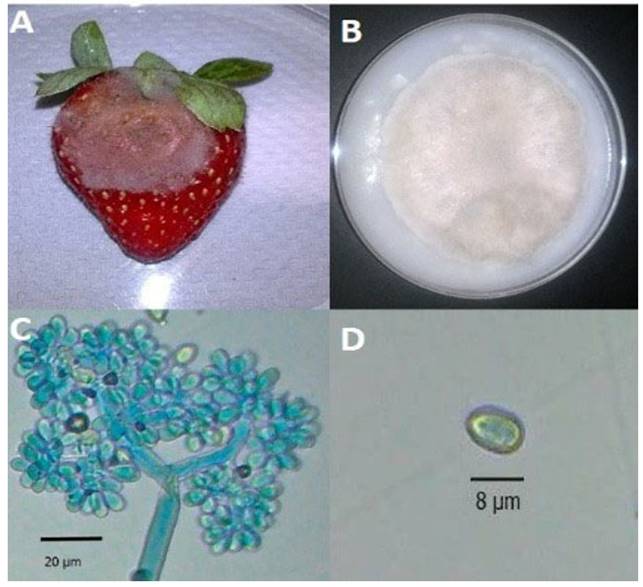
Cuatro días después de la inoculación con Botrytis sp., todos los frutos de fresa mostraron síntomas de pudrición gris, además de abundante esporulación del hongo (Figura 1A). Por otra parte, en el MCAvA las colonias exhibieron crecimiento micelial concéntrico, de consistencia afelpada y color blanco y siete días después, el micelio se tornó de color gris (Figura 1B). Bajo microscopia de luz, se observaron conidióforos largos, septados, pigmentados, con pared lisa, ramificados apicalmente y con racimos de conidios (Figura 1C). Los conidios fueron unicelulares, ovoides, lisos, hialinos y de 8-15 × 6-9 μm (Figura 1D). Todas las características observadas correspondieron a B. cinerea de acuerdo con la descripción de Ellis (1971). Por otro lado, la comparación en el BLAST de la secuencia mostró 100 % de similitud con la secuencia KR055051. Basado en características morfológicas y moleculares se confirmó que el agente causal de la pudrición gris del pimiento morrón en el CITT “Rancho el Islote” del ICAMEX es Botrytis cinerea.
Compuestos fenólicos
En los EHVS de las tres accesiones se determinó la presencia de ácido gálico y ácido ferúlico, mientras que en P-178 se determinó la presencia de resveratrol. Al aumentar la cantidad de EHVS por mililitro de MCAvA, se incrementó la concentración de los diversos fenoles indicados (Cuadro 1).
Actividad antifúngica
Todas las concentraciones de EHVS de las tres accesiones presentaron ICM. P-178 12 % presentó mayor ICM, superior al 70 % en relación a TA. SW a sus dos dosis más altas presentó 90 % de ICM, mientras que, de manera general, la ICM por RVS grado reactivo se ubicó entre SW y los EHVS. El EC inhibió no más de 25 % el crecimiento del micelio (Cuadro 2, Figura 2). La mayor IE se presentó con SW, seguida de RVS; mientras que el porcentaje de los EHVS fue entre 53 a 75 %, en relación al TA.
Cuadro 2. Actividad inhibitoria de diferentes tratamientos sobre crecimiento micelial (ICM), esporulación (IE) y germinación de la espora (IGC) de Botrytis cinerea in vitro.
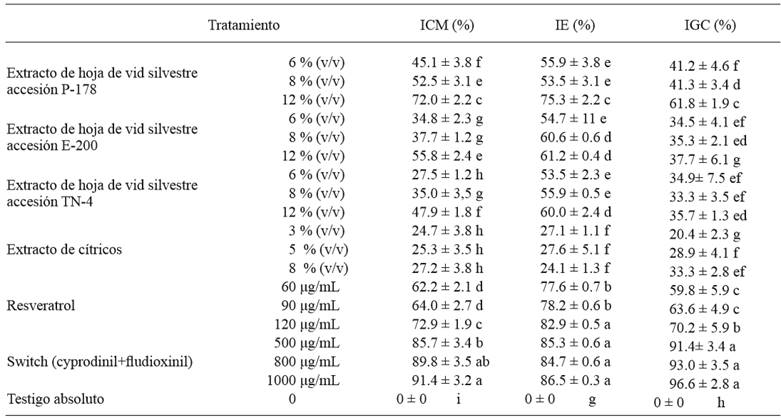
Los datos son la media ± EE de cuatro repeticiones, tres cajas de Petri por repetición. Medias seguidas con la misma letra en cada columna no presentan diferencia significativas con la prueba de Tukey a P≤0.05.
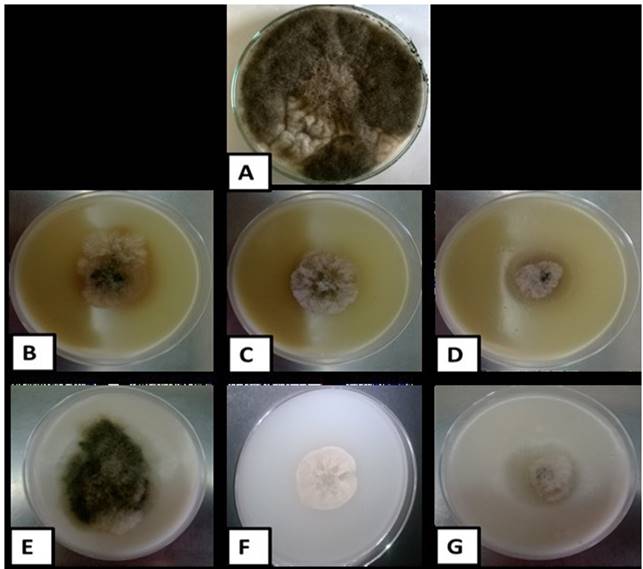
Figura 2. Crecimiento de Botrytis cinerea en medio avena agar a los 8 días de la inoculación a 26±2 °C A; testigo absoluto; B: extracto de hoja de la accesión de vid silvestre (Vitis spp.) E-200 12 % (v/v); C: extracto de hoja de la accesión de vid silvestre TN-4 12 % (v/v); D: extracto de hoja de la accesión de vid silvestre P-178 12 % (v/v); E: extracto de cítricos 8 % (v/v); F: resveratrol 120 μg/mL; G: cyprodinil + fludioxonil 1000 μg/mL.
Por otro lado, todos los tratamientos presentaron IGC. SW, en sus tres dosis, inhibió más del 90 %, seguido de RVS, cuyo promedio de las tres dosis fue de 64 %. La mayor IGC de un EHVS fue observada en P-178 12 % cuyo porcentaje fue superior a 60 %, en relación al TA.
Discusión
La mayor concentración de ácido gálico, ácido ferúlico y RVS en los EHVS de P-178 en relación a E-200 y TN-4 está relacionado con la variabilidad en la presencia y concentración de polifenoles en hojas de distintas accesiones de vid silvestre de México; identificando a los factores genético, ambiental y genético-ambiental como los responsables de esta variabilidad (Katalinić et al., 2009; Tobar-Reyes et al., 2011). En este trabajo, se sugiere que la diferencia entre accesiones en el contenido total de compuestos fenólicos y particular de los tres fenoles identificados, es debida principalmente a la genética, ya que los tejidos vegetales de las tres accesiones provinieron de un mismo banco de germoplasma.
El efecto inhibitorio del desarrollo de B. cinerea de los EHVS empleados puede deberse a la presencia de ácido gálico, ferúlico y resveratrol, polifenoles que han mostrado propiedades antifúngicas (Katalinić et al., 2009; Schnee et al., 2013; Mendoza et al., 2013). Vio-Michaelis et al. (2012), indicaron la presencia de ácido ferúlico en los extractos etanólicos de dos especies vegetales que poseen potencial para el control de B. cinerea; mientras que la aplicación de ácido gálico a un sistema in vitro implicó menor desarrollo de B. cinerea (Mendoza et al., 2013). Así, la mayor ICM, IE e IGC de EHVS P-178 12 % en comparación al resto de los EHVS puede estar relacionada tanto por la presencia, determinada y potencial, de más compuestos fenólicos, como por la mayor concentración de los mismos en relación a TN-4 y E-200. La elucidación completa de los polifenoles presentes en los EHVS y la actividad antifúngica particular de cada compuesto es una actividad científica a desarrollar.
Si bien la ICM, IE e IGC por P-178 12 % fue inferior a lo observado con SW y RVS, la actividad antifungica de este extracto es importante por ser superior a 70 % para ICM e IE y superior a 60 % de IGC. En este sentido, la ICM es similar a la reportada por El- Kateeb et al. (2013) con extractos metanólicos al 0.4 % de hojas de V. vinifera ‘Thompson seedless’ y ‘Flame seedless’ (entre 63 y 72 %). Particularmente, el modo de acción de los polifenoles contra B. cinerea no ha sido totalmente explicado, pero se ha sugerido que actúan sobre la membrana citoplasmática, produciendo cambios en su permeabilidad, ocasionando liberación del contenido celular, coagulación del material citoplasmático y desorganización de organelos y membrana celular, todo ello inhibe el desarrollo del micelio y evita su esporulación (Adrian y Jeandet, 2012; Minova et al., 2015). Por otro lado, se ha indicado que polifenoles del tipo ácido 3b-hydroxy-kaurenoico están involucrados con reducción en la germinación de B. cinerea (Cotoras et al., 2011).
La concentración de RVS en el MCAvA con EHVS P-178, a cualquier dosis, fue superior a la obtenida con la adición de cualquiera de los tratamientos con RVS grado reactivo, pero el efecto antifúngico de los EHVS fue menor. Estos resultados pueden deberse a lo reportado por Guerrero et al. (2010), indicando que entre los compuestos fenólicos presentes en un extracto vegetal existen interacciones sinérgicas y/o antagónicas, las cuales pueden modificar su efecto antifúngico. A pesar del menor control in vitro de B. cinerea con EHVS en relación a SW, RVS grado reactivo e incluso otros extractos vegetales reportados en la literatura i.e. extractos de Citrus paradisi (Xu et al., 2007); este trabajo indica el potencial de los EHVS de México como reductores de la dispersión e infección efectiva de B. cinerea, hongo causante de graves pérdidas económicas en diversos cultivos (Piesik et al., 2005). La amplia presencia de la vid silvestre en México y su bajo costo de adquisición son factores que también contribuyen al interés de identificar completamente a los polifenoles presentes en los EHVS y su efecto particular contra el hongo en estudio.
Conclusiones
Los extractos metanólicos de hojas tres accesiones de vid silvestre (Vitis spp.) mostraron actividad antifúngica in vitro contra B. cinerea; particularmente, el extracto de hojas de la accesión P-178 12 % inhibió 70 % el crecimiento micelial, 75 % la esporulación y 61 % la germinación de esporas, siempre en relación al testigo absoluto. Se detectó resveratrol, ácido gálico y ácido ferúlico en los extractos de dicha accesión y se sugiere la participación de estos fenoles contra Botrytis cinerea. Resveratrol grado reactivo produjo mejor control del hongo que los extractos de hoja de vid silvestre; generalmente, cualquier dosis de ambos, extracto de hoja de vid silvestre y resveratrol grado reactivo, no superaron la actividad antifúngica de cyprodinil + fludioxonil.











 texto en
texto en