INTRODUCCIÓN
Quaintance y Baker (1914) describieron el género Tetraleurodes incluyendo18 especies en el mundo, mencionando sólo a T. acaciae para México. Baker (1937) reportó para México a T. acaciae, T. fici, T. mori, T. pringlei, T. usorum. Posteriormente Sampson y Drews (1941) en un trabajo sobre moscas blancas de México describen a T. bidentatus, T. contigua, T. quadratus y T. truncatus; en tanto que Nakahara (1995) describió a T. caulicola, T. chivela, T. mexicana y T. quercicola, haciendo referencia de su presencia en México, este mismo autor describe otras especies más del género entre las que se encuentran T. bireflexa y T. melanops sin indicar su presencia en México. Martin (2005) estudiando los Aleyrodinae de Belice reportó la identificación de siete especies y mencionó a 17 no identificadas, de las cuales la mayoría podrían ser nuevas para la ciencia. En colectas realizadas a partir del 2002 en México se indicó la presencia de especies no conocidas como es el caso de una especie de género Tetraleurodes del grupo acaciae encontrada en Tepalcingo, Morelos México (Carapia et al., 2016). El presente estudio tiene como objetivo reportar la descripción de T. tepalcingo sp. nov., y proporcionar una clave para la identificación de especies del género Tetraleurodes encontradas en México.
MATERIALES Y MÉTODOS
Se realizaron montajes de especímenes (puparios) en portaobjetos para microscopio compuesto. La metodología seguida para la preparación de especímenes en portaobjetos fue la de Martin (2004) con algunas modificaciones.
Maceración de pupas en hidróxido de potasio al 40 % durante un lapso de 20 a 30 minutos en un vidrio de reloj; para las cubiertas pupales, de las que emergieron los adultos, se siguió directamente el paso tres.
Decolorado en peróxido de hidrógeno hasta una tonalidad amarillenta y lavado de pupasen agua destilada.
Eliminación de cera de pupas en cloral-fenol (hidrato de cloral 1 parte: fenol 1 parte) por 30 minutos a 60 °C.
Deshidratado en ácido acético glacial por 5 min.
Tratamiento en aceite de clavo por dos horas o más.
Montaje en bálsamo de Canadá.
Observaciones y mediciones de estructuras
Las preparaciones se examinaron en un microscopio Motica BA 310 a 40, 100, 400 y 1000 X en el laboratorio de Entomología de la EESuX-UAEM. Los especímenes se estudiaron con ayuda de descripciones y claves de Sampson y Drews (1941) y Nakarara (1995). Las microfotografías de Martin (2005) fueron de gran utilidad para la determinación de la especie.
RESULTADOS Y DISCUSIÓN
Tetraleurodes tepalcingo Carapia-Ruiz sp. nov. (Figs. 1-15)
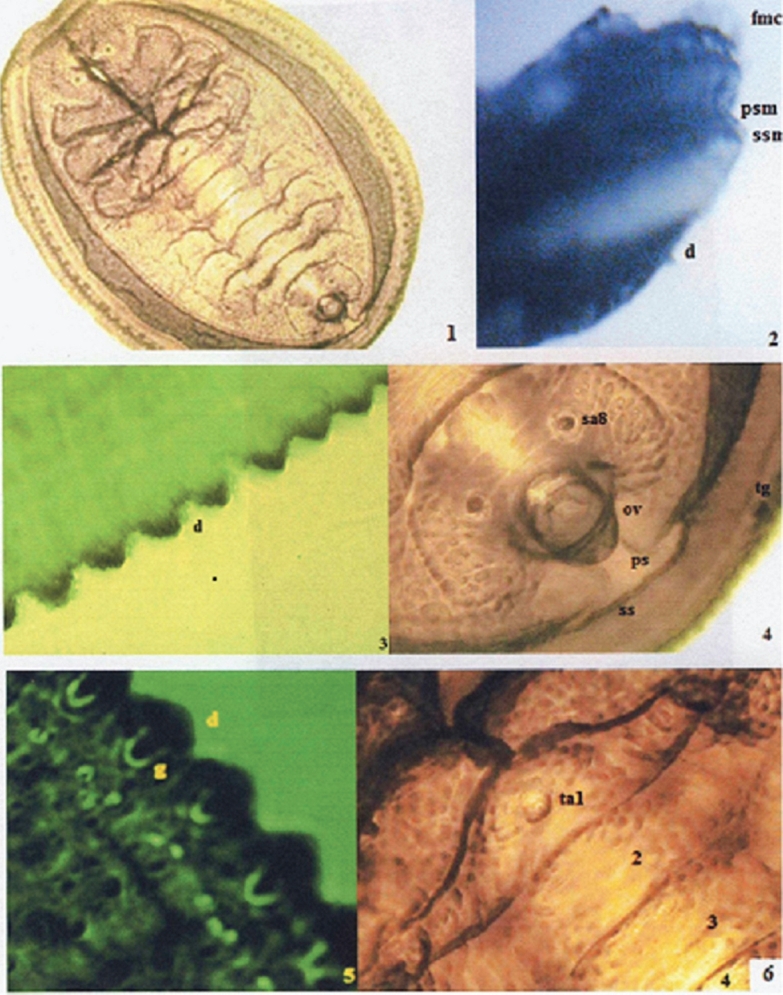
Figuras 1-6 Tetraleurodes tepalcingo Carapia-Ruiz sp. nov. 1) Cubierta pupal. 2) Cubierta pupal sin procesar mostrando el pliegue sobmarginal (psm), la franja marginal de cera (fmc), sutura submarginal (ssm). 3) Margen, dientes (d) mostrando sus tubérculos. 4) Parte posterior, tubérculo glandular (tg), orificio vasiforme (ov), sutura submarginal (ss), término del pliegue submarginal (ps), base setal del segmento abdominal VIII (sa8). 5) Dientes marginales (d) glándulas (g) en la base de los dientes marginales. 6) Área dorsal media, tubérculo medio en segmento abdominal I (ta1).

Figuras 7-11 Tetraleurodes tepalcingo Carapia-Ruiz sp. nov. 7) Área cefálica, seta marginal anterior (sma), sutura submarginal (ss), inicio del pliegue submarginal (ip), poro y porete (pp). 8) Área posterior, seta caudal (sc), seta marginal posterior (smp), término del pliegue submarginal (ip), tubérculo glandular (tg). 9) Depresiones abdominales medianas (da). 10) Región cefálica, seta cefálica (sc), sutura longitudinal de la muda (sl), poros y poretes (pp). 11) Meso-metatórax, sutura transversa de la muda (st), sutura longitudinal de la muda (sl), sutura metatorácica (ssmt), seta metatorácica (smt), seta mesotorácica (sms).
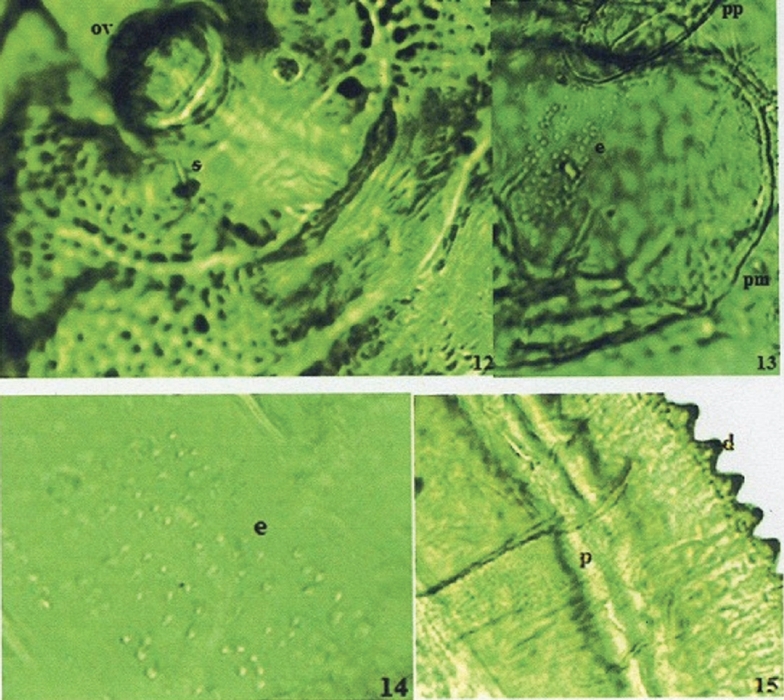
Figuras 12-15 Tetraleurodes tepalcingo Carapia-Ruiz sp. nov. 12) Segmento abdominal VIII, seta del segmento abdominal VIII (s). 13) Patas torácicas, espínulas (e), pata protorácica (pp), pata mesotorácica (pm). 14) Base de pata mesotorácica, espínula (e). 15) Pliegue toracico traqual (p), dientes (d).
Cubierta pupal: Alargada-oval, margen anterior redondeado, margen posterior redondeado; submargen medianamente elevado; disco dorsal con relieves en cefalotórax y abdomen, más alto que el submargen. Dimensiones del margen: longitud 1.35- 1.38 mm, ancho 0.98-99 mm, de color negro; cera ausente en el disco dorsal pero con una franja de cera blanca en el margen.
Margen: Dientes marginales cortos de 10-12 µm de largo ocupando 6 en 100 µm aparentemente lobulados, con tubérculos desde la base hasta su ápice lo que le da una forma irregular (Fig. 3), seta marginal anterior 20-25 µm; marginal posterior 50-60 µm de largo.
Submargen: Situado entre el disco dorsal y el ventral diferenciando dos pliegues uno ligero cerca de la línea de dientes marginales y la otra más profunda próxima a la línea del submargen ambos pliegues ausentes en la parte anterior y posterior (Figs. 2, 4, 7, 8). Con cerca de 36 pares de tubérculos glandulares de 9-12 µm de ancho en línea casi uniforme en alineamiento como en distanciamiento excepto en la región anterior y posterior donde no se presentan (Figs. 1, 4). Surcos transversos con tubérculos entre el margen y los tubérculos glandulares; surcos sin tubérculos entre los tubérculos glandulares y la línea submarginal; cerca de un surco por diente marginal cerca del margen y aproximadamente dos cerca de los tubérculos glandulares. Cada diente con un glandular pálido en forma de “u” cerca del área marginal (Fig. 5). Seta caudal de 45-50 µm de largo casi al nivel de la seta marginal posterior (Fig. 8).
Disco dorsal (Figs. 1, 2): Superficie con esculpido característico (Figs. 6-12), subdorso reflejado del submargen en su valor más alto. Sutura longitudinal de la muda de 520-530 µm extendiéndose hasta el margen anterior; sutura transversa de la muda de 510-520 µm extendida hasta la línea del submargen, terminando al nivel de la sutura metatorácica; margen de las suturas de la muda lisas; sutura mesotorácica llega al subdorso, no alcanza la línea submarginal. Marcas oculares ausentes. Seta cefálica 17-20 µm de largo, seta mesotorácica de 18-20 µm de largo (Fig. 11), seta metatorácica de 17-20 µm de largo (Fig. 11), octava seta abdominal 15-18 µm de largo, anterolaterada del orificio vasiforme, más cerca del orificio vasiforme que de la sutura del VIII segmento abdominal. Tres áreas elevadas en la región cefalotorácica; segmentos abdominales I-VIII con un par de depresiones en la parte media abdominal de 20 por 50 µm (Fig. 9). Poros del disco dorsal de 3 µm de diámetro distribuidos, siempre en conjunto de dos el poro ligeramente mayor y el porete ligeramente menor, como sigue: 10 cefálicos medianos (Figs. 7, 10), 10 cefálicos subdorsales, dos protorácicos medianos, cuatro protorácicos subdorsales, dos mesotorácico medianos, cuatro mesotorácicos subdorsales, dos metatorácico medianos, cuatro metatorácicos subdorsales, cuatro a seis en los segmentos abdominales I-III, normalmente 10 en los segmentos IV-VI, en los segmentos abdominales VII-VIII cuatro a seis. Segmento abdominal I normalmente con un tubérculo medio de 25 µm de diámetro (Fig. 6); líneas intersegmentales bien definidas entre la región media dorsal y la mitad del subdorso; área media de los segmentos abdominales 1-VI 60-70 µm, del segmento VII 50 µm, del segmento VIII (hasta el margen anterior del orificio vasiforme) 70 µm, distancia del orificio vasiforme al margen 110 µm. Orificio vasiforme semicordiforme a semioval de 60-65 µm de largo y 64-70 µm de ancho, Opérculo semicordiforme cubriendo completamente al orificio. Lingula cubierta por el opérculo, mitad apical agrandada de forma oval con espínulas. Surco caudal ausente, puede confundir el inicio del pliegue del submargen al nivel del orificio vasiforme (Fig. 4).
Vientre: Antena extendiéndose hasta el espiráculo anterior. Pliegues traqueales abdominales y torácicos bien definidos, 40-160 µm de ancho y 20-22 µm de largo, con granulaciones característica (Fig. 15). Patas mesotorácicas y metatorácicas con microseta. Espínulas pequeñas en la base de las patas (Fig. 13, 14). Sacos adhesivos bien desarrollados. Octava seta abdominal 30-35 µm de largo.
Holotipo: En tallos de Acacia farnesiana (L.) Willd. 14-marzo-1991. Tepalcingo, Morelos México, depositado en CNIN Instituto de Biología, UNAM, Ciudad de México. Paratipos, 2, mismos datos del holotipo y depositados en la misma colección, tres depositados en la colección del autor. Cinco en tallos de Acacia farnesiana (L.) Willd. 30-junio-1991. Tlayecac, Ayala, Morelos México, dos depositados en la colección del Museo Bohart de la Universidad de California, Davis, Ca, USA (UCD) y tres en la colección del autor.
Hospedero: Sobre tallos de Acacia farnesiana (L.) Willd. (Vachellia farnesiana (L.) Wight & Arn.) (Figs. 1, 2)
Distribución: Municipios de Tepalcingo y Ayala del Estado de Morelos, México. Es posible que se encuentre en otros lugares, al menos en el centro de México.
Etimología: el nombre especifico Tetraleurodes tepalcingo Carapia-Ruiz sp. nov., es referido a la región del municipio de Tepalcingo, Morelos, lugar donde se encontró la mayor cantidad de especímenes por planta.
Discusión: Tetraleurodes tepalcingo Carapia-Ruiz sp. nov., es la especie de mayor tamaño de Tetraleurodes grupo acaciae caracterizado por tener tubérculos glandulares en el submargen. En esta especie la sutura del octavo segmento abdominal no se dirige lateralmente como en Tetraleurodes caulicola Nakahara sino su dirección es hacia la parte caudal; también infestan tallos de leguminosa. El tamaño considerablemente mayor y la carencia de marcas oculares cefalicas permite separar y definir Tetraleurodes tepalcingo Carapia-Ruiz sp. nov., de T. tuberculosa Nakahara.
Clave para especies del género Tetraleurodes de México
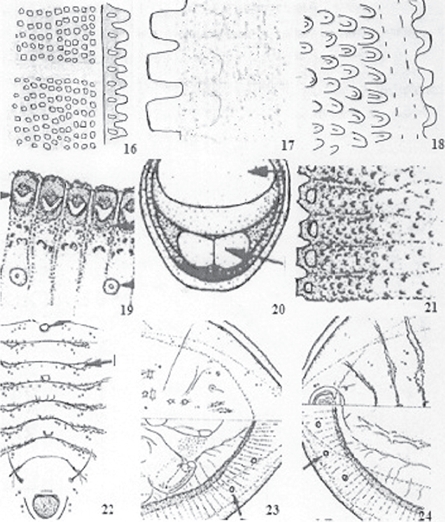
Figuras 16-24 (Sampson y Drews, 1941); 19-24 (Nakahara, 1995). 16) Area marginal de T. quadratus, 17) Área marginal de T. truncatus, 18) Área marginal de T. contigua. 19) Margen de T. caulicola, 20) Orificio vasiforme de T. bidentatus., 21) Margen de T. bidentatus. 22) Abdomen de T. acaciae, 23, 24) Área cefálica y caudal de T. birreflexa.
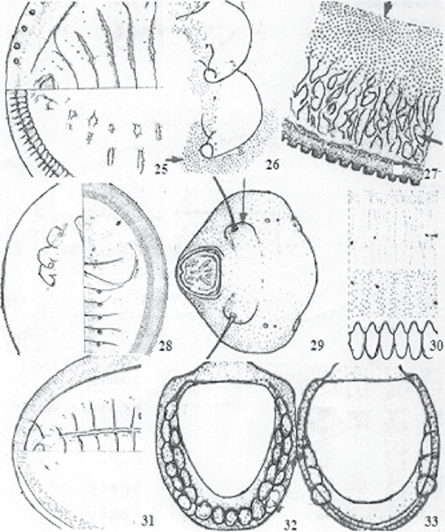
Figuras 25-33 (Nakahara, 1995). 25) Abdomen de T. mexicana. 26) Patas de T. chivela. 27) Submargen ventral de T. chivela. 28) Pupario de T. perseae. 29) Orificio vasiforme de T. perseae. 30) Margen y submargen de T. perseae. 31) Abdomen de T. pringle. 32) Orificio vasiforme de T. quercicola. 33) Orificio vasiforme de T. usorum.











 nova página do texto(beta)
nova página do texto(beta)



