Servicios Personalizados
Revista
Articulo
Indicadores
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Salud Pública de México
versión impresa ISSN 0036-3634
Salud pública Méx vol.47 no.4 Cuernavaca jul. 2005
ARTÍCULO ORIGINAL
Tendencia del perfil de sensibilidad antimicrobiana de los aislamientos de sangre en un hospital oncológico (1998-2003)
Trend of antimicrobial drug-susceptibility of blood isolates at an oncological center (1998-2003)
Patricia Cornejo-Juárez, MDI; Consuelo Velásquez-Acosta, QFBII; Adriana Díaz-González, QFBII; Patricia Volkow-Fernández, MD.I
IDepartamento de Infectología, Instituto Nacional de Cancerología (INCan). México, DF, México
IILaboratorio de Microbiología, INCan. México, DF, México
RESUMEN
OBJETIVO: Describir la frecuencia de la resistencia en microrganismos aislados en cultivos de sangre en pacientes de un hospital oncológico de tercer nivel.
MATERIAL Y MÉTODOS: De enero de 1998 a diciembre de 2003, en el Instituto Nacional de Cancerología se desarrolló un estudio retrospectivo en el cual se obtuvieron cepas de cultivos de sangre que fueron incluidas y procesadas por sistema Bactec y Microscan, para determinar identificación y sensibilidad antimicrobiana. Se determinó la tendencia anual de la resistencia de cada organismo especificado a los diferentes antibióticos. Se obtuvo la diferencia porcentual (incremento o decremento) comparando la frecuencia de resistencia al inicio y al final del estudio.
RESULTADOS: Se detectaron 2 071 cultivos positivos. Se recuperaron Gram negativos en 59.7% de las muestras, Gram positivos en 35.7% y levaduras en 4.6%. Escherichia coli fue el principal germen identificado (18.6%), seguido de S. epidermidis (12.7%) y Klebsiella spp (9%). Durante el periodo de estudio la sensibilidad se mantuvo estable y por arriba de 88% (excepto para Pseudomonas aeruginosa). La sensibilidad de ciprofloxacina para E. coli se encontró alrededor de 50%. Amikacina presentó mayor sensibilidad que gentamicina. Staphylococcus aureus presentó una sensibilidad a oxacilina de 96% y a vancomicina de 100%. S.epidermidis de 14% a oxacilina y de 98.6% a vancomicina. No se encontraron cepas de enterococo resistente a vancomicina. Todas las cepas de S. pneumoniae fueron sensibles a penicilina.
CONCLUSIONES: Se considera que los patrones de resistencia encontrados en este hospital son el resultado del control en el uso de antimicrobianos, del programa de vigilancia de infecciones nosocomiales y de la utilización de terapia combinada en todos los pacientes con bacteremia.
Palabras clave: resistencia y sensibilidad antimicrobiana; tendencia; hemocultivos
ABSTRACT
OBJECTIVE: To describe the patterns of antimicrobial resistance organisms isolated in blood cultures from patients detected in a tertiary level of care, teaching oncological hospital.
MATERIAL AND METHODS: All strains obtained from blood cultures from 1998 to 2003 were included and processed using the Bactec and Microscan system to determinate isolates and susceptibility to antimicrobials. The percent difference (increase or decrease) was obtained by comparing the frequency of resistance at baseline and at the end of the study.
RESULTS: A total of 2 071 positive blood cultures were obtained; 59.7% of isolates were Gram negative bacteria, 35.7% Gram-positive bacteria and 4.6% were yeasts. E.coli was the most frequent isolated (18.6%), followed by Staphylococcus. epidermidis (12.7%) and Klebsiella spp (9%). Throughout the study the susceptibility of Gram negative bacteria was stable and over 88% for most of the antimicrobials tested (except for Pseudomonas aeruginosa). Ciprofloxacin susceptibility for Escherichia coli stayed around 50%. Susceptibility to amikacin was higher than that to gentamicin. Staphylococcus aureus susceptibility for oxacillin was 96% and that for vancomycin 100%. S. epidermidis susceptibility for oxacillin was 14% and for vancomycin was 98.6%. No strains of vancomycin-resistant enterococci were found. All Streptococcus pneumoniae strains were penicillin susceptible.
CONCLUSIONS: The drug-resistance found in this hospital is the result of the control in the use of antimicrobials, the hospital nosocomial infection program and the use of drug combination in all patients with bacteremia.
Key words: antimicrobial resistance and susceptibility; trend; blood cultures
El incremento en los patrones de resistencia antimicrobiana, como resultado de la presión selectiva por el creciente uso de antibióticos, condiciona fallas en los esquemas antimicrobianos, aumento en la morbilidad y mortalidad, en la estancia hospitalaria y en los costos de atención.1-5
Por lo anterior, los pacientes oncológicos presentan factores que elevan el riesgo de adquirir infecciones pues son pacientes inmunosuprimidos, bajo tratamiento con quimioterapia o radioterapia, sometidos a cirugías extensas, con catéteres intravasculares de larga estancia y otros dispositivos que rompen las barreras naturales.6
Conocer los patrones de sensibilidad de las cepas responsables de las infecciones en tales pacientes permite adecuar tratamientos empíricos tempranos a través de políticas específicas de prescripción de antibióticos, además de detectar brotes en forma oportuna y tomar las medidas necesarias para su control y prevención.7,8
El objetivo de este estudio fue describir la tendencia de la resistencia antimicrobiana de los microrganismos aislados en cultivos de sangre, de enero de 1998 a diciembre de 2003, en el Instituto Nacional de Cancerología (INCan).
Material y métodos
El INCan es un hospital de tercer nivel, centro de referencia de toda la República Mexicana para pacientes adultos con cáncer, que cuenta con 150 camas y una media de 7 500 egresos hospitalarios/año y 3 100 cirugías mayores/año.
Se realizó un estudio retrospectivo basado en los informes del laboratorio de microbiología clínica del INCan, de enero de 1998 a diciembre de 2003.
Se tomaron hemocultivos de pacientes con fiebre o sospecha de un evento infeccioso. Se tomaron al menos dos muestras con un intervalo de 20 a 30 minutos entre cada una, con técnica estéril y barrera máxima. En pacientes con un catéter venoso central de larga estancia, se tomó un cultivo inicial por vía periférica y uno a través de cada lumen del catéter.
Se consideraron como casos los pacientes con datos clínicos de enfermedad sistémica y cultivos de sangre con crecimiento de bacterias. Se consideró como contaminante el crecimiento en un solo hemocultivo de organismos considerados como flora de piel (Staphylococcus epidermidis, Corynebacterium sp, Bacillus sp), y en el caso de los pacientes con catéter, cuando el crecimiento se presentó únicamente en el tomado a través del mismo y no en el de vía periférica.
Las muestras se inocularon en medio enriquecido Bactec Plus aerobic F (Becton-Dickinson, Sparks, MD, Estados Unidos de América [EUA]), y se procesaron de acuerdo con las instrucciones del fabricante. La identificación y sensibilidad antimicrobiana se realizaron por el micrométodo MicroScan (Dade-Behring, West Sacramento, CA, EUA). Se incluyeron los resultados de las cepas aisladas de Escherichia coli, Klebsiella spp, Enterobacter spp, Pseudomonas aeruginosa, Acinetobacter spp, Enterococcus faecalis, E. faecium, Staphylococcus aureus, S. epidermidis, Streptococcus pneumoniae, Listeria monocytogenes, Candida albicans y Candida spp. Solamente se incluyó un germen por episodio de bacteremia.
Los antibióticos que se analizaron para los gérmenes Gram negativos fueron: amikacina (AK), gentamicina (GM), cefazidima (CAZ), trimetroprim/sulfametoxazol (TMP/SMX), ciprofloxacina (CIP) e imipenem (IMP). Para P. aeruginosa se estudió, además, pieracilina (PIP) y se excluyó TMP/SMX. Para Enterococus spp ampicilina (amp), vancomicina (van) y CIP. Para S. pneumoniae penicilina (PEN), eritromicina (ERIT) y VAN. Y para Staphylococcus spp oxacilina (OXA), CIP, VAN Y GM.
Se consideraron cepas sensibles o resistentes de acuerdo con la concentración mínima inhibitoria determinada y conforme a los parámetros del National Committee for Clinical Laboratory Standards (NCCLS).9 Las bacterias que se encontraban en un rango intermedio se consideraron como resistentes.
Las cepas de S. aureus resistentes a oxacilina fueron confirmadas en medio de Müeller Hinton, suplementado con oxacilina. La susceptibilidad antimicrobiana para S. pneumoniae fue determinada por método de Kirby-Bauer.
Para el análisis estadístico se determinó la tendencia anual de la frecuencia de resistencia de cada uno de los organismos especificados a los diferentes antibióticos. Se obtuvo la diferencia porcentual (incremento o decremento), comparando la frecuencia de resistencia al inicio y al final del tiempo de estudio.
Resultados
Durante el periodo de estudio se detectaron 2 071 episodios de bacteremia, con una tasa promedio de 43.1/1 000 egresos. Se recuperaron gérmenes Gram negativos en 59.7% de las muestras, Gram positivos en 35.7% y levaduras en 4.6%. Los principales microrganismos aislados en orden de frecuencia fueron: E.coli, S. epidermidis, Klebsiella spp, S. aureus y Enterobacter spp. (cuadro I).

E. coli se aisló en 18.6% del total de cultivos. Gentamicina presentó un promedio de 16.3% menos en la sensibilidad al compararla con amikacina. El resto de los antibióticos estudiados no presentó cambios significativos (figura 1).

Klebsiella spp se aisló en 9% de los cultivos; la principal especie identificada fue K. pneumoniae. La sensibilidad de los antibióticos estudiados se encuentra por arriba del promedio al compararlo con el resto de las enterobacterias (figura 2).

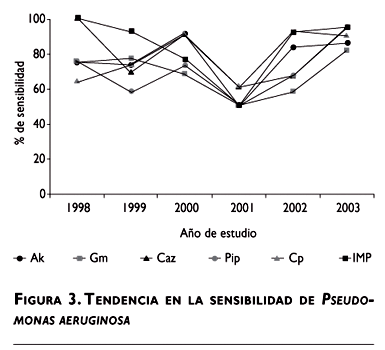
P. aeruginosa se aisló en 5.6% de las muestras. Durante el periodo de estudio se observó un incremento porcentual en la sensibilidad a ciprofloxacina de 42.8%. Gentamicina se notificó con un promedio de 8.2% menos en la sensibilidad al compararlo con amikacina (figura 3).
Enterobacter sp se identificó en 6.7% de los cultivos. Ceftazidima presentó un aumento de 20% de 1998 a 2003. Ciprofloxina y TMP/SMX se notificaron con un promedio de sensibilidad de 93.3 y 83.8% respectivamente; TMP/SMX tuvo un aumento en 35.7%.
Entre los años 2001 y 2002 se aislaron 83 cepas de Acinetobacter lwoffi (10.3% del total de aislamientos y 2.3% de los hemocultivos tomados), lo cual fue secundario a un brote de bacteremia asociado a catéter venoso central, donde la fuente de contaminación se atribuyó a la heparina que los pacientes se aplicaban a través del catéter en su domicilio.
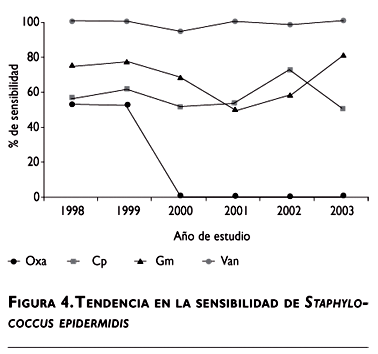
Respecto a los gérmenes Gram positivos, S. epidermidis se aisló en 12.7% de las muestras –segundo microrganismo más frecuentemente identificado. La sensibilidad a oxacilina se notificó en 8% –no hubo ninguna cepa sensible en los últimos cuatro años–, mientras que vancomicina se informó con una sensibilidad de 98.6% (figura 4).
S. aureus se aisló con una frecuencia de 8.9%, con una sensibilidad promedio a oxacilina de 96% y a vancomicina de 100%.
Enterococcus faecalis y E. faecium representaron 2.9% de los aislamientos; se notificó la sensibilidad a ampicilina de 73.8 y 16% respectivamente, mientras que para vancomicina fue de 100% en ambas especies.
Se identificaron 10 hemocultivos con S. pneumoniae; todas las cepas fueron sensibles a penicilina.
Se identificaron dos cepas de L. monocytogenes en 1997 y una en el año 2000.
Las levaduras representaron 4.6% de los aislamientos, siendo la principal C. albicans (1.2 %).
Discusión
En los resultados obtenidos destaca que, para el grupo de las enterobacterias, la sensibilidad de amikacina es mayor que la informada para gentamicina, por lo cual no se encuentra justificación para rotar estos antibióticos, como se ha propuesto en algunos estudios.10,11
Por otro lado, E. coli tuvo una sensibilidad a ciprofloxacina de 50%, por lo que no se recomienda el uso de quinolonas como parte del tratamiento empírico inicial en pacientes con bacteremia, al ser éste el principal germen aislado en hemocultivos. Este bajo porcentaje en la sensibilidad puede relacionarse con el uso indiscriminado de quinolonas en la comunidad.
Los carbapenémicos continúan mostrando una sensibilidad mayor de 95% para los gérmenes estudiados, excepto para P. aeruginosa (85.7%). Idealmente estos fármacos deben combinarse con un aminoglucósido y limitar su uso en pacientes con sepsis grave, con infecciones polimicrobianas y para cepas multirresistentes.12,13
S. aureus mantiene un alto porcentaje de sensibilidad a oxacilina (96%), mucho mayor que lo informado en otros estudios realizados en México, en los que varía entre 55 y 86%.14,15 Lo anterior es al contrario de lo que se encontró para S. epidermidis, donde la sensibilidad a oxacilina fue en promedio de 8%, y a diferencia de otros informes en nuestro país en los que varía entre 44 y 47%.14,15
No se encontraron cepas de enterococo resistentes a vancomicina. Otros informes de estudios en hospitales mexicanos destacan la frecuencia de cepas resistentes a vancomicina entre 0 y 14%.16,17 Por lo tanto, nuevos fármacos con espectro contra enterococo resistente a vancomicina, como quinupristina/dalfopristina, no son utilizados en este hospital.18
Destaca el reducido número de aislamientos de L. monocytogenes, tomando en cuenta que gran porcentaje de los pacientes que son atendidos presenta depleción de linfocitos CD4, factor de riesgo para infecciones por este patógeno, lo cual hace suponer que no es un problema de alta prevalencia en México.
Las levaduras se han mantenido en un promedio estable en el transcurso del periodo de estudio, y se aíslan con una frecuencia similar a lo notificado en hospitales oncológicos y no oncológicos en EUA.19
Se considera que, en el INCan, las políticas de control y restricción de antibióticos de amplio espectro han contribuido a mantener adecuados porcentajes de sensibilidad para los aminoglucósidos, cefalosporinas de tercera generación y carbapenémicos. Estas políticas se basan en la restricción de antibióticos y de su consiguiente disponibilidad en la farmacia del Instituto, la estandarización en los esquemas de profilaxis, la utilización de terapia combinada en el tratamiento empírico de pacientes con sepsis grave nosocomial o neutropenia grave y fiebre (ceftazidima más amikacina), y uso de vancomicina únicamente en pacientes con infecciones graves por gérmenes Gram positivos resistentes a beta-lactámicos y en aquellos pacientes con alergia a beta-lactámicos.20,21
Referencias
1. Levy S. Multidrug resistance – a sign of the times. N Engl J Med 1998; 338: 1376-1378. [ Links ]
2. Wise R, Hart T, Cars O, Streulens M, Helmuth R, Huovinen P et al. Antimicrobial resistance is a major threat to public health. BMJ 1998; 317: 609-610. [ Links ]
3. Ronald J. Resistance patterns among nosocomial pathogens*: Trends over the past few years. Chest 2001; 119 suppl 2: S397-S404. [ Links ]
4. Gold HS, Moellering RC. Antimicrobial drug resistance. N Engl J Med 1996: 335: 1445-1453. [ Links ]
5. Acar JF, Goldstein FW. Consequences of increasing resistance to antimicrobial agents. Clin Infect Dis 1998; 27 (S): 125-130. [ Links ]
6. Patterson JE. Hospital-acquired infections: Realities of risk and resistance. Chest 2001; 119 suppl 2: S426-S430. [ Links ]
7. Shlaes D, Gerding D, John JF Jr, Craig WA, Bornstein DL, Duncan RA et al. Society of Healthcare Epidemiology of America and Infectious Diseases Society of America Joint Committee on the Prevention of Antimicrobial Resistance: Guidelines for the prevention of antimicrobial resistance in hospitals. Clin Infect Dis 1997; 25: 584-599. [ Links ]
8. Goldmann DA, Huskins WC. Control of nosocomial antimicrobial-resistant bacteria: A strategy priority for hospitals worldwide. Clin Infect Dis 1997; 24 suppl 1: S139-S145. [ Links ]
9. National Committee for Clinical Laboratory Standards. Performance standards for antimicrobial susceptibility testing for bacteria that grow aerobically. (Eleventh Informational Supplement). Wayne (PA): NCCLS, 2001; Document M100-S11. [ Links ]
10. Raymond DP, Pelletier SJ, Cabtree TD, Gleason TG, Hamm LL, Pruett TL et al. Impact of a rotating empiric antibiotic schedule on infectious mortality in an intensive care unit. Crit Care Med 2001; 29: 1101-1108. [ Links ]
11. Landman D, Quale JM, Mayorga D, Adedeji A, Vangala K, Ravinshankar J et al. Citywide clonal outbreak of multiresistant Acinetobacter baumanii and Pseudomonas aeruginosa in Brooklyn, NY. Arch Intern Med 2002; 162: 1515-1520. [ Links ]
12. Goldmann DA, Weinstein RA, Wenzel RP, Tublan OC, Duma RJ, Gaynes RP et al. Strategies to prevent and control the emergence and spread of antimicrobial resistant microorganisms in hospitals. A challenge to hospital leadership. JAMA 1996; 275: 234-240. [ Links ]
13. Carmeli Y, Troillet N, Eliopoulos GM, Samore MH. Emergence of antibiotic-resistant Pseudomonas aeruginosa: Comparison of risks associated with different antipseudomonal agents. Antimicrob Agents Chemother 1999; 43: 1379-1382. [ Links ]
14. Kato-Maeda M, Bautista-Alavez A, Montes de Oca-Rolón AL, Ramos-Hinojosa A, Ponce de León A, Bobadilla del Valle M et al. Tendencia en el incremento de la resistencia antimicrobiana en organismos causantes de bacteremia en un hospital de tercer nivel: 1995-2000. Rev Invest Clin 2003; 55: 600-605. [ Links ]
15. Calderón-Jaimes E, Espinosa de los Monteros LE, Avila-Beltrán R. Epidemiology of drug resistance: The case of Staphylococcus aureus and coagulase-negative staphylococci infections. Salud Publica Mex 2002; 44: 108-112. [ Links ]
16. Calderón-Jaimes E, Arredondo-García JL, Aguilar-Ituarte F, García-Roca P. In vitro antimicrobial susceptibility in clinical isolates of Enterococcus species. Salud Publica Mex 2003; 45: 96-101. [ Links ]
17. Sifuentes-Osornio J, Ponce de León A, Muñoz-Trejo T, Villalobos-Zapata Y, Ontiveros-Rodríguez C, Gómez-Roldán C. Antimicrobial susceptibility patterns and high-level gentamicin resistance among enterococci isolated in a Mexican tertiary care center. Rev Invest Clin 1996; 48: 91-96. [ Links ]
18. Linden PK, Moellering RC, Wood CA, Rehm SJ, Flaherty J, Bompart F et al, for the Synercid emergency-use study group. Treatment of vancomycin-resistant Enterococcus faecium infections with quinupristin/ dalfopristin. Clin Infect Dis 2001; 33: 1816-1823. [ Links ]
19. Anaissie E. Opportunistic mycoses in the immunocompromised host: Experience at a cancer center and review. Clin Infect Dis 1992; 14 suppl 1: S43-S53. [ Links ]
20. Hughes WT, Armstrong D, Bodey GP, Bow EJ, Brown AE, Calandra T et al. 2002 Guidelines for the use of antimicrobial agents in neutropenic patients with cancer. Clin Infect Dis 2002; 34: 730-751. [ Links ]
21. Recommendations for preventing the spread of vancomycin resistance recommendations of the hospital infection control practices advisory committee (HICPAC): MMWR Morb Mortal Wkly Rep 1995; 44 (RR12): 1-13. [ Links ]
Fecha de recibido: 1 de julio de 2004
Fecha de aprobado: 11 de mayo de 2005
Solicitud de sobretiros: Dra. Patricia Cornejo Juárez. Departamento de Infectología. Instituto Nacional de Cancerología. Avenida San Fernando 22, colonia Sección XVI. Tlalpan 14000. México, DF, México. Correo electrónico: patcornejo@yahoo.com














