Introducción
El bloqueo auriculoventricular congénito (BAVC) ocurre en uno de cada 25,000 recién nacidos (RN).1 La causa más frecuente en corazones estructuralmente normales son las enfermedades autoinmunes, debido al paso transplacentario de autoanticuerpos anti-Ro/SSA y anti-La/SSB maternos que producen alteraciones en la célula cardiaca. Las cardiopatías estructurales representan la segunda causa de BAVC.2
Dentro de las alteraciones anatómicas existen los defectos de lateralidad donde se pierde el eje embrionario de desarrollo, dando lugar a la inversión de la simetría del corazón, lo cual se denomina situs inversus (SI).3 Esta es una entidad rara caracterizada por imagen en espejo de vísceras torácicas, estimándose que tiene una prevalencia de 1 a 2 en 10,000 RN vivos.4 El BAVC en fetos con síndrome de heterotaxia o isomerismo se comporta como un factor de riesgo de muerte en el periodo perinatal,5 en estos casos la tasa de mortalidad es superior a 50% en los primeros seis meses de vida y de hasta 67% a los dos años.6 El tratamiento de elección es la colocación de un marcapasos definitivo.7
Dado que hay pocos reportes en pacientes pediátricos, se presenta el caso de un RN prematuro con SI y BAVC sintomático a quien se le implantó un marcapasos unicameral endocárdico como tratamiento definitivo.
Presentación del caso
Femenino de dos días de vida extrauterina producto pretérmino de la primera gestación. La madre tenía 38 años y con diabetes mellitus tipo 1, en tratamiento con insulina.
A las 35 semanas de gestación un ultrasonido reportó bradicardia de 90 latidos por minuto (lpm), por lo que se decidió realizar cesárea, obteniéndose producto vivo hiporreactivo con cianosis generalizada y dificultad respiratoria. Su peso fue de 2,660 gramos, talla de 49 centímetros, Apgar de 6/7 puntos, Silverman de 3 y saturación de 88%; se realizaron maniobras básicas de reanimación con adecuada respuesta, sin embargo, persistió con bradicardia.
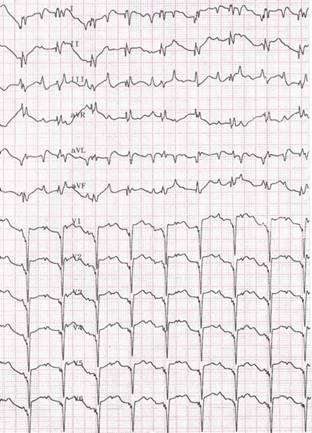
Se realizó un electrocardiograma de 12 derivaciones en el que se observó una frecuencia ventricular de 68 lpm, ondas P negativas en DI y aVL, es positiva en aVR; eje eléctrico a 150 grados y bloqueo auriculoventricular de 2 x 1 y un intervalo QTm de 0.36 segundos y QTc de 0.38 segundos (Figura 1). Por ecocardiograma, dado por análisis secuencial segmentario se concluyó: situs inversus del segmento auricular morfológicamente derecho con unión auriculoventricular concordante de asa ventricular D (derecha) y segmento arterial concordante; además se identificó una comunicación interventricular perimembranosa de 3 mm. La radiografía de tórax mostró dextrocardia (Figura 2); mientras que la tomografía toracoabdominal simple corroboró el SI.

Figura 1: Electrocardiograma de 12 derivaciones, ondas P negativas en DI y aVL, positiva en aVR, eje eléctrico desviado a la derecha; bloqueo auriculoventricular de 2 x 1 y un intervalo QTm de 0.36 segundos y QTc de 0.38 segundos.
A las 48 horas, continuaba con bradicardia y hemodinámicamente inestable, pese al tratamiento médico, por lo que se decidió la colocación de marcapasos definitivo al tercer día. Por supuesto, se descartaron causas transitorias de BAVC, como trastornos electrolíticos o procesos infecciosos.
La instalación del marcapasos se realizó bajo anestesia general e intubación endotraqueal. La punción de la vena subclavia derecha fue guiada por fluoroscopía; se utilizaron dilatadores 4, 5 y 6 F de forma progresiva y, finalmente, con introductor 7 F se introdujo un electrodo bipolar de fijación activa Fineline® Boston Scientific® de 52 cm, colocándolo a nivel medioseptal, se obtuvo una onda R de 18 mV, una impedancia de 876 Ohms y un umbral de captura de 1.4 V (0.4 ms). Se utilizó un generador de impulsos Microny®, Abbott® colocándose a nivel submuscular (Figura 3). No hubo complicaciones durante el procedimiento.

Figura 3: Proyecciones de fluoroscopía después del implante. A) Proyección AP. B) Proyección izquierda. C) Proyección derecha.
Días después se descartaron otras posibles causas de bloqueo mediante tamiz neonatal y perfil autoinmune.
A los dos meses de seguimiento la paciente se encontraba asintomática desde el punto de vista cardiovascular, manteniendo el marcapasos funcionando apropiadamente (Figura 4), observando aumento de peso (3,500 g).
Discusión
El BAVC puede asociarse a enfermedades maternas, tales como metabólicas, medicamentos o autoinmunes, siendo esta última la causa más frecuente. También se deben considerar las anomalías cardiacas anatómicas, las cuales llegan a alterar la conducción entre aurículas y ventrículos, lo cual se presenta entre 14 y 42% de los casos.8 Dentro de los defectos estructurales cardiacos congénitos las malformaciones complejas se llegan a presentar como un síndrome de heterotaxia (SH) en 0.8%,9 en estos casos se ha reportado taquicardia supraventricular, BAV y enfermedad del nodo.
En un estudio retrospectivo que evaluó la supervivencia de 35 lactantes, el SH se asoció a algún tipo de arritmia en 83% durante un seguimiento de 65 meses, falleciendo 34% de los pacientes. Otro estudio de 40 niños con SH la prevalencia de bloqueo AV fue de 19%.10 Escobar-Díaz y colegas11 reportaron que en 154 fetos con SH y arritmias 24% tenía BAVC, 79% sobrevivió al nacimiento y sólo 8% fue tratado con marcapasos definitivo, destacando que fallecieron los pacientes en quienes se difirió el implante de marcapasos.
La implantación de marcapasos en la población pediátrica representa menos de 1% del total de implantes.12 La técnica de implante transvenoso de electrodos de marcapasos en pacientes pediátricos (menores de 12 meses y con peso bajo) ha sido poco documentada. Vos y colaboradores13 reportaron una serie de siete casos en lactantes menores de 10 kg a quienes se trató con implante transvenoso unicameral cuya indicación más frecuente fue el BAV completo en 53.7%. La edad para implantar el marcapasos fue de dos días a 14 meses, y el promedio de peso al procedimiento fue de 3.5 kg. En el seguimiento a 14 años se observó que 85% requirió reintervención para recambio a marcapasos bicameral, aproximadamente a los nueve años de edad.
En estudios prospectivos se han reportado complicaciones tempranas por la implantación del marcapasos, tales como oclusión de la vena subclavia (lo cual parece ser inversamente proporcional al peso), pero no se ha descrito colapso completo del acceso venoso.14 A largo plazo se ha visto que la complicación más frecuente es el estiramiento del electrodo. Nakamoto y colegas15 describieron a un paciente en quien se decidió exceder la porción endovascular del Cable (8 mm), con el fin de evitar dicha eventualidad. No obstante, se debe considerar que es una reintervención.
Reportes de casos aislados argumentan que la técnica endocárdica tiene mayores ventajas que la epicárdica. Aunque los electrodos epicárdicos siguen siendo una opción importante en la estimulación de los pacientes pediátricos, es conocido que tienen diversos inconvenientes, como estar diseñados para pacientes adultos, la necesidad de una toracotomía, problemas de sensado y captura (en promedio consumen seis veces más energía que los endocárdicos) y menor longevidad. Por otro lado, la estimulación endocárdica tiende a tener un mejor umbral (aurícula y ventrículo) y un mejor acceso a los sitios de estimulación en comparación a la técnica abierta.14,15
En niños con peso menor a 10 kg, los sistemas de estimulación pueden ser endo- o epicárdicos. Silvetti y colaboradores16 reportaron 287 pacientes con marcapasos, de los cuales 40.7% tenía sistema endocárdico; el análisis mostró un riesgo mayor de falla en los pacientes con implantes epicárdicos comparado con quienes se implantó de forma endocárdica (50% versus 13%), lo cual fue estadísticamente significativo (p < 0.0001). Distintos autores en los últimos 20 años proponen como mejor opción la estimulación endocárdica; sin embargo, aún no hay estudios concluyentes, por lo que es necesario tener en cuenta las características particulares de cada paciente.17,18 Lo anterior, teniendo en cuenta que el diseño de electrodos endocárdicos con menor diámetro y longitud, así como generadores de menor peso y tamaño, facilitan la técnica de implante endocárdico.











 nova página do texto(beta)
nova página do texto(beta)