Introducción
El quilotórax se define como la presencia de linfa en la cavidad pleural, consecuencia de la disrupción u obstrucción del conducto torácico. La etiología puede ser traumática y no traumática y los traumáticos a su vez se pueden subdividir en iatrogénicos y no iatrogénicos.1 El quilotórax postraumático iatrogénico sigue siendo una complicación importante posterior a la cirugía torácica y particularmente difícil de manejar.2 La lesión del conducto torácico es una complicación poco frecuente de cualquier intervención quirúrgica intratorácica, observada hasta en 4%2,3 de las esofagectomías torácicas e inferior a 1%4 en cirugías de otra índole, pero potencialmente muy grave, con una mortalidad de hasta 50%5 si no se instaura un tratamiento adecuado.
Pueden ocurrir fugas linfáticas en cualquier lugar a lo largo de la vía de la linfa que comienza en las cuatro extremidades. La vía clínicamente más importante comienza desde los conductos linfáticos intestinales y continúa a través de la cisterna del quilo hacia el conducto torácico. El quilotórax es una condición grave que puede provocar rápidamente hipovolemia, anomalías electrolíticas, desnutrición e inmunocompromiso.6 Como resultado, la intervención temprana se ha convertido en la estrategia de tratamiento ideal.
En 1998 un nuevo método percutáneo para el tratamiento del quilotórax fue reportado por Cope7 así como algunas series más grandes3 desde esa fecha. La embolización percutánea del conducto torácico es una técnica mínimamente invasiva con bajas tasas de morbimortalidad y una tasa de curación o respuesta de hasta 73.8% en pacientes con etiologías no traumáticas y 71% en pacientes con etiología postraumática;2,3 por lo que es aceptada como alternativa terapéutica al tratamiento quirúrgico en los casos en los que no se controle la fístula de forma conservadora.3 Sin embargo, el procedimiento rara vez se realiza. Reportamos un caso exitoso de embolización del conducto torácico en quilotórax iatrogénico.
Presentación del caso
Paciente masculino de 66 años con antecedente de esofagectomía radical híbrida por neoplasia en el tercio inferior del esófago, tratado con radioterapia y quimioterapia neoadyuvante. En el posoperatorio mediato presentó derrame pleural bilateral. Se colocaron tubos de drenaje pleural a través de los cuales drenaba líquido de aspecto lechoso; el análisis bioquímico del líquido demostró cantidades elevadas de triglicéridos (176 mg/dL), hallazgo compatible con quilotórax. Después del tratamiento conservador, el débito del tubo de tórax no disminuyó, por lo que se decidió comentar el caso con el servicio de radiología intervencionista. Con el diagnóstico de quilotórax iatrogénico se realizó linfangiografía intranodal y embolización del conducto torácico con coils y cianoacrilato.
Técnica
Existen dos métodos de linfangiografía (LG): la linfangiografia bipedal (LP) y la linfangiografia intranodal (LN). La LG bipedal convencional implica la inyección de azul de metileno en el tejido celular subcutáneo entre el primer y tercer dedo del pie para identificar el curso de los vasos linfáticos en el dorso del pie. Posteriormente mediante una incisión en la piel se aísla un vaso linfático para administrar Lipiodol®. Este método requiere mucho tiempo y la incisión en el pie se puede infectar.8,9
La LG intranodal se desarrolló para evaluar la afectación tumoral de los ganglios linfáticos inguinales, pélvicos y lumbares. Se describen varias técnicas para la LN como la punción directa de los ganglios inguinales a ciegas o tras el aislamiento quirúrgico así como la punción guiada por ultrasonido, que actualmente es la más utilizada,8 ya que permite mayor precisión, técnicamente es más sencilla, y no requiere incisiones, por lo que se reduce el tiempo del procedimiento, la dosis de radiación y el volumen del medio de contraste.2
Además de identificar el punto de fuga, la linfografía puede tener un rol terapéutico atribuido a las propiedades embolizantes del Lipiodol®, que genera una reacción inflamatoria granulomatosa durante su extravasación y que debido a su viscosidad tiene la capacidad de acumularse en el punto de fuga, así como en los conductos linfáticos.9
Linfangiografía intranodal (LG)
Se identificaron los ganglios inguinales bilaterales más grandes y distales a la región inguinal bajo guía ultrasonográfica; posteriormente se inyectó Lipiodol® utilizando una aguja de calibre 22 G, la punta de la aguja se coloca en la zona de transición entre la corteza y el hilio del ganglio linfático. Se realizó una inyección manual lenta del Lipiodol® y se observó bajo guía fluoroscópica a fin de confirmar la posición correcta de la aguja. Se inyecta un volumen total de 10 a 20 mL de Lipiodol®. Posteriormente se obtienen imágenes bajo control fluoroscópico cada cinco a 10 minutos durante el transcurso de la inyección de Lipiodol® para observar la progresión a través de los conductos linfáticos pélvicos y abdominales (Figura 1).

Figura 1: A) Imagen de ultrasonido que muestra el acceso al ganglio linfático (punta de flecha) de la ingle con una aguja, la punta de la aguja se coloca en la zona de transición entre la corteza y el hilio (flecha). B) Imagen fluoroscópica obtenida durante la linfangiografía intraganglionar muestra un ganglio linfático como una tinción nodular sutil (flecha), que luego sigue los vasos linfáticos continuos con él (puntas de flecha). C) Se observa la progresión del mismo a través de los conductos linfáticos pélvicos bilaterales (flechas).
La linfangiografía intranodal se considera técnicamente satisfactoria si el ganglio linfático diana se selecciona con éxito y los canales linfáticos de interés, incluida la cisterna del quilo, se visualizan adecuadamente con Lipiodol®.
Embolización del conducto torácico
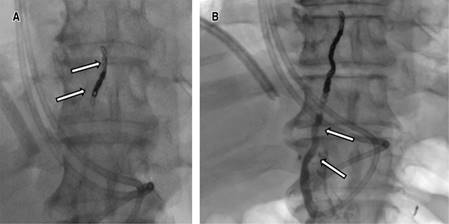
Una vez opacificada la cisterna del quilo, se visualizó una disrupción del conducto torácico y fuga del contraste hacia la cavidad pleural izquierda, bajo control fluroscópico se procede a cateterizar el conducto torácico utilizando una aguja Chiba de 22G por abordaje percutáneo abdominal en la zona epigástrica y con una angulación ligeramente craneal. Una vez que se accede, se introduce una guía de 0.014 pulgadas en el conducto torácico y se cambia la aguja por un microcatéter, el microcatéter se coloca lo más cerca posible al sitio de la lesión del conducto torácico, lo ideal es unir el punto de extravasación (Figura 2). Posteriormente se embolizó con microcoils de 2 y 3 mm de diámetro proximal a la fuga y se completó la embolización con cianoacrilato. En la ductografía de control se objetivó la resolución de la fuga (Figura 3).

Figura 2: A) Imagen de seguimiento que muestra un flujo ascendente continuo con llenado del conducto torácico (puntas de flecha) y de la cisterna del quilo (flecha). B) Se accede por vía percutánea con una aguja 22G (flecha) al conducto torácico (punta de flecha) y se evidencia extravasación del medio de contraste (círculo). C) Se utiliza una microguía (flecha) para asegurar el acceso, posteriormente se introduce microcatéter. Se corrobora extravasación del medio de contraste (círculo).
Discusión
El quilotórax se diagnostica por la presencia de líquido lechoso durante la toracocentesis con un contenido de triglicéridos superior a 110 mg/dL y un nivel de colesterol inferior al de la sangre,10,11 El tratamiento conservador se utiliza tradicionalmente para quilotórax de bajo volumen (< 1,000 mL/dL); sin embargo, la mortalidad permanece alta hasta 50%.5,12 Las principales causas de quilotórax traumático quirúrgico incluyen esofagectomía (28%), cirugía de cardiopatía congénita (28%), resección de cáncer de pulmón (6-27%).13 En términos generales, la esofagectomía está asociada con mayor frecuencia a quilotórax traumático: 3.9 versus 0.42% en cirugía torácica general.2,3
La embolización del conducto torácico fue descrita por primera vez por Constantine Cope en 1996 como alternativa al tratamiento de fugas quilosas que anteriormente no eran posibles sin la exploración quirúrgica.7 Se recomienda cuando persiste una fuga por más de dos semanas a pesar del tratamiento conservador, cuando las pérdidas superan los 1,000 mL diarios por más de cinco días o cuando aparecen complicaciones metabólicas y nutricionales severas.1,9 La descripción inicial requería una linfangiografía pedal para opacificar el sistema linfático; sin embargo, este método es técnicamente desafiante y requiere de mucho tiempo, por lo que ha sido reemplazado por la linfangiografía nodal percutánea guiada por ultrasonido.8,14
La embolización del conducto torácico tiene eficacia probada en el tratamiento de fugas quilosas causadas por una lesión en el conducto torácico. La mayor serie publicada en la literatura es la de Itkin et al., quienes evaluaron los resultados de la técnica en 109 pacientes con quilotórax traumático, reportando una tasa de éxito de 71%.2 Pamarthi et al. evaluaron los resultados en 105 pacientes con quilotórax traumáticos y no traumáticos tratados mediante técnicas percutáneas, alcanzando una tasa de éxito en los traumáticos de 62%, mayor que en pacientes con quilotórax no traumático.15 En la serie publicada por Cope et al.3 donde evaluaron el resultado del tratamiento percutáneo en 42 pacientes con quilotórax, obtuvieron una tasa de éxito de 76% en los casos traumáticos. Por lo que se le considera como una alternativa quirúrgica, dejando la cirugía como última opción de tratamiento en muchos casos.
En la serie más grande reportada no se informaron muertes y la tasa de complicaciones fue de 3% e incluyó un caso de embolización asintomática de la arteria pulmonar con cianoacrilato, dos casos de edema de pierna y dehiscencia de la sutura de pie.2 Esto es significativamente menor que la mortalidad de 82.1% y morbilidad de 38.3% en casos quirúrgicos.4
En nuestro caso se obtuvo un buen resultado técnico y clínico, sin recidiva del quilotórax ni necesidad de reintervenciones y sin morbilidad. Es en apoyo del nuevo enfoque de tratamiento del quilotórax defendido por algunos otros autores,2,3,15 que consideran la embolización del conducto torácico como una opción de primera línea en pacientes con derrames quilosos refractarios. A pesar de los resultados superiores, la embolización del conducto torácico es un procedimiento técnicamente desafiante que se realiza en muy pocos centros debido a la falta de familiaridad con la linfangiografía.
Conclusiones
La linfangiografía sigue siendo una herramienta importante en la localización de fugas quilosas. Ha evolucionado de un procedimiento laborioso y lento que dependía de la linfangiografía del pie, a uno en el que la linfangiografía intraganglionar inguinal acorta el tiempo y minimiza los riesgos. Con la selección de casos adecuada, la embolización del conducto torácico es una alternativa mínimamente invasiva a la cirugía en el tratamiento de casos traumáticos y no traumáticos de quilotórax.











 nova página do texto(beta)
nova página do texto(beta)