Antecedentes
La protección social de las enfermedades de origen ocupacional fue legalmente establecida en México con la promulgación de la Ley Federal del Trabajo (LFT) en 1936. En esta ley el artículo 326 reconoció 40 tipos de enfermedades profesionales, de las cuales 17 eran infecciosas y parasitarias, 3 de la vista y el oído y 20 correspondían a otras afecciones. En 1956, se adicionaron 9 fracciones más, es decir, nuevas enfermedades. En la reforma de la LFT de 1970,1 el artículo 513 retoma la tabla previa de enfermedades del trabajo, pero agrega otros 112 padecimientos para contabilizar un total de 161. El mayor número estaba compuesto por 47 enfermedades respiratorias ocupacionales (ERO) que incluyeron 30 padecimientos definidos como neumoconiosis o padecimientos broncopulmonares secundarios a inhalación de polvos o humos de origen mineral, vegetal o animal; además de otras 17 enfermedades de las vías respiratorias relacionadas con la inhalación de gases y vapores.
El artículo 515 de la LFT, el cual no sufrió modificación en la reforma 2012, encomienda a la Secretaría del Trabajo y Previsión Social (STPS) a realizar las investigaciones y estudios necesarios a fin de que el Presidente de la República pueda iniciar ante el poder legislativo la adecuación periódica de las tablas de enfermedades de trabajo y de evaluación de incapacidades permanentes de acuerdo al progreso de la medicina del trabajo. Bajo este contexto, la STPS integró grupos de trabajo que incluyeron especialistas clínicos, especialistas en salud en el trabajo, investigadores, académicos y peritos médicos dictaminadores, con la finalidad de actualizar la tabla de enfermedades de trabajo. Además, este proceso de actualización incluyó: 1) determinar de manera precisa a los trabajadores expuestos de acuerdo al tipo de actividad; 2) definir el tipo de daño a la salud de acuerdo al tipo de exposición; 3) actualizar los elementos clínicos, de laboratorio y de gabinete para la adecuada evaluación y diagnóstico de cada padecimiento; y 4) proveer la metodología más apropiada para la evaluación de la deficiencia o de incapacidad permanente de los trabajadores, así como la determinación de su capacidad residual en función a su calidad de vida y aptitud para el trabajo.
El grupo de trabajo de enfermedades del sistema respiratorio propuso para la actualización de la tabla de enfermedades de trabajo (artículo 513) un nuevo proceso de evaluación de la deficiencia respiratoria de acuerdo con las recomendaciones internacionales. Este proceso se basa en una evaluación objetiva sustentada en las pruebas de función respiratoria (PFR), las cuales deben realizarse bajo estándares vigentes internacionales. El objetivo de esta revisión es describir en detalle las PFR que se incluyen en este proceso, su fundamento fisiológico, técnico y clínico, su metodología y proceso de interpretación, así como las propuestas de evaluación de la deficiencia que son congruentes con los criterios internacionales. Finalmente, se hacen las propuestas que a juicio de los autores se deben implementar en el mediano plazo en las instituciones encargadas de la evaluación y seguimiento de estos enfermos.
Enfermedades respiratorias de origen ocupacional
Las ERO son un grupo de enfermedades crónicas cuya causalidad está ligada a la exposición crónica de contaminantes aéreos directamente relacionados al ambiente de trabajo.2 Estas enfermedades contribuyen significativamente a la carga de enfermedad de la población en general, en particular de la población económicamente activa. Se conoce que las enfermedades pulmonares crónicas como el asma, la enfermedad pulmonar obstructiva crónica (EPOC), las enfermedades pulmonares intersticiales y el cáncer pulmonar pueden tener como origen las exposiciones nocivas del ambiente laboral; incluso pueden ser clínicamente indistinguibles en su forma ocupacional y no ocupacional.2 Recién, se ha estimado que los agentes del ambiente de trabajo contribuyen etiológicamente entre 1 y 40% al cáncer de pulmón, entre 10 y 20% al asma y alrededor del 15% a la EPOC.2,3 Las ERO impactan la calidad de vida y el desempeño laboral de las personas que las padecen, lo cual también depende de la gravedad de las mismas y la frecuencia con que se puedan exacerbar. Además, las exacerbaciones también pueden depender de las exposiciones ambientales en el trabajo. Todo médico, no sólo debe estar familiarizado con la forma de explorar la exposición ambiental y laboral, sino también con los principales aspectos de diagnóstico y manejo de las ERO, además, debe ser un promotor de un ambiente de trabajo sano y seguro.
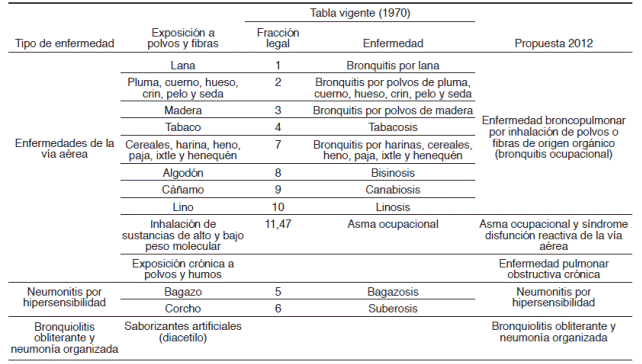
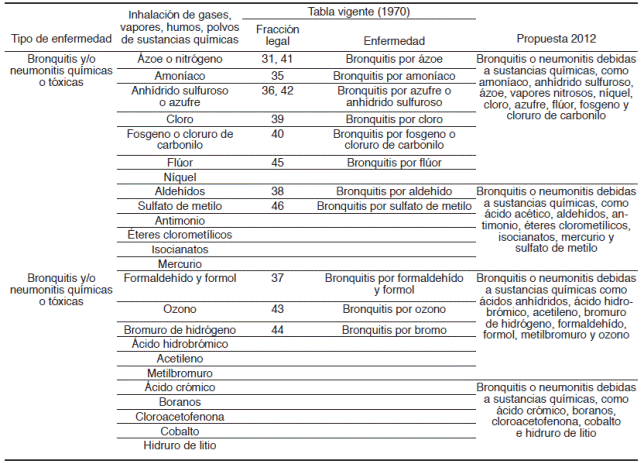
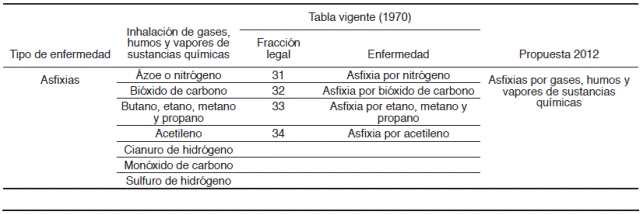
Las ERO pueden clasificarse de diferentes formas. Sin embargo, para fines clínicos es importante reconocerlas por su presentación clínica, su daño histopatológico primario y los agentes causales a los que se asocian. En las Tablas 1 a 4 se resumen las ERO reconocidas por la ley vigente, éstas son agrupadas en enfermedades de la vía aérea por partículas orgánicas, neumonitis por hipersensibilidad y bronquiolitis obliterante y neumonía organizada (Tabla 1), neumoconiosis (Tabla 2), bronquitis y/o neumonitis agudas o crónicas de origen químico o tóxico (Tabla 3) y asfixias por inhalación de gases, humos y vapores (Tabla 4). Se especifica el tipo de exposición y su agrupación actual de acuerdo con la nueva propuesta de la STPS. En esta propuesta, las ERO de tipo infeccioso o neoplásicas se encuentran en otros apartados, por lo que no se incluyen en esta descripción.
Deficiencia y discapacidad
Los términos deficiencia (impairment) y discapacidad (disability) han sido claramente definidos por la Organización Mundial de la Salud.4,5Deficiencia es la anormalidad o pérdida de una estructura corporal o de una función fisiológica. Esta alteración debe ser medida objetivamente, puede clasificarse como temporal o permanente y debe ser graduada en gravedad. Discapacidad se refiere a la restricción o pérdida de la capacidad para realizar una actividad en forma o dentro del contexto considerado como normal para una persona. Este término incorpora el efecto total de la deficiencia sobre la vida del paciente y se afecta por variables como la edad, género, nivel educativo y socioeconómico, medio ambiente, ocupación y requerimientos de energía que pueden limitar a realizar cierto tipo de trabajos. En consecuencia, dos personas con la misma deficiencia (por ejemplo, daño funcional) pueden tener diferente discapacidad, al grado que uno puede estar incapacitado para su empleo y el otro no. La evaluación de la deficiencia es responsabilidad de un especialista experto, quien debe cuantificarlo, mientras que la determinación de discapacidad es una decisión también experta, pero que requiere considerar variables médicas y no médicas (individuales, familiares, sociales y laborales).
Evaluación de la deficiencia: valoración funcional respiratoria
Dada la posibilidad de una ganancia secundaria por el dictamen de incapacidad, es esencial que la valoración se centre en pruebas objetivas, en este caso en PFR. El estudio de la función respiratoria es muy antiguo: los primeros intentos por medir los volúmenes pulmonares se originaron en el siglo XVII y para el año 1800 ya se habían hecho las primeras mediciones de volumen pulmonar por medio de dilución de gases. No obstante, fue hasta 1846 cuando el trabajo realizado por el médico inglés John Hutchinson incorporó a la espirometría como una prueba de uso clínico común para la evaluación de salud y de enfermedad respiratoria.6
Con frecuencia se piensa en la respiración solamente como el movimiento de entrada y salida del aire desde y hacia los pulmones. Este desplazamiento de aire se denomina mejor en fisiología como ventilación pulmonar. El proceso respiratorio, además de la ventilación, consiste en la transferencia de gases a nivel alvéolo-capilar, el transporte de oxígeno (O2) y bióxido de carbono (CO2) en la sangre, una segunda transferencia gaseosa a nivel celular y finalmente la respiración química en la mitocondria donde se incorpora el O2 al ciclo de Krebs para la producción de energía en forma de ATP.7-9 El compromiso respiratorio por enfermedad puede ser causante de deficiencia funcional temporal o permanente.
En la actualidad, la evaluación mínima de la función respiratoria requiere considerar la parte mecánica, la de intercambio de gases y la evaluación durante el ejercicio. La parte mecánica se refiere a la resistencia al paso del aire por la vía aérea, al volumen pulmonar y a la rigidez del pulmón y del aparato respiratorio. Varias enfermedades afectan de manera inicial la capacidad pulmonar para el intercambio gaseoso teniendo todavía pruebas normales de mecánica, como las que afectan la circulación pulmonar, las enfermedades intersticiales del pulmón y el enfisema pulmonar. De suerte que puede no haber una buena correlación entre la alteración mecánica y el daño al intercambio gaseoso. También cuando la lesión es inicial puede manifestarse solamente como una demanda adicional como la que se observa en el ejercicio.
Las PFR son una medición extraordinariamente objetiva y cuantitativa de la función pulmonar y, por lo tanto, también son útiles para la medición precisa de la mejoría o el agravamiento de las enfermedades. La espirometría es la prueba más simple, accesible y confiable para evaluar la función mecánica mientras que la medición de difusión pulmonar de monóxido de carbono (DLCO) es la prueba más recomendada en la actualidad para evaluar el intercambio de gases a nivel pulmonar; cuando estas pruebas no son concluyentes para determinar la deficiencia respiratoria, habitualmente en la minoría de los casos, se debe realizar una prueba cardiopulmonar de ejercicio (PCPE).
Es importante mencionar que las PFR no son completamente específicas ni diagnósticas de una enfermedad, así como un resultado normal tampoco descarta una enfermedad. Las pruebas en reposo (espirometría y DLCO) pueden tener una correlación variable con la capacidad funcional real del paciente que sólo puede ser medida de manera definitiva por PCPE. Asimismo, el daño funcional puede ser heterogéneo entre enfermedades respiratorias y entre pacientes con la misma enfermedad. La valoración de deficiencia debería ser idealmente individualizada por enfermedad, pero esto sólo se ha hecho en el caso del asma.
Espirometría
En la Figura 1 se muestra un espirograma normal cronometrado que ilustra los volúmenes y capacidades que pueden determinarse con las PFR. El volumen corriente (Vt) es el volumen de aire que se moviliza durante un ciclo respiratorio en reposo. Si el individuo adicionalmente inhala el máximo volumen de aire posible o volumen de reserva inspiratoria (VRI), alcanza su capacidad pulmonar total (CPT). Posterior a ello, puede realizar una espiración forzada hasta alcanzar el máximo volumen de aire espirado; a este volumen de aire se le denomina capacidad vital forzada (CVF). El volumen de aire que permanece en los pulmones después de exhalar la CVF se llama volumen residual (VR). La suma del VR y el volumen de reserva espiratoria (VRE) representan la capacidad funcional residual (CFR) que es el volumen de aire que normalmente existe dentro del tórax en estado de reposo y que es una reserva para el intercambio gaseoso.
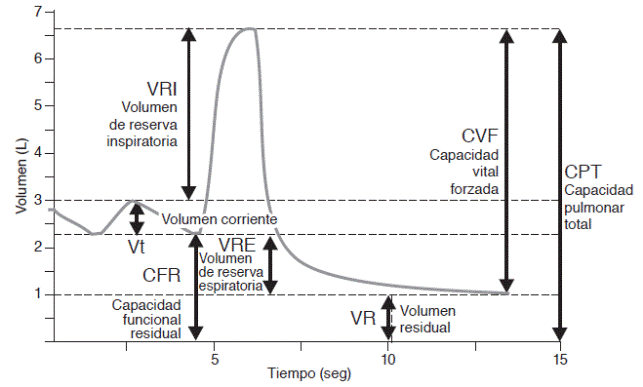
Figura 1 Espirograma normal cronometrado. Se muestra cada uno de los volúmenes y capacidades que lo componen. La espirometría permite medir los más importantes, particularmente la capacidad vital forzada (CVF) que es una estimación del tamaño pulmonar. Por el contrario, no permite medir el volumen residual (VR) y en consecuencia la capacidad funcional residual (CFR) y la capacidad pulmonar total (CPT).
La espirometría forzada es una prueba cronometrada y mide el volumen o el flujo de aire que un individuo inhala o exhala en función del tiempo (Figuras 1 a 3). El esfuerzo espiratorio es forzado o máximo y con frecuencia se le denomina maniobra de CVF. Además, la espirometría permite medir el volumen espiratorio forzado en el primer segundo (VEF1). El VEF1 es el volumen de aire exhalado durante el primer segundo de la maniobra de CVF y es el principal flujo espiratorio. Un adulto sano menor de 50 años puede exhalar 70% o más de su capacidad vital durante el primer segundo (VEF1/CVF > 70%). La espirometría forzada es la prueba considerada estándar de oro para definir obstrucción al flujo aéreo. Cuando existen procesos obstructivos de la vía aérea tiende a disminuir VEF1 y la relación VEF1/CVF. Los volúmenes medidos se expresan en litros (L) y los flujos en litros por segundo (L/s), ambos en condiciones estándar de presión barométrica y temperatura corporal (BTPS, por sus siglas en inglés).
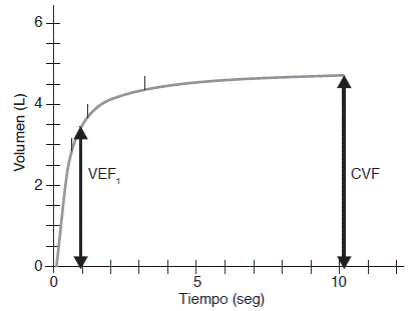
Figura 2 Curva volumen-tiempo de una espirometría normal. Se grafica el tiempo en segundo (x) contra el volumen en el eje vertical (y). La gráfica tiene un inicio muy vertical donde la mayor parte del volumen de aire se exhala en el primer segundo. Posteriormente, sigue una rodilla o transición donde el volumen tiende a caer y termina en una meseta cuando el individuo no exhala más aire, habitualmente después del segundo 6. En la gráfica se identifican con facilidad la capacidad vital forzada (CVF) al final de la espiración y el volumen espiratorio forzado durante el primer segundo de la espiración (VEF1).
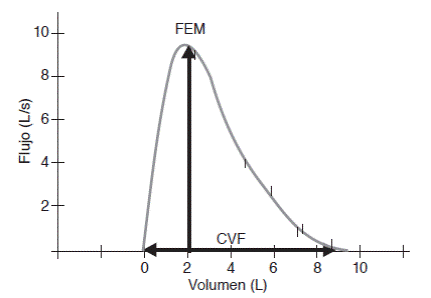
Figura 3 Curva flujo-volumen de una espirometría normal que corresponde a la misma prueba de la gráfica de la Figura 2. Se grafica el volumen (eje horizontal) contra el flujo de aire que equivale a la aceleración del volumen. La curva tiene una fase espiratoria con un inicio ascendente pronunciado que termina en un pico que determina el flujo espiratorio pico o máximo (FEP o PEF, por sus siglas en inglés), continúa con una caída lineal del flujo hasta alcanzar la capacidad vital forzada (CVF).
La espirometría debe incluir siempre las gráficas de volumen tiempo (Figura 2) y de flujo volumen (Figura 3); son de mucha utilidad para valorar la calidad de las maniobras y para fines de interpretación. La gráfica volumen tiempo presenta el tiempo en segundos en el eje horizontal (eje x) contra el volumen en litros en el eje vertical (eje y). Un esfuerzo aceptable muestra un incremento brusco en el volumen durante el primer segundo de la espiración. Después, la curva hace una transición en forma de rodilla entre los segundos 1 y 2 y al final una meseta donde no hay incremento significativo de volumen. La mayoría de los adultos alcanzan la CVF antes del segundo 6; sin embargo, algunos adultos mayores o personas con obstrucción al flujo aéreo requieren más de 10 segundos de espiración. En esta gráfica es fácil identificar la CVF, el VEF1 y el tiempo de exhalación forzada.
La gráfica flujo volumen (Figura 3) presenta el volumen en el eje horizontal y el flujo aéreo en el eje vertical. Esta curva es de gran utilidad para evaluar el esfuerzo inicial del paciente. Cuando la exhalación es con máximo esfuerzo, la fase espiratoria es de forma triangular, tiene un ascenso muy vertical y termina en pico llamado flujo espiratorio máximo o pico (FEM o FEP). La fase inspiratoria es semicircular y no siempre se presenta, ya que con frecuencia sólo se realiza la espiración. En esta curva se identifican la CVF en el eje horizontal y todos los flujos espiratorios, excepto el VEF1.
La espirometría es de gran utilidad para evaluar la salud y las enfermedades respiratorias, entre ellas las ERO, así como para monitorear evolución de una enfermedad y la respuesta a intervenciones, como los tratamientos. Además, sirve para valorar riesgos y exposiciones ambientales y correlaciona bien con la morbilidad y la esperanza de vida.10-12 Es la prueba de función pulmonar mejor estandarizada y la más reproducible, por lo que es la más confiable; no obstante, debe cumplir con las recomendaciones mínimas de estandarización (Tabla 5). Al presente, existen los procedimientos detallados tanto para su realización bajo estricto control de calidad como para su interpretación.12-18
Un panel de expertos internacionales auspiciado por la Asociación Americana del Tórax (ATS) y la Sociedad Europea Respiratoria (ERS) ha publicado las recomendaciones vigentes de estandarización de espirometría (estándares ATS/ERS 2005), las cuales se resumen en la Tabla 5.12 Es fundamental que los laboratorios de función pulmonar y las personas que realizan estas pruebas cumplan con estas recomendaciones. Sólo los espirómetros fabricados en los últimos años reúnen o superan las recomendaciones técnicas. El equipo debe tener un control de calidad periódico y es indispensable que cumpla una calibración o una verificación de calibración el día en que se realiza la prueba. Los técnicos deben ser entrenados y certificados para la prueba y para ello existen cursos especializados con reconocimiento internacional, como el certificado por el Instituto de Salud y Seguridad Ocupacional de los Estados Unidos (NIOSH) y por la Asociación Latinoamericana del Tórax (ALAT). En México, estos cursos son programados con frecuencia en el Instituto Nacional de Enfermedades Respiratorias Ismael Cosío Villegas y en la sede de la Sociedad Mexicana de Neumología y Cirugía de Tórax (SMNyCT). En cuanto a la prueba se deben cumplir todos los pasos de instrucción y demostración del esfuerzo al paciente y se deben completar tres maniobras aceptables y repetibles. Para la interpretación se deben usar valores de referencia generados bajo estándares actuales; en general, se prefieren valores de población local o externos validados en la población. Para población mexicana adulta existen tres valores predichos o de referencia que han sido propiamente publicados y que corresponden a las ecuaciones referidas para población México-americana y mexicana.19-21
La interpretación de la prueba debe realizarse por un profesional entrenado y siguiendo los lineamientos internacionales para la determinación del patrón funcional y la graduación de gravedad en caso de anormalidad.13,16-18 La Figura 4 ilustra el diagrama de flujo recomendado para la interpretación estandarizada de acuerdo con las recomendaciones de ATS/ERS 2005.13 La interpretación inicia con el análisis de la calidad técnica de la prueba. El patrón ventilatorio se determina con la evaluación inicial de la relación VEF1/CVF; si esta relación es menor al límite inferior normal (LIN), la prueba se interpreta como diagnóstica de obstrucción al flujo de aire. El LIN depende de la edad (Tabla 6), pero en términos generales debe ser mayor al 70% para personas menores de 50 años. Si la prueba confirma obstrucción, posteriormente se debe graduar la gravedad de acuerdo al porcentaje del predicho del VEF1 (Figura 4). Una relación VEF1/CVF normal (> LIN) con CVF mayor o igual al 80% define una espirometría normal (mecánica pulmonar normal) mientras que una relación VEF1/CVF normal con una CVF menor del 80% es compatible con un proceso pulmonar restrictivo (volumen pulmonar disminuido).
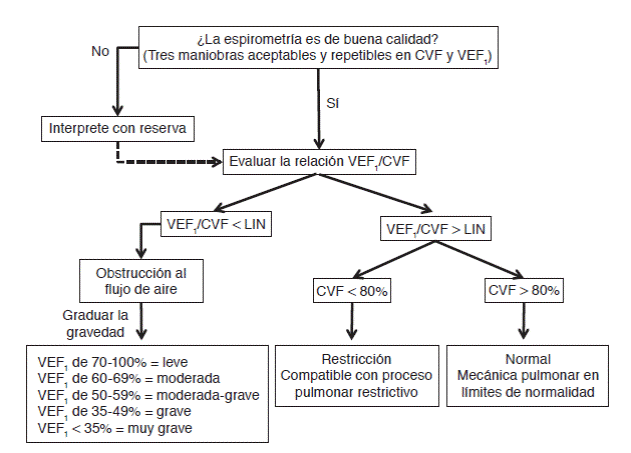
Figura 4 Diagrama de flujo recomendado para el proceso de interpretación de la espirometría. El primer paso recomendado es evaluar la calidad de la prueba de acuerdo a los criterios de aceptabilidad y repetibilidad. Para determinar el patrón ventilatorio se debe iniciar la interpretación con la evaluación de la relación VEF1/CVF. En términos generales debe ser mayor al 70% para personas menores de 50 años. Si la relación es menor al límite inferior normal (LIN) el cual depende de la edad (Tabla 6), la prueba se interpreta como diagnóstica de obstrucción al flujo de aire; posteriormente, debe graduarse la gravedad o el grado de obstrucción. Una relación VEF1/CVF normal (>LIN) con CVF mayor o igual al 80% define una espirometría normal (mecánica pulmonar normal) mientras que una relación VEF1/CVF normal con una CVF menor del 80% es compatible con un proceso restrictivo pulmonar (pulmón pequeño).
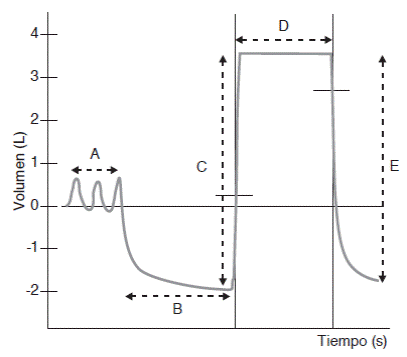
Figura 5 Maniobra respiratoria correspondiente a la prueba de difusión pulmonar de monóxido de carbono de respiración única (DLCO). La maniobra inicia con respiraciones en volumen corriente (A), seguidas de una maniobra de volumen de reserva espiratoria hasta llegar a volumen residual (B). Después, se realiza con inspiración máxima (C) o volumen inspiratorio (Vin) y que debe de ser > 85% de la mayor CVF, durante esta inhalación se libera el gas de prueba que contiene 0.3% de monóxido de carbono (CO) y un gas inerte que suele ser helio, neón o metano, el cual permite medir el volumen de aire ventilable en el pulmón. Posteriormente, se realiza un período de apnea de 10 segundos de duración (D) que es donde se transfiere el CO hasta la hemoglobina; al final se realiza una espiración mayor a 4 segundos (E) que es donde se capta el aire espirado proveniente de los alvéolos para calcular la proporción de CO transferido a la hemoglobina.
Espirometría con broncodilatador
Esta prueba es de utilidad para evaluar cambios en el volumen pulmonar (CVF) y en los flujos espiratorios (VEF1) posterior a la administración de un medicamento broncodilatador por vía inhalada.13,16,18 En términos generales, no se debe haber inhalado broncodilatadores de 4 a 24 horas antes de la prueba (de acuerdo a la vida media de cada medicamento). La respuesta fisiológica al broncodilatador integra el epitelio bronquial, nervios, mediadores y músculo liso de la vía aérea. Para realizar la prueba se recomienda completar una espirometría basal que cumpla las recomendaciones mínimas (Tabla 5). A continuación se administran 200 a 400 μg (2 a 4 inhalaciones) de salbutamol, usando cámara espaciadora. La espirometría se repite 15 minutos después, una respuesta al broncodilatador se considera positiva cuando la CVF y/o el VEF1 mejoran más del 12% y más de 200 mL con respecto al valor basal.
La prueba de broncodilatador siempre es de mucha utilidad en una espirometría diagnóstica. Un proceso obstructivo reversible inmediatamente con el broncodilatador o tardíamente (días o semanas) de manera espontánea o con tratamiento, habitualmente es compatible con asma, mientras que un proceso obstructivo no completamente reversible es típico de enfermedades con obstrucción al flujo aéreo fija y crónica, como es el caso de la EPOC.
Difusión pulmonar de monóxido de carbono
La medición de la difusión o transferencia de monóxido de carbono (DLCO o TLCO) es una prueba de intercambio gaseoso que mide con relativa facilidad el proceso de oxigenación a nivel alvéolo-capilar.22-24 La prueba es muy sencilla y toma unos 15 a 20 minutos realizarla. A diferencia de la espirometría, no requiere de maniobras forzadas por lo que puede resultar más cómoda. Para esta prueba se usa como marcador de oxigenación el monóxido de carbono (CO) que pasa libremente la membrana y que es altamente afín a la hemoglobina. La cantidad de CO administrada es muy pequeña y su transferencia se calcula a partir de la relación entre el volumen de CO inspirado y espirado.
El estudio de la difusión se basa en la Ley de Fick que describe que el paso de un gas a través de una membrana es directamente proporcional a la superficie de la membrana, la diferencia de concentración del gas entre los dos lados de la membrana y es inversamente proporcional a su grosor. La superficie de la membrana alvéolo-capilar es en promedio de 70 m2 y su grosor promedio es de 5 μm. Asimismo, el coeficiente de difusión del gas es directamente proporcional a su solubilidad e inversamente proporcional a su peso molecular; por ejemplo, el CO2 difunde unas 20 veces más rápido que el O2 ya que es mucho más soluble y su peso molecular no es mucho mayor. Además, la capacidad de difusión del O2 depende de la cantidad de hemoglobina disponible y el tiempo de exposición del eritrocito a los alvéolos que en reposo es de 0.7 a 1.2 segundos. En términos generales, la prueba de DLCO mide la integridad de la membrana alvéolo-capilar; las enfermedades que disminuyen la superficie de la membrana, como el enfisema pulmonar o que la alteran por inflamación o fibrosis, como las neumoconiosis, cursan con una DLCO proporcionalmente más baja de acuerdo al grado de daño alveolar.
La prueba de DLCO ha sido estandarizada internacionalmente (ATS/ERS 2005).24 Recomendaciones recientemente actualizadas,25 por lo que se sugiere seguir estos procedimientos para la técnica de una sola respiración.24,26 La maniobra (Figura 5) consiste en una exhalación máxima hasta llegar a volumen residual; posteriormente, se realiza con inspiración máxima equivalente a una capacidad vital inspiratoria o volumen inspiratorio (Vin), durante esta inhalación se libera el gas de prueba que contiene 0.3% de CO y un gas inerte que suele ser helio, neón o metano, el cual permite medir el volumen de aire ventilado en el pulmón. Después se realiza un período de apnea de 10 segundos de duración que es donde se transfiere el CO hasta la hemoglobina; finalmente, se realiza una espiración mayor a 4 segundos para captar el aire espirado proveniente de los alvéolos para calcular la proporción de CO transferido a la hemoglobina. La prueba completa consiste en dos mediciones consecutivas y que muestren una diferencia no mayor a tres unidades (mmol/min/kPa) o 10%.
La interpretación de la prueba también se realiza a partir de una comparación directa con los valores normales o predichos. Los estándares internacionales vigentes25 sólo recomiendan las ecuaciones de referencia generadas bajo los estándares previos (ATS/ERS 2005). Recientemente, se han publicado ecuaciones de referencia para población latinoamericana que incluye mexicanos y que están ajustadas por altitud y hemo globina.27 Al igual que flujos y volúmenes pulmonares, una disminución de la DLCO se define cuando está por debajo del LIN (aproximadamente 80% del predicho). Para graduar la gravedad se recomienda definir disminución leve con DL;CO ≥ 60% y < LIN, disminución moderada de 40 a 59% y grave cuando es menor al 40% del predicho.
Prueba cardiopulmonar de ejercicio
Las pruebas de función respiratoria convencionales en reposo suelen diagnosticar y graduar la gravedad de la mayoría de las enfermedades respiratorias crónicas. Aunque no dan información directa de la capacidad funcional del individuo, por lo que las pruebas de ejercicio, particularmente la PCPE puede tener un impacto en el proceso de decisión clínica para identificar origen de síntomas (disnea) y la contribución de diferentes órganos (pulmones, corazón o musculoesquelético) en la limitación al ejercicio.28,29 La PCPE puede ser requerida en una minoría de pacientes con ERO y permite definir de manera definitiva el grado de funcionalidad del individuo, ya que mide la capacidad de realizar trabajo físico; en consecuencia, mejora la precisión con que se evalúa el grado de deficiencia funcional.
La PCPE se realiza en un cicloergómetro o en una banda sinfín con protocolos de incremento progresivos de trabajo. Durante la prueba se mide el consumo de oxígeno (VO2), la producción de CO2 (VCO2) y la ventilación minuto; también se pueden monitorear otras variables de interés durante el ejercicio, como el electrocardiograma, la presión arterial y la saturación de oxígeno por pulsooximetría (SpO2). Asimismo, si se obtienen gasometrías arteriales se agrega información sobre el intercambio gaseoso durante el ejercicio.
La PCPE realizada en cicloergómetro electrónicamente controlado es preferible a la realizada en banda sinfín; es menos costoso y más seguro, permite medir directamente el trabajo realizado con menos artefactos en el ECG y facilita la toma de muestras de sangre arterial. Los protocolos de ejercicio son variados; se recomiendan incrementos de trabajo de 5 a 25 watts por minuto y la capacidad aeróbica se debe alcanzar en menos de 12 minutos, ya que la prueba resulta incómoda debido a la instrumentación.
El consumo máximo de oxígeno (VO2máx) se alcanza cuando existe meseta en el VO2, es decir, no aumenta a pesar de incrementos en el trabajo. Cuando no se alcanza meseta en el VO2 se denomina como consumo pico de oxígeno (VO2pico); para fines prácticos ambos parámetros son intercambiables y representan el mejor indicador de la capacidad de ejercicio. Estos parámetros deben informarse como valores absolutos (L/min) y como porciento del predicho. Un VO2máx normal refleja capacidad aeróbica y capacidad de ejercicio normales y descarta anormalidad funcional. En contraste, un VO2máx disminuido traduce pobre esfuerzo o problemas en la entrega de O2 que pueden tener origen en los pulmones, circulación sistémica y pulmonar, musculoesquelético o en el trasporte sanguíneo.
Evaluación de la deficiencia respiratoria
Varias organizaciones profesionales internacionalmente reconocidas han publicado sus recomendaciones para la evaluación de la deficiencia respiratoria. La ATS publicó en 1986 en conjunto con la Asociación Americana del Pulmón (ALA) las recomendaciones para evaluación de deficiencia y discapacidad secundaria a enfermedades respiratorias.30 Estas recomendaciones no han sido actualizadas de manera reciente, excepto para el caso de asma, revisada y publicada en 1993.31 La Sociedad Europea de Fisiología Respiratoria Clínica (SEPCR) publicó sus recomendaciones para graduar discapacidad respiratoria en 1990.32 Finalmente, la Asociación Médica Americana (AMA) en sus guías para evaluación de deficiencia que fueron revisadas en el año 2000, incluyen recomendaciones específicas para valoración del sistema respiratorio.33 Las recomendaciones de las tres organizaciones son muy similares, sin embargo, las de la AMA son las que con mayor frecuencia se utilizan y refieren en la literatura. Estas valoraciones son secuenciales como se describió. Si con la prueba más sencilla, la espirometría, se puede documentar una alteración funcional grave, ya no es necesario hacer pruebas adicionales. Se han promovido esquemas de evaluación «en paquete», que someten a los solicitantes a espirometría, DLCO, PCPE y quizá otras pruebas, pero el procedimiento en muchas ocasiones es redundante y además incrementa los costos. Es más eficiente en forma secuencial y las pruebas más sofisticadas pueden realizarse sólo en algunos centros especializados, ya que se requerirán en menos individuos.
La valoración médica de deficiencia respiratoria debe incluir una valoración clínica previa con historia médica y examen físico cuidadoso, radiografía de tórax y PFR estandarizadas que siempre deben incluir de inicio a la espirometría. Todas las recomendaciones publicadas se enfocan casi siempre en evaluar el grado de deficiencia respiratoria relacionada a una reducción de la función pulmonar, lo cual se asocia a una alta probabilidad de limitación para la capacidad de realizar ejercicio físico. Antes de la evaluación de deficiencia es recomendable que ya exista un diagnóstico médico establecido, ya que la función pulmonar puede estar disminuida directamente por enfermedades no respiratorias, como deformidades musculoesqueléticas del tórax, enfermedades neuromusculares o incluso por insuficiencia cardíaca. Las pruebas de función respiratoria deben realizarse con el paciente estable y siguiendo todas las recomendaciones de estandarización previamente referidas.
Las guías de la ATS, SEPCR y AMA recomiendan realizar la espirometría y prueba de DLCO en todos los casos y sólo una minoría de pacientes requiere de una PCPE. En el proceso de valuación se incluyen sólo los valores predichos de CVF, VEF1 y de DLCO. La SEPC y la AMA insisten en utilizar límites inferiores de normalidad de acuerdo con la distribución del valor en la población de referencia. La AMA especifica grados de deficiencia respiratoria de acuerdo a valores VO2máx (mL/kg/min) y trabajo realizado (Mets). La ATS y la SEPCR gradúan la deficiencia pulmonar como: no deficiencia y deficiencia leve, moderada o grave. Éstos son, respectivamente, equivalentes a las clases 1, 2, 3 y 4 de la AMA.
Propuesta de evaluación de deficiencia respiratoria en México
La propuesta del grupo de trabajo de la STPS para la graduación de la deficiencia respiratoria en presencia de ERO se resume en la Tabla 7 y en la Figura 6. En general, estos procedimientos son congruentes con las recomendaciones internacionales previamente descritas.30-33 La Figura 6 muestra el diagrama de flujo recomendado para la evaluación funcional respiratoria en el proceso de graduación de la deficiencia respiratoria. Éste es un esquema de uso progresivo de las pruebas de acuerdo con su complejidad y por lo tanto su disponibilidad, lo que debe facilitar y optimizar su utilización. La valoración funcional y la graduación de la deficiencia respiratoria siempre deben iniciar con la espirometría. Si la prueba confirma un valor de VEF1 o CVF igual o menor al 50% se determina deficiencia grave sin requerir de otras pruebas necesariamente. El segundo paso requiere valorar el intercambio de gases a nivel pulmonar con la prueba de DLCO. En la mayoría de los enfermos debe ser posible graduar el estado de deficiencia respiratoria sólo con la espirometría y la prueba de DLCO. En caso de existir duda, por resultados limítrofes y principalmente con la presencia de disnea o limitación referida excesiva para las alteraciones encontradas en la espirometría o la DLCO, es recomendable que se complete una PECP para medir VO2máx y determinar de manera definitiva el grado de deficiencia.
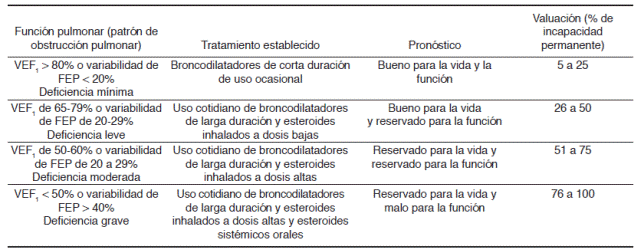
Tabla 7 Graduación de deficiencia respiratoria.
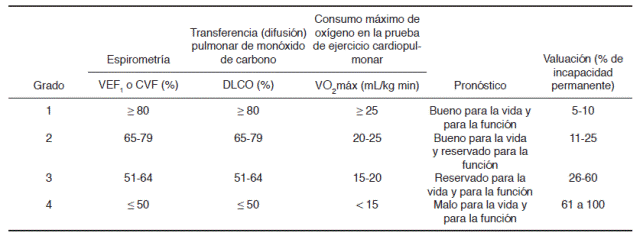
1. La evaluación funcional debe iniciar con espirometría como prueba de mecánica respiratoria, seguida de DLCO como prueba de intercambio gaseoso para valorar transferencia de oxígeno a nivel pulmonar. En caso de existir duda se recomienda prueba de ejercicio cardiopulmonar.
2. La incapacidad funcional es muy grave si cualquier valor de VEF1, CVF o DLCO está por abajo del 30% del esperado o cuando la VO2máx es menor a 10 mL/kg/min
3. El porcentaje de valuación lo determina la prueba de función respiratoria con el valor más bajo encontrado.
4. La valuación en grado 1 representa deficiencia orgánica, por ejemplo, afectación radiológica en presencia de pruebas de función respiratoria en límites normales.
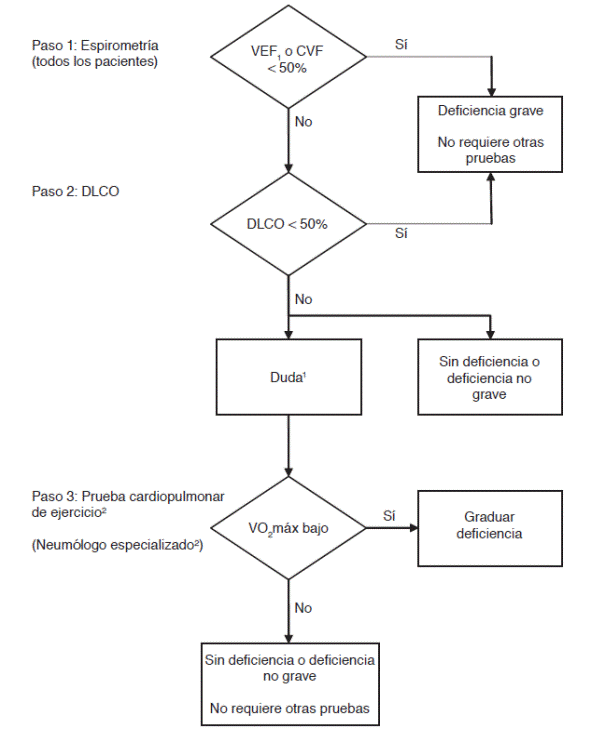
Figura 6 Diagrama de flujo recomendado para la evaluación funcional respiratoria en el proces de graduación de la deficiencia respiratoria con el uso progresivo de prueba de función respiratoria. Este esquema sugerido busca disminuir el número de pruebas que se realizan en los centros de referencia. El procedimiento inicia en todo enfermo con la realización de una espirometría. Si la prueba confirma un valor de VEF1 o CVF igual o menor al 50% se determina deficiencia grave sin requerir de mayor evaluación. El segundo paso requiere valorar el intercambio de gases a nivel pulmonar con la prueba de DLCO. En la mayoría de los enfermos sería posible graduar el estado de deficiencia respiratoria sólo con espirometría y DLCO. En caso de duda, principalmente con la presencia de disnea o limitación referida excesiva para las alteraciones encontrada en la espirometría o DLCO se recomienda una prueba de ejercicio pulmonar para determinar el consumo de oxígeno (VO2máx) para determinación definitiva del grado de deficiencia.
En la Tabla 7 se especifican los grados de deficiencia respiratoria de acuerdo con los resultados de las PFR, el pronóstico correspondiente y el porcentaje de valuación de la deficiencia respiratoria, como lo establece la LFT. El grado de deficiencia está determinado por el valor más bajo encontrado en cualquiera de la PFR que integra el procedimiento. Los grados propuestos son del 1 al 4, que corresponde a un estado funcional en límites normales (Grado 1) o un estado funcional disminuido en grados del 2 al 4 que proporcionalmente corresponden a una condición funcional levemente disminuida (Grado 2), moderadamente disminuida (Grado 3) o gravemente disminuida (Grado 4).
Una condición especial de evaluación de deficiencia respiratoria corresponde al asma y al síndrome de disfunción reactiva de la vía aérea. Estas enfermedades son complicadas y se han descrito recomendaciones de evaluación y graduación de acuerdo con puntajes específicos que involucran resultados de espirometría, requerimientos de medicamentos y reversibilidad en la obstrucción e hiperreactividad bronquial.23 Es decir, una persona con asma puede estar bien controlado y con función normal o cercana a la normal, debido al uso de varios medicamentos inhalados y de corticosteroides sistémicos a dosis altas; sin embargo, esto implica un mayor riesgo de eventos adversos y se considera con mayor incapacidad. En la Tabla 8 se muestran los criterios de graduación de la deficiencia respiratoria y su valuación correspondiente en estas enfermedades.
Consideraciones adicionales y perspectivas futuras
Previamente se han revisado estándares internaciones de PFR y recomendaciones de graduación de deficiencia. Empero, existen diversas limitaciones que deben considerarse en nuestro país y algunos puntos de oportunidad para desarrollo de investigación en nuestro medio.
La evaluación funcional y la determinación de la deficiencia respiratoria por medio de las PFR se recomiendan hace muchos años. Aunque la disponibilidad de las pruebas, incluyendo la espirometría, es muy limitada, mientras que la prueba de DLCO y la PCPE son casi inexistentes, aun en las instituciones encargadas de evaluar y decretar discapacidad laboral. La infraestructura física relacionada con laboratorios de referencia que funcionen como centros de valuación será una necesidad de mediano y largo plazo.
En general existe poca difusión y enseñanza en el ambiente en las especialidades de Neumología, Medicina del Trabajo y Medicina Familiar en cuanto a la forma de evaluar la deficiencia y la discapacidad respiratoria.
Como es de esperarse, la actualización de la tabla de enfermedades de origen ocupacional y de los procedimientos de valuación conlleva el reto que requiere de la creación de la infraestructura física, así como la capacitación y la formación de nuevos recursos humanos que garanticen la adecuada implementación de los procedimientos propuestos.











 text new page (beta)
text new page (beta)