OBJETIVO
Revisar un caso clínico sobre una paciente con síntomas oftalmológicos secundarios a un meningioma, y destacar la importancia de conocer las manifestaciones clínicas iniciales de esta patología, y así realizar un diagnóstico oportuno y el tratamiento indicado.
MOTIVO DE LA QUEJA
La paciente considera que la atención médica brindada por oftalmología careció de calidad, fue inadecuada e inoportuna, que no se realizó un diagnóstico oportuno y no se brindó el tratamiento requerido, lo que contribuyó a una alteración física y funcional que derivó en daños, complicaciones y secuelas; por lo que se busca una explicación médica del porqué se le brindó ese tipo de atención, así como una indemnización y un reembolso de los gastos erogados.
CASO CLÍNICO
Paciente mujer de 71 años de edad que acudió a un hospital de oftalmología refiriendo prurito en ambos ojos, epífora y disminución de la visión de 1 año de evolución en el ojo izquierdo. Tiene como antecedente hipertensión arterial sistémica de 10 años de diagnóstico en tratamiento. A la exploración física, se encontró agudeza visual del ojo derecho de 20/150, que se corrigió a 20/40 con agujero estenopéico, y en el ojo izquierdo de 20/400, que corrigió a 20/200; en el ojo derecho se observó la mácula con brillo disminuido. En el ojo izquierdo se encontró atrofia del epitelio pigmentado de la retina, exudados, líquido subretiniano, papila con excavación de 50%, por lo que se estableció el diagnóstico de membrana neovascular.
Un mes después acudió a revisión nuevamente, donde se halló empeoramiento de la agudeza visual del ojo izquierdo de 20/800, que corrigió con agujero estenopéico a 20/250. Se le realizó una tomografía óptica coherente y una fluorangiografía con hallazgos consistentes con su padecimiento. La paciente acudió a consulta mensualmente por un año, hasta que se incrementó la disminución de la agudeza visual en el ojo izquierdo, y sólo percibía movimientos de las manos. Se le aplicó bevacizumab en el ojo izquierdo en 5 ocasiones sin presentar mejoría, debido a ello se sustituyó con ranibizumab, el cual se empleó en 2 ocasiones.
Cinco meses después la paciente refirió que no había mejoría con el tratamiento empleado, manifestó disminución de la visión del ojo derecho, cefalea, alteración en la marcha e hipoacusia; asimismo percibía asimetría en la posición de los ojos a expensas de protrusión del ojo izquierdo. Se le realizó una campimetría por confrontación donde se detectó que la paciente cursaba con una hemianopsia de tipo heterónima bitemporal. Derivada al servicio de órbita se encontró en la tomografía una masa ocupativa en la órbita izquierda, que erosionaba el techo de la órbita, parecía comunicarse con la cavidad endocraneana y causaba compresión del nervio óptico, por lo que se refirió al servicio de neurocirugía de tercer nivel para su atención. En dicho servicio se encontró a la paciente neurológicamente íntegra; se revisó el par craneal II del ojo derecho, en donde se encontró con agudeza visual de 20/200, que no mejoraba con agujero estenopéico, en el ojo izquierdo no había percepción de la luz. Los reflejos pupilares se encontraron presentes así como la sensibilidad corneal, la sensibilidad en la cara era normal; los reflejos nauseoso, tusígeno y elevación del paladar estaban presentes; había ausencia de reflejos meníngeos y la respuesta plantar flexora estaba presente.
Se solicitó una tomografía de cráneo en donde se observó una masa isodensa que invadía el piso anterior del cráneo, con un discreto desplazamiento de estructuras intraorbitarias del lado izquierdo. Se diagnosticó a la paciente con meningioma esfenoidal izquierdo. La paciente ingresó para realizar resección quirúrgica total del meningioma, durante el procedimiento se observó extensión hacia el techo y pared lateral de la órbita, así también hacia la fosa temporal. La pieza extraída fue enviada al servicio de histopatología, donde se emitió el diagnóstico de meningioma fibroso1.
MARCO TEÓRICO
Introducción
El ojo es una ventana abierta al sistema nervioso central (SNC), proporciona múltiples y variados signos como resultado de una alteración a cualquier nivel de la vía óptica o de las numerosas estructuras asociadas que toman parte en el complejo proceso de la visión1.
Las alteraciones neurooftalmológicas tienen rasgos característicos. Los pacientes se presentan generalmente con visión borrosa, problemas para enfocar, dificultad para leer, fotofobia o diplopía, entre otros síntomas. La valoración del campo visual en estas patologías tiene una particular importancia, ya que los defectos perimétricos adoptan un patrón característico que permite ubicar topográficamente la lesión1),(2.
La vía óptica abarca un largo trayecto anatómico, que va desde el globo ocular hasta el extremo más distal de la corteza occipital, y los intrincados mecanismos neurológicos que gobiernan los movimientos oculares comprenden gran parte del encéfalo y el tronco cerebral2.
Se debe considerar la compresión del nervio óptico en cualquier paciente con signos de neuropatía o pérdida visual no explicable como consecuencia de lesión intraocular. En la compresión nerviosa resulta vital el reconocimiento oportuno. Dentro de la investigación por posible compresión del nervio óptico se requieren estudios de imagenología2),(3.
Ante un paciente que consulta en primera instancia al oftalmólogo, el reto consiste principalmente, en seleccionar el tipo de examen complementario y el momento más adecuado para realizarlo en cada caso. El elemento de mayor peso al momento de esta elección es la probable localización -sugerida por la evaluación oftalmológica- del problema en cuestión2.
Los meningiomas intracraneales que pueden comprimir el nervio óptico incluyen a los que surgen del ala esfenoidea, del tubérculo de la silla y del surco olfatorio. Los meningiomas del ala esfenoidal también producen proptosis como lo es el caso, trastornos de la motilidad ocular, pérdida sensitiva en el área del trigémino3.
Campos visuales
Se definen como la porción de un espacio en el que los objetos son visibles durante la fijación de la mirada en una dirección. Existen 3 partes en el campo visual: campo central (se extenderá 20° alrededor del punto de fijación), campo medio (entre 20 y 40°) y campo periférico (> 40°). Los trastornos de los campos visuales obedecerán al lugar anatómico de la lesión y se manifestarán por pérdidas visuales localizadas totales o segmentarias (Figura 1)4.

Figura 1 Campos visuales y vías ópticas 4. Los números indican los lugares de las lesiones y su correspondiente traducción en defectos del campo visual (rojo). 1. Ceguera en el ojo derecho con pérdida del reflejo fotomotor. 2. Hemianopsia bitemporal (tumores, hipofisarios, craneofaringioma, meningioma) 3 a y b. Hemianopsia binasal (infrecuente). 2 y 3b. Ceguera del ojo derecho asociada a hemianopsia temporal del campo visual izquierdo. 4. Hemianopsia homónima derecha con afección de la mácula (causa vascular, tumor) 5. Hemianopsia homónima derecha que respeta la visión macular. 6. Hemiescotoma central (macular) homónimo derecho4.
Defectos quiasmáticos
A partir de este nivel, cualquier lesión repercute en ambos campos visuales.
Hemianopsia bitemporal heterónima: La hemianopsia bitemporal, comienza afectando las fibras inferiores y, por tanto, las mitades superiores de los campos visuales, para irse extendiendo de forma progresiva hacia abajo hasta hacerse completa. Característicamente la agudeza visual suele ser normal, a menos de que se afecte el nervio óptico y suelen acompañarse de atrofia en banda ambos nervios ópticos por degeneración axonal retrógrada5.
Hemianopsia binasal: Se origina por daño de las fibras temporales de ambos nervios ópticos. Otro posible mecanismo en casos de hidrocefalia es la distensión III ventrículo que determina un desplazamiento lateral de los nervios ópticos contra la porción supraclinoidea de la arteria carótida interna5.
Defectos postquiasmáticos
Dado que a nivel de las cintillas ópticas se reúnen las fibras temporales homolaterales y nasales contralaterales, se comprende que el defecto postquiasmático típico sea una hemianopsia homónima contralateral. Uno de los datos que nos orienta sobre la localización de los mismos es el grado de congruencia, es decir, la similitud en localización, forma, tamaño y profundidad de las alteraciones campimétricas presentes en ambos ojos. La localización más frecuente de los defectos postquiasmáticos es el lóbulo occipital (40%), seguida por el parietal (33%) y temporal (24%), siendo muy infrecuente la afectación del tracto óptico o el ganglio geniculado5.
Síndrome de cintilla óptica. Se caracteriza por la siguiente triada: hemianopsia homónima incongruente, atrofia óptica hemianópsica y anomalías pupilares5.
Cuerpo geniculado lateral. La afectación aislada y localizada del ganglio geniculado lateral (GGL) es rara, siendo el defecto campimétrico más frecuente una hemianopsia homónima incongruente. Las lesiones del ganglio geniculado lateral pueden manifestarse por defectos campimétricos aislados o acompañarse de signos neurológicos por afectación talámica o del tracto corticoespinal, como serían alteraciones sensitivas, dolor o hemiparesia contralateral5.
Lóbulo temporal. Resecciones limitadas de la parte anterior del lóbulo temporal de menos de 4 cm pueden producir, defectos campimétricos. Teniendo en cuenta esta distribución, se produce típicamente una cuadrantanopsia homónima superior contralateral, que puede ser congruente o no según la localización de la lesión5.
Lóbulo parietal. Los defectos suelen ser más congruentes que en el lóbulo temporal, ya que la radiación óptica completa pasa a través del lóbulo parietal. El defecto campimétrico típico a este nivel es una cuadrantanopsia homónima inferior contralateral que puede ser incompleta, o si la lesión es extensa, determinar una hemianopsia homónima incompleta de mayor densidad en la zona inferior5.
Lóbulo occipital. La afectación a este nivel produce defectos casi exclusivamente homónimos y extraordinariamente congruentes, siendo la causa más frecuente el infarto en el territorio de la arteria cerebral posterior5.
Lesión completa área V1: Una lesión completa a nivel del área V1 podría producir una hemianopsia homónima contralateral completa, que suele ser causada por infarto de la arteria cerebral posterior. El respeto macular no se debe a una representación macular bilateral, como se pensaba anteriormente, sino que es atribuido a la combinación de dos factores, la presencia de una circulación colateral abundante de la arteria cerebral media y a que la representación macular está magnificada a nivel occipital5.
Meningioma
Los meningiomas son la neoplasia intracraneal de origen no glial más frecuentes del SNC, son tumores extraaxiales originados a partir de las células aracnoideas meningoteliales presentes en las granulaciones de Pacchioni o granulaciones aracnoideas, que son protrusiones de la membrana aracnoidea hacia el interior de los senos dúrales a través de orificios en la duramadre (Figura 2)4.
Fue descrito por primera vez como un tipo específico de tumor por el cirujano francés Antonie Louis en 1774, posteriormente, Cushing designa el término meningioma. Son los tumores cerebrales primarios más comunes y representan el 36.4% de todos los casos6),(7),(11.
Tienen una incidencia de 7.7 por 100,000 habitantes. Los meningiomas son más frecuentes en mujeres entre la cuarta y la sexta década de la vida, bajo influencia de factores hormonales. En hombres aparecen generalmente hasta después de la sexta década de la vida, cuando las concentraciones de testosterona disminuyen, con una relación mujer: hombres de 3.5:1. En niños son excepcionalmente raros14.
Los factores de riesgo incluyen la exposición a radiación ionizante, diabetes mellitus o hipertensión arterial y, posiblemente, el tabaquismo; el uso de teléfonos móviles no parece estar asociado con un mayor riesgo de tumor7),(14.
Son generalmente benignos; sin embargo, se han descrito estirpes malignas dentro de las que destacan las variantes anaplásicas y angiomatosas. Los meningiomas benignos son tumores de lento crecimiento (grado I de la Organización Mundial de la Salud [OMS]) potencialmente curables por resección total. Se caracterizan por tener una base amplia de implantación dural, morfología en copa de hongo, bordes lisos rodeados por un halo de líquido cefalorraquídeo y pedículo nutricio vascular5.
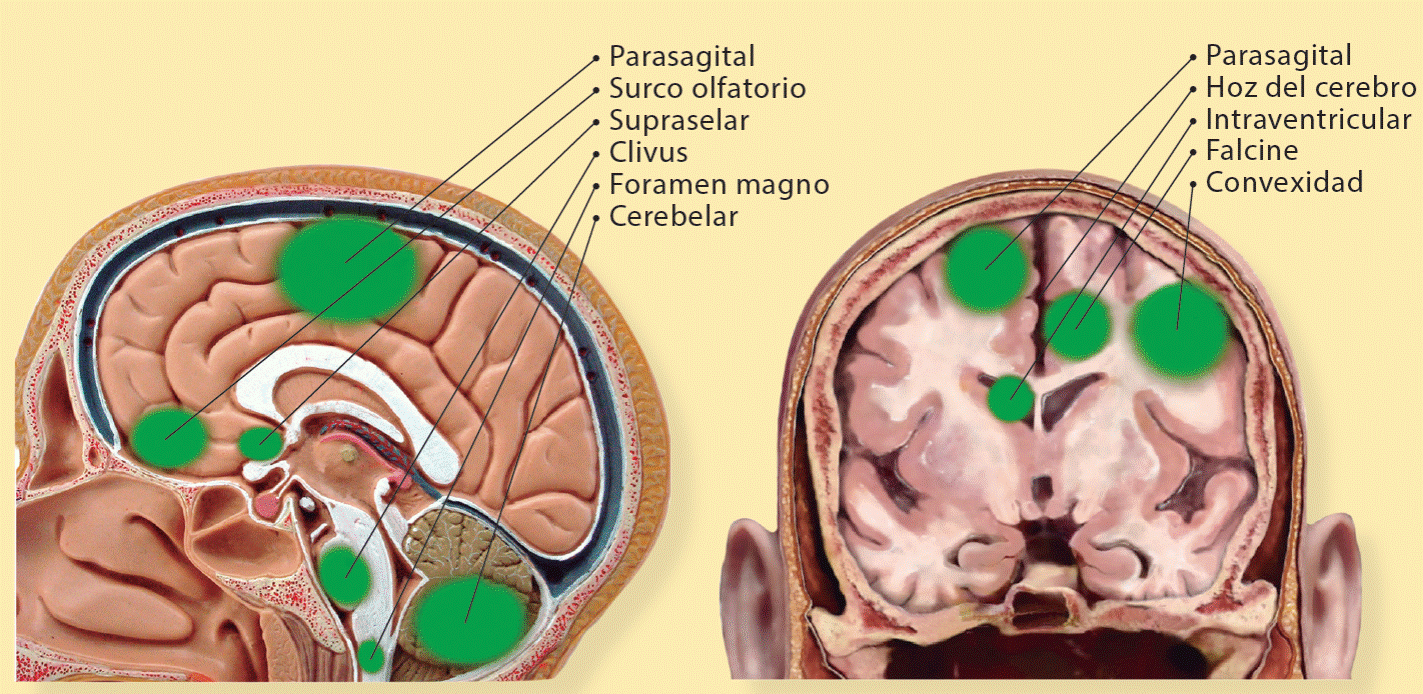
Las 3 localizaciones más frecuentes son las adyacentes al seno sagital superior (meningiomas parasagitales de la hoz), la convexidad cerebral (meningiomas de la convexidad) y a lo largo del reborde esfenoidal (meningiomas esfenoidales). Estas localizaciones comprenden alrededor del 60% de todos los meningiomas intracraneales (Figura 3). La mayor parte de los restantes se desarrollan a lo largo de la base del cráneo (meningioma del surco olfatorio, de la silla turca, tentoriales y petroclivales) (Tabla 1)9.
Tabla 1 Frecuencia de localización de los meningiomas2
| Localización | Porcentaje |
|---|---|
| Convexidad | 20-34% |
| Parasagital | 18-22% |
| Esfenoidal y fosa craneal media | 17-25% |
| Frontobasales | 10% |
| Ángulo cerebelopontino | 4% |
| Tienda del cerebelo | 3% |
| Clivus | 1% |
| Intraventricular | 2-5% |
| Orbitarios | 1-2% |
| Intraóseos | 3% |
Clasificación y presentación clínica
Aproximadamente 90% de los meningiomas se desarrolla a partir de las meninges craneales, el 10% restante ocurre en las meninges espinales. Los síntomas de presentación clínica reflejan la región anatómica que está involucrada y comprimida por el tumor o edema peritumoral14.
Como los meningiomas son de crecimiento lento, los síntomas de inicio suelen ser insidiosos. En la Tabla 2 se describe la localización y el cuadro clínico correspondiente.
Tabla 2 Clasificación de los meningiomas de acuerdo a su localización y cuadro clínico7
Realizada por Lizbeth Lara Moctezuma.
Clasificación histopatológica
La clasificación histopatológica se basa en el grado de atipia nuclear y la presencia de figuras mitóticas. Las características adicionales incluyen hipercelularidad, aumento del índice núcleo-citoplasma, nucléolo prominente, crecimiento en empalizada y necrosis9),(10),(11.
Con poca frecuencia son lesiones malignas, la OMS ofrece la clasificación con el objetivo de predecir las características clínicas, con un sistema de 3 grados basados en la correlación clínico-patológica (Tabla 3)10.
Tabla 3 Variantes histológicas del meningioma agrupados por grados por la OMS10
| Grado | Variante de meningioma |
|---|---|
| 1. Con bajo riesgo de recurrencia y crecimiento agresivo | |
| 2. Con alta probabilidad de recurrencia y/o comportamiento agresivo | |
| 3. Con alta probabilidad de recurrencia y/o comportamiento agresivo |
Por otro lado, la Tabla 4 señala los criterios utilizados para su clasificación.
Tabla 4 Criterios de la OMS para designar el grado de los meningiomas
| Meningioma benigno (Grado I OMS) | |
| Meningioma atípico (Grado II OMS), cualquiera de los tres criterios | |
| Meningioma anaplásico, maligno (Grado III OMS), cualquiera de los dos criterios |
CAP: Campo alto poder10.
Diagnóstico por imagen
Dentro de los tumores primarios del SNC de hallazgo incidental, el tumor benigno más común es el meningioma y su detección incidental es más frecuente en personas en la sexta década de la vida y de sexo femenino. Es común que los casos incidentales sean detectados durante el estudio de otras patologías del SNC11.
Tomografía computarizada
La mayoría de los meningiomas son diagnosticados primero con tomografía computarizada (TC) y posteriormente complementados con otras técnicas de imagen. La TC es superior a la resonancia magnética (RM) para evidenciar los efectos sobre el hueso adyacente, especialmente la destrucción ósea que puede aparecer en los meningiomas atípicos y malignos, o la hiperostosis asociada a los meningiomas benignos. La TC sin contraste detecta aproximadamente el 85% de las lesiones, mientras que con la administración de contraste intravenoso alcanza unas cifras de detección cercanas al 95%8.
El meningioma típico muestra una masa hiperdensa de morfología hemisférica, redondeada o lobulada, de contornos bien definidos, que alcanza la superficie de la duramadre, que suele presentar un engrosamiento en la porción que contacta con el tumor (cola dural). La cola dural de aspecto liso orienta a un grado I, mientras que si es irregular o con nódulos orienta a un grado mayor8),(10.
Resonancia magnética
La señal de RM es similar en todos los tipos de meningiomas, independientemente de su tipo histológico; la mayoría muestra una señal homogénea en las diferentes secuencias. El meningioma típico presenta isoseñal o ligera hiposeñal con respecto de la corteza cerebral en las secuencias T1, y varía desde hiposeñal a ligera hiperseñal en imágenes potenciadas en T2. Todos los meningiomas se realzan de forma rápida e intensa con el contraste intravenoso. En las variedades atípicas y malignas, presentan áreas necróticas, hemorrágicas y quísticas que le confieren una señal heterogénea, y los límites de separación con el parénquima circundante suelen ser menos definidos. En más de la mitad de los casos existe ‘cola dural’ que rodea la base de los meningiomas, y, aunque no es específico, sí es muy sugestivo de meningioma, relacionándose con infiltración tumoral o con engrosamiento reactivo de la duramadre8.
Angiografía cerebral
La angiografía convencional ya no constituye una prueba fundamental en el diagnóstico de los meningiomas intracraneales; sin embargo, en 2 situaciones, la angiografía convencional puede estar justificada: en los casos en que sea indispensable para la planificación quirúrgica de meningiomas íntimamente adheridos a grandes vasos intracraneales o cuando se realiza una embolización preoperatoria para minimizar la perdida hemática durante la cirugía8.
Tratamiento
La resección neuroquirúrgica y su grado son el pilar del tratamiento y el predictor de progresión. Cuando esta es incompleta se observa recidiva a los 5 a 10 años, según la agresividad del tumor. La radiocirugía posoperatoria podría ser de ayuda en los pacientes con resección tumoral incompleta10.
En los meningiomas asintomáticos la viabilidad de la cirugía debe evaluarse cuidadosamente sobre la base del control clínico-neurológico y por neuroimágenes, valorando la aparición de síntomas y el crecimiento tumoral; por ello, algunos autores recomiendan realizar un control periódico por neuroimágenes. En los pacientes añosos, las mismas pueden efectuarse 2 o 3 meses luego del diagnóstico inicial, y si hay ausencia de malignidad, pueden realizarse controles cada 6 o 12 meses10.
La tarea del neurooncólogo está orientada al diagnóstico y al tratamiento de los síntomas, el control posterior a la neurocirugía o radioterapia (RT)/ quimioterapia y sus potenciales complicaciones10),(12.
Tratamiento quirúrgico de los meningiomas
El tratamiento quirúrgico de un meningioma requiere de un balance entre el tratar definitivamente el tumor y evitar el daño neurológico del propio tratamiento. Así, factores específicos del paciente (edad, presencia o ausencia de síntomas, comorbilidades) y factores específicos del tumor (localización, tamaño, características histológicas del mismo) son importantes a la hora de determinar el tratamiento óptimo de un meningioma. La Tabla 5 señala en qué consiste la terapia inicial de un paciente con un meningioma de características benignas10),(12),(14.
Tabla 5 Opciones de tratamiento para meningioma11
| a) Cirugía | c) Solo radioterapia |
| b) Cirugía + Radioterapia | d) Solo observación |
Realizada por Diana Yolatl Barrios Calyecac.
Muchos pacientes con pequeños meningiomas asintomáticos pueden observarse de forma segura; se indica tratamiento solo si el tumor crece significativamente o se vuelve sintomático10),(12),(13.
Los meningiomas que deben ser resecados, de ser posible son los sintomáticos o asintomáticos que crecen, pacientes con edades ≤ 60 años, diámetro inicial ≥ 25 mm, ausencia de calcificaciones, los que infiltran o están asociados a edema a su alrededor. Una resección completa es preferible cuando el meningioma se ubica en un área accesible, ya que la completa exéresis tumoral y de la inserción dural suelen proporcionar un tratamiento curativo. Estudios observacionales han reportado que una resección completa, cuando es posible, está asociada significativamente con una sobrevida prolongada comparada con una resección parcial10),(13.
La graduación de Simpson (Simpson I-V) se sigue utilizando para describir la extensión de la resección quirúrgica (Tabla 6).
Tabla 6 Escala de Simpson. Extensión de la resección quirúrgica y porcentaje de recurrencia8
| Grado | Extensión de resección quirúrgica | Recurrencia (%) |
|---|---|---|
| Grado 1 | Resección completa, incluida la inserción dural y el hueso anormal | 9% |
| Grado 2 | Resección completa, con coagulación de la inserción dural | 19% |
| Grado 3 | Resección completa, sin resección o coagulación de la inserción dural | 29% |
| Grado 4 | Resección subtotal | 44% |
| Grado 5 | Solo descompresión tumoral (biopsia) |
En tumores localizados en sitios como la convexidad, el surco olfatorio, el tercio anterior del seno sagital, algunos meningiomas del tentorio y la fosa posterior, el neurocirujano busca, habitualmente, una resección completa. Sin embargo, para los meningiomas grado I de la OMS, al analizar el beneficio entre una resección Simpson 1 y 2, la diferencia podría ser insignificante. Por ello, ante un riesgo remoto pero posible de complicaciones (lesión vascular y cerebral, fístula del líquido cefalorraquídeo) al intentar remover el hueso hiperostótico y la duramadre adyacente, es preferible ser conservador. Una resección subtotal es, en general, más apropiada para tumores menos accesibles, por ejemplo, los meningiomas localizados en la parte posterior del seno sagital, la región petroclival o el tercio interno del ala del esfenoides10.
La incidencia de déficit neurológico postoperatorio varía entre el 2 y el 30%, y depende fundamentalmente de la localización del tumor y de la extensión de la resección. La mortalidad varía ampliamente entre una serie y otra; sin embargo, los factores asociados a un aumento de la mortalidad son los siguientes10),(13:
Radioterapia
El papel de la RT en el tratamiento de los meningiomas depende de factores asociados al paciente, como las comorbilidades y su preferencia, y factores asociados al tumor, como el tamaño tumoral, la resecabilidad y particularmente el grado histológico. La RT se recomienda, generalmente, en los meningiomas luego de una cirugía inicial (adyuvante), o como tratamiento único en los irresecables; también posterior a una resección de un meningioma maligno (grado III de la OMS), porque la supervivencia libre de progresión a 5 años es de 80% comparado con la cirugía sola (15%). La RT ha demostrado reducir la carga tumoral además de prevenir la recurrencia10),(12),(14.
Tratamiento farmacológico
Una variedad de fármacos han sido estudiados para el tratamiento de los meningiomas. Estos incluyen hidroxiurea, temozolomida, irinotecan, interferón-α, mifepristona, análogos del octreótido, acetato de megestrol, bevacizumab, sunitinib, vatalinib, imatinib, erlotinib y gefitinib. Desafortunadamente, la mayoría de estos agentes han mostrado ninguna o muy poca actividad en el tratamiento de los meningiomas. Ciertamente, los agentes antiangiogénicos parecen una oportunidad para proporcionar un tratamiento racional hacia los meningiomas; ejemplo de ello es la regulación positiva de las vías angiogénicas repetidamente descriptas en estos tumores10),(14.
Pronóstico
La recurrencia y la progresión tumoral dependen de las características individuales del tumor, así como de las modalidades y los resultados de los tratamientos aplicados10),(12),(13.
La histología predice la mortalidad y la recurrencia. Los meningiomas que se presentan con invasión ósea muestran peores resultados en comparación con los tumores no invasores (Tabla 7)10.
Tabla 7 Tasa de recaída de los meningiomas según grado de la OMS11
| Grado I | Grado II | Grado III |
|---|---|---|
| 7% | 40% | 80% |
Los tumores grado III de la OMS que incluyen los meningiomas malignos son más invasivos y tienen mayor recurrencia local luego del tratamiento inicial, incluyendo aquellos con resección “completa”. El pronóstico empeora cuanto más indiferenciado es el tumor. La tasa mitótica elevada es un factor pronóstico significativo. Esto conduce a una supervivencia más corta en comparación con los pacientes con tumores grado I y II10),(13.
EJERCICIO DE REFORZAMIENTO
-
¿De qué células derivan los meningiomas?
-
¿Cuáles son las 3 localizaciones más frecuentes de los meningiomas?
-
¿Cuáles son los síntomas iniciales en un meningioma de la fosa anterior?
Déficit visual uni o bilateral progresivo y deterioro de las funciones psíquicas superiores.
Déficit visual uni o bilateral, crisis epilépticas y crisis de cefaleas.
Crisis de cefaleas, neuralgias faciales y trastornos de memoria.
Déficit visual unilateral o bilateral progresivo, hipoestesia hemifacial y crisis epilépticas.
-
¿Cuál es el estudio de diagnóstico que puede evidenciar afectación a hueso adyacente?
REFORZAMIENTO
Los meningiomas son la neoplasia intracraneal de origen no glial más frecuentes del SNC, son tumores extraaxiales originados a partir de las células aracnoideas meningoteliales presentes en las granulaciones de Paccioni.
Los meningiomas benignos son tumores de lento crecimiento (grado I de la OMS) potencialmente curables por resección total.
Las 3 localizaciones más frecuentes son los meningiomas parasagitales de la hoz, meningiomas de la convexidad y meningiomas esfenoidales.
Son más frecuentes en mujeres entre la cuarta y la sexta década de la vida, bajo influencia de factores hormonales.
La presentación clínica depende de la localización del tumor, los síntomas de inicio suelen ser insidiosos.
La OMS ofrece la clasificación con el objetivo de predecir las características clínicas, con un sistema de 3 grados basados en la correlación clínico patológico: meningioma benigno (grado 1 OMS), meningioma atípico (grado 2 OMS) y meningioma anaplásico, maligno (grado 3 OMS).
En los tumores primarios del SNC de hallazgo incidental, el tumor benigno más común es el meningioma, su detección incidental es más frecuente en personas mayores y de sexo femenino.
La TC es superior a la RM para evidenciar los efectos sobre el hueso adyacente, especialmente la destrucción ósea que puede aparecer en los meningiomas atípicos y malignos, o la hiperostosis asociada a los meningiomas benignos.
El meningioma típico muestra una masa hiperdensa de morfología hemisférica, redondeada o lobulada, de contornos bien definidos, que alcanza la superficie de la duramadre, que suele presentar un engrosamiento en la porción que contacta con el tumor (cola dural).
La angiografía convencional ya no constituye una prueba fundamental en el diagnóstico de los meningiomas intracraneales.
La resección neuroquirúrgica y el grado de la misma son el pilar del tratamiento y el predictor de progresión.
Hay factores específicos que son importantes a la hora de determinar el tratamiento óptimo de un meningioma, factores del paciente (edad, presencia o ausencia de síntomas, comorbilidades) y factores específicos del tumor (localización, tamaño, características histológicas del mismo).
Una resección completa, cuando es posible, está asociada significativamente con una sobrevida prolongada comparada con una resección parcial.
La incidencia de déficit neurológico postoperatorio varía entre el 2 y el 30%, y depende de la localización del tumor y de la extensión de la resección.
La radioterapia se recomienda en los meningiomas luego de una cirugía inicial (adyuvante), o como tratamiento único en los irresecables.
Una variedad de fármacos se ha utilizado para el tratamiento del meningioma, sin embargo, la mayoría de ellos han mostrado ninguna o muy poca actividad en su resolución.
La histología predice la mortalidad y la recurrencia; se han reportado tasas de recaída en el grado I de la OMS (benignos)/ II (atípicos)/ III (malignos) de 7, 40 y 80%, respectivamente. Los meningiomas que se presentan con invasión ósea muestran peores resultados en comparación con los tumores no invasores.
RECOMENDACIONES GENERALES
La terapia de los pacientes con meningioma debe ser individualizada debido a su diferente naturaleza y las posibles consecuencias de los diferentes tratamientos para ellos.
Es necesario realizar un seguimiento para evitar futuros déficits neurológicos potencialmente irreversibles y para encontrar el momento óptimo para una potencial reintervención.
El seguimiento clínico debe ser realizado por un neurocirujano o neurooncólogo y en casos especiales debe estar acompañado por especialistas adicionales, por ejemplo, si la función del nervio craneal está amenazada.
El tratamiento agudo y a largo plazo de los pacientes con meningioma es similar al tratamiento y manejo de pacientes con otros tumores intracraneales como los gliomas.
RECOMENDACIONES POR NIVEL DE ATENCIÓN
Primer nivel
Los síntomas más comunes son epilepsia, dolor de cabeza durante semanas a meses, síntomas específicos de la ubicación, debilidad unilateral, pérdida del campo visual, cambios en la personalidad o problemas del habla.
La exposición a la radiación ionizante está firmemente relacionada con un mayor riesgo de meningiomas y tienen más probabilidades de ser atípicos, malignos y multifocales.
Segundo nivel
Cuando se utilizan en combinación, la resonancia magnética cerebral (IRM) y la tomografía computarizada (TC) permiten el diagnóstico de meningioma intracraneal con una alta probabilidad.
Si un meningioma se diagnostica accidentalmente por neuroimagen, es necesario verificar si el hallazgo tiene correlación clínica, sí los síntomas o signos, en su caso, pueden ser resueltos mediante el tratamiento del tumor y si los beneficios potenciales del tratamiento superan los riesgos asociados.
La observación es una estrategia preferida en muchos casos de sospecha de meningioma, especialmente en tumores pequeños descubiertos de manera incidental.
Si un paciente rechaza la observación como estrategia de manejo (incluso después de proporcionarle una información completa), el tratamiento puede estar justificado.
Si se decide manejar un meningioma sospechoso por observación, se debe acordar quién es responsable del seguimiento del paciente. En un entorno ideal, esto lo realiza un neurocirujano o neurooncólogo.
CONSIDERACIONES FINALES
En el caso clínico analizado, la paciente cursó con deterioro visual progresivo acompañado de cefaleas, hipoacusia y pérdida del equilibrio, lo que sugiere la presencia de un meningioma de la fosa anterior que comprime el nervio óptico.
Se tiene en consideración que la paciente presentaba factores de riesgo para desarrollar este tipo de neoplasia, como es el hecho de ser mujer y su edad.
La paciente fue diagnosticada con un meningioma fibroso, que corresponde a un grado 1, clasificación de la OMS.
A la paciente se le realizó una resección de tumoración de forma parcial, dejando residuo hacia piso orbitario, por lo que corresponde a un grado 4 de la escala de Simpson.
CONCLUSIONES CONAMED
No se aprecian elementos de mala práctica médica atribuibles al personal médico, debido a que realizo una atención diligente y debida, fue hasta 18 meses después de la primera atención que presentó cuadro clínico que sugería una tumoración intracraneal, para lo cual se solicitaron los estudios de extensión para valorar el caso: El diagnóstico de meningioma fue establecido de manera oportuna 5 días después de que inicio la sintomatología, finalmente la paciente voluntariamente dio continuidad a su atención en otra institución en donde recibió el tratamiento quirúrgico que ameritaba.











 nueva página del texto (beta)
nueva página del texto (beta)