INTRODUCCIÓN
El gato doméstico (Felis eatus) tiene una larga y, en lo general, favorable historia de asociación con los humanos. Su aparición como animal doméstico en el antiguo Egipto, data del tercer milenio antes de Cristo1. Cuando en Asia se inició el cultivo y almacenamiento de granos y cereales, los gatos eran apreciados por sus habilidades predatorias, con las que podían controlar a las plagas que habitaban en los graneros, principalmente a los roedores2. En el continente americano, su aparición se cita en el inicio del siglo XVI, con la llegada de los españoles, quienes ya practicaban la costumbre árabe de criar gatos. Los peninsulares descubrieron que los gatos también eran muy útiles para salvaguardar bienes culturales como libros y pinturas, así como herramientas de trabajo1. En el México antiguo, los gatos estaban relacionados con divinidades, con lo místico y oculto, con el inframundo, y en Europa se les asociaba con las brujas y la hechicería. En la actualidad, los gatos son apreciados por su habilidad para proveer compañía, sobre todo en las ciudades cosmopolitas donde cada vez ganan más terreno como mascotas, ya que ocupan poco espacio, son muy limpios y sumamente independientes; incluso existen en la Ciudad de México (CDMX) cafeterías y restaurantes que son albergues temporales o permanentes de un gran número de gatos, como el café La Gatería, en la Colonia Roma, lo que pone de manifiesto la cada vez más estrecha relación entre el humano y los gatos. Pero a pesar de que los propietarios de los animales de compañía han adquirido más conciencia acerca del cuidado de éstos, existe aún un gran número de personas que no les ofreсеn a sus mascotas los cuidados necesarios para su bienestar; en consecuencia, se vuelven reservorios de enfermedades infecciosas que pueden ser transmitidas al humano ya sea por contacto directo o por otros mecanismos de transmisión, como es el caso de la toxoplasmosis (Figura 1).
La toxoplasmosis es una enfermedad parasitaria producida por el protozoário apicomplexa Toxoplasma gondii, que infecta mamíferos acuáticos, terrestres y aves. Es de distribución mundial y se estima que aproximadamente una tercera parte de la población humana se encuentra infectada. Este parásito induce una enfermedad crónica normalmente asintomàtica en individuos inmunocompetentes; sin embargo, en personas inmunocomprometidas, la toxoplasmosis puede tener consecuencias graves o fatales. Con el reciente aumento de individuos inmunocomprometidos, sobre todo por la enfermedad del VIH-SIDA, se reconoce a la toxoplasmosis como una de las enfermedades oportunistas más comunes en el mundo3.
En países desarrollados, la seroprevalencia de la toxoplasmosis humana se encuentra del 10 al 50%; en países en vías de desarrollo alcanza hasta un 80%, sobre todo en zonas tropicales. En México la prevalencia es del 15 al 50%, mayor en las zonas costeras del Golfo de México y del Pacífico, y mucho menor en las zonas áridas. En 2012 se determinó que la prevalencia nacional de la infección por T. gondii fue del 60% con hiperendemicidad en las costas e hipoendemicidad en las zonas centrales del país4.
GENERALIDADES DE LA TOXOPLASMOSIS
Fases parasitarias de Toxoplasma gondii
Toxoplasma gondii presenta diferentes fases parasitarías durante su ciclo biológico y todas son infectantes. Los ooquistes (Figura 2) son los estadios parasitarios que son eliminados únicamente en las heces de los félidos domésticos y silvestres, y es la forma parasitaria infectante más importante desde el punto de vista de transmisión del parásito. Son de forma oval y miden aproximadamente 10 X 12 pm. Esta fase parasitaria, cuando es eliminada por los félidos, no es infectante para el humano, ya que tiene que formar en su interior esporozoítos infectantes y para ello requieren permanecer en el ambiente durante aproximadamente 5 días5.
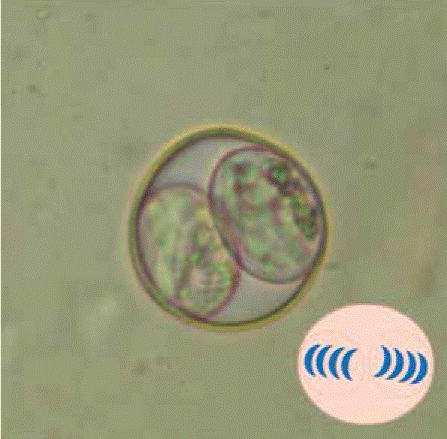
Foto: Juan Antonio Figueroa Castillo
Figura 2 Fotomicrografía tomada con objetivo 100x, ooquiste infectante esporulado de Toxoplasma gondii de forma oval y que contiene 2 esporoblastos con 4 esporozoítos cada uno. En el recuadro se aprecia una animación más clara de la morfología. Imagen: donada por Dr. Juan Antonio Figueroa Castillo, FMVZ, UNAM.
El taquizoíto es la fase infectante asexual y se caracteriza por su típica forma de arco o media luna, mide 3x7 pm (Figura 3). En su extremo apical posee estructuras involucradas en los procesos de motilidad, invasión y replicación. Carece de órganos de locomoción, sin embargo, se desplaza gracias a su motor de actina-miosina, y dentro de la célula hospedera forma una vacuola parasitófora dentro de la cual se divide exponencialmente5.

Foto: Norma Rivera Fernández
Figura 3 Fotomicrografía en contraste de fases que muestra una célula infectada con taquizoítos de la cepa RH de Toxoplasma gondii, esta cepa forma rosetas dentro de la vacuola parasitófora. Los taquizoítos tienen forma de media luna o gajos de naranja. Imagen: obtenida por la Dra. Norma Rivera Fernández en el Laboratorio de Patógenos Intracelulares, Departamento de Bioquímica del CINVESTAV Zacatenco.
Los bradizoítos son una forma parasitaria intracelular de poca motilidad, baja virulencia y lenta proliferación, los cuales transforman a la célula hospedera en un quiste tisular. Morfológicamente son similares a los taquizoítos, con la diferencia de que poseen abundantes granulos de amilopectina, el núcleo ubicado en la parte posterior y numerosos micronemos6.
El quiste tisular mide entre 50 y 70 μm y puede contener entre 1000 y 2000 bradizoítos (Figura 4). El tamaño del quiste depende tanto del tipo de la célula hospedera, como de la edad del quiste. En los tejidos del hospedero, los quistes inmaduros pueden llegar a medir hasta 5 μm y contener 2 bradizoítos en su interior6.

Foto: Norma Rivera Fernández
Figura 4 Fotomicrografía de un corte histológico sagital teñido con hematoxilina y eosina de un quiste tisular de T.gondii obtenido de cerebro de ratón infectado con la cepa ME49. Imagen: obtenida por la Dra. Norma Rivera Fernández, Laboratorio de Malariología, Departamento de Microbiología y Parasitología, Facultad de Medicina, UNAM.
Mecanismos de transmisión (Tabla 1)
a) Por el consumo de ooquistes infectantes que son eliminados con las heces de los gatos y distribuidos en el ambiente a través de la lluvia, el aire y el tránsito de vectores mecánicos como artrópodos, aves y pequeños mamíferos, que contaminan así el agua y la tierra. La ingesta de ooquistes se da cuando el individuo tiene contacto directo con tierra, como en las labores de jardinería, agricultura y la limpieza del arenero de los gatos sin utilizar guantes ni lavarse las manos después de concluir la tarea y por la ingesta de agua, frutas y verduras contaminadas.
b) Por el consumo o manipulación de carne cruda o mal cocida con quistes tisulares de T. gondii, principalmente carne de cordero, cerdo, cabra, oso y en menor proporción carne de res, caballo, conejo y aves.
c) Congénita. La infección del feto se da por la vía transplacentaria, y la afectación depende del tercio de la gestación en la que se infecte la madre.
d) Por trasplante de órganos, transfusión sanguínea e inoculación accidental en laboratorios.
Tabla 1 Mecanismos de infección por Toxoplasma gondii34
| Fase parasitaria | Mecanismos |
|---|---|
| Ooquistes | Ingesta de ooquistes en agua o alimentos contaminados o por no lavarse las manos después de tener contacto con tierra |
| Quistes tisulares | • Ingesta de carne cruda o semicruda, en especial
de cordero, cerdo, cabra y oso, y en menor medida de res,
caballo, conejo y aves • Trasplante de órganos |
| Taquizoítos | • Transplacentaria (toxoplasmosis congénita), por
transfusiones sanguíneas y trasplante de órganos • Los taquizoítos se han aislado de leche, saliva, esputo, orina, semen, lágrima y yemas de huevo, sin embargo, son sumamente lábiles a condiciones ambientales, por lo que la transmisión horizontal por los taquizoítos es poco frecuente. Existen reportes de transmisión por ingesta de leche de cabra no pasteurizada |
Ciclo biológico y patogenia
El ciclo biológico de T. gondii involucra a 2 tipos de hospederos: los definitivos, que incluyen a los félidos en quienes se desarrolla el ciclo sexual de reproducción, los intermediarios, como las aves y los mamíferos acuáticos y terrestres, en los cuales se lleva a cabo la reproducción asexual del parásito. El ciclo inicia cuando un hospedero definitivo, como el gato doméstico, ingiere presas como pájaros y ratones, entre otras, en cuyos tejidos se encuentran quistes tisulares que contienen bradizoítos, que son liberados a la luz intestinal por las enzimas digestivas del gato. Los bradizoítos invaden a los enterocitos intestinales y proliferan, diferenciándose en un macrogameto (célula femenina) y un microgameto (célula masculina). El microgameto posee un flagelo que le permite desplazarse sobre el epitelio intestinal para fecundar al macrogameto, lo que da origen a un cigoto. Este cigoto se transforma en un ooquiste que es liberado al ambiente con las heces del gato, contaminando así el agua y la tierra.
En condiciones de temperatura y humedad adecuadas, los ooquistes se vuelven infectantes aproximadamente 5 días después de haberse liberado con las heces y en su interior se forman 8 esporozoítos que, al ser ingeridos por un hospedero intermediario, inician una infección aguda. Los esporozoítos se transforman en taquizoítos dentro de cualquier célula nucleada del hospedero y proliferan rápidamente dentro de una vacuola parasitófora por un proceso asexual de división celular conocido como endodiogenia, por el cual se forman 2 parásitos de una célula madre. Los taquizoítos proliferan y atraviesan la lámina basal intestinal para iniciar su diseminación tisular por vía sanguínea o linfática у continuar con su replicación. Al saturar el espacio intravacuolar, los taquizoítos salen de la célula destruyéndola e invadiendo células vecinas. Durante la diseminación tisular del Toxoplasma, se activa el sistema inmune con la participación de diversas células efectoras incluyendo los linfocitos В con la consecutiva producción de anticuerpos, así como de linfocitos T y macrófagos que participan con acciones citotóxicas directas y mediante la secreción de citocinas tales como el interferon gama o el factor de necrosis tumoral y la producción de óxido nítrico.
Las citocinas mencionadas activan mecanismos moleculares no bien caracterizados, que resultan en la diferenciación de los taquizoítos en bradizoítos con la consecutiva transformación de la célula infectada en un quiste tisular. Estos quistes tisulares que contienen bradizoítos se localizan en todos los tejidos de los animales infectados y representan una forma de diseminación de la toxoplasmosis. Los quistes tisulares permanecen en forma latente hasta por varios años iniciando así una infección crónica en el hospedero.
En individuos inmunocomprometidos y crònicamente infectados con Toxoplasma, los bradizoítos salen del quiste tisular y se diferencian a taquizoítos, diseminándose por todo el organismo. Esta reactivación de los parásitos de un estado crónico a uno agudo se asocia con la migración de los taquizoítos a través de la barrera hematoencefálica hacia órganos como el cerebro, en donde se producen cuadros de encefalitis y posteriormente la muerte.
Cuando la infección con Toxoplasma ocurre durante la gestación, el parásito atraviesa la placenta e infecta al feto, y puede ocurrir alguno de los siguientes eventos: aborto, malformaciones, daños cerebrales, oculares y viscerales6. Las lesiones más frecuentes que pueden observarse en los tejidos con T. gondii son hidrocefalia, microcefalia, hepatoesplenomegalia, neumonía intersticial, miocarditis retinocoroiditis, necrosis, edema, vasculitis, granulomas. La tetrada clínica asociada, poco frecuente, incluye: hidrocefalia o microcefalia, retinocoroiditis y calcificaciones cerebrales bilaterales.
En el siguiente enlace se podrá observar el ciclo biológico de Toxoplasma gondii: http://www.ixtli.unam.mx/link/toxoplasma/, así como en la aplicación gratuita ToxoplasmApp, disponible en Google Playstore para teléfonos inteligentes con sistema operativo Android y en App Store para iPads con sistema operativo IOS.
Toxoplasmosis adquirida en hospedero inmunocompetente. Es asintomática en el 90% de los casos. El período de incubación es de 10 a 14 días. Se presenta inflamación de linfonodos cervicales y occipitales moderada, mal estado general, linfadenopatía supraclavicular e inguinal, fiebre moderada, odinofagia, cefalea y mialgias. En ocasiones se presenta anorexia, náusea, vómito y dolor abdominal. Podría encontrarse hepatoesplenomegalia, cuadro pulmonar o cardíaco, conjuntivitis y erupción cutánea. La toxoplasmosis aguda por lo general se autolimita al cabo de 3-4 semanas, pero hay cuadros crónicos con consecuencias importantes.
Toxoplasmosis adquirida en hospedero inmunocomprometido. Se manifiesta como una infección aguda generalizada con predilección por el sistema nervioso central, ojos, corazón, hígado y pulmones y en general por sitios donde la respuesta inmune es limitada; la infección conduce a lesiones como encefalitis, retinocoroiditis, pericarditis, derrame pericárdico, miocarditis, miositis, neumonía interstidal. En ocasiones se puede manifestar síndrome de Guillain-Barré. Los pacientes con alto riesgo son aquéllos con enfermedad de Hodgkin, los que reciben agentes inmunosupresores o corticosteroides y los pacientes con sida. Los pacientes presentan fiebre elevada, neumonía, erupción cutánea, hepatoesplenomegalia, miocarditis, miositis, orquitis.
Toxoplasmosis congénita. Transmisión vertical debida a infección en la madre durante la gestación, la cual puede ser por reactivación en una infección crónica en la que los bradizoítos presentes en los quistes tisulares revierten a taquizoítos por diferentes causas o por primoinfeción. El daño es más importante cuando la infección se presenta en el primer trimestre de la gestación. El sistema ventricular es el más afectado en el neonato, se presenta una obstrucción inflamatoria y en consecuencia hidrocefalia de los ventrículos tercero y lateral, calcificaciones y en los casos más severos destrucción del hipotálamo.
Toxoplasmosis ocular. La toxoplasmosis осular puede ocurrir en la mayoría de los casos como consecuencia de una toxoplasmosis congénita, sin embargo, puede adquirirse después del nacimiento. El cuadro clínico comprende diferentes signos y síntomas, desde dolor, fotofobia, lagrimeo, visión borrosa, hasta pérdida de la visión. El cuadro, por lo general, es poco específico.
Diagnóstico de laboratorio o gabinete
El diagnóstico se basa en gran medida en los resultados de pruebas serológicas que detecten anticuerpos específicos anti-T.gondii mediante técnicas de hemaglutinación, inmunofluorescencia, ELISA y Western blot. Se deben de detectar los anticuerpos de inmunoglobulina M (IgM) e inmunoglobulina A (IgA) (fase aguda), inmunoglobulina E (IgE) e inmunoglobulina G (IgG), así como determinar la avidez de IgG. La técnica de Sabin y Feldman es la prueba de referencia de IgG; se realiza en laboratorios de referencia, entre ellos los ubicados en los Centros para el Control y la Prevención de Enfermedades (CDC) y la Organización Mundial de la Salud (OMS), e implica la manipulación de parásitos vivos. Los estudios de gabinete utilizados son: radiografías, tomografía computarizada, resonancia magnética, ultrasonido y estudio oftalmológico. En pacientes inmunocomprometidos, con deficiencia inmune celular y humoral, se recomienda el empleo de la batería serológica, imagenología, histopatologia y PCR.
Tratamiento
No existen fármacos que destruyan a los quistes tisulares6. La mayoría de los pacientes inmunocompetentes con primoinfección no requieren de tratamiento, a menos de que exista compromiso visceral o manifestaciones clínicas persistentes.
Los fármacos de elección son espiramicina, ріrimetamina, sulfadiazina y ácido fólico, clindamicina, trimetoprima-sulfametoxazol.
EL PAPEL DEL GATO EN EL CICLO BIOLÓGICO DE TOXOPLASMA GONDII
Los gatos juegan un papel importante en el mantenimiento del ciclo biológico de T. gondii en la naturaleza porque son uno de los hospederos definitivos más comunes y en pocas ocasiones manifiestan un cuadro clínico consecuente a la infección por el parásito.
T. gondii realiza en sus hospederos una replicación asexual y una reproducción sexual. La reproducción sexual del ciclo únicamente se lleva a cabo en el intestino de los félidos y el resultado es la formación de ooquistes que son eliminados en las heces de estos y son resistentes a las condiciones ambientales.
La cantidad de ooquistes producidos por los gatos varía considerablemente, algunos eliminan de 3 hasta 10 millones y en ocasiones ninguno7. Los ooquistes de T. gondii puede permanecer viables varios meses en el suelo o en el agua, lo que aumenta la probabilidad de transmisión a los hospederos intermediarios que son las aves y los mamíferos en general. Los gatos eliminan ooquistes de T. gondii durante 3 a 5 días después de una primoinfección, que suele ocurrir la mayoría de las veces cuando son cachorros, y el periodo de eliminación puede durar aproximadamente de una a 3 semanas7.
La inmunidad que produce el parásito en el gato es excelente y parece ser de por vida, ya que en casos de reinfección la liberación de ooquistes es poco probable, al menos que el gato presente algún inmunocompromiso debido a diversos factores, como por ejemplo: desnutrición, terapia prolongada con dosis elevadas de corticosteroides, infecciones virales o infecciones severas con otros coccidios y en ocasiones, reinfecciones pasados 6 años o más después de la primoinfección8.
A pesar del corto periodo de latencia en el que los ooquistes son eliminados y de que la mayoría de los gatos los eliminan una sola vez en su vida, los gatos semidomésticos y ferales, quienes cazan para alimentarse y se reproducen continuamente, proveen una fuente inagotable de hospederos definitivos susceptibles a la infección por T. gondii que mantienen el ciclo del parásito en la naturaleza.
EL PAPEL DE LOS GATOS FERALES Y SEMIDOMÉSTICOS EN LA TRANSMISIÓN DE LA TOXOPLASMOSIS
Los gatos domésticos representan solo una pequeña parte del problema de la contaminación del medio con ooquistes de T. gondii. Existen extensas poblaciones de gatos sin propietarios que nunca o muy rara vez han tenido contacto con los humanos, por lo que no podrán socializar con ellos, a este grupo de gatos se les denomina ferales9. Por definición, los gatos ferales no pueden ser adoptados y pasarán la totalidad de sus vidas en el exterior. Los gatos semidomésticos son aquellos que alguna vez vivieron con los humanos pero fueron abandonados por sus propietarios o se extraviaron. Existe otra población de gatos semidomésticos que solo regresan a casa a dormir y se les permite en el día vivir en el exterior. Se estima que, de las poblaciones de gatos en zonas urbanas, el 36% son considerados animales en situación de calle. En Estados Unidos de América, se estima que existen alrededor de 40 millones de gatos ferales, lo que representa más del 50% de la población total de gatos de ese país2.
Los gatos ferales y los semidomésticos, son una fuente importante de suministro de ooquistes al medio y en consecuencia de reservorios silvestres y domésticos; por ejemplo, se ha comprobado que la seroprevalencia de T. gondii en cerdos, se eleva cuando aumenta la población de gatos jóvenes en los alrededores de las granjas10.
DISEMINACIÓN DE OOQUISTES DE TOXOPLASMA GONDII
Los insectos, lombrices e incluso roedores y aves actúan como vectores mecánicos que diseminan los ooquistes de Toxoplasma hacia lugares muy distantes del sitio original donde el gato los eliminó, contaminando así la tierra y el agua. Los brotes más severos de toxoplasmosis se han relacionado con beber agua contaminada con escorrentía11, como en el caso del brote de 1994 en la Columbia Británica de Canadá, en donde 100 individuos fueron diagnosticados con toxoplasmosis aguda y el mecanismo de transmisión fue la ingesta de agua de un reservorio contaminado con ooquistes12; los gatos defecaban en el reservorio de agua, y en consecuencia en la zona se había establecido un ciclo endémico de T. gondii entre la fauna local. Otro brote de toxoplasmosis aguda debido a la ingesta de agua contaminada con ooquistes ocurrió en Santa Isabel do Ivai, Brasil, en el año 200113. Estudios recientes han demostrado la presencia del parásito en moluscos bivalvos como las almejas, que sirven como hospederos paraténicos para los ooquistes14. En la nutria de mar Enhydra lutris nereis se ha reportado la presencia de T. gondii debido a la contaminación del agua con ooquistes del parásito15. La prevalência de toxoplasmosis en mamíferos marinos se debe a la contaminación de los mares con ooquistes provenientes de zonas costeras contaminadas con heces de gato16.
Los ooquistes de T. gondii permanecen viables en el agua dulce o de mar por varios meses y son resistentes al tratamiento con diversos medios fisicos y químicos, entre ellos al hipoclorito de sodio y el ozono, lo que deja abierta la posibilidad para que el agua de las ciudades sea un medio eficaz para la transmisión de la enfermedad a través de de ooquistes; únicamente la radiación con rayos ultravioleta, podría ser un método eficaz para la destrucción de los ooquistes en el agua17.
Como se mencionó con antelación, la tierra, además del agua, es otro reservorio de ooquistes de T. gondii. Varios estudios epidemiológicos han identificado como un factor de riesgo para contraer toxoplamsosis a las tareas desarrolladas con tierra como la jardinería o la agricultura y por la ingesta de frutas y verduras mal lavadas y regadas con aguas contaminadas. Cook et al. (2000)18 reportaron en un estudio realizado con mujeres gestantes, que aquellas con toxoplasmosis aguda tuvieron 2 veces más la probabilidad de haber adquirido la infección a través de la tierra en comparación con aquellas del grupo control no infectadas. Jones et al. (2005)19 demostraron que adultos y niños que trabajaban en jardines de Brasil eran 2.4 veces más propensos a ser diagnosticados con toxoplasmosis aguda en comparación con aquellos individuos que no tenían jardines. La mínima dosis oral infectante para desarrollar toxoplasmosis en humanos, cerdos y roedores es de un ooquiste7.
Desafortunadamente, la mayor parte de la población ignora que es mucho más probable adquirir toxoplasmosis a través de reservorios como el agua y la tierra, que por contacto directo con los gatos.
Otros mecanismos de transmisión para el humano se mencionan en la Tabla 1.
LA CONTAMINACIÓN DEL AMBIENTE POR OOQUISTES DE TOXOPLASMA GONDII
Existen pocas estimaciones reportadas relacionadas con la cantidad de heces que producen los gatos y cómo contaminan el ambiente. En San Francisco, Estados Unidos, se sabe que las heces de las mascotas son casi el 4% del total de la basura doméstica; los gatos generan aproximadamente 40 g de heces por día20, si se considera que existen aproximadamente 90 millones de gatos domésticos en Estados Unidos, se puede calcular que éstos producen alrededor de 1.2 a 1.3 millones de toneladas de heces al año2,lo que puede dar una cantidad de 193-774 ooquistes/m2;21 todos estos datos no son de utilidad si no se correlacionan con el porcentaje de gatos infectados con T. Gondii, y son muy pocos los estudios que se han publicado al respecto.
Afonso et al. (2006)22 reportaron un estudio en el que la incidencia anual de infecciones por T. gondii en una colonia de gatos ferales en Francia era del 0.17% por gato. Otro estudio realizado por Dabritz etai. (2007)23 en gatos domésticos, reportó una incidencia anual de infecciones por el parásito por gato del 0.04% y una seroprevalencia de 29.6%. Ruiz y Frenkel (1980)24 reportaron que aproximadamente 50% de los gatos cachorros (aquellos que pesan menos de 600 g o tienen aproximadamente 2 meses de edad), eliminaban ooquistes de T. gondii. En la década de los ochenta se estimó que, en América Central y Sudamérica, más del 80% de los gatos eran ferales o semidomésticos24. En 2008, la seroprevalencia de T. gondii reportada en gatos en la Ciudad de México fue de 21.8%25. En la Tabla 2 se puede observar la seroprevalencia de T. gondii en gatos en algunas ciudades del continente americano. La seroprevalencia en los humanos va del 3 al 64% en los países de Norteamérica, mientras que, en centro y Sudamérica, la seroprevalencia reportada es del 12 al 88%26.
Tabla 2 Seroprevalencia de T. gondii en gatos en algunas ciudades del continente americanoa
| Ciudad/país | Población | Número de gatos positivos/ evaluados | Método |
|---|---|---|---|
| San Pablo, Brasil28 | Pacientes en clínica veterinaria | 119/163 | Inmunofluorescencia indirecta |
| Bogotá, Colombia29 | Gatos abandonados | 52/170 | Aglutinación modificada |
| Ciudad de México, México30 | Gatos ferales | 4/6 | Fijación de complemento |
| Panamá, Panamá31 | Gatos semidomésticos | 110/241 | Aglutinación directa |
| Victoria, Canadá32 | Pacientes en clínica veterinaria | 16/63 | Aglutinación directa |
| British Columbia, Canadá32 | Gatos domésticos | 50/221 | Inmunofluorescencia indirecta |
| Florida, EUA33 | Gatos ferales | 49/533 | ELISA (IgG) |
| Illinois, EUA8 | Gatos de granja de cerdos | 223/295 | Aglutinación directa |
aAdaptado de Dabritz y Conrad, 2010.
Existen varios factores que dificultan el desarrollo de estudios epidemiológicos encaminados a reportar la incidencia de la infección por T. gondii en gatos, entre ellos se encuentran la poca sensibilidad de los métodos para la detección de los ooquistes en ellos23, además de que por microscopia de luz pueden confundirse fácilmente con los ooquistes de otros coccidios como Hammondia hammondi and Besnoitia darling27; hay dificultad para obtener muestras frescas de heces de gato de no más de 24 horas de haber sido eliminadas, sobre todo de los gatos semidomésticos a los que sus propietarios les permiten salir de casa la mayor parte del día y que son los que representan el mayor riesgo de transmisión.
¿CÓMO MINIMIZAR LA CONTAMINACIÓN DEL AMBIENTE POR OOQUISTES DE TOXOPLASMA GONDII!
Hasta ahora se ha mencionado el riesgo de adquirir toxoplasmosis por medio de la contaminación de agua y tierra con ooquistes; sin embargo, para los gatos el principal mecanismo de transmisión no es ésta, sino el carnivorismo, ya que las presas que cazan, en su mayoría, son portadores de quistes tisulares de T. gondii. Por este motivo, la principal medida de control contra la diseminación de ooquistes del parásito es evitar que los gatos domésticos deambulen libres en la calle y se alimenten de fauna peridoméstica.
En ausencia de métodos eficaces para detectar la presencia de ooquistes del parásito en la tierra y en el agua, las medidas de salud pública deben enfocarse a educar a los propietarios de los gatos y a la población en general. Medidas de higiene tan básicas como usar guantes desechables cuando se lleven a cabo tareas de jardinería o agricultura y el lavarse las manos después de tener contacto con tierra, podría prevenir un gran número de infecciones por T. gondii en el humano. Se les debe explicar a los propietarios de gatos domésticos, que al permitir que éstos salgan a la calle, están contribuyendo a la transmisión de T. gondii, sobre todo entre los gatos y los roedores, particularmente si los gatos defecan en el exterior2.
Se deben colectar las heces de los gatos de los areneros todos los días y lavar el arenero por lo menos 3 veces a la semana con jabón y agua hirviendo. Desafortunadamente en México, al igual que en otros países, no existen depósitos para colectar heces de mascotas e incinerarlas, por lo que su desecho debe de realizarse en drenajes cuyas aguas no serán utilizadas para riego de alimentos para consumo.
California, Estados Unidos, fue el primer estado en legislar la contaminación de aguas por T. gondii, la regulación requiere que los productores de arena para gatos incluyan en sus productos leyendas que instruyan a los propietarios a no desechar las heces del gato por los retretes. Los médicos veterinarios deben de insistir a los propietarios en castrar a los machos y ovariohisterectomizar a las hembras para evitar que se reproduzcan y terminen como animales en situación de calle, así como alimentarlos con productos comerciales de alta calidad para que no tengan que suplir nutrimentos cazando fuera del domicilio; es importante saber que los gatos comen en pequeñas cantidades, en promedio 15 veces al día, por lo que siempre deben tener libre acceso a su alimento.
Es fundamental que los propietarios conozcan el estado serológico para toxoplasmosis de sus gatos, ya que siempre será más seguro un gato que tiene anticuerpos que uno que no ha sido infectado por el parásito, en especial para las poblaciones en riesgo como pacientes con sida o algún otro inmunocompromiso, y mujeres gestantes o en edad reproductiva. Los gatos semidomésticos, incluidos aquellos que han sido abandonados por sus propietarios, deben ponerse en albergues para ser adoptados, las colonias de gatos ferales deben capturarse y trasladarse a reservas que estén lejos de parques públicos y de fuentes de agua para consumo humano. La producción de una vacuna para gatos resolvería en gran medida el problema de la contaminación del medio por ooquistes de T. gondii, sin embargo, hasta ahora solo se dispone de la vacuna Ovilis ® Toxvax para ganado ovino, que reduce principalmente el aborto y la mortalidad perinatal de los corderos causada por T. gondii.
CONCLUSIÓN
En conclusión, es muy poco probable que el humano adquiera toxoplasmosis por contacto el parásito una vez en su vida, por máximo 3 semanas y cuando son cachorros; sin embargo, existen situaciones de inmunocompromiso en las que los gatos pueden volver a eliminar ooquistes. Recordemos también que los ooquistes de T. gondii no son infectantes cuando son liberados en las heces de estos mamíferos, para que esto ocurra requieren de aproximadamente 5 días para esporular en el medio externo, por lo que una de las mejores medidas de control para disminuir el impacto ecológico que generan los ooquistes de T. gondii es el ser propietarios informados y responsables.











 nueva página del texto (beta)
nueva página del texto (beta)






