Introducción
El término obesidad se ha definido como un exceso de grasa corporal o tejido adiposo, y ha sido descrita y clasificada por gran cantidad de organizaciones. Se ha incrementado de manera exponencial a nivel mundial, y algunos autores la consideran una pandemia1.
La cirugía bariátrica es una rama de la medicina que se dedica al tratamiento de la obesidad y sus posibles comorbilidades a través de procedimientos quirúrgicos2),(3. El objetivo de este artículo es presentarle al lector con información completa sobre la manga gástrica, con base en su historia a lo largo de 20 años, su técnica y resultados actuales.
Origen
La primera cirugía bariátrica fue realizada en 1952 por el Dr. Viktor Henrikson de Göteborg, en Suecia4. El informe del Dr. Henrikson menciona haber realizado una resección de intestino delgado, y sólo especificó que fueron “105 cm de intestino delgado”5. El primer bypass gástrico fue realizado en 1954 por Kremen y Linner, fue hecho en animales para determinar la importancia metabólica de las diversas secciones de intestino y después proceder a realizar el bypass yeyuno-ileal en humanos6. En 1963 Payne y col. tomaron la idea de Kremen y Linner y crearon la técnica de shunt yeyuno-cólico, donde el tránsito alimenticio realiza un bypass total por una pequeña porción del yeyuno, todo el íleon y todo el colon ascendente. Esta técnica fue ampliamente descartada por sus múltiples efectos adversos como deshidratación, diarrea debilitante y desequilibrio electrolítico7.
Retomando las ideas de Henrikson, se le atribuye a Mason y col. ser los primeros en realizar de bypass gástrico en humanos en 1967. Su trabajo fue inspirado por observar una disminución de peso después de una gastrectomía para tratar úlceras gastrointestinales8. La existencia de estos efectos adversos de bypass yeyuno-ileal, motivó a Scopinaro y col. y abordaron la cirugía bariátrica de manera diferente: describieron una técnica llamada derivación biliopancreática en 1979.
Siguiendo los pasos de Kremen y Linner se realizaron primero procedimientos en animales y posteriormente en humanos9. Esta técnica fue modificada en 1993 por Marceau y col. donde se realizó una gastrectomía parietal, conservando la válvula pilórica y eliminando parte del fondo, cuerpo y antro del estómago a lo largo de la curvatura mayor; esto sería el componente restrictivo de derivación biliopancreática con switch duodenal10. Esta modificación representa el primer caso documentado de la manga gástrica, aunque aún sufriría una última modificación. Tomó el estatus como procedimiento únicamente restrictivo en la adaptación realizada por Johnston y col. la cual fue nombrada magenstrasse y mil11. En éste procedimiento se realiza una extirpación en forma circular en el centro del estómago y partiendo de ese punto se reseca hasta el ángulo de His, quedando semidividido el estómago de manera vertical, preservando el ámpula pilórica o mill con el propósito de conservar la habilidad para batir el alimento. También permanece una sección pequeña de estómago principal o magenstrasse que significa “avenida del estómago”, con la intención de producir un efecto restrictivo. La manga gástrica que se practica actualmente es una modificación de la técnica de magenstrasse y mill, la cual se describirá posteriormente. Fueron Baltasar y col. los primeros en proponer a la manga gástrica laparoscópica (MGL) como procedimiento bariátrico único, ya que observaron que en muchos casos no se necesitaba recurrir a una segunda fase quirúrgica porque se conseguía una disminución de peso importante utilizando MGL12.
Indicaciones
La MGL se puede realizar como un plan de un solo procedimiento o que preceda a una derivación biliopancreática con switch duodenal o bypass gástrico en Y de Roux (BGYR). Este esquema se hace para poder realizar una derivación biliopancreática con switch duodenal o BGYR de manera más sencilla ya que se cuente con menor panículo adiposo después de la MGL; adicionalmente disminuye la mortalidad en pacientes de alto riesgo (súper-súper obesidad, masculinos)12. Por lo tanto, una de las principales determinantes de las indicaciones es el grado de obesidad. Un panel de expertos con una experiencia colectiva de > 12,000 MGL concordaron con su indicación en pacientes con obesidad de índice de masa corporal (IMC) 30-35 kg/m2 con la justificación de comorbilidades ya determinadas (diabetes mellitus [DM], hipertensión arterial sistémica, dislipidemias, síndrome de apnea obstructiva del sueño, cáncer, etc)13. Esto difiere de la mayoría de instituciones y organizaciones que hasta el día de éste escrito sólo justifican la cirugía bariátrica con IMC ≥ 35 kg/m2 mas las comorbilidades mencionadas14. Las indicaciones para MGL están descritas en la Tabla 1.
Tabla 1 Indicaciones de diversas técnicas bariátricas
| Esquema de procedimiento | Circunstancias especiales |
|---|---|
| Procedimiento único | |
| IMC ≥ 35-40 kg/m2 | Con comorbilidades asociadas a la obesidad (DM, HTN, DL, SAOS, evento vascular cerebral, cardiopatía isquémica)26 |
| IMC > 40-50 kg/m2 | No hay necesidad de contar con comorbilidades pero se debe de tener historial de haber intentado bajar de peso con dieta convencional29,30 |
| Procedimiento inical | |
| IMC ≥ 35-40 kg/m2 | Con el propósito de conseguir disminución de peso antes de otros procedimientos no bariátricos (ortopédicos, trasplantes, etc.)24,30,3113-79 |
| IMC ≥ 50-60 kg/m2 (súper obesidad) | Se recomienda seguir con un segundo procedimiento como BGYR o DBP/SD4,23obstructive sleep apnea syndrome (OSAS |
| IMC ≥ 60 kg/m2 (súper-súper obesidad) | Se recomienda seguir con un segundo procedimiento como BGYR o DBP/SD4,23obstructive sleep apnea syndrome (OSAS |
BGYR: bypass gástrico en Y de Roux; DBP: derivación biliopacreática; DL: dislipidemia; DM: diabetes mellitus; IMC: índice de masa corporal; SAOS: síndrome de apnea obstructiva del sueño; SD: shunt duodenal.
Descripción del procedimiento
Se inicia anestesia general. El paciente en decúbito dorsal y en posición francesa. Asepsia y antisepsia de la región abdominal. Se procede a la colocación de 5 trocares (Figura 1).
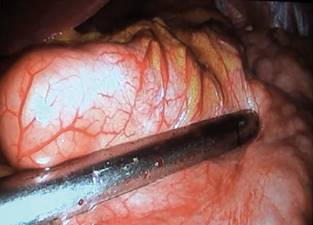
Una vez obtenido pneumoperitoneo a 12 mmHg se introduce cámara/lente de 30 grados y se realiza una inspección general de la cavidad abdominal. Se realiza tracción hepática y exposición de hiato esofágico mediante un separador hepático automático a través del trocar subxifoideo. Se identifica la válvula pilórica y ramas terminales del nervio de Latarjet. Se realiza la disección del ligamento gastrocólico con bisturí ultrasónico iniciando a 5-7 cm de la válvula pilórica para posteriormente entrar a la retrocavidad de los epiplones (Figura 2).
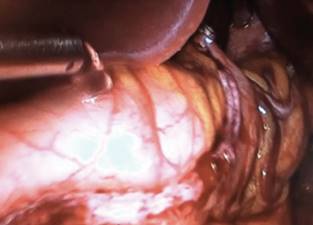
Continúa la disección con bisturí ultrasónico por toda la vascularidad de la curvatura mayor del estómago hasta alcanzar los vasos cortos y liberar de manera completa el ángulo de Hiz. Después, el anestesiólogo introduce una sonda orogástrica de 32 Fr, la cual se coloca de manera próxima a la curvatura menor hasta alcanzar la válvula pilórica. Inicia la resección gástrica de distal a proximal en forma vertical desde el inicio de la devascularización de la curvatura mayor hasta el ángulo de Hiz por fuera de la sonda de ferulización, con una engrapadora de 60 mm Ethicon Echelon® (Ethicon Endo-Surgery, Cincinnati, OH, USA) de cartuchos de diferentes grosores, adecuados a la conformación anatómica (verdes 60 × 4,1 mm, dorados 60 × 3,8 mm o azules 60 × 3,5 mm), hasta completar la resección (Figura 3).
Se extrae el estómago resecado. Posteriormente se realiza prueba hidroneumática, introduciendo 500 ml de solución salina a la cavidad abdominal hasta cubrir por completo el neoestomago. Se coloca una pinza de oclusión distal a la línea de grapado para solicitarle al anestesiólogo que insufle el mismo y poder observar burbujeo que pudiera corresponder a fuga de la línea de sutura. Se instila azul de metileno a través de la sonda para nuevamente corroborar hermeticidad del neoestómago (Figura 4).
Se corrobora la hemostasia del área quirúrgica, se retira la retracción hepática. Se coloca y fija un drenaje Jackson-Pratt® (Cardinal Health, McGaw Park, IL, USA, 19 Fr) con nylon de 2-0, revisando la hemostasia de sitios de acceso. Se sutura el tejido celular subcutáneo con catgut simple de 2-0. La piel se sutura con monocryl de 3-0 puntos subdérmicos.
Fisiología
En la MGL se inducen una disminución de peso por varios mecanismos. Se genera una reducción importante de la cámara gástrica y se disminuye la secreción de la hormona orexígena Ghrelina12. Primero examinaremos el componente restrictivo de esta cirugía. La ingesta de cierto volumen alimenticio produce una distensión de la pared estomacal, la cual induce una señalización neuronal procedente del nervio vago15, por lo tanto se necesitará un menor volumen de alimento para producir saciedad. El fondo gástrico funciona como reservorio de comida, y al rebasar su umbral envía el bolo alimenticio hacia el antro por peristalsis; al ser resecado el fondo, la función de reservorio recae en el remanente del antro. Este hecho, aunado a una falta de coordinación neuronal por resección de gran parte del estómago, parece crear una disrupción en el vaciamiento gástrico16. Otro mecanismo restrictivo que se debe considerar es el aumento de la presión intragástrica; esto pudiera ser el estímulo necesario para iniciar una descarga vagal, promoviendo saciedad y sustentando la teoría de un incremento de velocidad de vaciamiento gástrico17.
La ghrelina, hormona orexígena descubierta en 1999 por Kojima y cols., comprende otro mecanismo más por el cual se podría explicar la pérdida de peso observada en MGL18. Esta hormona es producida en su mayoría (65-90%) por células X/A de las glándulas oxínticas situadas principalmente en el fondo gástrico19. Aún no se comprenden por completo sus aspectos fisiológicos, esto se debe a la ubicuidad de los receptores de ghrelina (growth hormone secretagogue receptor), aunque se ha demostrado que la mayor cantidad de éstos receptores se encuentra en hipotálamo20. La función de ghrelina sobre la estimulación del apetito ha sido estudiada por varios autores y ha surgido gran interés por elucidar de manera completa el control neuroendocrino del apetito18. La teoría más aceptada sobre su fisiología es que actúa sobre los receptores de ghrelina en hipotálamo, incrementando la expresión de ácido ribonucleico mensajero (mRNA) y la subsecuente traducción de los neuropéptidos neuropéptido-Y y proteína r-agouti del núcleo arcuato. Es aquí donde se ejerce una acción que opone de manera directa otra adipoquina, la leptina21. La concentración plasmática de ghrelina normalmente aumenta previo a una comida, induciendo y amplificando el apetito; disminuye de manera enorme una vez que se llega a una sensación de saciedad19. Este aumento preprandial y supresión postprandial refuerza la teoría sobre su función orexigénica, incluso se ha correlacionado con una disminución proporcional al contenido calórico del alimento consumido22.
Otro mecanismo que explica una disminución de peso con MGL es la reducción de volumen de la cámara gástrica. Se han realizado varios estudios donde se ha demostrado que la distensión gástrica produce una sensación de saciedad en humanos23. Esta distensión inicia una cascada de activación sináptica que origina desde baroreceptores gástricos hacia el núcleo ventromedial viajando por axones del nervio vago24.
Complicaciones
Las complicaciones son inherentes a cualquier procedimiento quirúrgico y por lo tanto deben de ser considerados cuando se evalúa o considera una técnica, comparándola muchas veces con el “estándar de oro” es decir, con BGYR. Considerando a BGYR como el estándar de oro de cirugía bariátrica25, se compara cualquier procedimiento bariátrico contra éste. Desde el surgimiento de la MGL como procedimiento bariátrico único, muchos autores han realizado una comparación entre un grupo de pacientes que recibieron BGYR y otros MGL. Dentro de los puntos por los que ha surgido esta preferencia por la MGL sobre el BGYR están: la MGL es una técnica relativamente más fácil de realizar, preserva más estructuras y evita problemas relacionados con gastro-entero anastomosis.
Las complicaciones tempranas y tardías reportadas por algunos autores y algunas encontradas por nosotros se encuentran descritas en la Tabla 2.
Tabla 2 Complicaciones tempranas y tardías
GI: gastrointestinal; IVU: infección de las vías urinarias.
Tabla elaborada en parte con datos obtenidos de Vidal et al.71 más información obtenida de datos de nuestra clínica.
Vidal y cols.26 en 2012 se revisaron retrospectivamente 135 casos de BGYR y 114 de MGL; en éste estudio se encontró que la MGL se realiza en menor tiempo que BGYR (93 y 153 min respectivamente) y que las complicaciones menores (grado Clavien I y II)27 sucedieron en el 4,4% del grupo de MGL y 21,5% en el grupo de BGYR. En cuanto a complicaciones mayores (grado Clavien IIIa-V), se presentaron en el 4,4% de pacientes de MGL y en 5,9% de BGYR. El 3,5% de pacientes de MGL requirieron reintervención quirúrgica, en el grupo de BGYR el 4,4% la requirió. En otro estudio hecho por Lakdawala M. y cols.28 (2010) analizaron retrospectivamente 50 pacientes que recibieron MGL y 50 de BGYR; encontraron que ocurrió una complicación mayor que requirió de reintervención quirúrgica en un paciente con MGL y 2 complicaciones con BGYR.
Existen otros casos que reportan una menor tasa de complicaciones que las anteriormente mencionadas, como Lalor P. y cols.29 (2007), donde tuvieron 2,9% (4 de 148) de complicaciones con MGL.
En pacientes súper obesos (IMC 50-60 kg/m2) las tasa de complicaciones parece incrementar de manera importante. Esto se ha atribuido a varios factores: la dificultad de abordar quirúrgicamente a estos pacientes debido a su gran tamaño y el grado de comorbilidades que presentan al momento de ser intervenidos.
Resolución de comorbilidades
La obesidad cuenta con varias comorbilidades que ya fueron mencionadas, éstas son causa de enorme preocupación tanto médica como en el aspecto de salud pública30. En la fisiopatogenia más aceptada para la causa de obesidad y sus comorbilades radica un incremento en la secreción de proteínas por parte de los adipocitos (llamadas adipocinas o adipoquinas)31, por el efecto compresivo o el peso adicional que proporciona el tejido adiposo excesivo (hiperplasia de tejido adiposo), o por alguna combinación de estos 2 factores32. Debido a esto, se comenzó a cuantificar el impacto que tiene la reducción de comorbilidades y peso obtenida por la cirugía bariátrica versus tratamiento conservador33.
Aquí utilizaremos 2 términos diferentes: resolución y mejoría. Resolución es ausencia de una enfermedad o condición en una persona postcirugía bariátrica. Mejoría significa que ha disminuido la gravedad de la enfermedad o condición postcirugía bariátrica34.
La comorbilidad más importante es sin duda la DM. Desde que se llevó a cabo el comité de cirugía para diabetes en el 2008 se le ha atribuido a la cirugía bariátrica el estatus de “cirugía para diabetes” por su alta tasa de resolución y mejoría de DM35.
En varios estudios se hace énfasis en resolución de DM tipo 2, uno de ellos es el de Boza y Kehagias34),(36. Boza y cols. reportaron sus datos de 3 años de seguimiento, donde MGL causó remisión de DM tipo 2 en 90,9% de pacientes contra un 86,6% de BGYR34. Los pacientes de Kehagias y cols. también tuvieron 3 años de seguimiento y reportaron una remisión de DM tipo 2 igual para MGL y BGYR de 80%36. Dos estudios con seguimiento de 1 año mostraron también mayor resolución de DM tipo 2 con MGL que con BGYR: Nocca y cols. y Benedix y cols.37),(38 Nocca y cols. encontraron una resolución (de DM tipo 2) en MGL de 72% y en BGYR de 68,5%37. Benedix y cols. encontraron aún mayor diferencia, con una resolución de 83% con MGL y de 60% con BGYR38(Tabla 3).
Tabla 3 Resolución y mejoría de comorbilidades entre MGL, BGYR y BGA
| Estudio (Año) | Resolución de comorbilidades |
|---|---|
| Gentileschi P. (2012) (únicamente realizaron MGL) | Mejoría: Resolución: |
| Benedix F., et al. (2011) | |
| Nocca D., et al. (2011) |
BGA: banda gástrica ajustable; BGYR: bypass gástrico en Y de Roux; DM: diabetes mellitus; HAS: hipertensión arterial sistémica; MGL: manga gástrica laparoscópica; SAOS: síndrome de apnea obstructiva del sueño.
La hipertensión constituye otra comorbilidad que comparte lugar con DM tipo 2 como la comorbilidad más importante de la obesidad. Zhang y cols. muestran mayor resolución de hipertensión en el seguimiento de un año con MGL que BGYR con porcentajes de 37,8 y 25,8 respectivamente; sin embargo, se mostró menor mejoría de hipertensión con MGL que con BGYR con porcentajes de 22,5 y 23,5 respectivamente35.
Un estudio retrospectivo enorme realizado por Hutter M. y cols. consistió en información de 28,616 pacientes bariátricos39. De estos, sólo 944 fueron de MGL, 12,193 fueron de banda gástrica ajustable y 14,491 fueron BGYR. En este estudio, la resolución y mejoría de DM tipo 2 en MGL fue de 55% y en BGYR fue de 83%; la resolución y mejoría de hipertensión en MGL fue de 68% y en BGYR de 79%; la resolución y mejoría de dislipidemia en MGL fue de 35% y en BGYR fue de 66%; la resolución y mejoría de síndrome de apnea obstructiva del sueño en MGL fue de 62% y en BGYR fue de 66%. Tomando en cuenta la población diminuta de pacientes que pertenecieron al grupo de MGL (3,2% de la población del estudio contra un 50,6% que constituyeron los pacientes de BGYR) y que tuvo resultados sorprendentes que comparados con BGYR; parece indicar la posibilidad de mejor resolución o mejoría de comorbilidades con MGL si se realiza un estudio con poblaciones de cantidad similar.
Resultados
Dixon J.B. y cols. comentaron que no existe una manera estándar de reportar datos bariátricos; de tal manera que datos pre y postoperatorios se reporten con las mismas unidades: p. ej., IMC preoperatorio con porcentaje de exceso de IMC perdido40. Aunque en un escrito más reciente Rossi M. y cols. sugieren que el porcentaje de exceso de IMC perdido debe ser la medida estándar en pacientes bariátricos, ya que se correlaciona con una mejoría del síndrome metabólico41.
En cuanto a la eficacia de MGL frente a BGYR, Peterli R. y cols.42 publicaron un estudio clínico controlado aleatorizado realizado en el 2012 donde compararon MGL con BGYR y reportaron resultados a 12 meses. Encontraron un mayor porcentaje de exceso de índice de masa corporal perdido con BGYR al año después de la cirugía (con seguimiento de 100%); sin embargo en este estudio existieron ciertos sesgos. Uno fue que el grupo de MGL, que tenían menor IMC preoperatorio que los de BGYR y otro fue la diferencia de peso entre grupos, que fue bastante significativa: el grupo de MGL pesaba 120,2 ± 19,8 y el de BGYR 133,3 ± 30,8. Sin embargo en otros estudios controlados y aleatorizados muestran resultados a favor de MGL, esto se apoya con los hallazgos de Kehagias I., et al.36 (2011), otro estudio clínico aleatorizado donde se encontró un porcentaje estimado de peso perdido mayor en pacientes de MGL frente a BGYR. En este estudio ambos grupos contaban con un peso preoperatorio similar y se dieron resultados de hasta 3 años postoperatorios con un seguimiento reportado del 100%. Otro estudio que sostiene la premisa de mejores resultados con MGL que BGYR es de Karamankos S.N. y cols.43 (2008), donde encontraron un porcentaje estimado de peso perdido mayor en MGL en un seguimiento a 1 año (69,7 ± 14.6% contra 60,5 ± 10,7%). En un metaanálisis publicado en 2011 por Padwal R. Y cols.44 concluyeron que existe una mayor disminución de IMC en pacientes sometidos a MGL que en los sometidos a BGYR, −10,1 kg/m2 y −9,0 kg/m2 respectivamente. Algunos de los datos mencionados se encuentran representados en la Tabla 4.
Tabla 4 Resultados de MGL versus BGYR
| Estudio y año | Resultados |
|---|---|
| Kehagias I., et al. (2011) | |
| Karamanakos S.N., et al. (2008) | |
| Padwal R., et al. (2011) |
BGYR: bypass gástrico en Roux de Y; MGL: manga gástrica laparoscópica; PEPP: porcentaje de exceso de peso perdido.
Estos datos proporcionan una idea muy clara sobre la eficacia que se puede lograr con la MGL, especialmente cuando se compara con BGYR. La MGL es un procedimiento de menor dificultad técnica en su aplicación y con menor consecuencia metabólica debido a que no existe bypass; podría justificarse su preferencia de uso sobre el BGYR. Sin embargo, aún se necesita de una mayor cantidad de estudios donde se comparen estas 2 técnicas, con un mayor número de pacientes y a mayor plazo postoperatorio para que la MGL pueda desplazar por completo a BGYR como la técnica bariátrica estándar.











 text new page (beta)
text new page (beta)