Introducción
La esclerosis múltiple (EM) es una enfermedad neurológica desmielinizante de origen inmune-inflamatorio, que en los últimos años ha sido clasificada como crónico-degenerativa. Comprende una compleja interacción de factores ambientales tales como: el lugar de residencia (en adultos jóvenes) y la edad de exposición a ciertos virus como el Epstein Barr y la varicela zóster1),(2; estudios de genética han encontrado una asociación con 52 alelos de riesgo y una fuerte correlación con antígenos de histocompatibilidad DRB1 (HLA-DRB1)2.
En México las mujeres presentan EM con mayor frecuencia, la relación hombre-mujer es de 1:2. En los últimos años su prevalencia ha ido en aumento, y se conoce que varía según la latitud. En el norte del país es mucho mayor: en Chihuahua es de 12 por cada 100,000 habitantes; en Nuevo León, de 30 por cada 100,000, y en el Distrito Federal, de 10 por cada 100,0003. En personas de raza blanca la prevalencia es de 1 por cada 1000 habitantes, y se mantiene la afección en la relación hombre-mujer4.
La expectativa de vida disminuye en los pacientes con EM, en registros de Canadá se reduce de 4 a 7 años5, y en estudios de Dinamarca disminuye aún más: de 10 a 12 años6. La EM se presenta en un rango de edad de entre los 20 y los 40 años7),(8. Los altos costos directos e indirectos, solo en Estados Unidos, llegan a ser de cerca de 14 billones de dólares por año9.

Detalle de las lesiones de esclerosis múltiple en el tronco cerebral y la médula espinal, realizado por Robert Carswell en el año 1838.
En la EM y en la encefalomielitis autoinmune experimental (EAE) (esta última desarrollada en animales de experimentación) se han demostrado varios antígenos de la mielina: la proteína básica de la mielina, la proteína básica oligodendrocítica asociada a mielina, la glicoproteína de mielina de oligodendrocitos y los antígenos no mielina o astrocitarios como S100b y neurofilamentos, que son algunos de los antígenos blanco para autoanticuerpos y células del sistema inmunológico como macrófagos, interferón-g (IFN-g) e interleucina-17 (IL-17)10. Lo anterior se traduce en una lesión por pérdida de la integridad de la barrera hematoencéfalica y la afección a la sustancia blanca. Las lesiones de este sitio muchas veces no encuentran correlación con la discapacidad neurológica. Esta paradoja puede explicarse de cierta forma porque la lesión a la sustancia gris profunda es indetectable en la resonancia magnética (RM), que en estudios longitudinales se ha mostrado importante atrofia de la sustancia gris y se correlaciona con la discapacidad neurológica11. Al inicio de la enfermedad se presentan síntomas no neurológicos, principalmente dolor, fatiga, y posteriormente signos neurológicos, alteraciones sensitivas, dificultad para la movilidad, problemas de humor y afecto; en estadios avanzados o de recaídas frecuentes las alteraciones cognitivas ganan terreno, lo que se traduce en una gran incidencia de discapacidad por padecer EM12.
Los glucocorticoides son el tratamiento para las enfermedades autoinmunes con inflamación activa del sistema nervioso central, entre ellas la EM y la EAE en modelos animales10. Los bolos de metilprednisolona (MP) están indicados para las recaídas de la EM y se acompañan de una rápida reducción de la captación de gadolinio en las lesiones de EM, y los bolos de MP solos o con otros inmunomoduladores han sugerido beneficios para las recaídas, pero esto ha estado pobremente estudiados13. Las grandes dosis de esteroide no han mostrado mejoría respecto a dosis pequeñas. Se ha documentado que grandes dosis de metilprednisolona presentan un bajo número de efectos secundarios14. Los efectos secundarios que se han reportado son: infecciones menores, epilepsia, hiperglicemia, hipertensión arterial y hepatitis autoinmune15.
Por otro lado, la resonancia magnética nuclear (RM) es el método de diagnóstico más fiable, pero podría dejar pasar las lesiones por alto en un 15% de los casos16, aunque con las nuevas tecnologías, con resonadores más potentes y técnicas en la toma del estudio adecuadas, este porcentaje puede disminuir. Las lesiones son hiperintensas en las imágenes ponderadas en densidad protónica, para T2 y en las secuencias FLAIR17. Las lesiones ovoides suelen seguir el curso de las vénulas de la sustancia blanca periventricular, y se les denomina “dedos de Dawson”, lesiones que se visualizan hiperintensas en ponderación FLAIR y T218.
En el presente estudio proponemos que al regular las cascadas celulares inflamatorias que producen daño a la barrera hematoencefálica, a través del uso de bolos de metilprednisolona regular y haciendo de modo cada vez más espaciado, podríamos disminuir el daño inflamatorio, y por ende disminuir las lesiones a la barrera hematoencefálica, prevenir las recaídas y finalmente regular el daño neurológico a largo plazo con la muy probable remielinización de las zonas lesionadas.
Pacientes y métodos
Se estudiaron 16 pacientes del sexo femenino con EM, captadas por consulta externa de neurología en la Clínica de Neurotraumatología S.C. durante el periodo de enero del 1997 a enero 2011. De todos los casos estudiados solo se incluyó a las pacientes diagnosticadas que cumplen con los criterios diagnósticos de McDonald 2010 (National MS Society 2010). Todas las pacientes fueron sometidas a un protocolo estructurado de dosificación de tratamiento, que consiste en bolos de metilprednisolona; este procedimiento se realizó después de firmar el consentimiento informado, donde se hace énfasis sobre la existencia de otras alternativas de tratamiento con las que se ha demostrado mejoría, se informa que esos tratamientos existen en la atención privada y en instituciones de seguridad social, y que son tratamientos a los cuales nuestra población de estudio no tiene acceso.
Durante el estudio, se les realizó RM de encéfalo de manera inicial para complementar el diagnóstico de EM, y posteriormente cada año.
El tratamiento farmacológico presenta el siguiente protocolo: bolos de metilprednisolona de 1 g intravenoso, suministrados de la siguiente forma: en el día 1 (en el momento del diagnóstico), cada semana por 1 mes, cada 3 semanas por 3 meses, cada 4 semanas por 8 meses, cada 8 semanas por 12 meses, cada 12 semanas por 12 meses, y terminado este ciclo se da 1 bolo cada 6 meses de manera continua.
A los pacientes con comorbilidad de diabetes mellitus y alteraciones de la coagulación también se les brindó este tratamiento cuidando niveles de glucemia y tiempos de coagulación.
Resultados
Durante el periodo comprendido entre 1997 a 2011 se captaron a 16 pacientes del sexo femenino que se diagnosticaron según los criterios de McDonald en la Clínica de Neurotraumatología S.C.; la edad promedio de las pacientes fue de 33 años con un rango que va de 8 a 53 años. Cuatro de las pacientes presentan diabetes mellitus tipo 2, y 2 presentaban problemas de coagulación; ambas respondieron de forma satisfactoria al tratamiento y sin efectos secundarios.
En las valoraciones por imagen de resonancia magnética a las pacientes durante el tratamiento, se observó que al inicio presentaban grandes zonas de desmielinización, y al año de tratamiento con MP desaparecían pero no en su totalidad (figuras a1, a2 y a3), a los 3 y 5 años de tratamiento ya no se visualizaban las zonas de desmielinización en la sustancia blanca (figuras b1, b2, b3, c1, c2 y c3). A 10 años de tratamiento las lesiones de la sustancia blanca y gris cercanas a la corona radiada se han recuperado y la barrera hematoencefálica se encuentra íntegra, con una mínima actividad en sitios de la sustancia gris (figuras a1, a2 y a3).
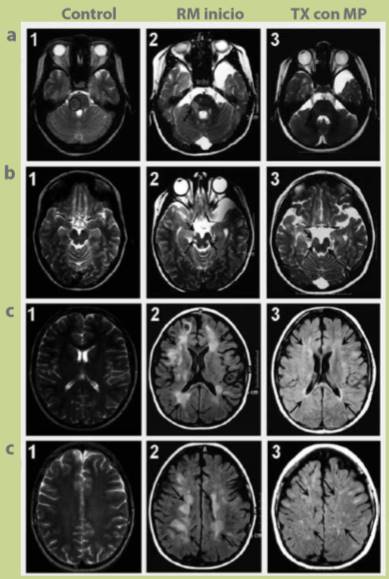
Foto: Contribución del autor
Figura 1 a1) Se muestran imágenes de cortes axiales de resonancia magnética en ponderación T2, de la región de la protuberancia y pedúnculo cerebeloso derecho. a2) Inicio del tratamiento; la imagen muestra lesiones con zonas grandes de desmielinización en la protuberancia y zonas periventriculares. a3) Imagen tomada un año después del tratamiento con metilprednisona; se observa que las lesiones tienden a desaparecer casi en su totalidad. b1) Se muestran cortes axiales de la región mesencefálica. b2) Al inicio de tratamiento presentaba lesiones hiperintensas en la zona peduncular derecha y tegmento del mismo lado, así como lesión tegmental izquierda. b3) Imagen tomada a los 3 años de tratamiento; se puede observar que en el mesencéfalo en las zonas antes descritas ya no se manifiesta lesión. c1) Se muestran cortes axiales de resonancia magnética en ponderación FLAIR, en región del núcleo caudado. c2) Al inicio de tratamiento muestra lesiones grandes hiperintensas de la sustancia blanca que van desde el lóbulo frontal hasta el lóbulo occipital y de predominio derecho. c3) Resonancia magnética a los 5 años de tratamiento se muestra una clara mejoría y recuperación de la barrera hematoencefálica. d1) Se presentan cortes axiales de resonancia magnética en ponderación FLAIR, región de la corona radiada. d2) Imagen de inicio de tratamiento se aprecian lesiones hiperintensas y grandes placas de desmielinización en la corona radiada, de predominio derecho. d3) Imagen tomada a los 10 años de tratamiento, podemos observar que se aprecia solo un pequeño número de lesiones hacia la sustancia gris y las lesiones de la sustancia blanca han desaparecido.
Conclusiones
Con el seguimiento, durante un largo periodo, de los resultados anteriores de RM principalmente en las ponderaciones T2 y FLAIR, por lo tanto, estudios de seguimiento en tiempo y espacio (criterios de MacDonald, 2010), mostramos que la barrera hematoencefálica mejora con los bolos de MP, debido a la exposición crónica y regular a éstos con dosis bajas e intervalos cada vez más amplios. Este argumento tiene fundamento al saber que al atenuar el sistema inmune de manera regular, aun cuando el paciente no tenga recaídas, logramos la estabilización de cascadas y factores proinflamatorios y con ello se da un menor índice de recaídas y un menor daño a largo plazo (principalmente cognitivo), lo que es muy válido para los pacientes donde la causa es la activación del sistema inmune; también vale la pena mencionar que las imágenes a 5 y 10 años no presentan atrofia corticosubcortical con espacio subaracnoideo conservado de manera adecuada, lo cual también es consistente con lo observado de manera perceptiva, el número de recaídas en nuestros pacientes es mínimo y no se presenta discapacidad, pues se encuentran efectuando actividades de la vida diaria.
Sabemos y reconocemos la importancia de otros fármacos, con los respectivos estudios que sustentan su eficacia, pero también para nosotros es tangible que no toda la población de México que padece EM es una población que tiene o tendrá acceso a estos medicamentos, y lo que mostramos es una alternativa para el tratamiento de una enfermedad inmuno-inflamatoria y crónico-degenerativa, en pacientes de estrato social bajo, con un costo mínimo y un beneficio máximo.
En este momento nos encontramos realizando, entre otros, estudios electrofisiológicos para fundamentar que no solo se repara la barrera hematoencefálica y por ende se modula el sistema inmune, sino que se produce una remielinización con la mejora resultante de la conducción axonal.











 nueva página del texto (beta)
nueva página del texto (beta)




