Publicado en el Boletín de Información Clínica Terapéutica de la ANMMa
ASPECTOS GENERALES
Dada la enorme frecuencia con la que un médico general atiende a mujeres embarazadas, el parto y el puerperio, y debido a que la trombosis venosa encefálica (TVEn) afecta con mayor frecuencia a este grupo específico de la población, consideramos de enorme interés, el que los médicos en general conozcan, tengan en mente y sospechen el diagnóstico con base en el cuadro clínico, en los antecedentes familiares y personales patológicos del paciente, así como en su contexto epidemiológico; evitando con ello, confundir un cuadro de trombosis venosa, con el de una enfermedad arterial cerebral, cuyo tratamiento, manejo y pronóstico con distintos.
Definición
Esta entidad fue descrita por primera vez a principios del siglo XX como un proceso infeccioso del seno sagital superior, que provocaba déficit motor, crisis convulsivas, estado de coma y, finalmente, en una inmensa mayoría de los casos, la muerte; sin embargo, con los grandes avances tecnológicos y científicos de las últimas décadas, se ha logrado determinar que el proceso no es desencadenado por una infección, sino por la obstrucción al drenaje de las venas intracraneales y de los senos venosos del SNC, desencadenando incremento en la presión endocraneana, edema vasogénico e infartos venosos hemorrágicos. De tal manera que en la actualidad, a la TVEn se la considera como una entidad no infecciosa, que da lugar a distintas manifestaciones clínicas, cuya mortalidad disminuye cuando el diagnóstico se establece en las etapas más tempranas de la enfermedad.
Epidemiología
No obstante que la TVEn también conocida como trombosis venosa cerebral puerperal es una entidad nosológica poco frecuente, representa entre el 15 y el 20% de los infartos cerebrales que se presentan durante la juventud, afectando especialmente a mujeres durante el embarazo y el puerperio; su tasa anual es de 3 a 4 por cada millón de habitantes y su mortalidad general es del 5 al 30%. Es más frecuente en la edad adulta y en el sexo femenino con una proporción de 3:1, considerando que durante el embarazo y el puerperio, el 50% de los casos de enfermedad vascular cerebral (EVC), tiene su origen en el territorio venoso.
En raras ocasiones se presenta en la población infantil, en especial durante el período perinatal, con una tasa aproximada de 0.67 casos por cada 100 000 habitantes por año; sin embargo, en los neonatos esta tasa llega a ser hasta de 2.6 casos por cada 100 000 habitantes por año, con una mortalidad menor al 10%; desafortunadamente, un 17 a un 79% de los casos en pediatría, presentan secuelas neurológicas que abarcan desde alteraciones motoras hasta problemas de naturaleza cognitiva.
Etiología
Se han descrito una serie de factores de riesgo para el desarrollo de trombosis venosa, de la misma manera como sucede con la trombosis arterial, algunos de ellos comunes para ambas entidades nosológicas. La edad por ejemplo, es un factor de riesgo directamente proporcional para el desarrollo tanto de trombosis venosa como arterial; la circunferencia abdominal superior a los 100 cm, es otro factor de riesgo para el desarrollo de ambas entidades; mientras que en la mujer la obesidad, el tabaquismo y la hipertensión, son factores predictivos independientes del tromboembolismo pulmonar. La hipertrigliceridemia durante la posmenopausia en cambio, duplica el riesgo de tromboembolismo venoso. De la misma manera, el síndrome metabólico, la diabetes mellitus, las hiperlipidemias en general y la hiperglicemia son factores de riesgo para el desarrollo de trombosis venosa profunda de origen desconocido. Otros factores predisponentes son los trastornos hemorreológicos durante el embarazo; el uso de anticonceptivos, la hiperglobulia, la deshidratación, el síndrome de plaquetas pegajosas (autosómico dominante) y los trastornos de la coagulación.
Por otro lado, existen una serie de factores de naturaleza molecular que son los que realmente propician el desarrollo de la trombosis venosa, como el incremento en los niveles del factor von Willebrand y de los factores VII, VIII y X de la coagulación, así como del fibrinógeno y de la proteína C; el déficit de antirombina III, o bien, la presencia de la mutación G20210A del factor V de Leiden y la protrombina; mientras que la hiperhomocisteinema y la mutación C677T del gen de la metilentetrahidrofolato reductasa, se pueden considerar como factores etiológicos entre el 27 y el 43% de los casos. No obstante lo señalado con anterioridad, en un 25% de los pacientes no se logra establecer el diagnóstico etiológico, catalogándose al proceso como idiopático.
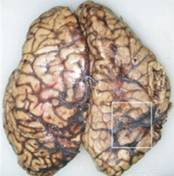
Patología
Sólo ocasionalmente se detecta hidrocefalia, a pesar del bloqueo en la reabsorción del fluido periencefálico, mientras que invariablemente se desarrolla edema cerebral intersticial. Se puede demostrar la aparición de coágulos localizados tanto en las venas cerebrales como en los senos venosos, con edema de la pared vascular y en la región perivascular intersticial. Además, hay infiltración intersticial de células sanguíneas y extravasación del tejido hemático; aunque también puede aparecer edema citotóxico con petequias que en ocasiones, producen enormes hematomas intra y extraparenquimatosos. El proceso anterior culmina con el bloqueo al libre flujo sanguíneo capilar, desencadenando infarto del tejido nervio localizado en la zona circunvecina al sistema venoso afectado.
MECANISMOS DE PRODUCCIÓN DE LA ENFERMEDAD
Las venas encefálicas se agrupan en un sistema venoso superficial que comprende a los senos sagitales y a las venas corticales que drenan la superficie de la corteza cerebral de ambos hemisferios y en sistema venoso profundo, que abarca a los senos lateral, recto y sigmoideo, permitiendo el drenaje de las venas corticales profundas. Ambas redes venosas desembocan en las venas yugulares que confluyen en la gran vena yugular interna.
Sobre este sistema venoso, ejerce una enorme influencia la función de dos grandes familias de moléculas de adhesión: 1. Las selectinas, que juegan un papel preponderante en el desarrollo de la TVEn mediante sus moléculas endotelial (E), plaquetaria (P) y leucocitaria (L); y 2. Las integrinas, que intervienen en la transducción de la señal transmembrana al encontrarse unidas a las proteínas del citoesqueleto. Cuando las selectinas se activan por diversos mecanismos durante el proceso inicial de la TVEn, se alteran los sistemas reológicos al adherirse los elementos formes de las sangre venosa entre sí, provocando flujos turbulentos y la adherencia incluso, de la pared venosa, colapsando el sistema de drenaje.
De la misma manera, los síndromes de hiperviscosidad, así como los estados de hipercoagulabilidad, están relacionados con la activación de las moléculas de adhesión y las proteínas de la coagulación. Sin embargo, curiosamente los mecanismos de la coagulación de la sangre en el sistema venoso difieren en algunos aspectos con relación al fenómeno que se presenta en el sistema arterial. Es en esta forma como la activación de las plaquetas en los ductos venosos pasa a un terreno secundario, mientras que las moléculas de adhesión y el factor X de la coagulación, adquieren una función preponderante en este sector de la circulación.
Finalmente, las alteraciones hemodinámicas que se presentan repercuten, en este caso, más que en el aporte de nutrientes a los tejidos, en el drenaje de los productos residuales de su metabolismo, cuya acumulación puede llegar a producir efectos tóxicos lo suficientemente severos, como para alterar el funcionamiento neuronal, actuar como un factor epigenético e inducir, finalmente, la muerte celular o bien desencadenar un estado apoptótico.
Cuando las células de epitelio alto que forman parte de la pared endotelial del sistema venoso encefálico expresan sobre su superficie a las moléculas de adhesión que las caracterizan, lentifican o detienen la migración de los granulocitos y contribuyen con la activación de algunos de los factores de la coagulación, como es el caso del factor X, promoviendo la formación de trombina y con ello, la aparición de coágulos sobre la superficie fosfolipídica de las células endoteliales. La obstrucción parcial o total que este fenómeno desencadena dentro del sistema venoso principia, por un lado, a reactivar los mecanismos que le dieron origen, perpetuando el evento fisiopatológico y por el otro, facilita que el contenido líquido comience a acumularse por detrás del sitio obstruido, distendiendo las pared venosa como resultado del incremento en la presión intravascular del vaso afectado. La presión hidrostática se eleva rápidamente y el contenido líquido de la sangre infiltra el intersticio de la pared, por lo que dependiendo de las presiones osmótica y oncótica que actúan entre el interior de las células de la pared venosa y su intersticio, estas células se deshidratan o se edematizan, contribuyendo en este último caso, a agravar el proceso obstructivo.
Inicialmente se internalizan las moléculas de adhesión y se activa el plasminógeno; mecanismos que tienden a contrarrestar la obstrucción de la luz del vaso sanguíneo, pero cuando las fuerzas se inclinan hacia la progresión de la obstrucción, el edema de la pared se acentúa y se inicia la extravasación de su contenido, incrementando paulatinamente la presión hidrostática del intersticio que rodea a los vasos sanguíneos en la región afectada. Este fenómeno tiende, a su vez, a vencer la presión intravenosa y obliterar a los vasos circundantes, tanto capilares venosos como arteriales. Las consecuencias son múltiples y de enorme gravedad. La presión parcial de CO2 tiende a aumentar, los ácidos pirúvico y láctico se acumulan, se comienzan a formar cuerpos cetónicos y acetaldehído, se generan moléculas inestables como radicales de distinto origen, se activa la â-oxidación y el pH local tiende a disminuir incrementando la permeabilidad de la membrana de las células que forman parte del tejido circundante. En estas circunstancias, se origina eflujo celular de K+ e influjo de Na+, lo que provoca despolarización de la membrana. Posteriormente, los cationes divalentes de Ca++ comienzan a fluir hacia el interior de la célula, alterando la función de la membrana mitocondrial tanto interna como externa, por lo que al no llevarse a cabo de una manera sistemática la fosforilación oxidativa disminuye el aporte de ATP para la función celular, perdiéndose la capacidad de la membrana para contener el protoplasma y sus organelos, cesando en este momento la función celular. En estas circunstancias, la lesión tisular permite que el tejido hemático abandone la luz de los vasos sanguíneos, infiltrando y produciendo enormes hematomas.
PRINCIPALES CARACTERÍSTICAS CLÍNICAS
El diagnóstico clínico de esta entidad nosológica, cuando no se sospecha con base en su epidemiología y factores de riesgo, es realmente difícil, dado que su presentación clínica es extremadamente variable. Sus manifestaciones pueden modificarse con la edad del paciente, el tiempo transcurrido entre el inicio del cuadro clínico y su admisión al hospital, la localización encefálica del fenómeno trombótico y la presencia o ausencia de lesión parenquimatosa; sin embargo, los signos y síntomas a los que con mayor frecuencia se enfrenta el clínico son dolor de cabeza, crisis convulsivas, diversos grados de déficit neurológico focalizado, alteraciones en la conciencia y edema de papila, ya sea en combinación o en forma aislada. De hecho, se han descrito cuatro grandes grupos de pacientes, considerando que el inicio del cuadro clínico puede ser agudo, subagudo e incluso crónico:
1. Hipertensión endocraneana aislada
Frecuentemente se presenta en casos subagudos, pero puede manifestarse en casos agudos. La cefalea ocurre en el 90% de los casos con TVEn y en un 64% se describe como subaguda, la que al exacerbarse con la maniobra de Valsalva o con los cambios de posición de la cabeza y asociase con alteraciones visuales y edema de papila, obliga al clínico a estudiarla de manera más profunda.
2. Alteraciones neurológicas focalizadas
Debilidad muscular e incluso hemiparesia y afasia son signos que suelen presentarse hasta en el 44% de los casos, mientras que difícilmente se manifiestan alteraciones sensitivas.
FUNDAMENTO DIAGNÓSTICO Y MANEJO TERAPÉUTICO
Ante la sospecha de un proceso de esta naturaleza, con base en los datos epidemiológicos, los antecedentes familiares y el cuadro clínico del paciente, el caso debe ser enviado de inmediato para su diagnóstico y tratamiento a un hospital que cuente con un nivel tecnológico adecuado y especialistas expertos en la materia.
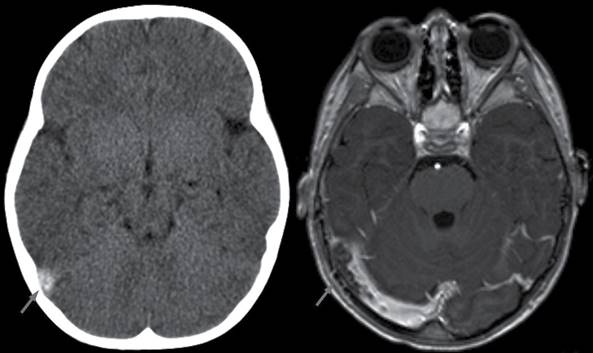
El estudio diagnóstico específico es la imagen por resonancia magnética asociada a la venografía por tomografía computarizada. Una vez confirmado el diagnóstico, el tratamiento de elección es la anticoagulación, ya sea con heparina no fraccionada, o bien con heparinas de bajo peso molecular, para posteriormente iniciar manejo con anticoagulantes orales como la warfarina y el rivaroxaban.
Solo se debe insistir que en estos casos el uso de antiagregantes plaquetarios como la aspirina, el clopidogrel, el ticagrelor y otros, carece de justificación, por lo que ante el riesgo de los efectos colaterales que pueden producir, se encuentran relativamente contraindicados. Otras terapias, como la fibrinolisis y el cateterismo con la extracción del trombo, aún no han sido lo suficientemente valoradas. El papel de la cirugía, en cambio, es de gran valor, sobre todo ante las grandes hemorragias encefálicas.











 nueva página del texto (beta)
nueva página del texto (beta)