Introducción
La sepsis es un síndrome complejo y devastador. Continúa siendo una causa importante de morbilidad y mortalidad entre los pacientes críticamente enfermos. La aparición de la sepsis y el choque séptico ha tenido un incremento significativo en las últimas dos décadas. Pese al desarrollo de la investigación básica dedicada al tema y a numerosos ensayos clínicos, no se han logrado avances notables en el desarrollo de terapias vanguardistas y eficaces para su manejo. Los trastornos fisiológicos inducidos por la sepsis son en gran parte debidos a la respuesta del huésped a los microorganismos invasores en contraste con los efectos directos del propio microorganismo.
La sepsis, entendida como la respuesta inflamatoria sistémica a la infección, está marcada por la producción desregulada de citocinas proinflamatorias. Pese a que normalmente la producción de éstas es indispensable para proteger contra los patógenos y promover la reparación de los tejidos, su producción desregulada y prolongada puede desencadenar una cascada inflamatoria sistémica mediada por quimiocinas, aminas vasoactivas, el sistema del complemento, de la coagulación y especies reactivas de oxígeno, entre otros. Estos mediadores conducen de manera colectiva a la insuficiencia orgánica múltiple, y en última instancia, a la muerte. Es en este sentido que el papel de la inflamación en la fisiopatogenia de la sepsis, aunque todavía no entendida completamente, resulta claramente crítico.
Antecedentes
El empleo original de la palabra “sepsis” (procedente del vocablo griego sepo que significa descomposición o putrefacción) fue utilizado para describir la descomposición de la materia orgánica que de alguna manera daba lugar a la decadencia o muerte de un ser vivo1. En el modelo hipocrático de salud y enfermedad, los tejidos vivos se “descomponen” por una de las 2 vías descritas: pepsis es el proceso a través del cual los alimentos ingeridos son digeridos promoviendo la salud del organismo, y sepsis, que denota la descomposición de los tejidos como producto de una enfermedad. Hipócrates utilizó este término para describir el proceso anormal de descomposición de los tejidos que da lugar a la fetidez, formación de pus y, en ocasiones, la muerte2,3.
Estado actual
Actualmente entendemos por sepsis al desequilibrio causado por la respuesta sistémica del organismo a la invasión de tejidos normalmente estériles por agentes patógenos o potencialmente patógenos. El estado de choque mediado por sepsis es definido como la condición en la cual la reducción profunda y generalizada de la perfusión tisular eficaz conduce de manera inicial a lesión celular potencialmente reversible, que luego de ser prolongada la injuria, el daño celular resulta irreversible4.
La sepsis grave y el choque séptico son el resultado de la compleja interacción entre los microorganismos infecciosos y elementos de la respuesta inmunológica del huésped, que da como resultado una inadecuada respuesta inmunológica del hospedador.
Fisiopatología de la sepsis grave y choque séptico
El punto clave que describe la cascada de eventos fisiopatológicos que caracterizan a la sepsis grave o choque séptico en cualquier punto de su fase evolutiva es el “desequilibrio” entre la respuesta del huésped y la intensidad del estímulo por parte del patógeno, lo que condiciona la disfunción y falla orgánica con o sin hipotensión arterial. Este “desequilibrio” da como resultado, entre otras alteraciones, el desarrollo de un patrón inmunológico de características predominantemente proinflamatorias, mixtas e inclusive antiinflamatorias, siendo el comportamiento de este perfil en muchas ocasiones de carácter dinámico.
La sepsis se caracteriza por una respuesta inflamatoria sistémica mediada por células de la inmunidad innata en la que se incluyen a los neutrófilos, monocitos y macrófagos. La producción de citocinas proinflamatorias como el factor de necrosis tumoral alfa (TNF-α), interleucina-1 (IL-1), Interleucina-6 (IL-6) e Interleucina-8 (IL-8), normalmente desencadenan una respuesta inmune innata eficaz para limitar la infección y el daño tisular. Sin embargo, en la sepsis la excesiva y prolongada producción de estas citocinas puede provocar una respuesta inflamatoria exagerada y aún más dañina que la infección original. Esta teoría es especialmente visible en la sepsis grave y el choque séptico, en donde la producción excesiva de citocinas proinflamatorias causa disfunción microvascular, daño tisular y falla orgánica múltiple5-7.
Se ha demostrado que la elevación de los niveles de citocinas proinflamatorias se relaciona directamente con la gravedad y mortalidad en la sepsis8,9.
El rol crítico de las citocinas proinflamatorias ha sido estudiado y demostrado en la fisiopatogenia de la sepsis. Dichas citocinas contribuyen al desarrollo de la respuesta de fase aguda manifestada como fiebre leucocitosis, alteraciones en el metabolismo de la glucosa a nivel muscular, así como la activación del complemento y de la cascada de la coagulación10. La elevación persistente de estas citocinas provoca una variedad de fenómenos patológicos, dentro de los que se incluyen modificaciones del endotelio vascular para la síntesis y expresión de moléculas de adhesión, activación de neutrófilos, síntesis de productos de la ciclo-oxigenasa, generación de óxido nítrico, especies reactivas de oxígeno e inducción de hipotensión arterial11-15. Además, las citocinas proinflamatorias pueden incrementar la expresión de mediadores inflamatorios por contraregulación positiva y en consecuencia inducir al desarrollo de otros fenómenos perjudiciales16.
Disfunción inmunoinflamatoria del choque séptico
Aunque el desequilibrio de los eventos que conducen al choque séptico implican múltiples sistemas biológicos, la respuesta inmunitaria sigue siendo fundamental para su desarrollo.
El sistema inmunitario incluye un componente estructural constituido por las barreras mucosas, una respuesta inmunitaria temprana no específica y una respuesta inmunitaria patógeno-específica tardía. El funcionamiento del sistema inmunitario normal requiere de la acción coordinada de todos estos componentes lo que resulta en el reconocimiento temprano de un patógeno potencial y su posterior eliminación con el mínimo daño tisular posible o interrupción de los procesos fisiológicos del hospedador.
El sistema inmunitario innato debe ser capaz de reconocer a los patógenos invasores de manera inmediata y ser capaz de montar una respuesta de intensidad suficiente para contener la amenaza. Además, esta respuesta inespecífica debe ser capaz de proteger a los tejidos del hospedador y favorecer su reparación.
La respuesta adaptativa se encarga de “afinar” los aspectos posteriores de la respuesta inmunitaria. Este “ajuste fino” se encarga de asegurar que, ante cualquier estímulo dado, la respuesta inmunitaria sea “específica” y “mesurada”.
Para entender el grado de disfunción en el hospedador y, por lo tanto, la fisiopatogenia del choque séptico, se deben valorar ciertos aspectos y características de la respuesta inmunitaria normal del huésped ante la infección.
La respuesta inmunitaria normal puede ser caracterizada como una fase inicialmente no específica y altamente proinflamatoria, con una respuesta antiinflamatoria compensatoria posterior, necesaria para restaurar la homeostasis inmunológica previniendo con esto la lesión hacia los tejidos sanos del hospedador.
La respuesta inmunitaria a un patógeno dado en un individuo determinado está dada por la interacción de muchos factores dentro de los que destacan pero que no quedan limitados a éstos, la virulencia de los patógenos, la composición genética del individuo y sus comorbilidades preexistentes.
Posterior a la activación de la respuesta inmunitaria desencadenada por un patógeno invasor, su gravedad depende del grado en que se expresa el sistema inmunitaria innato, que a su vez dependerá de factores genéticos y adquiridos. La respuesta fisiológica a la infección en curso, en relación a las comorbilidades preexistentes en el hospedador, difiere de la respuesta en el huésped por lo demás sano.
Sistema de reconocimiento del patógeno en sepsis
El evento inicial de la respuesta inmunitaria innata es el reconocimiento del patógeno invasor como una amenaza. Las bacterias y los virus tienen estructuras moleculares que no comparten con el hospedador, y son comunes e invariables entre los patógenos. Estos patrones moleculares también son expresados por bacterias no patógenas y comensales y, de acuerdo con el contexto, pueden ser denominados como patrones moleculares asociados a patógenos (PMAP) o patrones moleculares asociados a microbios (PMAM)17. Desde el punto de vista funcional, los equivalentes endógenos a estos PMAP son proteínas intracelulares expresadas o liberadas posteriores a la lesión de los tejidos del hospedador. Estas proteínas se conocen como alarminas y, junto con los PMAM se conocen como patrones moleculares asociados a daño (PMAD)18. Las células inmunes expresan un conjunto de receptores denominados receptores de reconocimiento de patrones (RRP) los cuales reconocen y se unen a los PMAD expresados en los patógenos invasores y tejidos lesionados del hospedador. Al menos 4 familias de RRP son reconocidos: los receptores de tipo Toll (TLR), nucleótido de oligomerización con dominio rico en leucina con repetición de proteínas (NOD-LRR), caspasa citoplasmática de activación y reclutamiento con dominio de helicasa como el gen inducible de ácido retinóico I (RIG-I) de tipo helicasa (RLH), y el receptor de lecitina tipo C expresado en células dendríticas y mieloides19,20. Estos receptores inician la respuesta por parte de la inmunidad innata y regulan la respuesta inmunitaria adaptativa contra la infección o lesión tisular (figura 1).
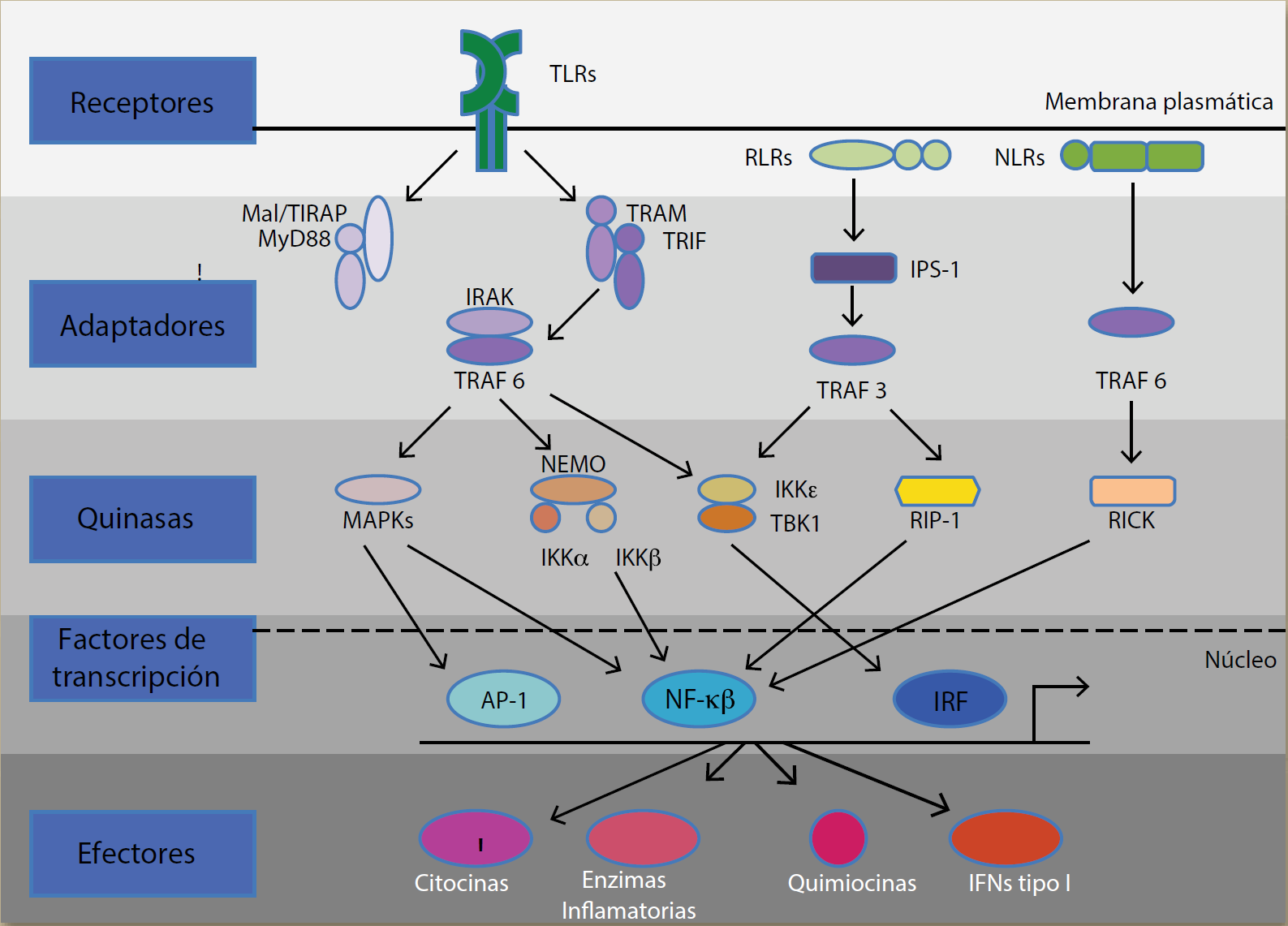
Los receptores tipo Toll (TLR) se hallan sobre todo en la membrana cellular, RLR (receptors tipo RIG-I) y NLR (receptors tipo NOD) se localizan en el citosol. Los TLR envían señal a través de Mal/TIRAP y MyD88 o bien TRAM/TRIF a IRAK/TRAF6 para activar cinasas corriente abajo. Los RLR usan IPS-1 y TRAF3 como moléculas adaptadoras y los NLR transmiten señales de activación a través de TRAF٦. Las señales de TLR, RLR, y NLR son entregadas a quinasas como MAPK, IKK, TBK1, RIP-1, y RICK para activar factor de transcripción, AP-1, NF-κB, e IRF. Los Factores de transcripción se unen a secuencias especificas de ADN y producen moléculas efectoras como citosinas, enzimas inflamatorias, quimiocinas e interferones tipo I.
Figura 1. Vías de señalización intracelulares de los receptores de reconocimiento de patrones.
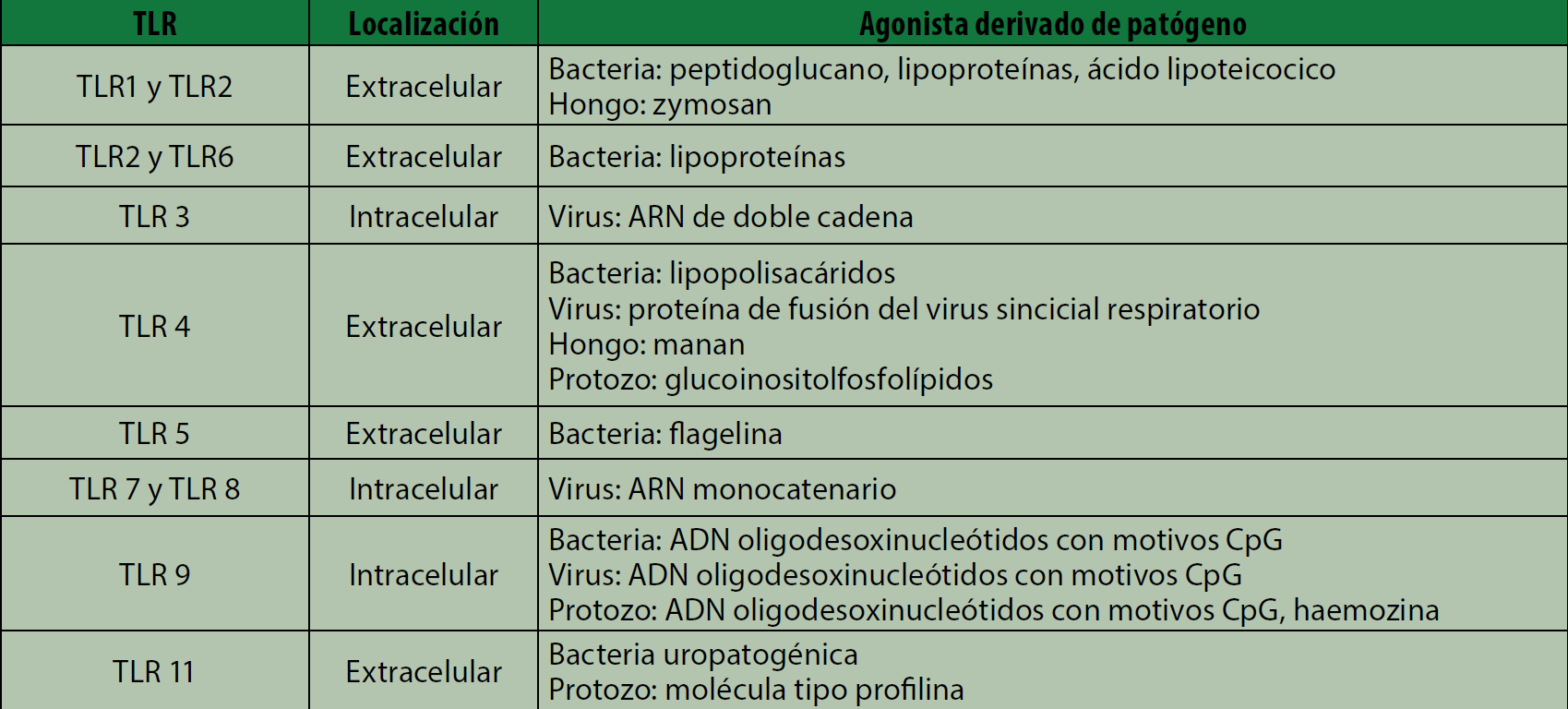
En los seres humanos, los TLR constituyen una familia de al menos 10 receptores expresados en la superficie de las células inmunes efectoras y constituyen el prototipo de RRP; su estructura y función ilustran muchos de los pasos involucrados en la interacción inicial huésped-patógeno de la sepsis. Los TLR son proteínas transmembrana de dominios extracelulares con repeticiones ricos en leucina y un dominio intracelular homólogo al receptor de interleucina-1 (tabla 1).
En sepsis, la activación de la respuesta inmunitaria debido a la liberación de grandes cantidades de PMAD procedentes de los microorganismos invasores o del tejido dañado, condiciona incremento en la expresión de los TLR21,22. La interacción de los TLR con los PMAD prepara al sistema inmunitario innato para incrementar la reactividad de los TLR. Circuitos de retroalimentación positiva entre PMAD/PMAP con sus respectivos receptores pueden conducir a la inmuno-activación excesiva, que se caracteriza por una respuesta de citocinas marcadamente desequilibrada con la resultante lesión de los tejidos23.
Posterior a la unión PMAD/PMAP con sus ligandos específicos (TLR) en sepsis, y posterior a la activación de las cascadas de señalización, se presenta una modificación en la actividad de las principales proteínas intracelulares, factores de transcripción y proteínas reguladoras citosólicas y nucleares.
Para los TLR, la señalización depende principalmente de 4 proteínas adaptadoras: la diferenciación mieloide primaria a través de la proteína de respuesta 88 (MyD88) y otras 3 proteínas No-MyD88 (TIR, TRIF y TRAM). Estas señales de transducción, MyD88-dependientes y MyD88-independientes, resultan en la activación del factor de transcripción prototipo, el factor nuclear-κB (FNκB).
Caspasas y complejo inflamasoma
Las caspasas son una familia de proteasas sintetizadas a partir de cisteína como proenzimas y activadas por proteólisis. Se subdividen en caspasas iniciadoras activadas por autoescisión y, caspasas ejecutoras que se activan mediante la escisición provocada por sus contrapartes iniciadoras. Las caspasas juegan un papel importante en los procesos celulares de inflamación y apoptosis que siguen a la interacción PMAD/PMAP-RRP. Después de la escisión, las caspasas producen múltiples cambios fenotípicos observados en la apoptosis, incluyendo la desintegración del citoesqueleto, la fragmentación del ADN e interrupción de la maquinaria molecular para la reparación del ADN celular. A pesar de que los TLR son los RRP más estudiados, los receptores similares a NOD son los más ubicuos. Se cree que, tras el reconocimiento de los patógenos por TLR, una señal es transmitida intracelularmente, la cual es reconocida por el dominio de unión a nucleótidos en el NLR. Dicho reconocimiento da como resultado la activación de un complejo multiprotéico denominado “inflamasoma”. Los inflamasomas son complejos multienzimáticos que sirven como plataformas moleculares para la activación de las capasas 1 y 5, resultando en la activación y secreción de citocinas proinflamatorias mediadas por caspasas como la IL-1β e IL-18.
Las señales y mecanismos que generan el ensamblaje/activación del inflamasoma son poco conocidos aún. Los complejos de inflamasoma montados en sepsis están bien caracterizados y se componen de 2 complejos multiproteínicos diferentes: el inflamasoma NALP1 y NALP3. IL-1β es una citocina proinflamatoria muy potente que requiere del ensamblaje del complejo inflamasoma como prerrequisito para la activación de la caspasa-1 antes de que su precursor (pro-IL-1β) sea liberado de su unión con TLR y convertirse en su forma activa, lo cual representa un mecanismos que previene la expresión incontrolada de IL-1β. Además de la liberación de citocinas proinflamatorias, las caspasas tienen como blanco de acción la enzima DNasa activada de caspasa (CAD). La activación de CAD induce la fragmentación del ADN que lleva a la apoptosis (figura 2). Dentro de los blancos de las caspasas en el citoesqueleto celular figuran la espectrina, la laminina nuclear y la enzima gelosina, la cual escinde a la actina; todos estos juegan un rol en la desintegración del citoesqueleto celular24,25.
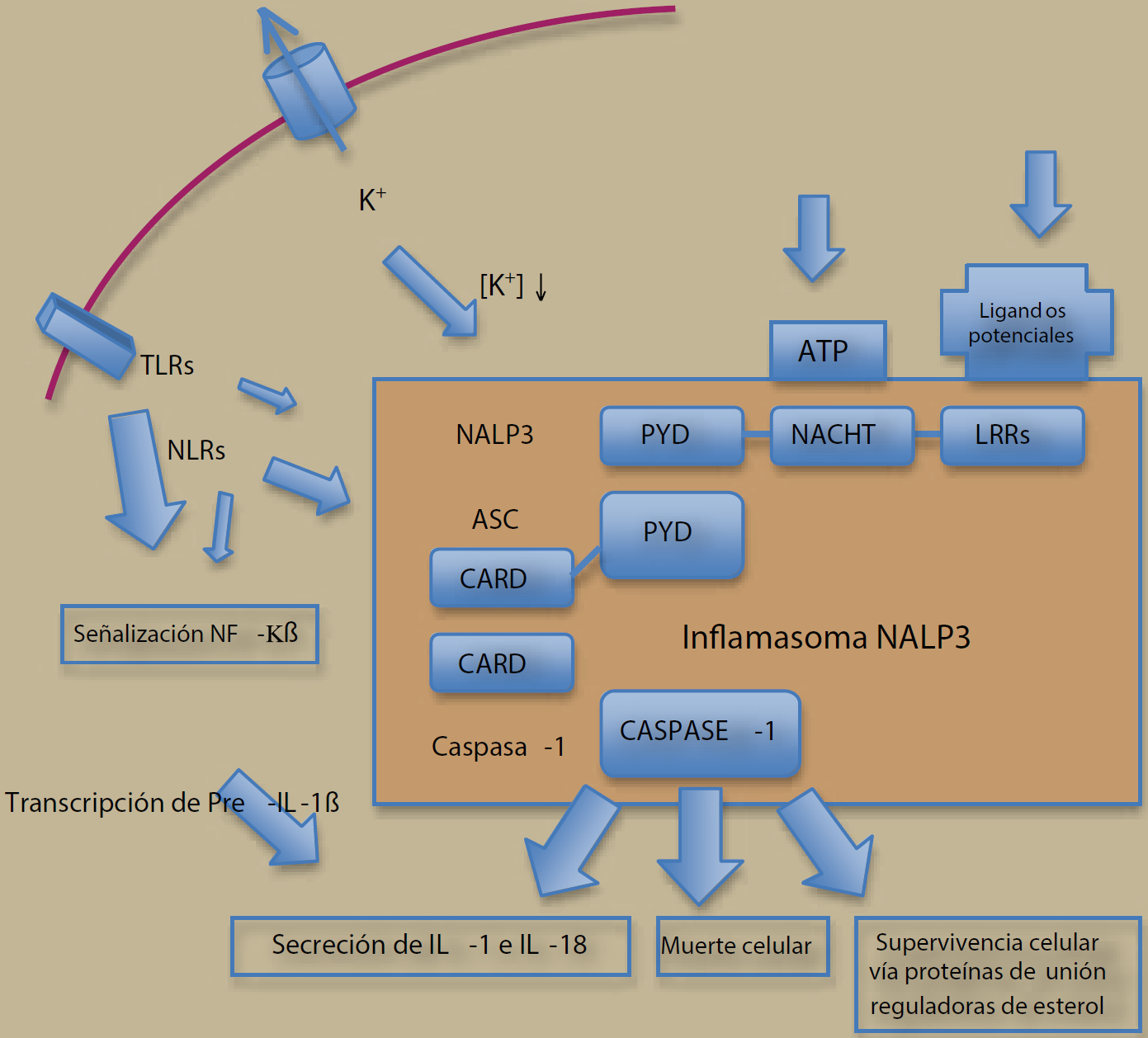
El complejo inflamasoma-NALP3 esta compuesto por NALP3, ASC, y caspasa-1. ASC interactúa con una de las proteínas de NALP a través del dominio “Cognate pyrin domain” (PYD) y con procaspasa-1 a través del dominio de reclutamiento homotipo de caspasa (CARD, de su traducción del inglés de “homotypic caspase recruitment domain”). El complejo del inflasoma humano brinda dos moléculas de procaspasa -1 en proximidad, provocando la autocatálisis y la subsecuente liberación de los dominios de caspasa-1 catalíticos activados (p20 y p10). NALP3 une ATP vía NACHT (dominio nucleósido trifosfato NTPasa), un precursor de IL-1B en su forma biológica activa, y un potente mediador de la fiebre e inflamación. (TLRs, receptor tipo Toll; ATP, adenosina trifosfato; NLRs, receptores tipo dominio de oligomerización de nucleotidos, NOD; ASC, proteína specklike asociada a apoptosis, que contiene un dominio CARD; NALP proteína que contiene dominios de NACHT-, LRR-, y PYD; LRRs, repeticiones ricas en leucina).
Figura 2. Complejo inflamasoma- NALP3.
Liberación de mediadores pro y antiinflamatorios
Una de las consecuencias inmediatas de la señalización celular en sepsis grave y choque séptico es la síntesis y liberación de cantidades crecientes de mediadores inflamatorios a la circulación sistémica en un intento de activar la mayor cantidad de células efectoras inmunes y reclutarlas al sitio de infección. Estas potentes moléculas se encuentran normalmente presentes en la circulación en bajas concentraciones, pero en altas concentraciones o en exposiciones prolongadas, pueden ejercer efectos biológicos potencialmente dañinos. La sobreexpresión de los mediadores de inflamación en las fases iniciales de la sepsis juega un papel preponderante para el posterior desarrollo del choque séptico. A esta liberación secuencial de mediadores inflamatorios se le ha denominado “tormenta de citocinas”.
Disfunción de la célula efectora inmune y no inmune
La respuesta efectora inmune normal en respuesta a la liberación de citocinas se pierde en la sepsis grave. Esta disfunción puede comprometer a todos los tipos celulares a partir de las células presentadoras de antígenos a neutrófilos y macrófagos.
Disfunción de los neutrófilos en sepsis
Los neutrófilos representan células clave en el sistema inmune innato actuando principalmente mediante el reconocimiento y destrucción de los agentes patógenos a través de una serie coordinada de pasos dentro de los que se incluyen la adhesión, quimiotaxis, fagocitosis y liberación de moléculas citotóxicas, seguido de la muerte celular por apoptosis. En sepsis grave se pierde la regulación funcional de los neutrófilos, lo que condiciona la excesiva activación de los neutrófilos con prolongada supervivencia. Estos neutrófilos activados favorecen la disfunción endotelial, la liberación de moléculas citotóxicas, condicionando lesión inflamatoria en los órganos del hospedador6.
Apoptosis acelerada linfocítica
Los linfocitos T colaboradores desempeñan un papel clave en la respuesta inmunológica adaptativa después de ser activados por las células presentadoras de antígenos del sistema inmunológico innato. Después de ser activadas, la respuesta inicial de los linfocitos es de tipo proinflamatorio, con la aparición de un fenotipo regulador después de varios días. La sepsis grave se caracteriza por la muerte acelerada por apoptosis de los linfocitos que conlleva a la depleción de los mismos con pérdida de su función reguladora6.
Ejes centrales nocivos en la sepsis
Es a partir del conocimiento de que los mediadores de la inflamación (no sólo los microorganismos invasores) están involucrados en la fisiopatogenia de la sepsis, que se han abierto nuevas líneas de investigación sobre los mecanismos fisiopatológicos de la inflamación. Diferentes mediadores se han relacionado con la fisiopatogenia de la sepsis, algunos de los cuales pueden ser considerados como “ejes centrales” de la compleja red inflamatoria. Aunque difieren en términos de su procedencia, la cinética de liberación y la fase de la sepsis en la cual predominan, estos ejes centrales pueden ejercer efectos pleiotrópicos al interconectar diversas vías de la respuesta inmunitaria.
Complementopatía
El sistema del complemento se puede activar a través de 3 vías diferentes que convergen en la generación de las anafilotoxinas C3a y C5a, C4a y el complejo de ataque a la membrana (MAC, también conocido como C5b-C9). En los ensayos clínicos de sepsis, el incremento plasmático de las concentraciones de C3a, C4a y C5a, se han relacionado con un peor pronóstico y sobrevida26,27. Destaca el hecho de que C3a podría, además de actuar como anafilotoxina proinflamatoria, tener propiedades antiinflamatorias. En el modelo murino de sepsis, los ratones con deficiencia de C3AR fueron más susceptibles a desarrollar estado de choque por endotoxemia, el cual fue acompañado de un incremento en la concentración plasmática de citocinas proinflamatorias. La unión de C3a a C3AR puede activar la secreción de hormonas antiinflamatorios a través la glándula hipófisis, lo que podría explicar la capacidad antiinflamatoria de C3a28,29.
Nuevos descubrimientos continúan incrementando nuestro acervo y comprensión acerca de los numerosos efectos nocivos derivados de la producción excesiva de C5a durante la sepsis. Los efectos derivadosde C5a contribuyen al desarrollo de la parálisis inmunitaria, disfunción y falla multiogánica, la apoptosis de timocitos y células de la médula suprarrenal así como el desequilibrio en el sistema de la coagulación30-34. Además, C5a está ampliamente relacionada con el desarrollo de cardiomiopatía mediada por sepsis35.
Estudios realizados de forma reciente, confirman el importante papel de C5a en la fisiopatogenia de la sepsis36. Además de C5AR, C5a puede unirse específicamente a un segundo receptor, C5L2, la función del cual era desconocida hasta hace poco tiempo. Originalmente se postuló que C5L2 funcionaba como un receptor “señuelo” para C5a, compitiendo con C5AR por la unión de C5a, aunque la evidencia reciente indica que C5L2 es un receptor funcional36-38. En la actualidad existe evidencia de que C5AR y C5L2 cooperan para potenciar la respuesta inflamatoria durante la sepsis, aunque cada receptor puede tener roles funcionales específicos y diferentes36.
Coagulopatía
En el ámbito clínico de la sepsis, la disregulación de la cascada de coagulación destaca por el desarrollo de múltiples complicaciones. La magnitud de la activación de la cascada de la coagulación durante la sepsis puede variar desde un nivel insignificante hasta la aparición de coagulación intravascular diseminada (CID) inclusive.
En la fase inicial de CID, la activación de la trombina da como resultado la formación intra y extra vascular de fibrina (proceso conocido como hipercoagulabilidad), seguido por el consumo de factores de la coagulación y disfunción plaquetaria. En la fase tardía de la CID, el acúmulo de fibrina a nivel microvascular se asocia a menudo con el desarrollo de disfunción y falla multiorgánica, este fracaso es atribuido a las perturbaciones de la microcirculación39. La CID desarrolla inflamación, activa la coagulación, e interactúa de manera bidireccional40. La trombina activada puede promover la activación de diversas vías proinflamatorias, dentro de las que se incluyen la producción de citocinas proinflamatorias (tales como TNFα, IL-1β e IL-6) y la generación de C5a, a su vez que pueden estimular la coagulación41,42. El factor tisular (FT), que es una molécula central para la iniciación de la CID, es expresado por las células endoteliales activadas y por células que no están normalmente expuestas al flujo sanguíneo, tales como las células subendoteliales, fibroblastos y también por células inmunes circulantes. En sepsis, el entorno proinflamatorio provoca en las células mononucleares la expresión de FT en su superficie, que conduce a la activación del sistema de coagulación43,44.
Otra consecuencia de la CID es la inhibición de la fibrinólisis. Además de la disfunción de las células endoteliales durante la sepsis, que también se produce como resultado del ambiente proinflamatorio, el aumento de los niveles del inhibidor del activador del plasminógeno-1 (PAI-1) y del inhibidor de la fibrinolisis activable por trombina (TAFI) dan lugar a alteraciones en la eliminación de la fibrina. Asimismo, el consumo de diversos factores que normalmente regulan la generación de trombina, tales como la antitrombina III, proteína C e inhibidor de la vía del factor tisular (TFPI), contribuye al desarrollo de CID45,46.
La proteína C, la cual es un regulador de la cascada de coagulación, es activada por la trombina unida a trombomodulina y por el receptor endotelial de la proteína C (EPCR) en las células endoteliales. Después de la disociación de EPCR, la proteína C activada se une a su cofactor, la proteína S, que luego resulta en la inactivación de los factores de coagulación Va y VIIIa.
Además de su actividad anticoagulante, la proteína C activada tiene propiedades antiapoptóticas y antiinflamatorias profundas. Disminuye notablemente la apoptosis de las células endoteliales y linfocitos y, ejerce efectos profibrinolíticos al inhibir al PAI-1. Los efectos antiinflamatorios de la proteína C activada están mediados a través delEPCR y su unión al receptor activado por la proteasa-1 (PAR1), el cual juega un papel central en la vinculación de la coagulación y la inflamación47-53.
La vía de la proteína C es particularmente susceptible de inhibición como respuesta a la inflamación en la CID mediada por sepsis41. Además de la disminución en el nivel de la proteína C, la regulación a la baja, la expresión y escisión del complejo trombomodulina-EPCR, son las principales causas de la disfunción de la vía de la Proteína C. El HMGB1 inhibe la vía de la proteína C al interferir con el complejo trombina-trombomodulina y también promueve la coagulación por estimulación del FT y la expresión e inhibición del activador del plasminógeno tisular (tPA), una proteasa de serina de la superficie de las células endoteliales que activa a la plasmina en la cascada de la fibrinólisis52,53.
Vinculación entre el sistema del complemento y la coagulación
Tradicionalmente los sistemas del complemento y de la coagulación se describen como cascadas separadas. Como descendientes de una vía ancestral común, ambas son cascadas proteolíticas compuestas de proteasas de serina con características estructurales comunes y estímulos activadores comunes40.
Esta relación no se limita a la similitud bioquímica de sus proteasas de serina, dado que, estas 2 vías también están vinculadas por muchas conexiones mutuas que conforman una red compleja.
Durante la sepsis, la vía de coagulación activada predispone a la trombosis y CID, lo cual puede agravar aún más la respuesta inflamatoria excesiva y activar al complemento. Una interacción bien conocida entre el complemento y la coagulación es la activación de la vía clásica del complemento a través del factor de la coagulación XIIa, el cual puede activar el componente C1 del complemento. De manera más reciente, se ha demostrado que la trombina puede funcionar como una C5 convertasa en un modo C3-independiente. Esta diafonía es particularmente interesante, no sólo porque la trombina y C5a son factores centrales de sus respectivas cascadas, sino también porque esto indica que C5a y el MAC pueden ser generados en ausencia de la activación del complemento. De forma similar a la trombina, la calicreína y la plasmina se unen directamente C3 y sus fragmentos activos. En un circuito de retroalimentación negativa indirecta, la trombina activada -TAFI inactiva a C3a y C5a54-56.
El sistema del complemento amplifica la coagulación mediante la modificación de los fosfolípidos de las membranas (requeridas para la iniciación de la coagulación a través de FT), por activación de las plaquetas, induciendo la expresión del FT y PAI-1 por los leucocitos57,58. Además, la proteasa 2 de serina-lecitina unida a manan (MASP2), una proteasa que es característica en la activación del complemento a través de la vía de la lecitina, puede activar la coagulación mediante la escisión de la trombina en trombina activada59 (figura 3).

Línea verde: efecto estimulante; línea roja: efecto inhibitorio; línea azul: efecto estimulante o inhibitorio.
EPCR: Receptor endotelial de la proteína C; IL: interleucina; PAI-1: inhibidor del activador de plasminógeno-1; TAFI: inhibidor de la fibrinolisis activable por trombina; TFPI: inhibidor de la vía del factor tisular; TM: trombomodulina; TNF: factor de necrosis tumoral; u-PA: activador de plasminógeno urinario; u-PAR: receptor activador de plasminógeno tipo urocinasa; Va: factor de coagulación V activado; VIIIa: factor de coagulación VIII activado; Xa: factor de coagulación X activado.
Figura 3. Esquema de los procesos involucrados en la interrelación entre las vías de coagulación, anticoagulación, fibrinólisis e inflamación.
Conclusión
La sepsis es un síndrome complejo en el que la activación de la inmunidad innata induce una intensa respuesta proinflamatoria caracterizada por una intensa respuesta molecular y por un desbalance con los mecanismos reguladores, en especial el antiinflamatorio y la coagulación, lo que condiciona disfunción y lesión del endotelio vascular y de la microcirculación.











 nueva página del texto (beta)
nueva página del texto (beta)