Introducción
El 15 de abril de 2022, la Organización Mundial de la Salud publicó una alerta sobre un brote de hepatitis aguda de etiología desconocida; inicialmente se presentó en el Reino Unido e Irlanda del Norte y posteriormente se han informado nuevos casos en 11 países de Europa y América del Sur. La edad de los pacientes oscila entre un mes y 16 años, con una mayor prevalencia entre los dos y cinco años. Aproximadamente 10 % ha requerido trasplante de hígado y hasta ahora se ha reportado al menos una muerte. La presentación clínica incluye síntomas gastrointestinales como dolor abdominal, diarrea, vómitos y finalmente se desarrolla hepatitis aguda grave, definida como un incremento de aminotransferasas (alanina aminotransferasa > 500 UI/L) e ictericia. La mayoría de los casos no presentó fiebre. El protocolo de estudio descartó la presencia de los virus comunes que causan hepatitis viral aguda (hepatotropos [virus de las hepatitis A, B, C y E]), pero 75.5 % de los casos en Inglaterra y 50 % de los de Escocia fueron positivos a adenovirus humanos (HAdV). En algunos casos se realizó subtipificación molecular: 18 niños resultaron positivos a adenovirus fenotipo tipo 41. Sin embargo, se han detectado otros tipos de HAdV en muestras sanguíneas y no sanguíneas (secreción bronquial, heces, etcétera), pero los bajos niveles de adenovirus presentes en las muestras de sangre dificultan la recuperación de genomas de alta calidad. También se detectó coronavirus 2 del síndrome respiratorio agudo grave (SARS-CoV-2) en 20 niños, 19 de los cuales tenían coinfección por HAdV y SARS-CoV-2. Los datos sobre las variantes del SARS-CoV-2 involucradas son limitados en este momento.1,2
La insuficiencia hepática aguda es una presentación rara y a menudo heterogénea de disfunción hepática grave en un paciente sin enfermedad hepática preexistente. Aunque la morbilidad y mortalidad son altas, la supervivencia general ha mejorado con los cuidados intensivos y los avances en el trasplante hepático de emergencia. Un alto índice de sospecha, la derivación temprana a un centro especializado en trasplante hepático y las medidas de apoyo adecuadas siguen siendo la piedra angular para el manejo de la falla hepática aguda grave, la cual se define como el desarrollo de lesión hepática aguda grave con encefalopatía y alteración de la función sintética (INR de 1.5 o superior) en un paciente sin cirrosis o enfermedad hepática preexistente y con una enfermedad de menos de 26 semanas de evolución.3,4
Uno de los principales agentes causales de los que se sospecha es el adenovirus F41, ya que en un porcentaje elevado de los casos estudiados se detectó infección por adenovirus y en aquellos en los cuales se dispuso de estudios moleculares se identificó el subtipo F41.5 Los adenovirus (AdV) constituyen una familia de patógenos muy contagiosos que infectan tanto a humanos como animales; en el humano son muy comunes y pueden causar infecciones en vías respiratorias, ojos, intestinos, tracto urinario y adenoides. Recientemente ya se habían señalado algunos adenovirus como posible causa de falla hepática en niños1 y, aunque es una asociación rara, se han reportado en pacientes pediátricos inmunocomprometidos. El HAdV se transmite de una persona a otra con facilidad, a través de secreciones y objetos contaminados. Puede ser a través del aire o por el agua, mediante contaminación fecal-oral. Hasta ahora, más de 100 tipos de adenovirus humanos (HAdV) han sido aislados, caracterizados y clasificados en siete especies (de A a G).
Los adenovirus están integrados por una cápside externa, un núcleo proteico central que cubre el ADN bicatenario lineal y varias proteínas accesorias. La unión del virus a la superficie celular es efectuada mediante la interacción de la fracción globular knob de la proteína fibrilar del pentón con el receptor CAR (coxsackie and adenovirus receptor).6,7
Además de causar enfermedades en humanos, algunos adenovirus se han utilizado como vectores para el diseño de vacunas contra enfermedades infecciosas como COVID-19 (Oxford, AztraZeneca, Johnson & Johnson y Sputnik V), síndrome respiratorio de Oriente Medio (MERS), enfermedad por el virus del Ébola, sida, fiebres de Lassa y del Zika. Las vacunas que emplean estos vectores son capaces de producir anticuerpos neutralizantes in vivo contra MERS y COVID-19, y aunque se ha sugerido la relación entre la vacunación contra COVID-19 y el origen de estas hepatitis, dicha teoría se ha descartado ya que los pacientes pediátricos con este tipo de hepatitis no habían sido vacunados.
Existen solamente dos miembros de especies de HAdV con un importante tropismo a células gastrointestinales, HAdV-70 y HAdv-71, los cuales causan diarrea que puede ocasionar la muerte de los niños con una frecuencia solamente inferior a la producida de Shigella y rotavirus. Por ahora, la hipótesis de un adenovirus es la más plausible y podría tratarse de una nueva variante con un perfil más hepatotropo.8
Por otro lado, es importante considerar que la respuesta inmunitaria en la hepatitis viral aguda puede ser otro factor en la presentación de estos casos atípicos (Figura 1). Se conoce que existe una diferencia significativa en el comportamiento de las citoquinas secretadas por los linfocitos TH1 y TH2 en el desarrollo de insuficiencia hepática fulminante, en comparación con una hepatitis viral aguda no grave: la sobreexpresión de TH1 (IGN-g, IL-2 y TNF-a) y Th2 (IL-10) en pacientes que desarrollaron insuficiencia hepática fulminante es bien conocida.9,10
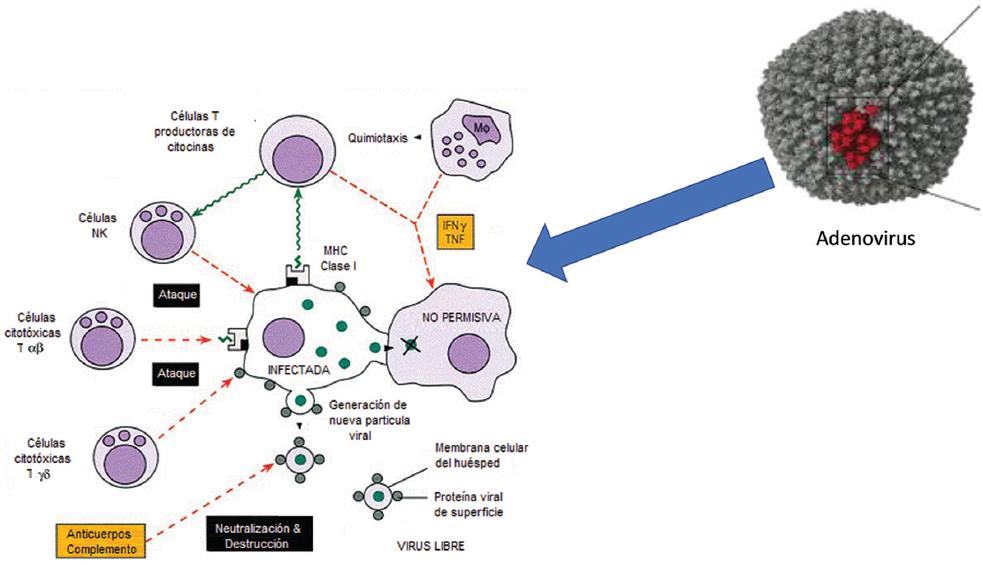
Figura 1 Activación de inmunidad hepática inducida por el adenovirus. Adaptada de: Defensa del huésped contra la infección [Internet].12
Otro aspecto importante en el desarrollo de la insuficiencia hepática aguda grave es el factor toxicológico; hasta ahora se han analizado muestras de todos los pacientes para compuestos orgánicos, compuestos volátiles y metales. Aunque se detectó paracetamol en algunos pacientes, a partir de la información disponible se determinó que su uso fue con fines terapéuticos y por debajo de los niveles tóxicos. Se han identificado otras sustancias, entre las cuales se investigó más estrechamente el uso terapéutico y los niveles del fluconazol, sin encontrar una relación significativa. También se investigó la posibilidad de que algunos metales fueran la causa, pero tampoco se han encontrado niveles altos de algún metal hepatotóxico. Respecto a los compuestos orgánicos, la atención se ha centrado en las micotoxinas y si bien se han detectado algunas en las muestras, no se han documentado diferencias significativas en la comparación de los casos con los controles.
Respecto al aumento de las presentaciones de hepatitis pediátricas agudas no A, B, C ni E, las siguientes hipótesis están siendo probadas activamente en las investigaciones en curso:
-
Una infección normal por adenovirus.
a) Susceptibilidad anormal o respuesta atípica del huésped que permite que la infección por adenovirus progrese con mayor frecuencia a hepatitis, ya sea por lesión directa al hepatocito o por afección inmunopatológica, quizá porque el aislamiento durante la pandemia de COVID-19 limitó la exposición habitual de los niños a los diferentes adenovirus.
b) Incremento significativo y excepcionalmente superior de infecciones normales por adenovirus, que hace posible la presentación de una rara complicación poco reconocida.
c) Susceptibilidad anormal o respuesta del huésped al adenovirus debido a la infección por SARS-CoV-2 (incluida la restricción de ómicron) u otra infección.
d) Susceptibilidad anormal o respuesta del huésped al adenovirus debido a una coinfección con SARS-CoV-2 u otro virus.
Una nueva variante del adenovirus, con o sin contribución de un cofactor enumerado previamente.
Un síndrome de SARS-CoV-2 posinfeccioso (incluyendo un efecto restringido de ómicron).
Una exposición a drogas, toxinas o medio ambiente aún no documentado.
Un nuevo patógeno que actúa solo o en coinfección.
Una nueva variante de SARS-CoV-2.11
Hasta existen más preguntas que respuestas, pero se está en la ruta de investigación para determinar en el menor tiempo posible la causalidad de esta complicación hepática grave en población pediátrica. Por lo pronto, en México existe ya una alerta epidemiológica para estos casos y se ha publicado la definición de casos sospechosos y casos probables:
Caso sospechoso: toda persona menor o igual a 16 años que presente hepatitis aguda con aspartato aminotransferasa o alanina aminotransferasa mayor de 500 UI/L sin etiología conocida.
Caso probable: todo caso sospechoso con resultado negativo a virus de la hepatitis A, B, C o E emitido por Instituto de Diagnóstico y Referencia Epidemiológicos “Dr. Manuel Martínez Báez”.
Conclusión
La hepatitis aguda grave de origen desconocido en niños ha mostrado un incremento inusitado y no esperado. Si bien el número de pacientes afectados aún es bajo, requiere una minuciosa investigación en todas las líneas para implementar medidas preventivas y curativas. Deberá realizarse todo el protocolo para descartar etiológicas conocidas a cualquier paciente que cumpla con la definición operacional de caso sospechoso y, si es necesario, derivarlo oportunamente a un centro especializado que cuente con programa de trasplante hepático.











 nueva página del texto (beta)
nueva página del texto (beta)


