Introducción
Los antagonista de la vitamina K (AVK) son una alternativa efectiva para la prevención y tratamiento de los pacientes con enfermedad tromboembólica venosa (ETV), fibrilación auricular no valvular (FA) y en los portadores de una válvula cardiaca mecánica (VCM). Aún constituyen un tipo de tratamiento frecuentemente empleado en la clínica, ya que tienen a su favor una gran cantidad de evidencia generada en ensayos clínicos, los cuales sostienen su eficacia; su uso es avalado por innumerables guías nacionales e internacionales.1-3
Mantener la calidad del control de la terapia con los AVK es necesario para reducir las complicaciones trombóticas y hemorrágicas asociadas a su uso, por lo cual se requiere un control frecuente de su efecto. Sin embargo, estos anticoagulantes no son fáciles de manejar debido a sus múltiples interacciones con alimentos y medicamentos y porque en numerosas ocasiones se indican en pacientes de edad avanzada con múltiples comorbilidades. Debido a todas estas dificultades y su consecuente impacto para mantener siempre el rango de anticoagulación terapéutica deseado, con frecuencia son subutilizados.4
Los AVK requieren dosificarse individualmente debido al número alto de factores que afectan su farmacología, un hecho que los convierte en un reto para alcanzar una anticoagulación estable. Por lo tanto, monitorear la terapia con AVK es una estrategia absolutamente necesaria para minimizar las fluctuaciones de su efecto farmacológico. Estudios recientes indican que en muchos sistemas de salud nacionales, menos de la mitad de los pacientes elegibles para usar AVK toman el medicamento y, aún menos, son mantenidos adecuadamente dentro del rango terapéutico deseado.5 Por lo tanto, las posibles consecuencias derivadas de un nivel de anticoagulación infra o supraterapéutica hacen imperativo lograr el mejor control.6,7
El cociente de estandarización internacional (INR) se usa para determinar el efecto anticoagulante de los AVK. El tiempo en rango terapéutico (TRT) del INR es la mejor herramienta para evaluar la efectividad a plazo largo del tratamiento con AVK.8 El TRT es el tiempo durante el cual el INR se mantiene dentro del rango terapéutico deseado y se expresa como porcentaje. El número de evaluaciones del INR que se encuentra dentro del rango terapéutico deseado en relación con el número total de evaluaciones del INR realizadas en un periodo específico permite obtener el TRT.6
Los AVK aún se consideran el estándar de oro de la anticoagulación oral, sin embargo, múltiples estudios muestran que el control con el INR de la terapia con AVK es subóptimo en la práctica clínica rutinaria. En efecto, los pacientes se mantienen hasta casi 40 % fuera del INR deseado. Estas cifras dependen del tipo y lugar de la atención médica, de si se indican en una clínica de anticoagulación o por médicos en general. Es un hecho que la calidad del tratamiento con AVK es mayor si el paciente es atendido en clínicas de anticoagulación.4,7
Los AVK son todavía la opción anticoagulante más utilizada en México, sin embargo, ningún estudio clínico se ha realizado para analizar la calidad real del efecto de estos medicamentos. Por lo tanto, el objetivo de este estudio fue evaluar la calidad de la anticoagulación oral con AVK en tres escenarios clínicos diferentes, en tres diferentes periodos en México.
Métodos
En este estudio prospectivo, descriptivo, controlado y anidado en una cohorte, incluimos pacientes tratados en tres diferentes escenarios clínicos del Instituto Mexicano del Seguro Social en la Ciudad de México:
– Hospital de Cardiología del Centro Médico Nacional Siglo XXI (HC-CMNSXXI).
– Servicio de Cardiología, Hospital General Regional “Carlos MacGregor Sánchez Navarro” (SC-HGRCMSN).
– Clínica de Anticoagulación del Servicio de Hematología, Hospital General Regional “Carlos MacGregor Sánchez Navarro” (CA-HGRCMSN).
El estudio comprendió tres fases: de enero de 2013 a diciembre de 2014, de noviembre de 2015 a diciembre de 2016 y de enero de 2018 a diciembre de 2019. El estudio se realizó en tres fases, ya que al final de las fases 1 y 2 se efectuó un análisis parcial de los resultados obtenidos para hacer ajustes para el control de la anticoagulación en HC-CMNSXXI y SC-HGRCMSN y reiniciar la evaluación de la calidad.
Incluimos a todos los pacientes de uno y otro sexo atendidos en la consulta externa, con cualquier indicación para ser tratados con AVK y que recibieron el tratamiento activo por al menos 12 meses. El tratamiento inicial intrahospitalario en ambos hospitales fue siempre decisión del médico tratante y, por lo tanto, esta información no fue analizada en este estudio. Una vez que el paciente fue egresado del hospital, fue tratado de acuerdo con el criterio del médico tratante o de la clínica de anticoagulación cuando el paciente fue derivado a este último servicio.
De los expedientes se obtuvieron los datos generales de cada paciente y sus evaluaciones del INR. Para ser incluidos, los pacientes debían tener al menos cuatro determinaciones del INR en el periodo de 12 meses para tener una estimación fiel del TRT. Ya que el estudio se realizó con la revisión de los registros de los INR en ambos hospitales, los médicos tratantes nunca supieron de las características e implicaciones del estudio. Si un paciente era identificado como candidato, su expediente clínico era revisado para recolectar los siguientes datos: edad, sexo, diagnóstico, comorbilidades, indicación para recibir un AVK (para establecer el rango óptimo del INR en ese paciente) y el tipo de AVK empleado (acenocumarina o warfarina). De las bases de datos de laboratorio se consiguieron los valores del INR, la frecuencia del monitoreo y el periodo de seguimiento. Los pacientes fueron excluidos del análisis cuando la información estaba incompleta, lo que incluía la falta de valores del INR.
El tamaño de la muestra fue determinado por conveniencia; se consideró el máximo número de pacientes en los tres periodos descritos. Originalmente se intentó incluir 900 pacientes en cada fase del análisis. Todos los pacientes se asignaron a uno de dos grupos de tratamiento de acuerdo con las recomendaciones mundialmente aceptadas para el uso de AVK:7,8
Al inicio de la fase 1 del estudio, las recomendaciones internacionales para la anticoagulación con AVK para pacientes portadores de prótesis valvular cardiaca mecánica era de 3.5 a 4.5; sin embargo, durante el estudio, estas recomendaciones cambiaron de 2.5 a 3.5.9,10 Este cambio no afectó el análisis de los resultados ya que se estandarizaron de acuerdo con el INR obtenido al momento del análisis respectivo y a las recomendaciones específicas en ese periodo. De acuerdo con la intensidad de la anticoagulación recomendada evaluada por el INR, los pacientes se clasificaron como:
– Con rango terapéutico inferior al deseado (INR < 2.0 o < 3.5).
– Dentro del rango terapéutico deseado (INR = 2.0-3.0 o 3.5-4.5).
– Con rango terapéutico superior al deseado (INR > 3.0 o > 4.5).
De acuerdo con el periodo específico en el que el paciente fue evaluado, se obtuvieron tanto el TRT como el porcentaje de pacientes entre los rangos terapéuticos deseados. El TRT se calculó de acuerdo con la herramienta más aceptada mundialmente, para lo cual se aplicó un método de interpolación lineal, que asume una relación lineal entre dos valores de INR y coloca un valor específico de este a cada día entre las pruebas de cada paciente.11,12
Todas las evaluaciones del INR se realizaron mediante una estrategia point-of-care (trombotest), con la que se evalúa directamente el valor mediante un equipo CoaguChek® XS, el cual utiliza tiras reactivas que contienen tromboplastina humana recombinante, de acuerdo con las instrucciones del fabricante (Roche Diagnostics, Alemania).13 Esta técnica está ampliamente validada y aceptada en la literatura para el control de la anticoagulación con AVK en múltiples escenarios clínicos.14,15 El equipo requiere una cantidad muy pequeña de sangre recolectada por punción de un dedo.
En algunos pacientes seleccionados aleatoriamente, cada tres meses se obtuvo sangre periférica por punción de la vena antecubital, para evaluar la concordancia de los resultados de la táctica habitual del tiempo de protrombina (TP) con la prueba de trombotest. Esta sangre fue colectada en tubos de plástico que contenían citrato de sodio, 0.109 M (vol.:vol. 1:9, Na Citrate, BD Vacutainer, Franklin Lakes, NJ, Estados Unidos). Las muestras se centrifugaron por 15 minutos a 2000 g para obtener el plasma pobre en plaquetas, necesario para medir el TP y calcular el INR en un equipo automatizado ACL 1000 (IL Werfen, Hartwell Road Bedford, MA, Estados Unidos), con el reactivo HemosIL PT-Fibrinogen HS PLUS y valor de ISI de 1.0 (IL Werfen).
El protocolo de estudio fue aprobado por los comités locales de investigación de ambos hospitales. Este estudio representó un riesgo mínimo para los pacientes, ya que solo se revisaron los resultados del INR de los pacientes, requerimiento necesario y rutinario en quienes reciben AVK. Por lo tanto, no se obtuvo consentimiento por escrito por parte de los pacientes antes de ingresar al estudio. Los datos conseguidos siempre fueron anónimos.
Para el análisis descriptivo, los datos continuos se expresaron como promedios y rangos. Los datos categóricos se indicaron con porcentajes. La comparación de los datos categóricos entre los grupos de estudio se realizó mediante una prueba de chi cuadrada, mientras que para comparar los datos cuantitativos se usó una prueba de Anova de una vía. Los análisis estadísticos se realizaron utilizando el programa Statistical Package for the Social Sciences, versión 26 (SPSS Inc., Chicago, IL, Estados Unidos). Un valor de p > 0.05 se consideró significativo.
Resultados
Las características generales de los pacientes, el tipo de AVK y la indicación para el uso de estos anticoagulantes se muestra en la Tabla 1. No hubo diferencias significativas entre los grupos durante las tres fases del estudio, excepto en las indicaciones para usar un AVK, ya que la mayoría de los pacientes de la CA-HGRCMSN fueron tratados por padecer una ETV a diferencia de las indicaciones cardiológicas en el HC-CMNSXXI y SC-HGRCMSN.
Tabla 1 Características generales de los pacientes
| Característica | HC-CMNSXXI | SC-HGRCMSN | CA-HGRCMSN | p | |||
|---|---|---|---|---|---|---|---|
| Edad en años, mediana (rangos) | 63.6 (16-89) | 65.1 (16-88) | 65.9 (16-92) | NS | |||
| Fase 1 | 62.4 | 62.9 | 63.8 | NS | |||
| Fase 2 | 63.8 | 65.7 | 64.6 | NS | |||
| Fase 3 | 64.6 | 66.8 | 65.3 | NS | |||
| n | % | n | % | n | % | ||
| Número de pacientes | 1755 | 100 | 900 | 100 | 1763 | 100 | NS |
| Fase 1 | 500 | 28.5 | 300 | 33.3 | 500 | 28.4 | NS |
| Fase 2 | 613 | 34.8 | 300 | 33.3 | 600 | 34.0 | NS |
| Fase 3 | 642 | 36.8 | 300 | 33.3 | 663 | 37.6 | |
| Sexo (mujer/hombre) | 868/887 | 50.3/49.7 | 450/450 | 50/50 | 877/886 | 49.8/50.2 | NS |
| Fase 1 | 250/250 | 50/50 | 150/150 | 50/50 | 250/250 | 150/150 | NS |
| Fase 2 | 308/305 | 50.2/49.8 | 150/150 | 50/50 | 302/298 | 50.3/49.7 | NS |
| Fase 3 | 310/332 | 48.3/51.7 | 150/150 | 50/50 | 325/338 | 49.0/51.0 | NS |
| Antagonista de la vitamina K indicado | |||||||
| Acenocumarina | 986 | 56.1 | 479 | 53.3 | 1019 | 57.8 | NS |
| Warfarina | 769 | 43.9 | 421 | 46.7 | 744 | 42.4 | NS |
| Indicación para el uso de antagonista de la vitamina K | |||||||
| Enfermedad tromboembólica venosa | 124 | 7.1 | 92 | 10.2 | 1,615 | 91.6 | 0.001 |
| Fibrilación auricular | 1188 | 67.7 | 586 | 65.1 | 92 | 5.2 | 0.001 |
| Válvula cardiaca mecánica | 422 | 24.0 | 206 | 22.9 | 14 | 0.8 | 0.001 |
| Otras indicaciones | 21 | 1.2 | 16 | 1.8 | 42 | 2.4 | 0.030 |
| INR deseados | |||||||
| Rango terapéutico bajo (2.0-3.0) | 1312 | 74.8 | 678 | 75.3 | 1707 | 96.8 | 0.045 |
| Rango terapéutico alto (3.5-4.5/2.5-3.5) | 422 | 23.9 | 206 | 22.9 | 14 | 0.8 | 0.0007 |
HC-CMNSXXI = Hospital de Cardiología, Centro Médico Nacional Siglo XXI, SC-HGRCMSN = Servicio de Cardiología, Hospital General Regional “Carlos MacGrégor Sánchez Navarro”, CA-HGRCMSN = Clínica de Anticoagulación, Servicio de Hematología, Hospital General Regional “Carlos MacGrégor Sánchez Navarro”, NS = no significativo.
Analizamos los resultados de las evaluaciones del INR realizadas en 5576 pacientes; sin embargo, los resultados de 1428 individuos (25.6 %) no fueron considerados en el análisis, ya que no cumplían los criterios de inclusión. Las causas más frecuentes de exclusión de los pacientes fue la falta de al menos cuatro evaluaciones del INR en el periodo de 12 meses (n = 1282, 89.8 % de todos los pacientes excluidos). Al final, 4148 pacientes se incluyeron del análisis a lo largo de todo el estudio. La evaluación de todo el estudio incluyó 40 833 pruebas de INR, sin embargo, 2285 fueron excluidas; 2039 (89.2 %) fueron calculadas con el método tradicional con base en la prueba del TP. Finalmente, 38 548 evaluaciones del INR fueron analizadas (Tabla 2). Específicamente, las evaluaciones de INR superior a 5.0 fueron analizadas para determinar el porcentaje de pacientes con el nivel de riesgo hemorrágico más alto (Tabla 3).
Tabla 2 Análisis de las evaluaciones de los INR a través de las tres fases del estudio
| Evaluaciones | INR | p | |||||
|---|---|---|---|---|---|---|---|
| Bajo | Deseado | Alto | |||||
| n | % | n | % | n | % | ||
| Fase 1 (n = 11 613) | |||||||
| HC-CMNSXXI (n = 4452) | 2204 | 49.5 | 859 | 19.3 | 1389 | 31.2 | < 0.001* |
| SC-HGRCMSN (n = 2420) | 1308 | 54.1 | 445 | 18.3 | 667 | 27.6 | |
| CA-HGRCMSN (n = 4741) | 498 | 10.5 | 3371 | 71.1 | 872 | 18.4 | |
| Fase 2 (n = 12 740) | |||||||
| HC-CMNSXXI (n = 4854) | 2291 | 47.2 | 1082 | 22.3 | 1481 | 30.5 | < 0.001* |
| SC-HGRCMSN (n = 2502) | 1186 | 47.4 | 578 | 23.1 | 738 | 29.5 | |
| CA-HGRCMSN (n = 5384) | 614 | 11.4 | 3747 | 69.6 | 1023 | 19.0 | |
| Fase 3 (n = 14 195) | |||||||
| HC-CMNSXXI (n = 5086) | 2512 | 48.7 | 901 | 17.7 | 1673 | 32.9 | < 0.001* |
| SC-HGRCMSN (n = 2651) | 1251 | 47.2 | 486 | 18.3 | 914 | 34.5 | |
| CA-HGRCMSN (n = 6458) | 536 | 8.3 | 4527 | 70.1 | 1395 | 21.6 | |
| Total (n = 38 548) | |||||||
| HC-CMNSXXI (n = 14 392) | 7007 | 48.7 | 2842 | 19.8 | 4543 | 31.5 | < 0.001* |
| SC-HGRCMSN (n = 7573) | 3745 | 49.6 | 1509 | 19.9 | 2319 | 30.5 | |
| CA-HGRCMSN (n = 16 583) | 1648 | 10.0 | 11 645 | 70.3 | 3290 | 19.7 | |
HC-CMNSXXI = Hospital de Cardiología, Centro Médico Nacional Siglo XXI, SC-HGRCMSN = Servicio de Cardiología, Hospital General Regional “Carlos MacGrégor Sánchez Navarro”, CA-HGRCMSN = Clínica de Anticoagulación, Servicio de Hematología, Hospital General Regional “Carlos MacGrégor Sánchez Navarro”.
*INR deseado, CA-HGRCMSN versus los otros grupos.
Tabla 3 INR altos a través de las tres fases del estudio
| INR alto | INR alto | p | |||||||
|---|---|---|---|---|---|---|---|---|---|
| 5-6 | 6-7 | 7-8 | > 8 | ||||||
| n | % | n | % | n | % | n | % | ||
| Fase 1 (n = 2928) | |||||||||
| HC-CMNSXXI (n = 1389) | 671 | 48.3 | 486 | 35.0 | 144 | 10.4 | 88 | 6.3 | < 0.001* |
| SC-HGRCMSN (n = 667) | 295 | 44.2 | 208 | 31.2 | 101 | 15.1 | 63 | 9.4 | |
| CA-HGRCMSN (n = 872) | 496 | 56.9 | 274 | 31.4 | 61 | 7.0 | 41 | 4.7 | |
| Fase 2 (n = 3242) | |||||||||
| HC-CMNSXXI (n = 1481) | 786 | 53.1 | 471 | 31.8 | 152 | 10.3 | 72 | 4.8 | < 0.001* |
| SC-HGRCMSN (n = 738) | 297 | 40.2 | 225 | 30.5 | 167 | 22.6 | 49 | 6.7 | |
| CA-HGRCMSN (n = 1023) | 469 | 45.8 | 392 | 38.4 | 122 | 11.9 | 40 | 3.9 | |
| Fase 3 (n = 3982) | |||||||||
| HC-CMNSXXI (n = 1673) | 955 | 57.1 | 528 | 31.6 | 111 | 10.8 | 79 | 4.7 | < 0.001* |
| SC-HGRCMSN (n = 914) | 381 | 41.7 | 299 | 32.7 | 158 | 17.3 | 76 | 8.3 | |
| CA-HGRCMSN (n = 1395) | 998 | 71.5 | 269 | 19.3 | 96 | 6.9 | 32 | 2.3 | |
| Total (n = 10 152) | |||||||||
| HC-CMNSXXI (n = 4543) | 2412 | 53.1 | 1485 | 32.7 | 407 | 8.9 | 239 | 5.3 | < 0.001* |
| SC-HGRCMSN (n = 2319) | 973 | 41.9 | 732 | 31.6 | 426 | 18.4 | 188 | 8.1 | |
| CA-HGRCMSN (n = 3290) | 1963 | 59.7 | 935 | 28.4 | 279 | 8.5 | 113 | 3.4 | |
HC-CMNSXXI = Hospital de Cardiología, Centro Médico Nacional Siglo XXI, SC-HGRCMSN = Servicio de Cardiología, Hospital General Regional “Carlos MacGrégor Sánchez Navarro”, CA-HGRCMSN = Clínica de Anticoagulación, Servicio de Hematología, Hospital General Regional “Carlos MacGrégor Sánchez Navarro”.
*INR altos, CA-HGRCMSN versus los otros grupos.
Durante el periodo de estudio, el número de evaluaciones del INR fue significativamente diferente entre los grupos de estudio (Tabla 4). En la fase 1, los promedios de evaluaciones para el periodo de 12 meses en el HC-CMNSXXI, SC-HGRCMSN y CA-HGRCMSN fueron 5.7 (rango 4-9), 5.6 (rango 4-9) y 9.0 (rango 6-11), respectivamente (p < 0.001 para CA-HGRCMSN versus los otros dos grupos). Los mismos datos fueron para la fase 2: 6.1 (rango 4-10), 5.8 (rango 4-9) y 9.2 (rango 6-17), respectivamente (p < 0.001 para CA-HGRCMSN versus los otros dos grupos). Finalmente, para la fase 3, los promedios fueron 6.0 (rango 4-9), 5.8 (rango 4-9) y 9.6 (rango 6-15), respectivamente (p < 0.001 para CA-HGRCMSN versus los otros dos grupos).
Tabla 4 Número de evaluaciones del INR a lo largo del estudio
| Evaluaciones del INR/paciente/año | Número de evaluaciones | p | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | > 12 | X | ||
| Fase 1 | ||||||||||||
| HC-CMNSXXI (n = 500) | 71 | 121 | 204 | 85 | 11 | 8 | 0 | 0 | 0 | 0 | 5.7 | < 0.001* |
| SC-HGRCMSN (n = 300) | 64 | 75 | 98 | 49 | 11 | 3 | 0 | 0 | 0 | 0 | 5.6 | |
| CA-HGRCMSN (n = 500) | 0 | 0 | 24 | 45 | 78 | 192 | 125 | 20 | 10 | 6 | 9.0 | |
| Fase 2 | ||||||||||||
| HC-CMNSXXI (n = 613) | 74 | 142 | 199 | 117 | 35 | 29 | 17 | 0 | 0 | 0 | 6.1 | < 0.001* |
| SC-HGRCMSN (n = 300) | 52 | 71 | 102 | 55 | 13 | 7 | 0 | 0 | 0 | 0 | 5.8 | |
| CA-HGRCMSN (n = 600) | 0 | 0 | 26 | 51 | 101 | 227 | 130 | 61 | 9 | 5 | 9.2 | |
| Fase 3 | ||||||||||||
| HC-CMNSXXI (n = 642) | 63 | 185 | 201 | 94 | 64 | 35 | 0 | 0 | 0 | 0 | 6.0 | < 0.001* |
| SC-HGRCMSN (n = 300) | 47 | 75 | 92 | 67 | 10 | 9 | 0 | 0 | 0 | 0 | 5.8 | |
| CA-HGRCMSN (n = 663) | 0 | 0 | 12 | 27 | 89 | 114 | 304 | 94 | 12 | 11 | 9.6 | |
| Totales | ||||||||||||
| HC-CMNSXXI (n = 1755) | 208 | 448 | 604 | 296 | 110 | 174 | 17 | 0 | 0 | 0 | 5.9 | < 0.001* |
| SC-HGRCMSN (n = 900) | 163 | 221 | 292 | 171 | 34 | 19 | 0 | 0 | 0 | 0 | 5.7 | |
| CA-HGRCMSN (n = 1763) | 0 | 0 | 62 | 123 | 268 | 533 | 559 | 175 | 31 | 22 | 9.3 | |
HC-CMNSXXI = Hospital de Cardiología, Centro Médico Nacional Siglo XXI, SC-HGRCMSN = Servicio de Cardiología, Hospital General Regional “Carlos MacGrégor Sánchez Navarro”, CA-HGRCMSN = Clínica de Anticoagulación, Servicio de Hematología, Hospital General Regional “Carlos MacGrégor Sánchez Navarro”.
*CA-HGRCMSN versus los otros grupos.
Los TRT obtenidos en las tres sedes clínicas durante las tres fases del estudio, así como los datos acumulados resultantes se ilustran en la Figura 1, paneles A-D. Cada panel muestra los datos obtenidos para el INR deseado: 2.0-3.0, 3.5-4.5 o 2.5-3.5.
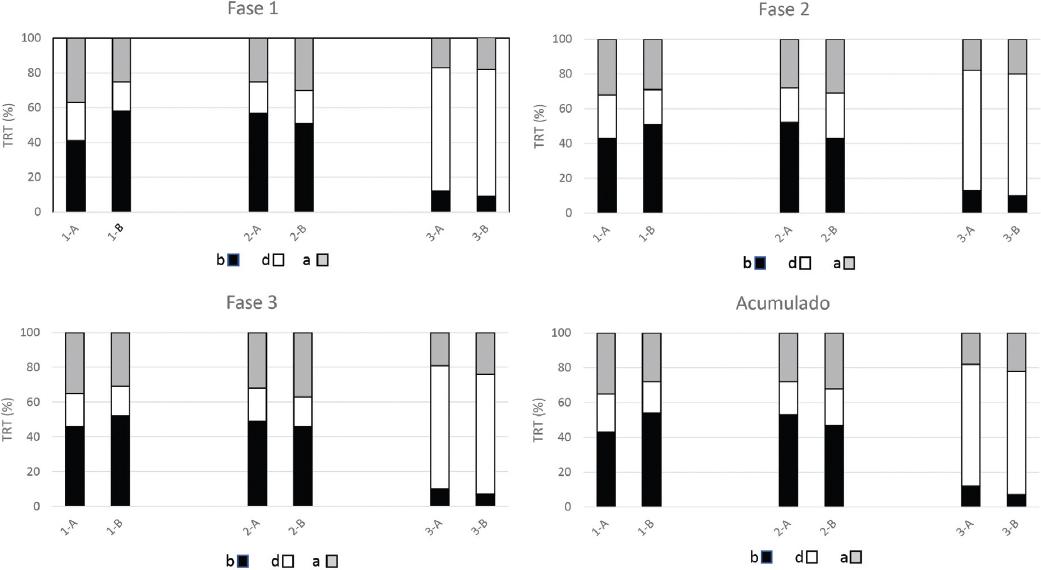
Figura 1 TRT obtenidos en los diferentes servicios clínicos durante las tres fases del estudio y los datos acumulados. 1. Hospital de Cardiología, Centro Medico Nacional Siglo XXI; 2. Servicio de Cardiología, Hospital General Regional “Carlos MacGrégor Sánchez Navarro”; 3. Clínica de Anticoagulación, Servicio de Hematología, Hospital General Regional “Carlos MacGrégor Sánchez Navarro”. A) INR deseado = 2.0-3.0, B) INR deseado = 3.5-4.5/2.5-3.5. b) INR por debajo el deseado, d) INR deseado, a) INR superior al deseado.
Después de evaluar los resultados de los grupos en términos del TRT, ni la edad ni el sexo ni el tipo de AVK empleado se asociaron significativamente con los resultados obtenidos. Por el contrario, los resultados del TRT se asociaron significativamente con el número de visitas por paciente en los 12 meses de seguimiento (p = 0.001).
Discusión
La trombosis, arterial o venosa, es la principal causa de mortalidad en el mundo; en México, el panorama es similar, aunque esté mal reconocido hasta hoy por el sistema de salud. Al revisar las estadísticas, la causa de muerte final en una proporción alta de pacientes con enfermedades crónicas no transmisibles y transmisibles es una trombosis; además, también se registra como causa de morbilidad asociada a índices altos de discapacidad temporal o definitiva, parcial o completa. Evidencia creciente muestra que también afecta negativamente los resultados clínicos de otros escenarios como cáncer, periodo posparto o población pediátrica, aunque esto se desconoce o se omite frecuentemente.16 Para prevenir o tratar pacientes con riesgo de trombosis deberían prepararse más médicos de medicina interna y cirugía, aunque también de ginecobstetricia y pediatría. En el futuro cercano, un porcentaje alto de la población requerirá tratamiento antitrombótico, temporal o permanente, una realidad que debe considerarse en el diseño de estrategias públicas y privadas que promuevan y establezcan la base para atender el problema. La cuestión es, ¿estamos preparados en México para encarar este problema?
El tratamiento antitrombótico incluye antiplaquetarios, anticoagulantes y trombolíticos; los últimos se usan en escenarios agudos, mientras que los primeros dos se emplean también en la prevención y tratamiento crónicos de la trombosis. La base del tratamiento y prevención crónicos han sido los AVK, acenocumarina y warfarina, inhibidores de la producción de factores hemostáticos dependientes de la vitamina K, especialmente del factor VII, lo cual alarga el TP;17 por lo tanto, se requiere el monitoreo permanente de su efecto con el INR.17
Las ventajas principales de los AVK son su eficacia, costo bajo aparente y la reversión rápida de su efecto. No obstante, su uso se complica por diversos factores, algunos de los cuales, propios del paciente o externos a él, no son fácilmente controlables. Entre los primeros se encuentra el metabolismo de los AVK, que presenta variaciones interindividuales, además de los cambios metabólicos del mismo paciente durante el tratamiento: en la absorción, eliminación y metabolismo hepáticos.18 Por otro lado, los factores externos son frecuentes y difíciles de controlar: la dieta y contenido de vitamina K en la misma modifican el efecto del AVK, casi todos los fármacos afectan su efecto, el rango terapéutico es estrecho y se requiere un control permanente del efecto. Los factores externos inducen una adherencia pobre al tratamiento, lo que dificulta el control. Los factores propios del paciente y los externos imposibilitan proponer un esquema terapéutico o una dosis general para todos los pacientes. De tal forma, lograr la dosis exacta requiere tiempo y una relación estrecha con el paciente, a quien se debe convencer del motivo y beneficio del tratamiento.
Los anticoagulantes están entre los fármacos asociados a un grado alto de eventos adversos generando índices de hospitalización y muerte altos en el anciano, especialmente.19,20 Si se consideran los casos de sobredosificación, los AVK se asocian a 70 % de las sobredosis no intencionales e inducen 33 % de los eventos adversos asociados a medicamentos en pacientes > 50 años.21 La frecuencia de hemorragia por AVK va de 1.7 a 17 %.22,23 Al analizar las causas más frecuentes de hospitalización, consistentemente se encuentra que los AVK y antiplaquetarios son los medicamentos más asociados a hemorragia.24,25 A pesar de la utilidad de los AVK, la hemorragia es la razón principal que explica su subutilización clínica.26
La efectividad y seguridad de los AVK se relacionan fuertemente con la calidad del control, aunque ambos parámetros no dependen solo de que este se encuentre en el rango terapéutico, sino de mantenerlo el mayor tiempo posible. Sabemos que el paciente no se encuentra en niveles óptimos de anticoagulación hasta 80 % del tiempo.27 En un metaanálisis, solo 56 % de pacientes tenían INR dentro del rango deseado con TRT de apenas 61 %; en > 50 % de los pacientes ocurrieron trombosis recurrentes cuando el INR era < 2 y > 40 % de las hemorragias apareció con INR superior al rango deseado.3 Otro estudio analizó la práctica clínica rutinaria con el TRT;28 con el rango de INR deseado entre 2.0 y 3.0, 58.9 % de los pacientes presentó TRT < 65 %.28 Se mostró que el paciente con control pobre del INR tiene más riesgo de enfermedad vascular cerebral, hemorragia mayor y mortalidad por todas las causas. Los eventos adversos fueron más frecuentes al principio del tratamiento: el riesgo de enfermedad vascular cerebral isquémica en los primeros cuatro meses se asoció a TRT < 65 %, mientras que la variedad hemorrágica no cambió con TRT < 65 %, pero sí con TRT > 65 %.28
El TRT es el porcentaje del tiempo en el cual el INR se mantiene dentro del rango terapéutico, un parámetro eficiente de la calidad del manejo con AVK.11,12,29-31 No evalúa pacientes individuales (esto lo hace el INR), sino que analiza críticamente la calidad de la anticoagulación de un servicio clínico, hospital o sistema de salud.11,12,29-31 Nosotros usamos el TRT para evaluar, por primera vez en México, la calidad de la anticoagulación con AVK.
Antes, los estudios con AVK se enfocaban en metas prácticas como el monitoreo clínico o por laboratorio o las estrategias para revertir su efecto.15 Hoy sabemos que la eficacia del sistema de monitoreo es mundialmente muy pobre por factores que incluyen el desinterés de la mayoría de los médicos que indican estos medicamentos. Hace tiempo se mostró que la mejor manera de controlar bien los AVK era crear clínicas de anticoagulación, estrategia casi ausente en México.
Para disminuir las complicaciones asociadas a los AVK, se sugiere que el control debe hacerse en estas clínicas ya que, por ejemplo, la frecuencia de hemorragia disminuye casi 40 %.32 Los datos de nuestro estudio muestran que el TRT obtenido en una clínica de anticoagulación es superior al de un servicio clínico regular. Aunque el TRT disminuye con el tiempo,33,34 en este estudio no hallamos esta tendencia entre los grupos analizados, hecho clave en la Clínica de Anticoagulación, ya que la calidad se mantuvo sostenidamente (Figura 1). El enfoque actual de las clínicas de anticoagulación no es solo el control de AVK sino también el de los demás anticoagulantes y antiplaquetarios; además, estas clínicas deben promover, debatir y asesorar acerca del mejor uso de antitrombóticos, incluidos los trombolíticos. Por esto, el nombre propuesto ahora para estos servicios es clínicas antitrombóticas, concepto que expande su espectro de acción.
Los resultados de nuestra investigación fueron independientes de las características generales de la población analizada (principalmente edad y sexo) y no se asociaron con un AVK específico, contrario a lo informado previamente.35 Este hallazgo es importante porque en México existe una creencia generalizada de que la warfarina es superior en la práctica clínica. Hace tiempo se demostró que un factor crítico para lograr una anticoagulación exitosa con AVK era la frecuencia del monitoreo, cuyo periodo ideal es cada cuatro a seis semanas, estrategia que permite una vigilancia estrecha y evita nuevas trombosis o hemorragias. Nuestros resultados muestran que un determinante clave del éxito de la Clínica de Anticoagulación es la frecuencia de las citas, nunca más allá de seis semanas. Consideramos necesario implementar clínicas de anticoagulación en los hospitales de segundo y tercer nivel en el sistema de salud, un paso que podría elevar la calidad de la atención del paciente y disminuir el costo institucional secundario a nuevos episodios trombóticos o hemorrágicos debidos a una anticoagulación pobre.
Nuestro estudio tiene limitaciones. Debido a las características de los pacientes de cada grupo, los TRT obtenido podrían explicarse por las diferencias significativas asociadas a la indicación para anticoagular. La diferencia elevada en los TRT entre los servicios podría deberse, en parte, a la diferencia de los INR deseados (rangos altos y bajos); sin embargo, quizá tales diferencias se deban a los criterios más estandarizados para la decisión terapéutica en una clínica de anticoagulación. Esto no es una sorpresa, ya que la mayoría de los hospitales de nivel alto en países desarrollados tiene clínicas de anticoagulación que logran TRT elevados. Desafortunadamente, excepto por algunos hospitales, dichas clínicas no existen en México.
Conclusión
Debido a que la incidencia de las trombosis aumenta en casi todas las áreas de la medicina en una población que está envejeciendo, parece obligatorio comenzar a concebir una estrategia eficiente y ahorradora que permita ofrecer un mejor tratamiento antitrombótico a millones de mexicanos que están ya expuestos o que estarán a los factores de riesgo tromboembólico en el futuro cercano. Indudablemente, la creación de clínicas antitrombóticas es una alternativa real para resolver este pendiente importante del sistema de salud mexicano.











 text new page (beta)
text new page (beta)


