Services on Demand
Journal
Article
Indicators
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Gaceta médica de México
On-line version ISSN 2696-1288Print version ISSN 0016-3813
Gac. Méd. Méx vol.142 n.1 Ciudad de México Jan./Feb. 2006
Artículo original
Analgesia preventiva postoperatoria con dexmedetomidina en hernioplastia inguinal
Dexmedotomidine as preventive postoperative analgesia in inguinal hernioplasty
R. Del Angel García,a* A. Castellanos Olivaresb y C. Munguia Mirandac
a Hospital General de Zona 68, Instituto Mexicano del Seguro Social, Tulpetlac, Edo. De México.
b Hospital de Especialidades Bernardo Sepúlveda, Centro Médico Nacional Siglo XXI, México, D.F.
c Coordinación Delegacional de Investigación Médica, Delegación 15 Estado de México, Instituto Mexicano del Seguro Social.
Recibido en su versión modificada: 29 de junio del 2005
Aceptado: 11 de julio del 2005
*Correspondencia y solicitud de sobretiros:
Dr. R. Del Angel García.
Departamento de Anestesiología, Hospital General de Zona 68, Instituto Mexicano del Seguro Social,
Antigua Carretera México–Pachuca Km. 19.5,
Tel. 5776–7331
Tulpetlac, Estado de México.
Resumen
Antecedentes: La analgesia preventiva es obtenida por antagonistas de aspartato y glutamato, neurotransmisores liberados por lesión tisular.
Objetivo: Valorar analgesia preventiva con dexmedetomidina y consumo de analgésicos en postanestesia.
Material y Métodos: Previa aceptación del protocolo y obtención de carta de consentimiento informado, se incluyeron pacientes, de sexo masculino, de 20 a 65 años aleatorizados a tres grupos para uso de dexmedetomidina como analgesia preventiva en hernioplastia inguinal.
Resultados: Se obtuvo promedio de edad, 45.3 ± 13.2 años. De los pacientes a los que se administró dexmedetomidina, previo a la anestesia, tres tuvieron: frecuencia cardiaca inferior a 60 lpm y requerimiento de analgésicos de 3.14 hs. De los pacientes que se administró dexmedetomidina transanestésica, dos registraron frecuencia cardiaca inferior a 60 lpm., y requerimiento de analgésicos de 2.27 minutos. En el grupo control un paciente tuvo frecuencia cardiaca de 43 lpm, con promedio de aplicación de analgésico fue de 39 minutos. No hubo variaciones significativas de la presión arterial en los tres grupos. Para el análisis estadístico se usó ANOVA, y T Student de muestras pareada dependientes para valorar analgesia y consumo de analgésico con p< 0.001
Conclusiones: La dexmedetomidina aplicada vía intravenosa previo a la anestesia, disminuyó la intensidad del dolor y consumo de analgésicos en el periodo postoperatorio.
Palabras Clave: Analgesia, preventiva, anestesia, dexmedetomidina
Summary
Background: Preemptive analgesia, is obtained via aspartate antagonists and glutamate, neurotransmitters released during tissular injury. Objective Asses preemptive analgesia with dexmedetomidine and consumption of a postanesthesia analgesic.
Material and methods: Male patients, 20–65 years ago were recruited after protocol review and informed consent was obtained. Patients were randomized in three groups, using dexmedetomidine as preemptive analgesia in inguinal hernioplasty.
Results: Subjects had a mean age of 45.3± 13.2 yrs. Among patients where dexmedetomidine was administered prior to anesthesia, three had, low heart frequency (60 bpm) and required that analgesia be given for 3.14 hrs. Among patients in whom dexmedetomidine was administered during transanesthesia, two registered low heart frequency (60 bpm.) and required analgesia for 2.27 hrs. In the control group, one patient had a heart frequency of 43 bpm; mean analgesic administration time was 39 minutes. There were no significant variations in arterial pressure. Statistical analysis included Anova, and Student's T–test to assess analgesia and initial time of analgesia consumption at p < 0.001.
Conclusion: Intravenous dexmedetomidine administered prior to anesthesia decreases pain intensity and consumption of postoperative analgesia.
Key words: Analgesia, preemptive, anesthesia, dexmedetomidine
Introducción
El dolor es una complicación en el proceso de recuperación postoperatoria.1 Asociado a la lesión quirúrgica se produce hiperalgesia, por sensibilización periférica y central. La analgesia preventiva, se obtiene por antagonistas de receptores de aspartato y glutamato, neurotransmisores liberados por lesión tisular. Se han usado antagonistas α2 adrenérgicos, como dexmedetomidina, por la alta selectividad en producir sedación, analgesia y ansiolisis; reduciendo así los requerimientos de analgésicos y anestésicos. La administración de analgésicos previo a la incisión quirúrgica, baja la percepción e intensidad del dolor postoperatorio, debido a cambios en la función neural central, se presume son efectos inducidos por la incisión quirúrgica y otras entradas nocivas durante la operación quirúrgica. Estudios realizados entre 1970–1980 informan que 45–75% de los pacientes hospitalizados, experimentaron altos niveles de dolor, con intensidad de moderado a severo en cirugía ginecológica, y general, por: subestimar, submedicar o exagerar la intensidad del dolor, adicción, y efectos adversos de la analgesia y factores demográficos.
El propósito del presente estudio; es valorar si la dexmedetomidina aplicada por vía intravenosa previo a la anestesia disminuye la intensidad del dolor postoperatorio.
Antecedentes Científicos
El dolor es una complicación en el proceso de recuperación posquirúrgica, se presenta aún con el uso de analgésicos previos a la anestesia o después de la cirugía.1
Diversos estudios realizados entre 1970 y 1980 informan que 45–75% de los pacientes hospitalizados, experimentaron altos niveles de dolor, con intensidad de moderado a severo.2
La administración de analgésicos previo a la incisión quirúrgica, ocasiona una baja percepción de la intensidad del dolor postoperatorio y reduce los requerimientos de analgésicos. Por cambios en la función neural central, se presume que son subyacentes a los efectos inducidos por la incisión quirúrgica y otras entradas nocivas durante la cirugía.3
El dolor en la periferia es detectado por dos tipos de neuronas, las fibras C y fibras A delta. Cuando el tejido es lesionado, se liberan aminoácidos excitadores como aspartato o glutamato, los cuales estimulan receptores de los nervios periféricos que transmiten el estímulo a los ganglios de la raíz dorsal de la médula;4 donde la información es procesada para ser enviada hacia el sistema nervioso central a través de dos vías: espinotalámica y espinoreticular. La vía espinotálamica cruza al lado contrario de la médula por la comisura del asta anterior y asciende por los cordones anteriores y laterales hasta el tálamo. La vía espinoreticular, asciende en posición antero–interna al fascículo espinotalámico lateral. El tálamo y la sustancia reticular hacen sinapsis con la corteza parietal en los centros somato–sensoriales primarios, localizados en la región pre y postrolándica, que modifican la intensidad del dolor y envían estímulos inhibitorios vía opioide y aminérgicas, a las astas posteriores de la médula donde se liberan sustancias inhibitorias.5
Se sabe que el daño tisular asociado a lesión quirúrgica a menudo produce hiperalgesia, como respuesta exagerada a estimulación nociva y respuesta espontánea al dolor por sensibilización periférica y central.6
La analgesia preventiva, se obtiene por la acción de fármacos antagonistas de los receptores de aspartato y glutamato, neurotransmisores que son liberados durante la lesión tisular, que al unirse a sus receptores, producen hiperalgesia. Estos antagonistas de aspartato y glutamato, disminuyen la percepción del estímulo doloroso a nivel de las terminaciones nerviosas periféricas, que envían los estímulos a los ganglios posteriores de la médula, posteriormente a la sustancia gris de la médula, el estímulo es transmitido al sistema nervioso central. Del tálamo y sustancia reticular, el estímulo es enviado a la corteza cerebral, al lóbulo parietal y a la zona somato–sensitiva primaria, esta última envía respuestas inhibitorias descendentes hacia las astas posteriores de la médula a través de la vía opioide y aminérgica. En la práctica clínica, recientemente se han usado estos antagonistas por su selectividad para producir sedación, analgesia y ansiolisis, reduciendo los requerimientos de analgésicos y anestésicos.7
La dexmedetomidina es un agonista de los receptores α2 adrenérgicos, bloquea los receptores de aspartato y glutamato liberados por el tejido lesionado, por lo que es útil en analgesia preventiva.8 Se ha observado que dexmedetomidina produce sedación y analgesia, a dosis de 1 mcg/kg de peso, con una concentración plasmática de 0.6 ng/ml, proporcionando sedación, hipnosis y analgesia sin depresión respiratoria.9 El sitio de acción de la dexmedetomidina, es el locus coeruleus. Su acción analgésica es mediada por un mecanismo similar a nivel del cerebro y médula espinal. Reportes de varios experimentos han demostrado que el sitio de acción de los agonistas α2 adrenérgicos, para efectos analgésicos, es espinal.10
La dexmedetomidina tiene propiedades simpaticolíticas, disminuye la ansiedad, produce estabilidad hemodinámica, e interrumpe la respuesta al estrés. Su acción está mediada por receptores adrenérgicos α2 post–sinápticos, que a su vez actúan sobre las proteínas G inhibitorias sensibles a toxina pertusis. Los agonistas α2 adrenérgicos, son usados como analgésicos y sedantes; con acción en el núcleo del rafe magno, localizado en la región rostroventromedial de la médula, considerados una importante fuente de control descendente de las neuronas receptoras espinales del dolor.11
Su acción analgésica es debida a inhibición de la liberación de neurotransmisores excitadores en la médula espinal, donde existe gran número de excitadores α2 adrenérgicos.12
Se sabe que la información pre–operatoria al paciente, puede reducir la ansiedad del mismo, los requerimientos de analgesia y días de estancia hospitalaria.13
El dolor se ha valorado a través de la escala visual análoga, para medir la percepción del dolor y para comparar la potencia y eficacia de analgésicos.14
Material y Métodos
Previa aceptación del protocolo de estudio por el comité local de ética e investigación y habiendo obtenido una carta de consentimiento informado, considerando los principios de la Declaración de Helsinki, se procedió a reclutar pacientes masculinos para el estudio, en el periodo de junio a octubre del año 2003, con los siguientes criterios de inclusión: edad 20 a 65 años, riesgo ASA (Sociedad Americana de Anestesiología) 1–2, sanos. Se excluyeron pacientes con hipotensión arterial, hipertensión arterial, bradicardia, ingesta de analgésicos y analgésicos narcóticos previos, así como alergia al medicamento de estudio. Se calculó el tamaño de muestra de 19 pacientes por grupo, se consideró el efecto de la morfina en la literatura como analgésico, a dosis de 0.1 mg/kg de peso cada 4–6 h, como el 100%. Los pacientes fueron aleatorizados y asignados a tres grupos de 20, para uso de dexmedetomidina intravenosa para analgesia preventiva en preanestesia y postincisional, programados para hernioplastia inguinal, bajo efecto de anestesia por bloqueo peridural (BP). En sala de quirófano se realiza asepsia del dorso, se inyecta botón de anestesia con lidocaina 2 % simple, a nivel de L2–L3 con técnica de Gutiérrez, dosis de lidocaina mixta al 2%, 350 mg (50%); inserción de catéter peridural cefálico, latencia de 10 minutos aproximadamente. A los pacientes del grupo 1; 30 minutos previo a la anestesia por bloqueo peridural, se inyecta intravenosa, solución fisiológica 50 ml al 0.9 %, con 25 mcg de dexmedetomidina, para infundir en 5 a 10 minutos, de una dosis calculada de 0.6 ng/ml. como dosis estándar. Los pacientes del grupo 2, Postincisional, se les infunde dexmedetomidina 25 mcg intravenosa diluidos en solución fisiológica al 0.9% para pasar en 5 a 10 minutos. Los pacientes del grupo 3 de control, solo se aplica lidocaína al 2 % mixta en el bloqueo peridural.
Los pacientes se monitorizaron durante la anestesia, con el equipo, DATES–OHMEDA SERIE NS 4029511, para control de signos vitales: basales, transanestésicos y postanestésicos; presión arterial (PA), frecuencia cardiaca (FC), trazo de electrocardiograma (EKG) en derivación II y saturación parcial de oxígeno (Spo2), cada 5 minutos.
La intensidad del dolor fue valorada por la escala visual análoga (SVA) para requerimiento de analgésicos en el postoperatorio inmediato. Se consideraron efectos adversos del medicamento: náusea, vómitos, somnolencia, urticaria, y escalofríos. El dolor fue controlado a base de metamizol 1 gr. (a dosis de 15 mg /kg de peso), intravenoso, a requerimientos del paciente, posterior a la recuperación del efecto anestésico. El alta de los pacientes se realizó posterior a 6 h de observación postanestésica. Al ser dados de alta del servicio, se les prescribió metamizol tabletas de 0.5 gr. cada 8 horas. Se continuó seguimiento por 24 horas en su domicilio, por comunicación telefónica, para valorar intensidad del dolor postoperatorio.
Análisis estadístico
Para el análisis de las variables numéricas se utilizó el programa estadístico SPSS 9: frecuencias, promedio y rangos, así como desviación estándar. Se utilizó la prueba estadística de ANOVA de una vía para comparar promedios entre los grupos,; T de Student para muestras independientes, para valorar tiempo de analgesia y requerimientos de analgésicos, entre los grupos, siendo significativa en un intervalo de confianza del 95 % y á = 0.05.
Resultados
De los tres grupos de pacientes, se obtuvo edad promedio 45.3 ± 13,.2 años. Tiempo de cirugía de 40 ± 10.5 minutos, tiempo de anestesia: 90 ± 20 minutos. En el cuadro I se representan los signos vitales, frecuencia cardiaca y presión arterial basales, transanestésicos y postanestésicos, promedio y desviación estándar.
Tres pacientes a los que se administró dexmedetomidina previo a la anestesia, registraron frecuencias cardiacas inferiores a 60 latidos por minuto (lpm). El requerimiento promedio de analgésicos en el postoperatorio fue de 3.14 horas. por dolor leve, se controló a base de metamizol 1 gr intravenoso. No hubo cambios hemodinámicos, un paciente tuvo escalofríos, (Figura 1).
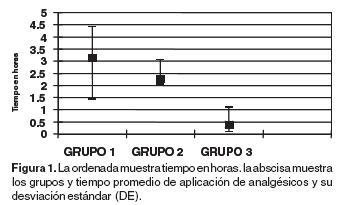
Los pacientes a los que se administró, dexmedetomidina postincisional, evolucionaron con presión arterial y frecuencia cardiaca en valores normales. Dos pacientes registraron FC menor a 60 lpm. transitoria, siendo controlados con atropina 0.2 mg intravenosa. El tiempo promedio de requerimiento de analgésicos fue de 2.27 horas. La aplicación de metamizol 1 gr. intravenoso. se realizó por dolor leve, en recuperación postanestésica. Se observó estabilidad de los signos vitales (Figura 1).
En el grupo control, la variación de los signos vitales fue mínima. Sólo un paciente tuvo una frecuencia cardiaca de 43 lpm, controlado con atropina 0.2 mg intravenosa, no refirió manifestaciones clínicas, el tiempo de soporte analgésico por dolor leve, fue de 39 minutos en recuperación postanestésica (Figura 1).
Los pacientes al término del efecto anestésico y durante el periodo de observación postanestésica durante 6 horas, evolucionaron sin complicaciones. Se excluyeron 3 pacientes: dos pacientes por aplicación de buprenorfina peridural y un paciente por midazolam intravenoso. Ningún paciente que intervino en el estudio fue excluido por efecto de anestesia deficiente. Se dieron de alta del servicio de recuperación a su domicilio con la prescripción de metamizol en tabletas de 0.5 gr. cada 8 h para control del dolor. Se valoraron los signos vitales basales con medidas de tendencia central, promedio sin diferencias. Se utilizó la prueba de ANOVA de una vía para contrastar los tiempos de aplicaciones de analgésicos, entre los grupos, sin significancia estadística. Se valoró la aplicación de analgésicos con la prueba t de Student, para muestras pareadas, entre los grupos de dexmedetomidina en preanestesia, transanestesia, comparado con el grupo control, con una p < .0001. La disminución del consumo de analgésicos fue de un 78.3 %. Considerando la aplicación de morfina a 0.6 mg/kg de peso cada 4 horas.
Discusión
Los resultados del presente estudio, demuestran los beneficios de la aplicación preincisional vs. postincisional intravenosa de dexmedetomidina en analgesia preventiva para disminuir el dolor. Como lo refieren (Paulin y cols. 002) que el dolor es una complicación postoperatoria.1 La lesión produce cambios a nivel del sistema nervioso central2 por daño asociado a lesión quirúrgica.3 Recientemente la dexmedetomidina, se ha usado por producir analgesia.4 El tiempo sin dolor, requerimiento y consumo de analgésicos en el grupo 1, fue en promedio de 3.14 horas, mayor al tiempo promedio de consumo de analgésicos del grupo 2, de 2.27 horas. y comparado con el grupo 3 de 39 minutos. Como lo refieren Yates y cols., ha sido una de las preocupaciones en los avances científicos y tecnológicos dirigidos a reducir los niveles del dolor.5
El metamizol usado como analgésico de rescate, inhibe la COX, principalmente la isoforma COX–2 (Campos y col., 1999) con disminución de la biosíntesis de prostaglandinas en tejidos periféricos, activa el sistema inhibitorio descendente endógeno de la sustancia gris periacueductal (SGPA) a nivel supraespinal, (Carlsson y col, 1986, Carlsson y Jurna, 1987) el cual es mediado por la liberación de péptidos opioides (Tortoci y col. 1996). También disminuye la actividad de fibras espinales ascendentes, (Carlsson y col, 1986, Neugebauer y col, 1994) inhibiendo la transmisión del impulso nociceptivo a nivel espinal (Vanegas y col. 1997). A nivel supraespinal modula positivamente la liberación de â–endorfinas y/o encefalinas endógenas, responsables de su acción central. Inhibe los receptores de glutamato por modulación pre y post–sináptica de la liberación y/o acción de glutamato a nivel espinal (Beirith y col, 1998). El analgésico reduce primariamente la hiperalgesia postraumática.6 Los pacientes que recibieron dexmedetomidina tuvieron mayor tiempo sin dolor en el postoperatorio. La analgesia preventiva proporcionada por dexmedetomidina protege al paciente del dolor, por efecto de la incisión quirúrgica y otros eventos perioperatorios. Actúa en el locus coeruleus donde existe gran número de receptores α2 adrenérgicos; al unirse a los receptores α2 adrenérgicos, inicia un estímulo transmembrana en los canales de K+ con la salida de K+ e inhibe el voltaje de los canales de Ca2+. La disminución de hiperpolarización de las neuronas del locus coeruleus facilita la inhibición de sus terminales, y puede ser el mecanismo de inicio de acción de dexmedetomidina,7 proyecta neuronas noradrenérgicas hacia la médula, cordón dorsolateral y el puente, donde hay receptores mu, delta, kappa. Como lo refieren (Kanda y cols.). estos antagonistas de aspartato y glutamato disminuyen la percepción del estímulo doloroso.8 (Eisenach JC y cols.) refieren que los analgésicos proveen suficiente analgesia cuando se aplican por vía sistémica, epidural o subdural.9 La dexmedetomidina a la dosis utilizada, en el presente estudio los pacientes no manifestaron sedación como lo refiere (Groeben H y cols.).10 En los pacientes de este estudio, los valores, de los signos vitales permanecieron sin cambios importantes a las cifras basales. Sin embargo, (Ruesch S y cols.) informan aumento de la presión arterial posterior a la infusión de dexmedetomidina.11 En cambio, (Wienbroun AA y cols.) informan estabilidad hemodinámica.12 En las dosis utilizadas para el estudio no hubo sedación. (Shahbaz RA y cols.) informa que logró obtener sedación sólo a dosis de 1 mµ/ kg de peso.13
Los resultados de este estudio confirman que el uso de dexmedetomidina en dosis mínimas de 6 ng/ml como dosis estándar y la información preoperatoria redujo la ansiedad de los pacientes14 y evolucionaron satisfactoriamente en el postanestésico con menor dolor y consumo de analgésicos.
Conclusión
La dexmedetomidina, aplicada vía intravenosa previa a la incisión quirúrgica, disminuye la intensidad del dolor en 78.3 % y consumo de analgésicos en el postoperatorio, comparado con el grupo control.
Agradecimientos
Al personal Médico de anestesiología, enfermería del Hospital General de Zona 68 IMSS, por su valiosa colaboración en la recolección de los datos y cuidados proporcionados a los pacientes. Al personal de la biblioteca por su valiosa ayuda para obtener información de Internet. A los Laboratorios Abbott por proporcionarme desinteresadamente el producto Dexmedetomidina para realizar el trabajo de investigación.
Referencias
1. Paulin DJ, Chen C, Penaloza DA, Polissar NL, Buckley FP. Pain as a factor complicating recovery and discharge after ambulatory surgery. Anesth Analg 2002; 95(3):627–634. [ Links ]
2. Katz, J. Brian P y cols. Preemptive Analgesia. Anesth. 1992; 77:439–446. [ Links ]
3. Celerier E, Rivat C, Jun Y, Laulin JP, Lancher A, Reynier P, Simonnet G. Long–lasting hiperalgesia induced by fentanyl in rats. Anesth 2000; 92:465–72. [ Links ]
4. Belleville JP, Denham SW, Bloor Byron C, Maze M. Effects intravenous dexmedetomidine in Humans. Anesth 1992; 77:1125–1133. [ Links ]
5. Yates P, Dewar A, Edwards HN., Fentiman B, Najman J, Richardson V, Fraser J. The prevalence and perception of pain among hospital in–patients. J Of Clin Nur 1998; 7(6):521–530. [ Links ]
6. Mikito K, Hiroaki W, Nishikawa K, Takahashi Toshiyuki T, Kozuka Y, Tomoyuki K, Keiichi O, Akiyoshi N. Different mechanisms of development and maintenance of experimental incision–induced hyperalgesia in human skin. Anesth 2002; 97(3):550–559. [ Links ]
7. Nelson LE, Lu J, Guo T, Saper CB, Franks NP, Maze M. The á2 adrenoceptor agonist dexmedetomidina converges on an endogenous sleep– promoting pathway to exert its sedative effects. Anesth 2000; 98:428–36. [ Links ]
8. Kanda T, Ohta Y, Kida A, Kemmotsu O. The effect of alpha 2 adrenergic drugs on the activity of neurons in the rat nucleus raphe magnus in vitro. Anesth analg 1999; 88(2):459–461. [ Links ]
9. Eisenach JC. ¿Preemptive Hyperalgesia, Not Analgesia? Anesth 2000; 92(2):308–309. [ Links ]
10. Groeben H, Mitzner W, Brown RH. Effects of the á2 adrenoceptor agonist dexmedetomidine on bronchoconstriction in dogs. Anesth 2004; 100:359–63. [ Links ]
11. Ruesch S, Levy, Jerrold H. Treatment of persistent tachycardia with dexmedetomidine during off pump cardiac surgery. Anesth Analg 2002; 95(2):316–318. [ Links ]
12. Wienbroun AA, Ben AR. Dextromethorphan and dexmedetomidine, new agents for the of perioperative pain. Eur J Surg 2001; 167:563–9 Internet. [ Links ]
13. Shahabaz RA, Ebert, Thomas J. The efficacy side and recovery characteristics of dexmedetomidine versus propofol when used for intraoperative sedation. Anesth Analg 2002; 95(2):461–466. [ Links ]
14. Hughes S. The effects of giving patients pre–operative information. NUR ST 2002; 16(28):33–37. [ Links ]














