Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Gaceta médica de México
versión On-line ISSN 2696-1288versión impresa ISSN 0016-3813
Gac. Méd. Méx vol.140 no.6 Ciudad de México nov./dic. 2004
Artículo de revisión
Cuidados del paciente cardiópata tras una intervención coronaria percutánea
Care for the Cardiopathy Patient after Percutaneous Coronary Interventions
Carlos Felipe Barrera–Ramírez,* Luis Ramón Pineda Pompa,* Carlos E. Guzmán*
* Servicio de Hemodinamia y Cardiología Intervencionista. Centro Hospitalario La Concepción, 28230 Saltillo, Coahuila, México.
Correspondencia y solicitud de sobretiros:
Dr. Carlos Felipe Barrera–Ramírez.
Servicio de Hemodinamia y Cardiología Intervencionista.
Centro Hospitalario La Concepción.
Blvd. V. Carranza 4036;
Saltillo, Coah., México. 28230.
Coreo electrónico: CARDIOJMAGEN@hotmail.com
Recepción versión modificada: 28 de noviembre de 2003
Aceptación: 5 de marzo de 2004
Resumen
En la actualidad, las indicaciones y alcances de la cardiología intervencionista permiten que cada vezmás pacientes puedan ser revascularizados mediante intervenciones coronarias percutáneas. Es esencial para los médicos que están en contacto o tienen a su cargo el cuidado de estos pacientes conocer los beneficios, características y riesgos del procedimiento. En este trabajo revisamos los conceptos generales actuales de la angioplastía coronaria.
Palabras clave: Angioplastía coronaria, revascularización miocárdica, intervención coronaria percutánea, stents.
Summary
At present, new indications and frontiers of interventional cardiology led to percutaneous treatment of a wide spectrum of patients who require myocardial revascularization. The physician must understand the potential benefits, procedural characteristics, andrisks of percutaneous coronary intervention. In this paper, we review general concepts concerning coronary angioplasty.
Key words: Coronary angioplasty, myocardial revascularization, Percutaneous coronary intervention, stents.
Introducción
En la actualidad, las indicaciones y alcances de la cardiología intervencionista permiten que cada vez más pacientes puedan ser revascularizados mediante intervenciones coronarias percutáneas. Nuevos desarrollos farmacológicos y técnicos, como el advenimiento de los inhibidores de la glucoproteína IIb/IIIa, sistemas de protección distal coronario, la braquiterapia y los stents liberadores de fármacos han permitido ampliar la gamma de pacientes que pueden beneficiarse de esta terapéutica. Es esencial para los médicos que están en contacto o tienen a su cargo el cuidado de estos pacientes conocer los beneficios, características y riesgos del procedimiento.
Antecedentes
Parece lejano el momento en que Werner Forssman en 1929 y siendo aún un cirujano en pleno adiestramiento, cateterizó una vena de su antebrazo y alcanzó su aurícula derecha, guiado mediante control fluoroscópico;1 es probable que nunca se imaginara el potencial diagnóstico y terapéutico que se lograría en nuestros días. Posteriormente gracias a Cournand, Ross, Seldinger, Richards y Sones, entre otros, se consolida el conocimiento de la anatomía, función y patología cardiaca.1,2
Lo que hoy por hoy es denominado cardiología intervencionista es el conjunto de técnicas de cateterismo aplicadas a la terapéutica de la enfermedad cardiaca, de este modo es posible realizar por vía percutánea, revascularizaciones coronarias y periféricas, cierre de defectos septales congénitos, tratamiento de aneurismas aórticos, oclusión de fístulas, valvuloplastías y todavía es posible el nuevo desarrollo de instrumentos que nos permitan tratar otros padecimientos.
El inicio de esta apasionante y nueva era se origina con la atrioseptostomía de Raskind en 19673 para el drenaje venoso anómalo y una década más tarde el radiólogo suizo Andreas Grüentzig desarrolla la angioplastía coronaria trasluminal percutánea (ACTP),4 que ha permitido ver un vertiginoso y portentoso desarrollo en esta área de la medicina en las últimas dos décadas.
En este breve ensayo describiremos los cuidados que deben tenerse en cuenta al manejar a pacientes en quienes se ha realizado una ACTP.
Indicaciones del procedimiento
En un inicio, y como es de suponerse, la limitada experiencia, las limitaciones en calidad y disponibilidad de equipo y materiales aptos para la intervención coronaria percutánea (ICP), obligaban al cardiólogo a ser muy selectivo al elegir a los pacientes en quines se iba a realizar una ACTP. De esta forma las indicaciones se limitaban a tratar enfermedad coronaria de un solo vaso, estenosis cortas, proximales y no complejas en pacientes refractarios a tratamiento médico. Así, sólo 5 a 10% de los pacientes portadores de cardiopatía isquémica se consideraban candidatos para una ACTP.5
Durante los primeros años de década de los ochenta la mejora tecnológica y el nuevo diseño de los catéteres guía, los balones con mejor perfil y más resistentes, alambres guías más finos y la experiencia acumulada, permiten al cardiólogo acceder con éxito a lesiones cada vez más complejas y además en situaciones agudas. Así, ahora la ACTP es un recurso que se usa en más de 50% de los pacientes que requieren revascularización coronaria, desde luego las condiciones de cada país e incluso de cada institución matizan de manera particular esta cifra y en muchos países son aceptables las intervenciones en tronco común no protegido e intervenciones multivaso. De una manera muy resumida podríamos decir que en terreno clínico la ICP se realiza en pacientes con angina estable, angina inestable, infarto agudo del miocardio e inclusive choque cardiogénico. El número de vasos a tratarya no es una limitante, se realiza ICP en injertos coronarios ya sea venosos o de arteria mamaria, y se pueden tratar lesiones largas, difusas, calcificadas, ostiales, oclusivas crónicas y agudas, en tándem, tronco común protegido o no.
Desde luego los resultados varían de acuerdo a las características del pacientes, el escenario clínico, la experiencia del operador y el volumen del centro donde se efectúan dichas ICP.
Efecto de la angioplastía coronaria en la placa de ate roma
Aunque la ACTP causa compresión de la placa de ateroma. Básicamente el procedimiento consiste en la introducción de un balón de bajo perfil sobre un alambre guíaque previamente se ha insertado en la coronaria y una vez que se posiciona el balón en el sitio de la estenosis a tratar, se infla a alta presión. El mayor cambio en la geometría y en lumensedebe a fisura de la placa, la extensión y profundidad de dichas fisuras hacia las paredes del vaso es variable, además se desencadenan respuestas inflamatorias y un proceso local de trombosis y activación plaquetaria. Este mecanismo "controlado" de lesión es el responsable de las dos mayores limitaciones de la ICP: el cierre agudo del vaso y la reestenosis.6
Evolución de los procedimientos coronarios intervencionistas
De este modo, en 1986 se introduce en la práctica clínica el usode prótesis metálicas intracoronarias, más familiarmente llamados stents, con el objetivo de controlar la disección de la íntima y evitar el retroceso elástico inicial superando así el problema de la oclusión temprana del vaso intervenido. Los estudios iniciales además demostraron fehacientemente la superioridad del implante de stents sobre la angioplastía convencional, tanto desde el punto de vista clínico como angiográfico.7–10
Desde luego el mayor talón de Aquiles de la angioplastía es la reestenosis y ya desde mediados de los ochenta se implementaron diversas técnicas de ablación de placa con el fin de disminuir la "cantidad" de tejido ateroescleroso, es así como asistimos al nacimiento de técnicas como la aterectomía rotacional y direccional, el catéter de extracción trasluminal (TEC) y el láser excimer. Sin embargo su impacto en la disminución de la reestenosis nofuetan importante, además existía el inconveniente de su compleja curva de aprendizaje, del costo y el tiempo qu ese requería para su desarrollo, y esto aunado a las grandes ventajas que demostraron los stents han ocasionadoqueen la actualidad prácticamente se hayan abandonado estos dispositivos o se han relegado a casos muy seleccionados como es el de las lesiones muy calcificadas, en que se usa la aterectomía rotacional.11–17
Realización de una intervención coronaria percutánea
Toda vez que se han evaluado los potenciales beneficios y riesgos de una ICP, se debe proporcionar al paciente la suficiente información para que entienda la importancia y trascendencia del procedimiento, sus alcances y limitaciones, de una manera clara y realista.
Una vez efectuada la coronariografía, el cardiólogo intervencionista está en posición de evaluarel riesgo de una ICP. De una manera muy general las consideramos de bajo, moderado y alto riesgo (Cuadro I), desde luego entran en juego otros factores como son el estado general del paciente, la función renal, un volumen circulatorio óptimo y un estado electrolítico apropiado y la presencia o no de otras comorbilidades.
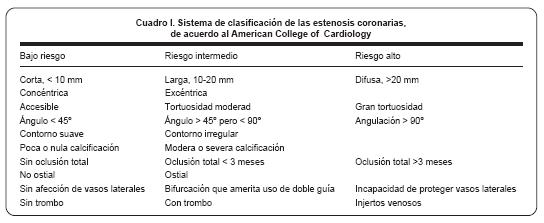
Si el paciente ha comprendido los riesgos y beneficios de procedimiento y nos ha otorgado su consentimiento mediante la firma de un documento que así lo avale, se realiza la ICP; ésta debe efectuarse en una sala de hemodinámica completa, que cuente con el equipo necesario para enfrentar posibles complicaciones, se recomienda que el procedimiento sea efectuado o por lo menos supervisado por un intervencionista de alto volumen (> 75 procedimientos anuales).
En los casos electivos se recomienda una adecuada expansión del volumen circulatorio con cristaloides previo a la ICP con el fin de evitar nefrotoxicidad; si no existe contraindicación, habitualmente con una infusión de solución salina 0.9% a razón de 75–150 cc/hr es suficiente. Recientemente se ha sugerido que otras medidas tales como la profilaxis de daño renal con N–acetilcisteína18 o fenoldopam19 pueden ser efectivas, su uso no es aún una práctica generalizada. En pacientes con disfunción ventricular izquierda podría ser necesario el usar diuréticos.
Puede o no darse un suave sedación, sobre todo en pacientes con gran ansiedad, es efectivo el Midazolam a dosis de 0.5 a 1.0 mg IV, otros narcóticos de utilidad pueden ser el Sulfato de morfina 1–2 mg IV o el Fentanil a 1–2 µg/kg IV.
Es recomendable iniciar un doble tratamiento antiagregante plaquetario lo más tempranamente posible una vez que se ha decidido realizar una ICP. El esquema más aceptado en la actualidad es una dosis de por lo menos 100 mg de ácido acetil salicílico y una dosis de carga de tienopiridinas. Durante el procedimiento se administran 100 Ul/kg de heparina no fraccionada para mantener un tiempo de coagulación activada (ACT) < 250 segundos; en muchos casos se recurre al uso de inhibidores de la glucoproteína llb/llla y en esos casos habitualmente se disminuye la dosis de Heparina a 70 UI/kg.
Es menester recordar, que la duración de una ICP, es muy variable y depende del estado clínico del paciente y de la complejidad y número de vasos o lesiones a tratar.
El acceso vascular se realiza bajo anestesia local, habitualmente con Xlocaína o Mepivacaína, siendo los sitios de abordaje más frecuentemente utilizados, la arteria femoral, la radial y en ocasiones la braquial.
Se usa un introductor arterial generalmente de 6F y se recurre al usode catéteres guías de punta suave de 6F para el sondaje selectivo de la arteria diana. Éste catéter está conectado a una pieza en Yque sirve para inyectar contraste y medir continuamente la presión intracoronaria y por el otro extremo se introducen los implementos (alambre guía, balones y stents) que ayudarán a realizar el PCI (Figura 1).
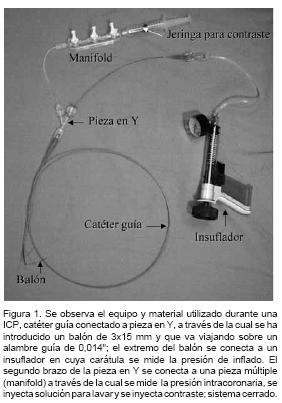
Bajo control fluoroscópico y mediante la inyección de medio de contraste se visualiza la lesión diana, una vez localizada la mejor proyección angiográfica para trabajar, se cruza el alambre guía, que tiene usualmente un diámetro de 0,014" (0,36 mm) a través de la arteria coronaria y se cruza el sitio de la estenosis, el alambre guía debe posicionarse en la parte más distal del vaso a tratar para dar el mejor soporte posible. La estenosis puede predilatarse con un balón o se dilata directamente al implantarel stent, esta decisión la toma el cardiólogo intervencionista tomando en cuenta numerosos factores. Es importante señalarque durante el inflado ya sea del balón o del stent, se está ocasionando una oclusión transitoria pero completa del vaso, generalmente por lapsos de 30 a 60 segundos, pero que en ocasiones son suficientes para ocasionar problemas hemodinámicos, angina, cambios electrocardiográficos y arritmias (Figura 2).
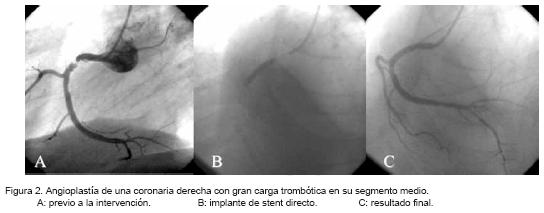
En pacientes de alto riesgo y con importante deterioro de la función contráctil del ventrículo izquierdo es apropiado considerar la instalación de un catéter de flotación previo al procedimiento, así como en casos seleccionados contarcon el apoyo quirúrgico de respaldo, lo que significa que una sala de operaciones y un equipo quirúrgico debería estar lista para intervenir de inmediato a un paciente con una ICP fallida.
Una vez concluido el procedimiento el paciente debe ir a una sala de recuperación donde haya vigilancia continua. El introductordebe retirarse porpersonal especializado una vez que el ACT es menor a 100 segundos (alrededor de cuatro horas tras la ICP) y haciendo una compresión manual directa o puede instalarse un dispositivo oclusor vascularque deja un tapón de colágena en sitio de punción. La compresión es un punto importante ya que puede ocasionarse complicaciones como hematomas, pseudoaneu–rismas o hemorragias importantes. En la actualidad, el uso rutinario de Heparina tras una ICP no se recomienda a menosque exista una indicación formal de anticoagulación, v.gr.: prótesis mecánicas, uso de balón de contrapulso, trombos intraventriculares.20
Tratamiento concomitante
Aspirina: además de los beneficios cardiovasculares reconocidos de la aspirina, este fármaco reduce también la frecuenciade las complicaciones isquémicasdespuésde la ACTP.21 El mecanismo de acción es mediante inhibición de la enzima ciclooxigenasa con la consecuente disminución en la producción de tromboxano A2 y prostaciclina. El tromboxano A2 facilita la entrada de calcio a la plaqueta permitiendo el cambio conformacional de la GP llb/llla. La dosis debe ser de al menos 100 mg al día.
Tienopiridinas: este grupo está representado por la ticlopidina y el clopidogrel. Ambos son agentes antipla–quetarios que inhiben la agregación plaquetaria inducida por ADP. Son prodrogas que el metabolismo hepático mediado por la citocromo P–450 transforma en metabolitos activos.21–24 La respuesta plaquetaria al ADP está mediada por una gran familia de receptores de nucleótido unidos a la membrana, llamados receptores P2 y que se subdividen en P2X, que están ligados a canales iónicos, y P2Y, ligados a proteína–G. Existen además diferentes subtipos de cada uno de ellos.23–25 Aunque el mecanismo de acción de las tienopiridinas no está completamente definido, se postula que antagonizan de manera no competitiva e irreversible el receptor plaquetario P2Y1 para el ADP.21–23
Numerosos estudios, cuyo análisis exhaustivo escapa del objetivo de este ensayo, han demostrado que en la actualidad el esquema de ienopiridina más seguro y efectivo es el Clopidogrel con dosis de carga de 300 mg previo a la ICP y con dosis de mantenimiento de 75 mg al día durante por lo menos cuatro semanas,26–37 aunque en la actualidad algunos estudios sugieren un mayor beneficio cuando se administra por periodos mayores hasta de un año 38–41 Los efectos secundarios más frecuentes son la diarrea (20%), eritema cutáneo (10%), y el más grave aunque afortunadamente más raro es la neutropenia quese observa en 2,5% de los pacientes y solo profunda (menos de < 450 plaquetas/µl).35,39–41
Inhibidores de la glucoproteína IIb/IIIa: a pesar del pretratamiento con aspirina, los eventos isquémicos precoces aún se siguen presentando, con incidencia que va de 3% a 12,8%. Tras la angioplastía otros potentes agonistas plaquetarios siguen presentando gran actividad, y son capaces de inducir la formación de adenosín difosfato y serotonina y con ello fomentar la expresión de receptores de GP IIb/IIIa en la superficie plaqueta ria.42–45 Una vez que se han activado dichos receptores, éstos funcionan como puentes entre las plaquetas el fibrinógeno y otras moléculas de adhesión plaquetaria y constituyen de este modo la vía común final de la formación del trombo plaquetario. De este modo es como los receptores GP IIb/IIIa se convirtieron en una diana más para el tratamiento de los síndromes coronarios agudos.41–45 En el cuadro II se enuncian los inhibidores GP llb/llla de uso más frecuente, las dosis habituales y sus principales características.
Fármacos coadyuvantes: además es habitual el uso de fármacos coadyuvantes para mitigarla isquemia miocárdica como son la Nitroglicerina que se utiliza porvía endovenosa a dosis 10–40 µg/min, se deben usarcon mucha precaución cuando hay hipotensión y compromiso del ventrículo derecho. Los betabloqueadores como el carvedilol y Metoprolol son los más habitualmente usados tras la ICP; en la sala de hemodinámica pudiese sernecesario usar Esmolol, que es el único betabloqueadorendovenoso disponible en México y que se administra en bolo (500 µg/kg) o en infusión de 25–50 µg/kg/min. Los antagonistas del calcio se usan en sala de hemodinámica porvía intracoronaria para resolveres–pasmos coronarios o el fenómeno de no–reflujo. Para los casos en que existe compromiso hemodinámico durante o tras la ICP se recurre a los agentes inotrópicos como la Norepinefrina,Fenilefrina o Dobutamina a los dosis habituales.
Cardiología intervencionista en México
Particularmente en nuestro país hasta hace poco tiempo no contábamos con datos fiables sobre este tipo de intervenciones, a pesarde que esta subespecialidad se ha consolidado como una de las ramas de la cardiología de más desarrollo. Recientemente se han dado a conocer los resultados del RegistroNacionalde Intervenciones Coronarias Percutaneas (RNICP)46 en este primer y valioso intento de iniciar un registro, se contabilizaron los datos de 536 procedimientos en 628 vasos intervenidos. En 20% de los casos se recurrió a ACTP convencional con balón y 80% restante se implantó un stent coronario. En 59% de los casos se trató de una intervención en un solo vaso, sin embargo la angioplastia multivaso no fue infrecuente, informándose 20% en dos vasos, 10% en tres vasos y 1 % en cuatro vasos. La arteria coronaria más frecuentemente tratada fue en orden decreciente la descendente anterior (40.4%), coronaria derecha (26.1%), circunfleja (15.7%) y diagonales (6%), marginales obtusas (5.6%), además de seis pacientes en quienes se intervino el tronco de la coronaria izquierda. Los resultados inmediatos reportaron éxito técnico en 95% de loscasos. En 27% de los pacientes se usó como terapia adyuvante un inhibidor de la glucoproteína IIb/IIIa. En este registro se da cuenta de 14% de complicaciones, siendo el fenómeno de no reflujo el más frecuente con una incidencia de 4.3% de los pacientes, seguido porel infarto agudo del miocardio en 2.2% de los casos, aunque no se especifica el tipo de necrosis. Una observación interesante es que a pesar del alto porcentaje de implantación del stent, el uso de tienopiridinas fue muy bajo, menos de la mitad de los pacientes recibieron dicha terapia que se considera obligada actualmente tras una ACTP con implante de stent.
No obstante las limitaciones claras que muestra este registro, en elque a pesardesernominativamente nacional, solamente incluyó laboratorios de hemodinámica del D.F. y área metropolitana, debemos llamar la atención de que representa un esfuerzo sin precedentes en la cardiología nacional. Es muy deseable que dicho registro se amplíe y perfeccione para conocer de manera más real la forma en que realizamos estas intervenciones en nuestro medio y contemos con datos fidedignos como en otros países.
Sólo por poner un ejemplo en el registro español de intervenciones coronarias durante el 2002 se informa de la realización de 34 723 ICP, contabilizadas en 95 centros con actividad en adultos.47 De las ICP realizadas, 4766 (13,7%) fueron en el contexto de infarto agudo del miocardio (ACTP primaria). En el RNCIP se informaron 150 ACTP primarias (28% de las ICP). Para poner en contexto estos datos en cuanto a la actividad intervensionista mundial, la media europea de ACTP por millón de habitantes en 1996 era de 599, en ese año España estaba por debajo de la media con 380 ICP por millón de habitantes, para el año 2000 se incrementó en 671 por millón de habitantes48 (Figura 3).
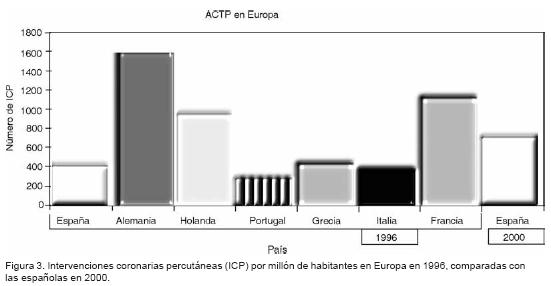
Complicaciones
Desde luego la tasa de complicaciones varía entre los distintos centros y en ello intervienen factores demográficos, elvolumendepacientesque maneja cada institución y desde luego de la experiencia del grupo médico. Actualmente se ha reconocido una disminución en la incidencia de complicaciones isquémicas intrahospitalarias de 3.6% a 1.6%.49 Las complicaciones mayores son la muerte que puede presentarse en 0.2% a 1.0% de los casos y desde luego es mayor en grupos de alto riesgo, el infarto agudo del miocardio 1.0% al 1.5%; evento vascular cerebral 0.5%, taponamiento cardiaco 0.5%, hemorragia importante 0.5%.50–57 Otras complicaciones están relacionadas al abordaje vascular y pueden ser hematomas locales, disecciones vasculares y pseudo–aneurismas o relacionadas con el mismo procedimiento como perforación coronaria, daño ocasionado con catéteres, disecciones, daño ocasionado con las guías.55
Finalmente debemos decir que, la cuidadosa selección de los casos, la modificación de factores de riesgo, una técnica óptima, la farmacoterapia adyuvante y el soporte circulatorio, entre otros factores, ayudan a minimizar los riesgos de una ICP.
El último reto a venceres la reestenosis, y en este campo los stents liberadores de fármacos citostáticos están demostrando enormes avances.58 Creemos que aún estamos en un punto, en que el los futuros desarrollos en este apasionante campo nos seguirán sorprendiendo.
El reto final... la reestenosis
Como hemos mencionado, sigue siendo el talón de Aquiles de las ICP. La reestenosis se debe a una inadecuada respuesta adaptativa de la pared vascular tras el daño producido durante la ICP, que se manifiesta principalmente por una hiperplasia intimal. Aunque existen numerosas definiciones de la reestenosis, quizá la más sencilla y ampliamente difundida es la de un decremento luminal mayor a 50% respecto al resultado final tras la ACTP. Con el advenimiento del stent, las tasas de reestenosis lograron abatirse,10 sin embargo la incidencia de reestenosis con stent está presente de 10 a 30% de los casos. En la actualidad el advenimiento de stent liberadores de fármacos ha venido a modificar dramáticamente estos resultados, aunque es un terreno todavía en estudio y sólo el tiempo y la medicina basada en evidencias podrá ayudarnos a decantar el justo sitio de estos nuevos dispositivos.
Stents liberadores de fármacos (SLF)
Se trata de stents convencionales cubiertos de un polímero que almacena y libera a dosis progresivas sustancias que inhiben el ciclo celular; los estudios iniciales han demostrado un beneficioso efecto utilizando sirolimus y paclitaxel.
Sirolimus: es un antibiótico macrólido con importantes efectos antifúngicos inmunosupresores y antimitóticos, producido por Streptomyces hygroscopicus, un actinomiceto propio de la tierra. Su acción antimitótica se debe a que impide el paso de la fase G1 del ciclo celular a la fase S (replicación del DNA).58
En el estudio piloto con 30 pacientes que recibieron SLF con liberación lenta y rápida de sirolimus, el SLF virtualmente eliminó la reestenosis59 incluso hasta los 12 meses. Posteriormente el estudio RAVEL con 238 pacientes, quienes al azar recibieron o no stent convencional vensus SLF, en el grupo que recibió SLF no hubo reestenosis binaria mientras con el stent convencional se observó en 27% de los pacientes, la pérdida luminal tardía intrastent fue de –0.01 mm con sirolimus y 0.8 mm con el stent convencional (p< 0.001).60 En la actualidad se encuentran en marcha varios estudios probando análogos de la sirolimus, como el estudio FUTURE, FUTURE II y PREFER,58 y con FK 506 (tracolimus), que es un agente inmunosupresor, antibiótico macrólido producido por Streptomyces tsukabaenesis usado para los transplantes renales y que inhibe la liberación de interleucina–2 y la activación de las células T, se realizan en este momento los estudios EVIDENT y PRESENT.58
Paclitaxel: es una molécula lipofílica derivada del árbol de tejo del Pacífico, Taxus brevifolia, capaz de inhibir la división celular.61
En el estudio TAXUS 1 se comparó stent convencional versus SLF en 61 pacientes y la pérdida tardía intra stent fue 0.71 mm contra 0.36 mm respectivamente. La incidencia de eventos adversos cardiacos mayores a un alo fue de 10% vs. 3% respectivamente. A los seis meses la reestenosis angiográfica fue de 0% versus 10%.62
El estudio TAXUS II fue un ensayo multicéntrico, triple ciegoyaleatorizadoque probó la eficacia de dos formulaciones diferentes de paclitaxel. El estudio incluyó a 536 pacientes en cuatro brazos: 267 pacientes con stent convencional (136 pacientes) o SLF de liberación lenta (131 pacientes) y 269 pacientes se trataron con stent convencional (134 pacientes) o SLF de liberación moderada (135 pacientes). Este interesante estudio demostró una reestenosis binaria de 2.3% y 4.7% en los SLF de liberación lenta y moderada respectivamente y en los grupos control de 17.9% y 20.2%.
El estudio TAXUS III incluyó a 30 pacientes con reestenosis intrastent y todos se trataron con SLF. Seis meses después la pérdida tardía intrastent fue de 0,44 mm y la reestenosis binaria de 16%.
Recientemente se publicaron los resultados del TAXUS IV, ensayo multicéntrico, aleatorizado, y doble ciego que incluyó a 1314 pacientes, 652 recibieron stent convencional y 662 pacientes recibieron SLF de liberación lenta, se hizo coronariografía de control sólo a 732 pacientes. La necesidad de revascularización del vaso diana indicada por isquemia a nueve meses fue de 12% versus4,7% respectivamente. La reestenosis angiográfica binaria fue del 26.6% contra 7.9% a favor del SLF.64
Stents liberadores de fármacos... ¿La última frontera?
Sin duda alguna, los SLF se han posicionado como la promesa más atractiva para el tratamiento percutáneo de la enfermedad arterial coronaria. Sin embargo, aún falta precisar algunas interrogantes importantes, como porejemplo si la reestenosis en verdad se abate o sólo se retrasa, si existe o no una asociación con trombosis intrastent tardía o con la formación de aneurismas coronarios, la duración más apropiada del tratamiento concomitante con tienopiridinas que deben recibirlos pacientes tras el implante de un SLF, e inclusive determinar con estudios comparativos que diseño y fármaco son más convenientes para la elaboración de estos nuevos dispositivos. Aún no sabemos el efecto local y sistémico que podría ocasionar el implante de varios SLF en un mismo paciente,65 tampoco sabemos cuál es la mejor forma de tratar la reestenosis en un SLF,65 ni tampoco sabemos si en un paciente tratado previamente con braquiterapia podemos usar con seguridad un SLF.66 Otro punto importante que es menester mencionar, es el importante impacto económico que los SLF representan, en la actualidad estos dispositivos pueden alcanzar costos entre 2000 y 3000 dólares, casi tres veces mayor que el del stent convencional.66,67
Finalmente debemos enfatizar que los pacientes incluidos en los ensayos multicéntricos son pacientes cuidadosamente seleccionados bajo estrictos criterios de inclusión y exclusión, y no es fácil extrapolar los resultados a población abierta, lo que se conoce como "el mundo real", aunque poco a poco tendremos a nuestra disposición información sobre los resultados iniciales68 de los SLF usados de forma más generalizada en pacientes con anatomía menos favorable.
En un intento por tratar de unificar criterios, algunos autores han tratado de esbozar y sugerir los escenarios clínicos en que los SLF pueden ser utilizados (cuadro III).67
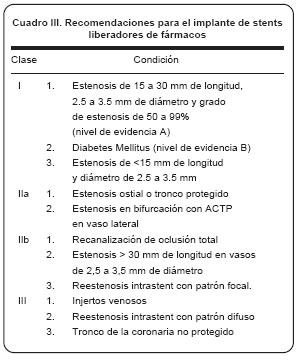
El péndulo esta en movimiento y sólo las pruebas aportadas por la medicina basada en la evidencia ayudarán, seguramente en futuro muy cercano, a encontrar el justo medio en cuanto a costo–beneficio y seguridad, para optimizar el uso de estos nuevos dispositivos.
Referencias
1. Forssman W, Klin Worach; 1929. Citado en: Martínez–Ríos MA, Gil Moreno M, Turnero G, Galante CJ, Gutiérrez Fuster E, editores. Generalidades del cateterismo cardíaco. En: Martínez–Ríos E, editor. Cateterismo cardíaco. Diagnóstico y tratamiento de la cardiópatas. México: Ed. Trillas; 1990. pp. 19–38. [ Links ]
2. Martínez–Ríos MA, Gil Moreno M, Turnero G, Galante CJ, Gutiérrez Fuster E. Generalidades del cateterismo cardíaco. En: Martínez–Ríos E, editor. Cateterismo cardíaco. Diagnóstico y tratamiento de las cardiopatías. México; Ed.Trillas; 1990. pp. 19–38. [ Links ]
3. Delcán JL. Del cateterismo diagnóstico a la cardiología intervencionista. MApfre Med 1995; 6 (Supl II):7–8. [ Links ]
4. Grüentzig AR. Traslumination dilatation of coronary artery stenosis. Lancet 1978; l:263. [ Links ]
5. García EJ. Utilidad clínica del stent coronario. Mapfre Med 1995; 6(Supl II):28–36. [ Links ]
6. Topol EJ, Serruys PW. Frontiersin interventional cardiology. Circulation 1998;98:1802–20. [ Links ]
7. Serruys PW, Strauss BH, van Beusekom HM, van der Giessen WJ. Stenting of coronary arteries: has a modern Pandora's box been opened? J Am Coll Cardiol 1991;17(6SupplB):143B–154B. [ Links ]
8. Serruys PW, Strauss BH, Beatt KJ, Bertrand ME, Puel J, Rickards AF. Angiographic follow–up after placement of a self–expanding coronary–artery stent. N EnglJ Med 1991 ;324:13–17. [ Links ]
9. Fischman DL, Leon MB, Bairn DS, Schatz RA, Savage MP, Penn I, et al. A randomized comparison of coronary–stent placement and balloon angioplasty in the treatment of coronary artery disease. Stent Restenosis Study Investigators. N Engl J Med 1994;331:496–501. [ Links ]
10. Serruys PW, de Jaegere P, Kiemeneij F, Macaya C, Rutsch W, Heyndrickx G, et al. A comparison of balloon–expandable–stentimplantation with bal loon angioplasty in patients with coronary artery disease. Benestent Study Group. N Engl J Med 1994;331 (8):489–495. [ Links ]
11. Macaya C, Iñiguez RA, Goicolea RJ. Papel de la aterectomía coronaria (de Simpson, de extracción y de rotación en la revascularización miocárdica) Mapfre Med 1995; Supl 11:15–27. [ Links ]
12. Grech ED. Percutaneous coronary intervention. I: History and development. Br Med J 2003:326:1080–82. [ Links ]
13. Linnemeier TJ. The hot and cold issues of laser angioplasty. Cathet Cardiovasc Diag 1992;27:1–4. [ Links ]
14. Margolis JR, Menta S. Excimer laser coronary angioplasty. Am J Cardiol 1992;69:3F–11F. [ Links ]
15. Warth DC, Leon MB, O'Neill W, Zacea N, Polissar NL, Buchbinder M. Rotational atherectomy multbenter registry: acute results, complicationsand 6–month angiographic follow–up in 709 patients. J Am Coll Cardiol 1994;24:641–648. [ Links ]
16. Jain D.SchaferU, Debdorfer A, Kurz T, Lindemann C, Tolg R,etal. Neurohumoral activation in percutaneous coronary interventions: apropos of ten vasoactive substances during and immediately following coronary rotastenting. Indian Heart J 2001: 53:301–307. [ Links ]
17. Brogan WC III, Popma JJ, Pichard AD, Satler LW, Kent KM, Mintz GS, et al. Rotational coronary atherectomy after unsuccessful coronary balloon angioplasty. Am J Cardiol 1993: 71:794–798. [ Links ]
18. Solomon R, Werner C, Mann D, Elia J, Silva P. Effects of saline, manitol and furosemide to prevent acute decrease in renal function induced by radiocontrast agents. N EnglJ Med 1994;331:1416–420. [ Links ]
19. Stevens MA, McCullough PA, Tobin KJ, Speck JP, Westveer DC, Guido–Allen DA, et al. A prospective randomized trial of prevention measures in patients at high risk for contrast nephropathy: results oft he PRINCE Study. Prevention of radiocontrast induced nephropathy clinical evaluation. J Am Coll Cardiol 1999;33:403–411. [ Links ]
20. Barrera–Ramírez CF, Jiménez–Mazuecos J, Alfonso F. Apical thrombus associated with left ventricular apical ballooning. Heart 2003;89:927. [ Links ]
21. Kam PC, Nethery CM. Thethienopyridine derivatives (platelet adenosine diphosphate receptor antagonists), pharmacology and clinical developments. Anaesthesia 2003:58:28–35. [ Links ]
22. QuinnMJ, Fitzgerald DJ. Ticlopidine and clopidogrel. Circulation 1999; 100:1667–16672. [ Links ]
23. Jin J, Daniel J, Kunapuli S. Molecular basis for ADP induced platelet aggregation: the P2Y1 receptor mediates ADP–induced intracellular calcium mobilization and shape change in platelets. J Biol Chem. 1998; 273:2030–2034. [ Links ]
24. Leon MB, Bairn DS, Popma JJ, Gordon PC, Cutlip DE, Ho KK, et al. A clinical trial comparing three antithrombotic–drug regimens after coronary–artery stenting. Stent Anticoagulation Restenosis Study Investigators. N Engl J Med 1998;339:1665–1671. [ Links ]
25. Schomig A, Neumann FJ, Kastrati A, Schuhlen H, Blasini R, Hadamitzky M, et al. A randomized comparison of antiplatelet and anticoagulant therapy after the placement of coronary–artery stents. N Engl J Med 1996;334:1084–1089. [ Links ]
26. Urban P, Macaya C, Rupprecht HJ, Kiemeneij F, Emanuelsson H, Fontanelli A, et al. Randomized evaluation of anticoagulation versus antiplatelet therapy after coronary stent implantation in high–risk patients: the Multicenter Aspirin and Ticlopidine Trial after Intracoronary Stenting (MATTIS). Circulation 1998;98:2126–2132. [ Links ]
27. Bertrand ME, Legrand V, Boland J, Fleck E, Bonnier J, Emmanuelson H, et al. Randomized multicenter comparison of conventional anticoagulation versus antiplatelet therapy in unplanned and elective coronary stenting. The Full Anticoagulation versus Aspirin and Ticlopidine (FANTASTIC) Study. Circulation 1998; 98:1597–1603. [ Links ]
28. Bennett CL, Weinberg PD, Rozenberg–Ben–Dror K, Yarnold PR, Kwaan HC, Green D. Thrombotic thrombocytopenic purpura associated with ticlopidine. A review of 60 cases. Ann Intern Med 1998;128:541–544. [ Links ]
29. BennettCL, DavidsonCJ, Raisch DW, Weinberg PD, Bennett RH, Feldman MD. Thrombotic thrombocytopenic purpura associated with ticlopidine in the setting of coronary artery stents and stroke prevention. Arch Intern Med 1999; 159:2524–2528. [ Links ]
30. Steinhubl SR, Tan WA, Foody JM, Topol EJ. Incidence and clinical course of thrombotic thrombocytopenic purpura due to ticlopidine following coronary stenting. EPISTENT Investigators. Evaluation of Platelet IIb/IIIa Inhibitor for Stenting. JAMA 1999; 281:806–810. [ Links ]
31. Barrera–Ramírez CF, Fernández–Ortiz A, Angiolillo DJ, Bernardo E, Viveros M, Fantidis P, Soto H, Alfonso F, Escaned J, Macaya C. Baseline platelet function in low responders to antiplatelet treatment following coronary stent implantation. Circulation 2002 November; 106(19) Suppl 11:517. [ Links ]
32. Kolansky DM, Klugherz BD, Curran SC, Herrmann HC, Magness K, Wilensky RL, et al. Combination therapy with clopidogrel and aspirin after coronary stenting. Catheter Cardiovasc Interv 2000;50:276–279. [ Links ]
33. Bhatt DL, Bertrand ME, Berger PB, L'Allier PL, Moussa I, Moses JW. Meta–analysis of randomized and registry comparisons of ticlopidine with clopidogrel after stenting. J Am Coll Cardiol 2002;39:9–14. [ Links ]
34. Muller C, Buttner HJ, Petersen J, Roskamm H. A randomized comparison of clopidogrel and aspirin versus ticlopidine and aspirin afterthe placement of coronary–artery stents. Circulation 2000;101:590–593. [ Links ]
35. Bertrand ME, Rupprecht HJ, Urban P, Gershlick AH. Investigators FT. Double–blind study of the safety of clopidogrel with and without a loading dose in combination with aspirin compared with ticlopidine in combination with aspirin after coronary stenting: the Clopidogrel Aspirin Stent International Cooperative Study (CLASSICS). Circulation 2000; 102:624–629. [ Links ]
36. Steinhubl SR, Lauer MS, Mukherjee DP, Moliterno DJ, Lincoff AM, Ellis SG, et al. The duration of pretreatment with ticlopidine prior to stenting is associated with the risk of procedure–related non–Q–wave myocardial infarctions. J Am Coll Cardiol 1998;32:1366–1370. [ Links ]
37. Steinhubl SR, Ellis SG, Wolski K, Lincoff AM, Topol EJ. Ticlopidine pretreatment before coronary stenting is associated with sustained decrease in adverse cardiac events: data from the Evaluation of Platelet llb/llla Inhibitor for Stenting (EPISTENT) Trial. Circulation 2001; 103:1403–1409. [ Links ]
38. Berger PB. Results of the Ticlid or Plavix Post–Stents (TOPPS) Trial: do they justify the switch from ticlopidine to clopidogrel after coronary stent placement? Curr Control Trials Cardiovasc Med 2000;1(2):83–87. [ Links ]
39. Mehta SR, Yusuf S, Peters RJ, Bertrand ME, Lewis BS, Natarajan MK, et al. Effects of pretreatment with clopidogrel and aspirin followed by long–term therapy in patients undergoing percutaneous coronary intervention: the PCI–CURE Study. Lancet 2001 ;358:527–533. [ Links ]
40. Yusuf S, Zhao F, Mehta SR, Chrolavicius S, Tognoni G, Fox KK, et al. The Clopidogrel in Unstable Angina to Prevent Recurrent Events Trial Investigators. Effects of clopidogrel in addition toaspirin in patients with acute coronary syndromes without ST–segment elevation (CURE). N Engl J Med 2001; 345:494–502. [ Links ]
41. Steinhubl SR, Berger PB, Mann JT 3rd, Fry ET, DeLago A, Wilmer C, Topol EJ. Early and sustained dual oral antiplatelet therapy following percutaneous coronary intervention: a randomized controlled trial (CREDO). JAMA 2002; 288:2411 –2420. [ Links ]
42. Ross R. The pathogenesis of atherosclerosis– an update. N Engl J Med 1986;314:488–500. [ Links ]
43. Cassar K, Bachoo P, Brittenden J. Plaque rupture, thrombosis, andtherapeutic implications. Haemostasis 1996;Suppl 4:269–284. [ Links ]
44. Lecompte T. Thrombogenese arterielle: le role decisif des plaquettes. Arch Mai Coeur Vaiss 2002; 95(Spec No 7):7–9. [ Links ]
45. Flores NA. Las plaquetas y la enfermedad cardiaca: ¿Cuánto más puede la ciencia básica influir en la práctica clínica? Arch Inst Cardiol Mex 2000;70:213–218. [ Links ]
46. De la Llata Romero M, Vargas CM, Magaña Serrano JA, Leal CC, Férez Santander S, Lupi Herrera E, et al. El Registro Nacional de las Intervenciones Coronarias Percutáneas (RNCIP). Arch Cardiol Mex 2003;73:304–312. [ Links ]
47. Hernández JM, Goicolea J, Duran JM, Auge JM. Resgistro español de hemodinámica y cardiología intervensionista. XII Informe oficial de la sección de hemodinámica y cardiología intervensionista de la Sociedad Española de Cardiología. Rev Esp Cardiol 2003; 56:1105–1118. [ Links ]
48. Hernández JM, Goicolea J, Duran JM, Auge JM. Registro de actividad de las secciones de hemodinámica y cardiología intervencionista de la sociedad española de cardiología. Rev Esp Cardiol 2001; 54:1426–438. [ Links ]
49. Harrell L, Schunkert H, Palacios I. Risk predictors in patients scheduled for percutaneous coronary revascularization. Cathet Cardiovasc Interv 1999; 48:253–60. [ Links ]
50. Barrera–Ramírez CF, Oseguera J. Taponamiento cardíaco. En: Manual de Urgencias del Instituto Nacional de la Nutrición Salvador Zubirán. México, D.F.: McGrawHill; 2000. p. 927. [ Links ]
51. Grech ED. Percutaneous coronary intervention. II: The procedure. Br Med J 2003; 326:1137–1140. [ Links ]
52. Kimmel SE, Berlin JA, Laskey WK. The relationship between coronary angioplasty procedure volume and major complications. JAMA 1995;274:1137–42. [ Links ]
53. Esplugas Oliveras E, Hernández Antolín R, López Béseos L, Moreu Burgos J, Pomar Moya–Prats JL. The performance of coronary angioplasties at centres without cardiac surgery. The Recommendations of the Sociedad Española de Cardiología. Rev Esp Cardiol 1999;52:5–12. [ Links ]
53. Martínez–Ríos MA, Eid–Lidt G, Luna Guerra J, Villavicencio Fernández R, Ban Hayashi E, et al. The benefit of a coronary stent in the reduction of major cardiac complications in acute coronary síndromes. Arch Inst Cardiol Mex 1999;69:121–6. [ Links ]
54. Alfonso F, Flores A, Escaned J, Sanmartín M, Hernández R, Fernández–Ortiz A, Bafluelos C, et al. Pressure wire kinking, entanglement, and entrapment during intravascular ultrasound studies: a potentially dangerous complication. Catheter Cardiovasc Interv 2000;50:221–5. [ Links ]
55. Soriano J, Alfonso F, Cequier A, Moris C. The Registry of the Activities of the Hemodynamics and Interventional Cardiology Section in 1998. Rev Esp Cardiol 1999; 52:1105–20. [ Links ]
56. Gaspar J, Ban Hayashi E, Villavicencio R, de la Garza PJ, Gil GM, Martínez–Ríos MA. Theprimary outcome intransluminal coronary angioplasty:therecent experience of the lnstituto Nacional de Cardiología (1991–1992).Archlnst Cardiol Mex 1992; 62:499–505. [ Links ]
57. Morice MC, Serruys PW, Sousa JE, Fajadet J, Ban Hayashi E, Perin M, et al. A randomized comparison of a sirolimus–eluting stents with a standard stent for coronary revascularization. N Engl J Med 2002; 346:1773–1780. [ Links ]
58. Sousa JE, Serruys PW, Costa MA. New frontiers in cardiology. Drug–eluting stents: Part 1. Circulation 2003; 107:2274–2279. [ Links ]
59. Sousa JE, Costa MA, Abizaid A, Abizaid AS, Feres, Pinto IM, et al. Lack of Neointimal Proliferation after Implantation of Sirolimus–Coated Stents in Human Coronary Arteries: A Quantitative Coronary Angiography and Three–Dimensional Intravascular Ultrasound Study. Circulation 2001 Jan 16; 103(2):192–195. [ Links ]
60. Morice MC, Serruys PW, Sousa JE, Fajadet J, Ban Hayashi E, Perin M, et al. A randomized comparison of a sirolimus–eluting stent with a standard stent for coronary revascularization. N Engl J Med 2002 Jun 6;346(23):1773–1780. [ Links ]
61. Bhargava B, Karthikeyan G, Abizaid AS, Mehran R. New approaches to preventing restenosis. Br Med J 2003 Aug 2;327(7409):274–279. [ Links ]
62. Grube E, Silber S, Hauptmann KE, Mueller R, Buellesfeld L, Gerckens U, et al. TAXUS I: six– and twelve–month results from a randomized, double–blind trial on a slow–release paclitaxel–eluting stent for de novo coronary lesions. Circulation. 2003 Jan7; 107(1):38–42. [ Links ]
63. Tanabe K, Serruys PW, Degertekin M, Guagliumi G, Grube E, Chan C, et al. Chronic arterial responsesto polymer–controlled paclitaxel–eluting stents: comparison with bare metal stents by serial intravascular ultrasound analyses: data from the randomized TAXUS–II trial. Circulation 2004 Jan 20; 109(2):196–200. [ Links ]
64. Stone GW, Ellis SG, Cox DA, Hermiller J, O'Shauhnessy C, Mann JT, et al. A polymer–based, paclitaxel–eluting stent in patients with coronary artery disease. N Engl J Med 2004; 350:221–231. [ Links ]
65. Kereiakes DJ. Hippocratesrevisited. Theevidencefordrug–eluting stents. Circulation 2003; 1073012–14. [ Links ]
66. Angiolillo DJ, Sabate M. Paasato, presente e futuro della brachiterapia intracoronarica. Ital Heart J Suppl 2003; 4:794–796. [ Links ]
67. O'Neill WW, Leon MB. Drug–eluting stents. Costsversusclinical benefit. Circulation 2003; 107:3008. [ Links ]
68. Lemos PA, Serruys PW, van Domburg RT, Saia F, Arampatzis CA, Hoye A, et al. Unrestricted utilization of sirolimus–eluting stents compared with conventional bare stent implantation in the "real world": the Rapamydn–Eluting Stent Evaluated at Rotterdam Cardiology Hospital (RESEARCH) Registry. Circulation 2004 Jan 20; 109(2):190–195. [ Links ]














