Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Archivos de cardiología de México
versión On-line ISSN 1665-1731versión impresa ISSN 1405-9940
Arch. Cardiol. Méx. vol.78 no.1 Ciudad de México ene./mar. 2008
Investigación clínica
Evaluación del efecto de carvedilol en niños con cardiomiopatía dilatada
Evaluation of the effect of Carvedilol in children with dilated cardiomyopathy
Norma Alicia Balderrábano Saucedo,* Alfredo Vizcaíno Alarcón,* Gonzalo Espinosa Islas,* Lorenzo Reyes De La Cruz*
* Hospital Infantil de México Federico Gómez.
Correspondencia:
Dra. Norma Alicia Balderrábano Saucedo.
Dr. Márquez Núm. 162, Col. Doctores,
06720. México, D.F.
Teléfonos: 52289917 ext. 1307,
0445591970283 (celular).
Recibido: 29 de marzo de 2007
Aceptado: 25 de septiembre de 2007
Resumen
Objetivo: Evaluar el efecto del carvedilol administrado durante 8 meses a niños con disfunción ventricular izquierda secundaria a cardiomiopatía dilatada.
Material y métodos: Se administró carvedilol a los pacientes con cardiomiopatía dilatada que presentaron persistentemente una fracción de eyección baja (< 40%) a pesar de haber recibido el tratamiento habitual para la insuficiencia cardíaca. Se evaluó en ellos la función ventricular izquierda sistólica y diastólica basal y a los 4 y 8 meses después de iniciado el tratamiento con carvedilol.
Resultados: Se incluyeron 19 pacientes, 10 mujeres, con edad media de 6.7 años y tiempo de evolución de 17 meses. La fracción de eyección aumentó significativamente después de 8 meses de tratamiento con carvedilol (m: 33.5 a 52.6%, p = 0.01) así como la fracción de acortamiento (m: 14.8 a 25.8%, p = 0.01), en tanto que, el índice de rendimiento miocárdico alterado en todos los pacientes se normalizó en 5 al final del estudio. Adicionalmente, se observó que el flujo Doppler mitral alterado en 9 pacientes se normalizó en 3 y el flujo de las venas pulmonares alterado en todos, se normalizó en 13. Sólo 1 paciente presentó efectos secundarios mínimos.
Conclusiones: El uso de carvedilol aunado al tratamiento habitual para la insuficiencia cardíaca en pacientes con cardiomiopatía dilatada, mejora la función ventricular izquierda y es bien tolerado en la edad pediátrica, con efectos secundarios mínimos.
Palabras clave: Insuficiencia cardíaca. Cardiomiopatía dilatada. Función ventricular izquierda.
Abstract
Objective: To evaluate the effect of carvedilol administrated during 8 months in children with heart failure secondary to dilated cardiomyopathy.
Methods: We initiated carvedilol in patients who, despite optimization of standard treatment, had persistent left ventricular ejection fraction < 40% and evaluated the systolic and diastolic left ventricular function before and after 4 and 8 months of treatment.
Results: 19 patients were included in the study, 10 women; median age: 6.7 years and 17 ± 12.4 months after the diagnosis. The ejection fraction improved significantly from entry to eight months (median: 33.5 to 52.6%, p = 0.01) as did the shortening fraction (m: 14.8 to 25.8%, p = 0.01). The myocardial performance index abnormal in all 19 patients became normal in 5 at the end of study. In addition mitral Doppler flow which was altered in 9 improved in 3 and pulmonary venous flow abnormal in all patients improved in 13. Only 1 patient presented minimal adverse effects.
Conclusions: Carvedilol added to standard therapy for dilated cardiomyopathy improves left ventricular function, is well tolerated, and has minimal adverse effects in childhood.
Key words: Heart failure. Dilated cardiomyopathy. Left ventricular function.
Introducción
La cardiomiopatía dilatada (CMD) es una enfermedad intrínseca del músculo cardíaco en la que están alteradas tanto su estructura como su función. Afecta primordialmente al ventrículo izquierdo aunque el ventrículo derecho puede estar también involucrado con un grado variable de dilatación y disminución de su contractilidad.
La CMD es la forma más común de cardiomiopatía, con una incidencia anual de 2 a 8 casos por 100,000 en los Estados Unidos y Europa y con una prevalencia estimada de 36 individuos afectados por 100,000 habitantes.1
La presentación clínica de la CMD es variable, desde la forma asintomática hasta la insuficiencia cardíaca grave, tromboembolia, infarto, arritmia y muerte.
La insuficiencia cardíaca (IC) por disfunción ventricular izquierda secundaria a CMD es el problema clínico más importante en los niños; cuando es grave y refractaria al tratamiento representa el motivo de referencia de por lo menos el 50% de los casos para trasplante cardíaco.2 El manejo farmacológico habitual de la IC en niños está basado en el uso de digoxina, diuréticos e inhibidores de la enzima convertidora de angiotensina. En CMD este manejo resulta con frecuencia insuficiente, teniendo que suplementarse con períodos de tratamiento aminérgico, uso de antiarrítmicos, apoyo ventricular etc.
El carvedilol es un β–bloqueador que inhibe los efectos deletéreos de la sobreestimulación adrenérgica crónica en el miocardio y mejora la función miocárdica; por su efecto bloqueador a–1 actúa como vasodilatador arterial sistémico reduciendo la postcarga ventricular. Además en el animal experimental se ha demostrado su efecto como antioxidante, agente antiproliferativo e inhibidor de citocinas pro–inflamatorias.3
En la actualidad los β–bloqueadores forman parte integral del manejo de la ic del adulto, sin embargo la experiencia clínica en los niños, en particular con carvedilol, es aún muy limitada.4–7 El objetivo de este estudio fue evaluar el efecto del carvedilol administrado dos veces al día durante 8 meses en niños con diagnóstico de cardiomiopatía dilatada idiopática.
Material y métodos
Diseño del estudio
Se realizó un estudio prospectivo en el que se administró carvedilol a niños con disfunción ventricular izquierda secundaria a cardiomiopatía dilatada. A los 0, 4 y 8 meses de tratamiento se evaluaron: la clase funcional (CF), el electrocardiograma (ECG) y la función ventricular izquierda.
Pacientes
Se incluyeron a pacientes con diagnóstico de CMD idiopática que continuaron con fracción de eyección ventricular izquierda (FEVI) persistente < 40% a pesar de haber recibido el tratamiento habitual para la IC en edad pediátrica incluyendo diuréticos, digoxina e inhibidores de la enzima convertidora de angiotensina. Se excluyeron los casos con cardiomiopatía dilatada secundaria a padecimientos sistémicos o con historia o evidencia de enfermedad vascular pulmonar, arritmia, intercurrencia de infecciones graves, insuficiencia renal o hepática, padecimientos endocrinos o miocarditis aguda. Se excluyeron los casos con CMD idiopática que habían recibido tratamiento previo con carvedilol u otro β–bloqueador así como aquéllos inestables que requirieron hospitalización y/o medicamentos por vía endovenosa para el manejo de la IC, agonistas adrenérgicos P (incluyendo inotrópicos como dopamina o dobutamina) o vasodilatadores (amrinona o milrinona) dentro de las cuatro semanas previas al inicio del estudio.
Evaluación clínica
Se realizó un examen físico completo en todos los pacientes antes de ingresar al estudio y durante el seguimiento. Aunque la clasificación de la New York Heart Association (NYHA) es la más ampliamente utilizada para la evaluación clínica de la insuficiencia cardíaca; en los pacientes en edad pediátrica se recomiendan otras escalas;8,9 para este estudio se utilizó la clasificación de Ross8 que se detalla en la Tabla I.

Manejo con carvedilol
El manejo con carvedilol se inició a 0.1 mg/kg/ día. La primera dosis del medicamento se administró junto con los alimentos en el hospital con un monitoreo estricto durante las siguientes 4 horas para determinar la tolerancia al medicamento. Los pacientes con adecuada tolerancia, se enviaron a su domicilio con carvedilol a dosis de 0.2 mg/kg/día en dos tomas y se citaron para una segunda y tercera visitas con intervalo de una semana incrementando la dosis a 0.4 mg/kg/día y 0.8 mg/kg/día respectivamente con monitoreo estricto de frecuencia cardíaca, presión arterial y ECG. Se vigilaron efectos secundarios, tolerancia al medicamento y causas de interrupción del tratamiento.
Evaluación ecocardiográfica
Para la evaluación de la función ventricular izquierda se utilizó el ecocardiograma transtorácico. Los estudios se realizaron en un ecocardiógrafo Sonos 5500 de Philips con trazo electrocardiográfico simultáneo y las mediciones se obtuvieron promediando 5 ciclos consecutivos. En los ejes para esternal largo y apical de cuatro cámaras se evaluó la función sistólica y diastólica del VI mediante: FEVI, fracción de acortamiento (FA), flujo Doppler mitral, el flujo Doppler de las venas pulmonares (FVP) y el índice de rendimiento miocárdico (IRM) o índice de Tei. La metodología seguida para la medición de estos parámetros fue la misma a la reportada previamente.10–12
Los valores normales utilizados como referencia aparecen en la Tabla II.

Análisis estadístico
Para el análisis de los datos se utilizó el programa de estadística SPSS para Windows versión 9 (SPSS Inc, Chicago, Illinois). Se realizó estadística descriptiva. Los cambios antes y después del carvedilol se compararon con la prueba t de Student ya que las diferencias tenían una distribución normal. Se consideró una p significativa si era < 0.05.
Aspectos éticos
El estudio se apegó a la declaración de Helsinki de la Asociación Médica Mundial y a los principios éticos para las investigaciones médicas en seres humanos. Antes de iniciar el estudio se explicó claramente a los padres de los pacientes la naturaleza del mismo y sólo se incluyeron a los pacientes cuyos padres firmaron una carta de consentimiento informado. Se explicaron los posibles efectos secundarios del medicamento y se entrenó a los padres sobre qué hacer en caso de presentarse. Se proporcionaron los teléfonos móviles de los investigadores responsables para cualquier duda o comentario durante el mantenimiento con el medicamento.
Resultados
Se incluyeron 19 pacientes en el estudio, de ellos 10 eran mujeres. La edad al inicio del estudio fue de 1.1 a 14.3 años (m: 6.7 ± 4.3 años). El tiempo de evolución de la fecha del diagnóstico al inicio del estudio fue de 2 a 49 meses (m: 17 ± 12.4 meses). Diez pacientes se encontraban en clase funcional (CF) I, 6 en CF II y 3 en CF III antes del inicio del carvedilol. Un paciente en CF III, falleció en espera de trasplante cardíaco sin mostrar mejoría después de 5 meses de tratamiento con carvedilol. Los otros dos pacientes en CF III no han mejorado y están en espera de trasplante cardíaco. Dos en CF II pasaron a CF I y 10 permanecieron en CF I. Por tanto en la actualidad 2 pacientes están en CF III, 4 en II y 12 en I. Al final del estudio, se observó una reducción de la frecuencia cardíaca (FC) de 100–160 lpm (m: 132.8 ± 19.7) a 80–150 lpm (m: 117.6 ± 20.5). La tensión arterial sistólica (TAS) varió de 80–120 mmHg (m: 101.5 ± 15.4) a 70–100 mmHg (m: 95 ± 14.3), la tensión arterial diastólica (TAD) de 45–90 mmHg (m: 62.5 ± 12.2) a 40–80 mmHg (m: 56.8 ± 11.8) y se observó una prolongación del intervalo QT corregido (QTc) de 37– 41 mseg (m: 38.7 ± 1.59) a 39 – 43 mseg (m: 40.3 ± 1.5). Antes del inicio del carvedilol, 12 pacientes tenían cierto grado de insuficiencia mitral (IM) (9 ligera, 2 moderada y 1 grave). Después de 8 meses de manejo con carvedilol 5 pacientes continúan con insuficiencia mitral (todos ligera). El paciente con IM grave falleció a pesar del tratamiento. Los 2 pacientes con IM moderada evolucionaron a IM ligera y la IM ligera desapareció en 6 pacientes.
La Tabla III muestra detalladamente las mediciones ecocardiográficas encontradas en los pacientes antes del manejo con carvedilol así como los cambios observados a los 4 y 8 meses de iniciado el medicamento. Como lo muestra dicha tabla, a los 4 meses de tratamiento se observaron algunos cambios en la evaluación ecocardiográfica de la función sistólica y diastólica del ventrículo izquierdo con tendencia a la mejoría sin embargo, estos cambios no fueron estadísticamente significativos en FEVI, IRM y en la evaluación del flujo Doppler mitral; aunque sí en la FA que incrementó de 14.8 ± 4.1% a 21.3 ± 4.5% (p = < 0.05) y en las mediciones de la onda A reversa (AR) la cual disminuyó significativamente tanto en su velocidad como en su duración.
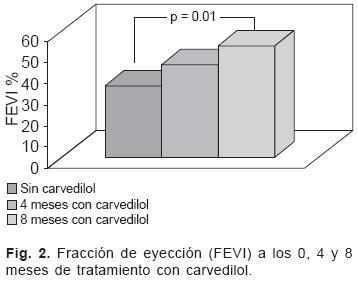
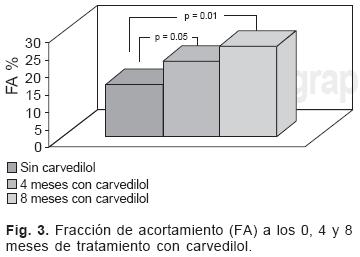
Después de 8 meses de tratamiento, La FEVI aumentó de 19–40% (m: 33.5 ± 7.2) a 26–62% (m: 52.6 ± 11.4), con un incremento en la media de 19.1 ± 9.3% (p = 0.01). La FA aumentó de 720% (m: 14.8 ± 4.1) antes del carvedilol a 1332% (m: 25.8 ± 5.6), con un incremento en la media de 11 ± 4.8 % (p = 0.01).
Antes del inicio de carvedilol, 9 pacientes tuvieron alterado el patrón E/A mitral. A los 8 meses con carvedilol se normalizó en 3 pacientes y 6 continuaron con una relación E/A anormal.
Todos los casos tuvieron alterado el FVP antes del inicio del carvedilol y en 11 pacientes la relación entre la onda S y la onda D (S/D) fue menor de 1. A los 8 meses, sólo 6 continuaron con el FVP alterado y de ellos la S/D fue menor de 1 sólo en 2 pacientes. Antes del carvedilol, en todos los pacientes se encontró una onda A reversa (AR), con una velocidad de 5.5 – 79 cm/ seg (m: 25.8 ± 18.4 cm/seg). Después de 8 meses con carvedilol sólo 11 pacientes continuaban con una AR y en ellos la velocidad de la AR había disminuido a 1 – 23 cm/seg (m: 7.5 ± 7.19 cm/seg) (P = 0.01). La duración de la onda AR (ARd) antes del inicio de carvedilol fue mayor que la duración de la onda A mitral (Ad) en todos los pacientes con una ARd media de 113 ± 34.9 mseg que disminuyó a 21.16 ± 23.0 mseg (P = 0.01), de tal manera que al final del estudio ningún paciente tuvo una diferencia ARd–Ad positiva.
El tiempo de contracción isovolumétrica (TCI) fue mayor de 42 mseg en todos los pacientes antes del tratamiento con un rango de 60–120 mseg (m: 81.7 ± 17.6 mseg), a los 8 meses disminuyó a 50–90 mseg (m: 60 ± 10.9 mseg) (p = 0.02). El tiempo de relajación isovolumétrica (TRI) también era mayor de 42 mseg en todos los pacientes al inicio del estudio con un rango de 60–99 mseg (m: 75.1 ± 10.5 mseg) y después de carvedilol disminuyó a 50–85 mseg (m: 56.6 ± 9.0 mseg) (p = 0.02). El tiempo de eyección (TE) fue menor de 230 mseg en todos los pacientes antes del carvedilol con rango de 75 a 260 mseg (m: 192.1 ± 49.7 mseg) y a los 8 meses de tratamiento sólo en 5 pacientes era menor de 230 mseg con un rango de 200 a 280 mseg (m: 243.8 ± 28.6 mseg) (p = 0.05). Con estos datos, se calculó el índice de rendimiento miocárdico (IRM) que estuvo alterado en todos los pacientes antes del manejo con carvedilol de .43 – 1.02 (m: 0.6 ± 0.15) y disminuyó a 0.39 – 0.87 (m: 0.48 ± 11) (p < 0.05) después de 8 meses con el medicamento. Al final del estudio, 14 pacientes continúan con IRM anormal y 5 pacientes con IRM normal menor de 0.42 (Tabla III).
Todos los pacientes tuvieron buena tolerancia al medicamento sin registrarse efectos secundarios con excepción de un paciente que no toleró el incremento a la dosis de 0.8 mg/kg/día reportándose somnolencia e hipoactividad y su ECG mostró disminución en la FC de 150 lpm a 120 lpm con prolongación del QTc de .37 a .45 mseg por lo que se redujo la dosis a 0.6 mg/kg/día normalizándose los datos mencionados.
Discusión
Una mejor comprensión de la fisiopatología de la IC, se logró en gran medida gracias a los trabajos pioneros sobre las respuestas neuro–humorales a la IC y sobre los efectos potencialmente deletéreos a largo plazo de la activación del sistema nervioso adrenérgico. En presencia de IC, la estimulación adrenérgica produce un incremento de catecolaminas circulantes,13,14 benéfico en la fase aguda ya que incrementa la frecuencia cardíaca (FC), la presión arterial (TA) y la contractilidad miocárdica. Sin embargo, con el tiempo, la sobreestimulación adrenérgica puede tener efectos deletéreos profundos en la hemodinámica de la IC.13,15 Estos efectos directos incluyen daño a los miocitos que puede llegar a la necrosis inducida por catecolaminas circulantes.16,17 Además ocurre una pérdida de miocitos por apoptosis, el proceso natural de muerte celular programada, acelerado por dicha estimulación adrenérgica.18 El consumo de oxígeno miocárdico y el estrés de la pared condicionan daño a los miocitos y al aumento de la fibrosis con deterioro en la función cardíaca.19 De esta manera, si bien la sobreestimulación adrenérgica condiciona una mejoría hemodinámica aguda, crónicamente conduce al deterioro anatomofuncional miocárdico. Esta información dio lugar a la hipótesis de que los β–bloqueadores podían prevenir el deterioro crónico en pacientes con IC. A partir de la segunda mitad de la década de los 80 se realizaron numerosos estudios en adultos que demostraron que la terapia con β–bloqueadores mejora la función sistólica,20,21 favorece la remodelación de los ventrículos dilatados,22 mejora los síntomas20,21,23 y disminuye el riesgo de hospitalización y muerte.24–26 Sobre esta base los β–bloqueadores se recomiendan en la actualidad como parte integral del tratamiento del paciente adulto con IC crónica.27
En la edad pediátrica la experiencia con el uso de β–bloqueadores es muy limitada. En 1998, Shaddy utilizó metoprolol en 4 niños con IC y clase funcional IV, que estaban en lista de espera de trasplante cardíaco. En 2 pacientes la clase funcional y los índices ecocardiográficos de función ventricular mejoraron y fueron removidos de la lista de espera, 1 paciente falleció después de 17 meses del inicio de metoprolol y a otro se le realizó el trasplante cardíaco con éxito.28 Un año más tarde, el mismo autor presentó la experiencia de tres instituciones con el uso de metoprolol en 15 niños con CMD encontrando mejoría en la función ventricular izquierda valorada exclusivamente por FEVI y FA, después de 23.2 ± 7 meses de iniciado el manejo.29 En 2001 Bruns y cols., resumen la experiencia pediátrica inicial con carvedilol en un estudio retrospectivo de 6 centros pediátricos. Incluyeron a 46 niños, 37 con CMD y 9 con cardiopatía congénita demostrando que el carvedilol puede ser útil en el manejo de los pacientes pediátricos con IC, que los efectos benéficos son similares a los observados en los adultos y que los efectos secundarios del medicamento son ocasionales y leves en los niños.4 Laer y cols en 2002, investigaron el efecto del carvedilol y su farmacocinética en 15 niños con IC comparándolos con 9 adultos. Después de 6 meses de tratamiento el carvedilol incrementó la FEVI de 36 a 54% (p < .05). Además demostraron que los niños eliminan el carvedilol más rápidamente que los adultos, ya que el tiempo de vida media fue 50% más corto en la población pediátrica que en los adultos (2.9 vs 5.2 h; p < .05).5
Otros estudios clínicos más recientes en población pediátrica también sugieren que el carvedilol mejora los síntomas y la función ventricular en pacientes con CMD.6,7 Actualmente se está llevando a cabo en los Estados Unidos de Norteamérica un estudio prospectivo, randomizado y placebo controlado para determinar la seguridad y eficacia de carvedilol en niños desde recién nacidos hasta 17 años con insuficiencia cardíaca sintomática secundaria a disfunción sistólica ventricular sistémica en el que se incluirán 150 niños con cardiomiopatías de diferentes etiologías y cardiopatías congénitas complejas incluso pacientes con fisiología de ventrículo único.30 Dicho protocolo es muy importante ya que se trata de un estudio multicéntrico que incluirá el número necesario de pacientes a tratar para lograr un suficiente poder estadístico; sin embargo aún no se tienen resultados.
El presente trabajo, muestra los resultados preliminares con un pequeño número de pacientes con diagnóstico de CMD idiopática en los que la evaluación minuciosa de la función del VI muestra cambios favorables después de 8 meses de tratamiento con carvedilol aunado a la terapia convencional. Estos cambios se expresan al parecer por vez primera en la literatura pediátrica utilizando no sólo los índices endocárdicos habituales que evalúan la función sistólica (FEVI y FA) sino además incorporando la evaluación del FVP y el IRM con lo cual se logra tener una idea más completa de la función global del ventrículo izquierdo. De esta manera, los cambios se encontraron tanto en el análisis de la función sistólica con un incremento de la FEVI en un 57% de sus cifras basales y de la FA en un 73% (Figs. 1, 2 y 3), como en la valoración de la función diastólica ya que el patrón del flujo Doppler mitral estaba alterado en la mitad de los casos antes del medicamento y se normalizó en 3 de ellos al final del estudio. A este respecto, el FVP es un parámetro muy útil para la evaluación de la función diastólica del VI sobre todo en pacientes con una relajación ventricular alterada en los que es frecuente encontrar un patrón del flujo mitral "pseudo–normalizado".11 Al analizar el FVP en adultos con IC, se ha observado que una relación S/D menor de 1, una onda AR aumentada y la duración de la onda AR (ARd) mayor a la duración de la onda A mitral (Ad) con una diferencia ARd–Ad mayor de 30 mseg correlacionan bien con el grado de deterioro de la clase funcional y la muerte.11 Al analizar el FVP en este estudio todos nuestros casos tenían un patrón alterado que se normalizó en el 68% después del manejo con carvedilol.

El índice de Tei o el índice de rendimiento miocárdico (IRM) es otro parámetro ecocardiográfico de reciente introducción hasta ahora no utilizado en casos de CMD en la edad pediátrica. Evalúa la función ventricular izquierda tanto sistólica como diastólica al incorporarse en su cálculo el tiempo de contracción, el tiempo de relajación y la expulsión del VI. Cuando este índice es mayor de .42 traduce disfunción ventricular izquierda global. En este estudio el IRM estuvo alterado en todos los pacientes antes del inicio del medicamento, normalizándose después de 8 meses de tratamiento en 5. (< .42, p = 0.05).
Si bien los estudios pediátricos previos cuantifican la respuesta al tratamiento con carvedilol utilizando exclusivamente índices endocárdicos basados en la variación del tamaño del ventrículo y dado que el acortamiento de la fibra miocárdica en casos con CMD no es uniforme, en este estudio además de encontrar cambios significativos en FEVI y FA (p = < 0.05), se observaron también cambios importantes en la evaluación del FVP y en el IRM, por lo que consideramos que la evaluación ecocardiográfica que incluye a todos los parámetros mencionados permite valorar precozmente la respuesta de la función ventricular izquierda al manejo terapéutico de la CMD y es un recurso valioso en la selección de los candidatos a ingresar a lista de espera de trasplante cardíaco.
Limitaciones del estudio
En el estudio se incluyeron únicamente a pacientes con diagnóstico de CMD idiopática en un solo centro hospitalario, por lo que el número de pacientes es pequeño, esto aunado a la falta de un grupo control con placebo no permite asegurar que los cambios observados son debidos exclusivamente al manejo con carvedilol o si forman parte de la mejoría espontánea observada en algunos casos de CMD.
Conclusiones
Los resultados observados en este trabajo, sugieren un efecto benéfico del carvedilol en adición a la terapia habitual para el manejo de la IC secundaria a CMD en niños. El medicamento es bien tolerado, con efectos secundarios mínimos en la edad pediátrica. Se requieren estudios comparativos, que incluyan un mayor número de pacientes y un seguimiento más prolongado para determinar la eficacia real del carvedilol en niños con IC secundaria a CMD.
Referencias
1. Manolio TA, Baughman KL, Rodeneffer R, Pearson TA, Bristow JD, Michels VV, et al: Prevalence and etiology of idiopathic dilated cardiomyopathy (Summary of a National Heart Lung and Blood institute workshop). Am J Cardiol 1992; 69: 1458–66. [ Links ]
2. Bristow MR, Gilbert EM, Abraham WT, Adams KF, Fowler MB, Herhberger RE, et al: Carvedilol produces dose–related improvements in left ventricular function and survival in subjects with chronic heart failure. MOCHA Investigators. Circulation 1996; 94: 2807–16. [ Links ]
3. Yuan Z, Shioji K, Kihara Y, Takenaka H, Onozawa Y, Kishimoto Ch: Cardioprotective effects o Carvedilol on acute autoinmmune myocarditis: anti–inflamatory effects associated with antioxidant property. Am J Physiol 2004; 286: 83–90. [ Links ]
4. Bruns L, Kichuk M, Lamour J, Shaddy R, Pahl E, Blumme E, et al: Carvedilol as therapy in pedlatric heart failure: An initlal multicenter experience. J Pediatr 2001; 138: 505–11. [ Links ]
5. Läer S, Mir Th, Behn F, Eiselt M, Scholz A, Meibohm B, et al: Carvedilol therapy in pediatric patients with congestive heart failure: A study investigating clinical and pharmacokinetic parameters. Am Heart J 2002; 143: 816–22. [ Links ]
6. Rusconi P, Gómez–Marín O, Rossique–González M, Redha E, Marín J, Long–Young M, et al: Carvedilol in children with cardiomyopathy: 3–Year Experience at single institution. J Heart Lung Transplant 2004; 23: 832–838. [ Links ]
7. Blume E, Canter C, Spicer R, Gauvreau K, Colan S, Jenkins K: Prospective single–arm protocol of carvedilol in children with ventricular dysfunction. Pediatr Cardiol 2006; 27: 336–342. [ Links ]
8. Ross R: Grading the graders of congestive heart failure in children. J Pediatr 2001; 138:618–20. [ Links ]
9. Connolly D, Rutkowski M, Auslende M, Artman M: The New York University Pediatric Heart Failure index: new method of quantifying chronic heart failure severity in children. J Pediatr 2001; 138: 644–8. [ Links ]
10. Schiller NB: Two dimensional Echocardiography determination of left ventricular volume, systolic function and mass: summary and discussion of the 1989 recommendations of the American Society of Echocardiography. Circulation 1991; 84(Suppl): 1–280. [ Links ]
11. Tomotsugu T, James D, Klein A: Pulmonary Venous Flow by Doppler Echocardiography: Revisited 12 Years Later. J Am Coll Cardiol 2003; 4: 1243–50. [ Links ]
12. Tei C, Ling LH, Hodge DO, Bailey KR, Oh JK, Rodeheffer RJ, et al: New index of combined systolic and diastolic myocardial performance: a simple and reproducible measure of cardiac function – a study in normals and dilated cardiomyopathy. J Cardiol 1995; 26(6): 357–66. [ Links ]
13. Waagstein F, Hjalmarson A, Varnauskas E, Wallentin I: Effect of chronic beta–adrenergic receptor blockade in congestive cardiomyopathy. Br Heart J 1975; 37: 1022–36. [ Links ]
14. Chidsey CA, Harrison DC, Braunwald E: Augmentation of the plasma norepinephrine response to exercise in patients with congestive heart failure. N Engl J Med 1962; 267: 650–4. [ Links ]
15. Francis GS, Benedict C, Johnstone DE, Kirlin PC, Nicklas J, Llang C, et al: Comparison of neuroendocrine activation in patients with left ventricular dysfunction with and without congestive heart failure. Circulation 1990; 82: 1724–9. [ Links ]
16. Cohn JN, Levine TB, Olivari MT, Gerberg V, Lura D, Francis GS, et al: Plasma norepinephrine as a guide to prognosis in patients with cronic congestive heart failure. N Engl J Med 1984; 311: 819–23. [ Links ]
17. Yates JC, Beamish RE, Dhalla NS: Ventricular dysfunction and necrosis produced by adrenochrome metabolite of epinephrine: relation to pathogenesis of catecolamine cardiomyopathy. Am Heart J 1981; 102: 210–21. [ Links ]
18. Sabbah HN: Apoptotic cell death in heart failure. Cardiovas Res 2000; 45: 704–12. [ Links ]
19. Mann DL, Kent RL, Parsons B, Cooper G: Adrenergic effects on the biology of the adult mamallan cardiocyte. Circulation 1992; 85: 790–804. [ Links ]
20. Packer M, Colucci WS, Sackner–Bernstein JD, Llang C, Goldscher DA, Freeman I, et al: Double–blind, placebo–controlled study of the effects of carvedilol in patients with moderate to severe heart failure. Circulation 1996; 94: 2793–9. [ Links ]
21. Kukin KL, Kalman J, Charney RH, Levy DK, Bucholz–Varley C, Ocampo ON, et al: Prospective, randomized comparison of effect of long–term treatment with metoprolol or carvedilol on symptoms, exercise, ejection fraction, and oxidative stress in heart failure. Circulation 1999; 99:2645–50. [ Links ]
22. Lowes BD, Gill EA, Abraham WT, Larrain J–R, Robertson AD, Bristow MR, et al: Effects of carvedilol on left ventricular mass, chamber geometry, and mitral regurgitation in chronic heart failure. Am J Cardiol 1999; 83: 1201–5. [ Links ]
23. Colucci WS, Packer M, Bristow MR, Gilbert EM, Cohn JN, Fowler MB, et al: Carvedilol inhibits clinical progression in patients with mild symptoms of heart failure. Circulation 1996; 94:2800–6. [ Links ]
24. Packer M, Bristow MR, Cohn JN, Colucci WS, Fowler MB, Gilbert EM, et al: The effect of carvedilol on morbidity and mortality in patients with heartfailure. N Engl J Med 1996; 334: 1349–55. [ Links ]
25. Bristow MR, Gilbert EM, Abraham WT, Adams KF, Fowler MB, Hershberger RE, et al: Carvedilol produces dose–related improvements in left ventricular function and survival in subjects with chronic heart failure. Circulation 1996; 94:2807–16. [ Links ]
26. Packer M, Coats A, Fowler M, Katus H, Krum H, Mohacsi P, et al: Effect of carvedilol on survival in severe Chronical heart failure. N Engl J Med 2001; 344: 1651–1658. [ Links ]
27. Packer M, Cohn JN: Consensus recommendations for the management of chronic heart failure. Am J Cardiol 1999; 83: 39A–42A. [ Links ]
28. Shaddy R: B–Blocker therapy in young children with congestive heart failure under consideration for heart transplantation. Am Heart J 1998; 136:19–21. [ Links ]
29. Shaddy R, Tani L, Gidding S, Pahl E, Orsmond G, Gilbert E, et al: Beta–blocker treatment of dilated cardiomyopathy in children: a multi–institutional experience. J Heart Lung Transplant 1999; 18: 269–74. [ Links ]
30. Shaddy R, Leigh E, Sower B, Tani L, Burr J, La Salle B, et al: The pediatric randomized carvedilol trial in children with chronic heart failure: rationale and design. Am Heart J 2002; 144: 383–389. [ Links ]














