Introducción
Una pregunta que siempre ha surgido en la unidad de cuidados intensivos (UCI) es cuál es el momento oportuno para desconectar y retirar a un paciente de la ventilación mecánica. Siempre que se coloca una cánula endotraqueal para ventilar a un paciente debe considerarse en ese preciso momento el tiempo en el que pueda retirarse y decanularse. El tiempo que toma retirar un paciente de ventilación mecánica ocupa 40% del tiempo total de ventilación mecánica.1
Es uno de los procedimientos más frecuentes en las unidades de cuidados intensivos. Se ha observado que más de la mitad de los enfermos que requieren ventilación mecánica llegan a ser extubados tras un proceso de desconexión. De ellos 57% son extubados tras una primera prueba de respiración espontánea, mientras que el restante 43% precisan de aproximadamente tres días para ser extubados. En términos generales, este proceso supone 40% del tiempo total del apoyo ventilatorio como ya hemos mencionado.1-3
La desconexión de la ventilación mecánica es un proceso que inicia con la identificación diaria de los pacientes que pueden realizar una prueba de respiración espontánea y se continúa con la aplicación de tres pruebas diagnósticas consecutivas: medición de predictores de tolerancia a la prueba de ventilación espontánea (por sus siglas en inglés SBT, spontaneous breathing trial), una prueba de respiración o ventilación espontánea y una prueba de extubación. Los estudios sugieren que los pacientes que toleran SBT 30-120 minutos tienen una posibilidad de aproximadamente 77% de extubación satisfactoria y una tasa de error de extubación (necesitan nueva intubación) de 4 a 23%.4,5
Con esta estrategia, un grupo de enfermos podrá ser extubado en el primer intento de respiración espontánea, lo que se ha denominado weaning simple o fácil, pero alrededor de 45% de los enfermos va a precisar una desconexión progresiva de la ventilación mecánica. Para ello disponemos de los métodos convencionales de desconexión: tubo en T, presión positiva continua en la vía aérea (CPAP), ventilación mandatoria intermitente sincronizada (SIMV) y presión de soporte (PS). Estos métodos han sido evaluados comparativamente en varios trabajos, los cuales a su vez han sido analizados en una revisión sistemática.6-8 Las diferencias en el diseño de los protocolos en lo referente a la forma de disminución del soporte ventilatorio con el SIMV, en la presión de soporte y en los criterios de extubación son la causa de que en esta revisión no haya sido posible identificar una técnica superior entre los tres modos comparados, pero lo que sí parece haberse confirmado es que el SIMV prolonga la desconexión más que el tubo en T o la reducción gradual de la presión de soporte.9
En los últimos años se han descrito nuevas aplicaciones de técnicas habituales y nuevos métodos de ventilación que pudieran tener alguna función en la desconexión de la ventilación mecánica en los enfermos con desconexión difícil o prolongada. Estos métodos incluyen la ventilación mecánica no invasiva, la compensación automática del tubo, el weaning automático con sistemas de circuito o asa cerrada y la ventilación adaptativa de soporte. A diferencia de los dos métodos previamente descritos, los sistemas de weaning automatizados disponibles no son nuevos métodos de ventilación, sino estrategias automáticas de desconexión de la ventilación mecánica basadas en un modo de ventilación ya existente como es la presión de soporte. Actualmente disponemos de un sistema de weaning automatizado: SmartCare® disponible en el ventilador Evita XL (Draeger Medical). El sistema SmartCare® aplica continuamente un protocolo de desconexión con cambios en la presión de soporte basados en mediciones de la frecuencia respiratoria, del volumen corriente y de la presión parcial de CO2 al final de la espiración (etCO2). Para iniciar el funcionamiento del sistema, el médico introduce información del paciente (peso, antecedentes de enfermedad pulmonar crónica y/o enfermedad neurológica), tipo de vía aérea (tubo endotraqueal o traqueotomía) y tipo de humidificación (intercambiador de calor-humedad o humidificador de calor activo). A continuación se inicia el proceso de desconexión; en un principio el sistema se adapta para mantener al paciente en un estado de confort respiratorio (ventilación normal), para lo cual modula la presión de soporte aumentando o disminuyendo entre 2 y 4 cmH2O, según los datos de frecuencia respiratoria (límites normales de 15-30 respiraciones por minuto [rpm]) (en enfermos con patología neurológica aumenta el límite superior a 34 rpm), volumen corriente (límites normales > 300 mL) y de etCO2 (límites < 55 mmHg, en pacientes con enfermedad pulmonar crónica sube el límite a 65 mmHg) cuyo promedio se calcula cada 2-5 minutos. Una vez que el paciente se encuentra en la situación de ventilación normal, el sistema reduce o aumenta la presión de soporte, dependiendo de las necesidades del enfermo, cada 15, 30 o 60 minutos dependiendo del nivel previo de Presión Soporte hasta llegar a una presión de soporte variable dependiendo del tipo de vía aérea artificial y del tipo de humidificación (5 cmH2O para humidificador de calor activo y traqueotomía, 7 cmH2O para humidificador de calor activo y tubo endotraqueal, 9 cmH2O para humidificador calor-humedad y traqueotomía y 12 cmH2O para humidificador calor-humedad y tubo endotraqueal). Una vez que se llega a este nivel de soporte se considera que el enfermo inicia una prueba de respiración espontánea cuya duración es determinada por el patrón respiratorio y el nivel de Presión Soporte al que inició el proceso de desconexión. Si durante ese tiempo el enfermo presenta un patrón respiratorio diferente a la ventilación normal o a la hiperventilación, se considera que el sistema no ha superado la prueba de respiración espontánea y aumenta la presión de soporte hasta obtener un patrón ventilatorio normal. En caso de estabilidad del patrón respiratorio, el respirador mostrará un mensaje indicando que el enfermo está preparado para ser extubado.10
Los sistemas de circuito cerrado han anunciado una época apasionante de la ventilación mecánica que tiene como objetivo simplificar el proceso de destete y retiro de la ventilación haciéndolo interactivo, sensible y adaptable. Sin embargo, la automatización durante el destete todavía no reemplaza la necesidad de una estrecha observación y monitorización de pacientes, ni suplanta la necesidad de los médicos de tomar importantes decisiones clínicas durante el destete y eventos críticos como la aptitud para la extubación. El papel de la automatización en el destete puede ser complementado por la perspicacia clínica y la atención brindada por los médicos en la optimización del proceso de cuidar a los pacientes críticamente enfermos que requieren ventilación invasiva en la UCI. Hacen falta investigaciones clínicas para evaluar si las promesas de automatización pueden realizarse en diferentes poblaciones de pacientes y entornos de práctica y para dilucidar el impacto de los sistemas de circuito cerrado más recientes en otros resultados clínicos relevantes.11
Automatizar el proceso de destete tiene varias ventajas importantes. En primer lugar, con la automatización el destete se vuelve interactivo con el ventilador y el paciente para adaptar la salida del ventilador de acuerdo con sus necesidades individuales e instantáneas. En segundo lugar, la tecnología de circuito cerrado permite a la ventilación mecánica ajustarse y adaptarse de forma continua durante el destete. En consecuencia, el destete no se retrasa ni se ve impedido por la disponibilidad limitada del personal clínico en la UCI que pudiera estar ocupado. En tercer lugar, la decisión durante el destete se optimiza mediante el reconocimiento de ventilación de los acontecimientos clave. Por estas razones, el destete automatizado es prometedor como un medio de reducir el patrón de variaciones prácticas y de facilitar la traducción de los nuevos conocimientos en práctica para mejorar los resultados del paciente.12 Los sistemas de circuito cerrado disponibles actualmente tienen limitaciones generales y específicas. A pesar de ser altamente eficientes en el logro de objetivos preestablecidos, los sistemas automatizados corren el riesgo de perseguir sin descanso valores objetivos. Además, los creadores de sistemas automatizados en algunos casos pueden ser particularmente susceptibles a la tentación de desarrollar sistemas para traducir modelos complejos en algoritmos simplificados con aplicaciones clínicas limitadas y para gestionar todos los aspectos de la ventilación mecánica.13-15 Para este fin, los sistemas que se revisaron para sintetizar parámetros básicos fisiológicos en modelos simples que integran el razonamiento clínico en los algoritmos pueden aplicarse en la cama del paciente. Si bien se han desarrollado algunos sistemas para apoyar a los pacientes que requieren ventilación controlada o asistida, se han creado otros sistemas específicamente para pacientes con respiración espontánea y para guiar los aspectos de la ventilación mecánica (por ejemplo, el destete). Por último, estos sistemas no se han probado completamente en poblaciones específicas de pacientes (con broncoespasmo severo, abundantes secreciones, polineuropatía severa en enfermedad crítica o miopatía) en los que a menudo resulta difícil el destete de la ventilación mecánica, independientemente del modo o estrategia utilizada.16
Un estudio realizado por la base de datos Cochrane identificó 21 ensayos elegibles para un total de 1,676 participantes. Los datos agrupados de 16 ensayos indicaron que los sistemas automatizados reducen la media de duración de destete en 30% (IC 95%, 13-45%), con heterogeneidad significativa (I 2 = 87%; p < 0.00001). La reducción de la duración de destete se observó en poblaciones de UCIs médicas mixtas con 42%, (IC 95%, de 10% a 63%) y SmartCare®/PS ™ 28%, (95% CI 7% a 49%), pero no en poblaciones quirúrgicas o usando otros sistemas. Los sistemas automatizados reducen la duración de ventilación sin heterogeneidad en 10%, (de IC 95%, 3% a 16%) y disminuyen la estancia en UCI en 8%, (95% CI de 0% a 15%). No hubo pruebas sólidas de efecto en la mortalidad, estancia en el hospital, reintubación, autoextubación y ventilación no invasiva tras la extubación. Los sistemas automatizados reducen la ventilación mecánica prolongada y la traqueotomía. En general la calidad de las pruebas fue alta. Los sistemas automatizados pueden reducir el destete y la duración de la ventilación y por tanto la estancia en la UCI. Debido a juicio sustancial es necesario un ensayo de alta calidad, multicéntrico controlado aleatorio con poder estadístico adecuado.17
Justificación: La ventilación mecánica sigue siendo una base importante en la atención del paciente en estado crítico, es una medida de soporte orgánico temporal para el paciente. Se han logrado grandes avances en los ventiladores mecánicos que se tienen en la actualidad, pues son más seguros y ofrecen mayor confort a los pacientes durante los días que requieran este tipo de ventilación. A pesar de dichos avances los días de ventilación mecánica deben limitarse al mínimo debido a que son un factor de riesgo del desarrollo de infecciones de vías aéreas inferiores y su duración está asociada al mal pronóstico en la evolución de dichas infecciones. Por ello, el destete de la ventilación mecánica debe realizarse tempranamente. Se han llevado a cabo diversos protocolos para realizar el destete de la ventilación mecánica; no obstante, las tasas de extubaciones fallidas siguen siendo considerables y la reintubación conlleva un mayor riesgo y empeora el pronóstico de los pacientes. Con la llegada de los nuevos ventiladores microprocesados de cuarta generación surgieron algunos métodos de destete automático basados en varias mediciones de dinámica respiratoria del paciente a través de un programa de datos que ejecuta un algoritmo para ajustar la demanda ventilatoria del sujeto, cuyo objetivo es que la transición del destete sea más confortable, que se realice de forma más precoz y que se intente que la extubación no sea fallida. La evidencia actual es aún limitada cuando estos métodos son comparados con los protocolos habituales de extubación, pero es de notarse que existe una tendencia a que con el uso de estos protocolos automáticos se logren destetes más rápidos y que haya menos fracasos en la extubación. La evidencia en nuestro país es limitada y en nuestra región es nula, por lo que se decidió llevar a cabo este estudio en el que se compara la eficacia en el destete de la ventilación mecánica y extubación con el sistema automático (SmartCare®) vs los protocolos con uso de Presión Soporte y Pieza en T.
Objetivo general: Evaluar la eficacia del protocolo automático de destete (SmartCare®) comparado con protocolos no automatizados, Presión Soporte y Pieza en T en la desconexión de la ventilación mecánica.
Objetivos específicos: Comparar el tiempo medido en horas y minutos del destete de la ventilación mecánica entre el protocolo automático de destete (SmartCare®) y métodos no automatizados. Determinar los destetes fallidos en el protocolo automático de destete (SmartCare®) vs protocolos no automatizados. Comparar el índice de oxigenación (PaO2/FiO2) y la ventilación alveolar (PaCO2) antes, durante y posterior al destete de la ventilación mecánica con el sistema automático de destete (SmartCare®) versus los protocolos no automatizados. Describir las variables hemodinámicas TA, FC, TAM, SO2, SvCO2 y lactato antes, durante y posterior al destete de la ventilación mecánica entre el método automático (SmartCare®) vs métodos no automatizados. Cuantificar los días de ventilación mecánica entre los pacientes en los que se utilizó el protocolo automático de destete (SmartCare®) versus métodos no automatizados. Cuantificar los días de estancia en la unidad entre los pacientes en los que se utilizó el protocolo automático de destete (SmartCare®) versus método no automatizado Presión Soporte.
Hipótesis: Hipótesis de investigación (Hi): el protocolo automático de destete (SmartCare®) es más eficaz comparado con protocolos no automatizados (Presión Soporte y Pieza en T) en la desconexión de la ventilación mecánica. Hipótesis nula (Ho): el protocolo automático de destete (SmartCare®) no es más eficaz comparado con el protocolo no automatizado (Presión Soporte y Pieza en T) en la desconexión de la ventilación mecánica
Material y Métodos
Diseño: ensayo clínico controlado aleatorizado abierto. Tipo de estudio: experimental, prospectivo, longitudinal, analítico y comparativo. Universo del estudio: pacientes que ingresaron a la unidad de cuidados intensivos y que ameritaban ventilación mecánica invasiva durante el periodo del 31 de mayo al 31 de agosto de 2015. Población en estudio: pacientes que se encontraban en la fase de retiro de la ventilación mecánica. Tamaño de la muestra: se usó la fórmula para el cálculo de la muestra para estudios de contraste de hipótesis, en los que se utilizan proporciones de dos muestras diferentes:
Resultando un total aproximado de 27 pacientes por cada grupo de estudio, ajustado a un margen de seguridad de pérdida de individuos de estudio a 10%, quedando un total de 30 pacientes por cada grupo. Por lo que N = 90 pacientes.
Técnica de muestreo: sistema de probabilístico no intencional a base de «tómbola».
Método de asignación: se tomaron los pacientes de la lista de ingresos de la unidad de cuidados intensivos que ameritaban ventilación mecánica invasiva orotraqueal mediante el sistema de muestreo tipo «tómbola», quienes serían asignados al azar a tres grupos de experimentación, al grupo S correspondiente al método automático SmartCare®, al grupo P que corresponderá al método no automático de Presión Soporte y por último al grupo T del método no automático de destete de Pieza en T, se seleccionaron de este modo hasta completar la muestra.
Criterios de inclusión: pacientes de uno u otro género, entre 18 y 75 años de edad, que ameriten soporte mecánico ventilatorio con intubación orotraqueal o traqueostomía. Otorgar (pacientes o familiar responsable) el consentimiento informado de participación en el estudio.
Criterios de exclusión: pacientes con problemas pulmonares crónicos. Enfermos con cardiopatía crónica previa. Sujetos con problemas neurológicos.
Criterios de eliminación: Pacientes que durante la fase de destete se hayan extubado de forma incidental. Sujetos que ameriten cambio en el modo de destete por alteraciones respiratorias, hemodinámicas o de otra índole que ponga en peligro su vida.
Definición operacional de las variables: Independientes: Protocolo automático destete SmartCare ® : sistema automatizado que ventila al paciente con soporte de presión, ajustando de forma automática la frecuencia respiratoria, volumen corriente y la fracción espirada de dióxido de carbono (etCO2) evaluando el soporte de presión para satisfacer la demanda del paciente, disminuyendo o aumentando el soporte ventilatorio hasta que el paciente esté en condiciones de extubación alertando al médico tratante que puede intentar una extubación y separación del ventilador mecánico.
Protocolo no automático de destete Presión Soporte: se basa en un protocolo en el que el médico tratante mantiene una Presión Soporte inicial que asegure un volumen tidal de 6-8 cm3/kg, con un PEEP de 5 cmH2O, posteriormente se inicia la disminución de la presión de soporte hasta un mínimo de 7 cmH2O y que al tolerar 30 minutos en estos parámetros se decide la extubación del paciente.
Protocolo no automático de destete Pieza en T: se basa en un protocolo en el que el clínico tratante decide, de acuerdo con su criterio, retirar al paciente de la ventilación mecánica una vez que éste supere una prueba de ventilación espontánea: se coloca un dispositivo plástico de no reinhalación llamado «Pieza en T» que permite un flujo alto de oxígeno sin PEEP externa ni presión de soporte.
Variables dependientes: eficacia del destete de la ventilación mecánica: se define como al éxito en la extubación de la ventilación mecánica una vez superadas 48 horas sin deterioro de la mecánica ventilatoria del paciente, sin que haya ameritado algún tipo de terapia de soporte ventilatorio o que haya sido reintubado durante dicho periodo.
El Cuadro I muestra las escalas de medición empleadas.
Cuadro I: Escalas de medición
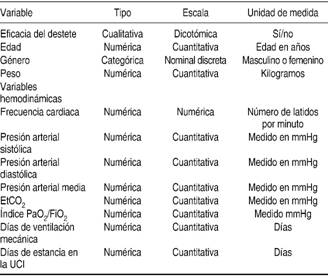
Abreviaturas: EtCO2 = CO2 al final de la espiración, PaO2 = Presión parcial de oxígeno arterial, FiO2 = Fracción inspirada de oxígeno, UCI = Unidad de Cuidados Intensivos.
Descripción de procedimientos: Previa aprobación del Comité de Investigación y Ética del «Hospital General Agustín O’Horán» de Mérida, Yucatán y previa autorización del familiar responsable del paciente, el equipo de investigación realizó un ensayo clínico controlado abierto en todos los pacientes que ingresaron a la unidad de cuidados intensivos adultos durante el periodo comprendido entre el 31 de mayo al 31 de agosto de 2015, que cumplieran con los criterios de inclusión y que básicamente ameritaran ventilación mecánica invasiva con intubación orotraqueal o traqueostomía. La secuencia de acción fue la siguiente: se asignaron y aleatorizaron de la lista diaria de ingreso a la unidad mediante el sistema «tómbola», asignando a los pacientes en tres grupos, grupo S correspondiente al método automático SmartCare®, al grupo P que corresponde al método no automático de Presión Soporte y por último al grupo T del método no automático de destete de Pieza en T, de este modo se seleccionaron hasta completar la muestra de 90 participantes, correspondiendo 30 pacientes a cada grupo. Al ingreso se tomaron todos los datos demográficos así como la aplicación de las escalas de gravedad APACHE II y SAPS III, homogeneizando la muestra de acuerdo con la gravedad que presentaron los pacientes, asimismo se midió la escala SOFA todos los días. A todos los pacientes se les aplicó el mismo ventilador modelo Draeger Evita Xl®, los parámetros de ventilación de inicio y la sedoanalgesia fueron asignados por el médico tratante, la duración de la ventilación mecánica fue con base en la mejoría del paciente y el inicio de la fase de destete de la ventilación mecánica fue determinada por el médico tratante, al momento de empezar el destete se inició uno de los tres protocolos de este mismo que correspondía según el grupo al que fue asignado en el momento del ingreso. Durante esta fase se inició la recolección de datos, tiempo de destete y las variables hemodinámicas como TA, FC, FR, TAM, So2, Svco2 y Lactato, así como la medición de los índices de oxigenación PaO2/FiO2 y de ventilación alveolar PaCO2 antes, durante y posterior al destete de ventilación mecánica. Se midieron en cinco tiempos, T1 al momento de iniciar el protocolo de destete de la ventilación mecánica, T2 previo al momento del destete de la ventilación mecánica, T3 a las 2 horas posterior a la extubación, T4 a las 24 horas posterior a la extubación y T5 a las 48 horas posterior a la extubación, siempre y cuando no se necesitara algún método de rescate en la ventilación del paciente, ya sea de forma invasiva o no invasiva. De igual forma se registraron los días de ventilación mecánica y de estancia en la unidad de cuidados intensivos durante todo el periodo de estudio de los pacientes hasta el alta de la unidad, también se registraron las complicaciones que se presentaron durante la fase de destete de la ventilación mecánica en los tres protocolos. Se determinó como éxito del destete una vez que el paciente cumplió 48 horas sin ningún tipo de soporte mecánico ventilatorio invasivo o no invasivo.
Validación de datos: obtenida la recolección de datos se hizo una base de información tipo Excel y se aplicó el Programa Estadístico SPP versión 22.0
Los datos categóricos se expresaron como cuentas o proporciones. Se usó prueba de Wilcoxon en dos colas en la que se comparan datos continuos entre los grupos. Se utilizaron diagramas de caja para los datos en el momento de la extubación. El análisis Kaplan-Meier y la prueba de log rank se emplearon para comparar el tiempo de la extubación entre los grupos. Se recurrió a la prueba de Cox para el análisis de riesgos proporcionales para controlar la línea de base y las diferencias entre los grupos, usando el tiempo de extubación como la variable de resultado. Se validó la hipótesis utilizando Chi cuadrada (χ2) para valorar la relación de las variables nominales.
Resultados
Se logró reclutar a 97 pacientes divididos en tres grupos, 31 correspondieron al Grupo SmartCare®, 33 al grupo Presión Soporte y 33 al grupo Pieza en T, no se encontraron diferencias significativas en las características somatométricas en los tres grupos. Sesenta y dos por ciento correspondió a pacientes con diagnóstico de índole médica y 37.2% quirúrgico. El resto de las características demográficas se expresan en el Cuadro II.
Cuadro II: Características demográficas de los participantes en el estudio.

Abreviaturas: TCE = Traumatismos craneoencefálicos, EVC = Enfermedad vascular cerebral, PO = Posoperado, LAPE = Laparotomia exploradora, SAPS = Simplified Acute Physiologic Score (Puntuación simplificada fisiológica aguda), SOFA = Sequential Organ Failure Assessment (Evaluación secuencial de falla orgánica), A/C= Modo asisto-controlado, SIMV = Synchronized Intermittent Mandatory Ventilation (Ventilación mandatoria intermitente sincronizada), APRV= Ventilación con liberación de presión.
La media de tiempo del destete para el grupo S fue de 93 ± 12 minutos, grupo P de 189 ± 21 minutos y para el grupo T de 198 ± 17 minutos. Cuando se compararon ambos grupos de destete habitual contra el destete automatizado se encontraron diferencias significativas, con una disminución en el tiempo de destete de 50.7% cuando se comparó SmartCare® con Presión Soporte (p = 0.002) y una reducción de 53% cuando se comparó con el grupo de Pieza en T (p = 0.003).
El porcentaje de destete fallido en el grupo S fue de 6.4% (n = 2), en el grupo P 9% (n = 3) y en el grupo T fue de 12.2% (n = 4), con una tendencia a presentar más destetes fallidos en el grupo en el que se utilizó el método de Pieza en T; sin embargo, no se hallaron diferencias significativas al momento de comparar los tres grupos (p = 0.52) (Figura 1). En cuanto a los índices de oxigenación, se observó un promedio durante todo el tiempo de destete en el grupo S de 389.34, en el grupo P de 323.45 y en el grupo T de 302.5, obteniéndose un mejor índice de oxigenación en el grupo en el que se utilizó SmartCare® (p = 0.003). Las variables hemodinámicas se mantuvieron dentro de rangos normales y sin diferencias significativas antes, durante y después del destete. Tampoco se encontraron diferencias significativas en los días de ventilación mecánica ni en los de estancia en la unidad de cuidados intensivos (Cuadro III).

Figura 1: Porcentaje de destete fallido en los tres modos estudiados. No se hallaron diferencias significativas.
Cuadro III: Variables de oxigenación, hemodinámicas, días de ventilación y estancia en la UCI.
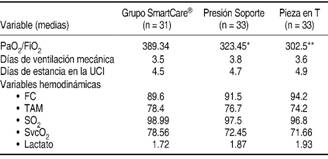
* Diferencia significativa al comparar con grupo SmartCare®.
** Diferencia significativa al comparar con grupo SmartCare®.
Abreviaturas: PaO2 = Presión parcial de oxígeno arterial. FiO2 = Fracción inspirada de oxígeno. UCI = Unidad de Cuidados Intensivos. FC = Frecuencia cardiaca. TAM = Tensión arterial media. SO2 = Saturación venosa mixta de oxígeno. SvcO2 = Saturación venosa central de oxígeno.
Discusión
El destete de la ventilación mecánica es un proceso activo integral y depende mucho de la interacción del paciente y del médico. Este estudio reveló que un método en el que se descarga parte de la atención sanitaria en el paciente que va a ser desconectado de la ventilación mecánica ofrece resultados prometedores en cuanto al tiempo y estabilidad hemodinámica y respiratoria. Este ensayo reveló que se obtuvo un tiempo de destete en el modo automatizado SmartCare® de 93 minutos, con una reducción de más de 50% en el tiempo de este proceso cuando se comparó con los otros dos métodos no automatizados de destete. Cuando lo anterior se compara con la revisión de Cochrane,17 se obtiene una superioridad de aproximadamente 20%, ya que en ese metaanálisis se obtuvo una reducción en el tiempo de destete de 30%. Cabe mencionar que en su grupo de análisis la mayoría de los pacientes fueron postquirúrgicos, a diferencia de nuestro estudio en el que se observó una mayor cantidad de pacientes de índole médica.
Tanto Burns11 como Lellouche12 descubrieron unidades de cuidados intensivos que no contaban con terapistas respiratorios. El uso de métodos automatizados de destete de la ventilación mecánica ofrece una alternativa útil y descarga gran parte del trabajo de enfermería y médico al momento de iniciar el destete, lo cual fue demostrado de igual forma en nuestro estudio, ya que se requirió menos trabajo del personal en la atención del paciente durante el destete y sólo fue necesaria la atención cuando el sistema de destete automatizado informaba que el paciente estaba listo para la separación.
Un aspecto que no había sido valorado en estudios previos son los índices de oxigenación con que cursaban los pacientes durante el proceso de destete; sin embargo, en nuestro estudio se obtuvo un PaO2/FiO2 de 389 mmHg que resultó ser mayor y significativo cuando se le comparó con los métodos no automatizados, dejando claro que los métodos automatizados valoran de forma óptima la dinámica ventilatoria y repercuten de manera más eficiente en la estabilidad en los índices de oxigenación.
Uno de los puntos a notar fue que gran parte de los pacientes evaluados tenían diagnóstico de sepsis o choque séptico, que dista mucho de lo reportado por estudios previos,17 en los que la mayoría de los pacientes eran quirúrgicos o de postcirugía cardiaca, con lo cual se abre la puerta al uso de este sistema en pacientes que tengan periodos de ventilación más prolongados.
Acorde con lo reportado en la literatura,15-17 no fue posible evaluar pacientes que presentaban una cardiopatía previa, situación en la que el destete de la ventilación mecánica cursa con aspectos más específicos, en la que quizá el método automatizado no sea capaz de hacer una evaluación óptima, asimismo están los eventos como broncoespasmo, secreciones o algún artefacto mecánico que pudiera generar algún tipo de diagnóstico erróneo del sistema de destete automático.
No obstante, cuando el juicio clínico del médico intensivista logra balancearse con este tipo de tecnología, puede llegarse a resultados muy alentadores al momento de desconectar a un paciente de la ventilación mecánica.
Conclusiones
El protocolo automático de destete SmartCare® es más eficaz que los métodos no automatizados «Presión Soporte» y «Pieza en T» en el retiro y desconexión de la ventilación mecánica.
Hay una reducción en el tiempo de desconexión de la ventilación mecánica con respecto al protocolo automatizado de destete SmartCare®.
No existen diferencias significativas en los destetes fallidos, días de ventilación mecánica, variables hemodinámicas y días de estancia en la UCI en los tres métodos de destete de ventilación mecánica.
Se obtuvo una mejoría en los índices de oxigenación en el método automatizado de destete SmartCare® cuando se comparó con los métodos no automatizados.











 nueva página del texto (beta)
nueva página del texto (beta)


