Introducción
El prolapso valvular mitral arrítmico (PVMA), definido por la presencia de prolapso valvular mitral (PVM) con o sin disyunción del anillo mitral (DAM) combinado con arritmias ventriculares (AV) frecuentes (≥ 5% carga extrasistólica ventricular o complejas en ausencia de otra etiología)1 está presente en el 10% de pacientes con PVm2, y las arritmias determinarán la toma de decisiones terapéuticas3. Debido a que el PVM se ignora previo a la muerte súbita cardiaca (MSC), el evento raramente es monitorizado4. La presente revisión enfatizará los métodos diagnósticos y la estratificación para dar el tratamiento apropiado.
Anatomía
El aparato valvular mitral posee dos valvas (anterior y posterior), divididas en faldones según Carpentier y unidas por comisuras5, compuestas histológicamente por tres capas mecánicamente diferentes6 y unidas a los músculos papilares por cuerdas tendinosas7. El anillo mitral en diástole adquiere forma circular, formado por una región anterior rígida y otra posterior flexible8, esta última constituida por cuatro elementos unidos por un cordón fibroso discontinuo9. El anillo mitral reduce el estrés del cierre valvular mediante tres movimientos, disminuyendo la altura coaptante e incrementando el área valvular telesistólica10.
Epidemiología
El PVM, la valvulopatía más común (prevalencia del 2-3%)11, presente principalmente en mujeres (1.2:1)12, es la principal indicación de cirugía mitral13. Las AV (presentes en el 43% de casos) son habitualmente benignas14, aunque un grupo poblacional tiene mayor riesgo de MSC (incidencia del 0.14-0.8% anual) sin anomalía estructural concomitante, el 1% con insuficiencia mitral (IM) grave asintomática sin disfunción sistólica del ventrículo izquierdo (DSVI), el 3.1% con IM grave en clase funcional II con DSVI, el 4.9% con fibrilación auricular, el 7.8% por año en clase funcional III-IV y el 12.7% con una fracción de expulsión del ventrículo izquierdo (FEVI) < 50%15,16. El PVMA origina el 4-13% de las MSC inexplicables17,18 y el 6.6% en caso de fibrilación ventricular idiopática19. Afecta principalmente a jóvenes (edad promedio: 30 años) y con antecedentes familiares20.
Prolapso valvular mitral
El PVM (desplazamiento telesistólico de uno o ambos velos > 2 mm por debajo del plano anular dentro de la aurícula izquierda en la vista paraesternal o apical de eje largo)21 es una condición progresiva22 manifestada en dos formas: la enfermedad de Barlow y la deficiencia fibroelástica23. La enfermedad de Barlow implica un grosor bivalva ≥ 3 mm, dilatación anular y cuerdas tendinosas resistentes debido a una esponjosa rica en glucosaminoglucanos y calcificación in situ en pacientes de 40-60 años de edad24. La deficiencia fibroelástica (fenotipo más común) manifiesta adelgazamiento de un solo segmento prolapsado (habitualmente P2) y se asocia a una cuerda rota por déficit conectivo en individuos de edad avanzada24. En ambos fenotipos, el 78.4% tienen prolapso posterior, el 4.6% anterior y el 17% bivalvo25. Hereditariamente se presenta como enfermedad de Barlow, a diferencia de la forma esporádica (deficiencia fibroelástica), y ambos tipos son clasificados como primarios (mendeliano) o secundarios (sindrómico)26. La asociación con variantes patogénicas de genes relacionadas con miocardiopatías (titina [TTN] y filamina C [FLNC]) podría explicar la remodelación desproporcionada del ventrículo izquierdo27, que ocurre en el 8-16% de los pacientes28, donde la IM actuaría como disparador29.
Disyunción del anillo mitral
La DAM (separación sistólica entre la unión de la pared auricular y la pared libre del ventrículo izquierdo ≥ 2 mm en la proyección de eje largo)30, que tiene una prevalencia del 8.7-96%31,32, está asociada con PVM (22.9-54% de los pacientes)31,33. Es habitual en prolapsos bivalva34 con una incidencia del 20% con IM grave concomitante35, detectada en dos tercios de la circunferencia del anillo mitral36 bajo P1-P2 (69.2%)34 y globalmente bajo la valva posterior (98% de los casos)37 intercalado con tejido sano36, clasificándose como tipo 0 (ausente, 7.6%), tipo I (segmento ventricular basal hipermóvil sin DAM, 66.5%), tipo II (DAM < 5 mm, 25.4%) y tipo III (DAM ≥ 5 mm, 0.5%)38. La disyunción aplana y expande el anillo mitral sistólicamente, causando mayores área anular diastólica (1646 ± 410 mm2), diámetro intercomisural (48 ± 7 mm)28 y diámetro anteroposterior (34-41 mm)34, predisponiendo a prolapso en ausencia de enfermedad intrínseca35 y causando dilatación, DSVI, hipertrofia miocárdica regional y fibrosis39, asociada con AV que es el mayor predictor (hazard ratio: 1.90; p < 0.0001)40, con incidencia arrítmica del 33% a 5 años y del 66% a 10 años tras el diagnóstico14.
Fisiopatología
La DAM y el PVM desencadenan AV por estiramiento de los músculos papilares y de la base inferolateral del ventrículo izquierdo28 y por el contacto valvar diastólico, prolongando el período refractario funcional y desarrollando posdespolarizaciones precoces (hipótesis de Padua)41. Los mecanorreceptores prolongan y dispersan el intervalo QT por activación miofibroblástica22 y la actividad simpática incrementada produce extrasístoles ventriculares debido a mecanismos homeostáticos del calcio intracelular, causando posdespolarizaciones tardías42. Las fibras de Purkinje en la base papilar crean una reentrada funcional originando fibrilación ventricular (FV) y MSC41. La tracción sistólica del músculo papilar provoca inflamación y fibrosis, estableciendo un sustrato (primer golpe) y requiriendo un segundo impacto (extrasístoles ventriculares) para sostener arritmias malignas41. Además, la inserción apical de los músculos papilares (57% de los casos) incrementa dicha fibrosis43. Las AV a menudo son polimórficas, originándose principalmente del músculo papilar posteromedial, y favorecen anisotropía con diversas morfologías electrocardiográficas44. También los agregados plaquetarios y los depósitos de fibrina en la zona disyuntiva provocan microémbolos coronarios como fuente adicional arrítmica45, junto con variantes genéticas patogénicas miocárdicas arrítmicas (FLNC/lámina A [LMNA]) y de canales iónicos46,47.
Evidencia patológica en el prolapso valvular mitral arrítmico
La prevalencia de PVM en series de autopsias se estima en un 4-7%17 con afección bivalva en el 70% de los casos48. La MSC se manifiesta como FV y taquicardia ventricular sostenida (TVS) en el 70% y el 30% de los casos, respectivamente16. La histopatología revela colágeno tipo 1 en los músculos papilares (100%), la pared inferior basal del ventrículo izquierdo (88%)18 y el tabique interventricular (24%)49, con afección subendocárdica-intramural en el 85% de las muestras50, existiendo fibrosis perivascular51 y DAM en el 5% de los casos sin PVM48.
Manifestaciones clínicas
Se presentan palpitaciones, dolor torácico atípico y signos ortostáticos con o sin AV14. El síncope en ausencia de AV, presente en el 2-3.6% de los casos52, existe en el 35% de las MSC20 y predice AV graves (odds ratio [OR]:6.96; intervalo de confianza del 95% [IC95%]: 1.05-46.01; p = 0.044)53, siendo el 15% de los casos de MSC previamente asintomáticos20. Las AV ocurren en reposo (53%), al esfuerzo (29%) y en el sueño (12%)18,54. En la enfermedad de Barlow se ausculta un clic mesotelesistólico a nivel del ápex, con o sin soplo de IM, mientras que la deficiencia fibroelástica tiene frecuentemente un soplo holosistólico55.
Biomarcadores
Un valor elevado del factor de supresión soluble de la tumorogenicidad 2, producto del estrés biomecánico local, está asociado con FEVI reducida y fibrosis papilar en comparación con sujetos controles (31.6 ± 10.1 vs. 25.3 ± 9.2 ng/ml; p = 0.01), junto con niveles altos del factor de crecimiento transformante beta 156.
Electrocardiografía
Un intervalo QRS fragmentado es un marcador cicatricial miocárdico asociado con AV complejas57, pero no así su duración58. Las ondas T negativas o bifásicas en las derivaciones inferolaterales (65.3-80% de los casos con MSC)15,19 son marcadores de riesgo de MSC (p < 0.00001)40 y junto con la depresión del segmento ST duplican el riesgo de AV leves/moderadas e incrementan ocho veces las formas graves14,15. Existe prolongación del intervalo QTc (450 ± 38 ms) y dispersión14,59, vinculado al grosor valvar mitral anterior y prolapso grave60. Las AV complejas (extrasístoles ventriculares multifocales, taquicardia ventricular no sostenida [TVNS] > 180 lpm y TVS/FV14) están presentes en > 80% de los casos de MSC15. La morfología de las extrasístoles ventriculares puede estimar su origen en el aparato mitral (sensibilidad y especificidad del 100%)61. El síndrome de QT largo puede coexistir, experimentándose más AV que si existe aislado (p = 0.009)62. Además, las máquinas de inteligencia artificial capaces de detectar AV tienen un futuro prometedor63.
Evaluación ecocardiográfica
Los ecocardiogramas transtorácico y transesofágico evalúan detalladamente la VM, principalmente con la función en tercera dimensión64 y con técnicas nuevas (Fig. 1)65, definiendo cuatro fenotipos de PVM: deficiencia fibroelástica, deficiencia fibroelástica plus, forma frustrada y enfermedad de Barlow66. El grosor valvar (≥ 0.49 mm; p < 0.0001)67, el número de velos prolapsados (p < 0.001)68 y una mayor longitud valvar (valva anterior 24.1 ± 4 mm, valva posterior 17 ± 4.1 mm) se asocian con MSC14,69. Al diagnosticar la DAM (precisión del 88.7% para el ecocardiograma transtorácico y del 94.7% para el transesofágico)70 deberá excluirse al determinar la FEVI71, calculando su índice de disyunción72. La DAM es un predictor de AV complejas (p = 0.002)73, con un valor > 4.8 mm asociado a fibrosis local74 y > 8.5 mm con TVNS (OR: 10; IC95%:1.2-78.1)75, y lo mismo que un anillo mitral dilatado (área 5.7 ± 1.3 cm2/m2; p = 0.02)69. La DSVI manifestará un strain radial y circunferencial reducido76, con valores longitudinales segmentarios supranormales (> 24%) en el tridente posterolateral e infranormales en segmentos opuestos77. La fibrosis regional provoca dispersión mecánica, manifestada como una relación de dispersión basal/medial ≥ 122 ms asociada con AV independientemente de la DSVI y de la gravedad de la IM, siendo mayor en pacientes portadores de desfibrilador automático implantable (DAI)69,78. Además, la contracción postsistólica de los segmentos posterolaterales medio/basal del ventrículo izquierdo por la tracción del músculo papilar origina un movimiento discinético relativo («pie de bailarina»)79. La tracción del músculo papilar posteromedial desplaza la pared basal ventricular hacia el ápex a gran velocidad, dando una señal mesotelesistólica por Doppler tisular pulsado ≥ 16 cm/s, conocida como pickelhaube, en el 20% de los pacientes19, relacionada con AV (p < 0.08)69 y realce tardío con gadolinio en la resonancia magnética cardiaca80. Existe un incremento del índice de trabajo miocárdico en el segmento lateral basal (≥ 2200 mmHg%) asociado con MSC (p < 0.001) coincidiendo con un strain longitudinal regional ≥ −25%81. La IM degenerativa suele ser meso/telesistólica con un flujo excéntrico opuesto al segmento prolapsado, donde el método PISA (proximal isovelocity surface area) para cuantificarla en su variante en tercera dimensión es muy preciso82. Así, el 70% de los pacientes con PVM tienen algún grado de IM (grave en el 4-7%)83, presente en el 36.3% de aquellos con MSC15, presagiando AV (RR: 8.92)14, teniendo precaución al cuantificarse al considerar el volumen prolapsado (grave > 15 ml)84. Además, existe dilatación del área anular tricúspidea principalmente con la enfermedad de Barlow vinculada a insuficiencia tricuspídea residual tras una anuloplastia mitral85. Ante síndromes genéticos, hay que excluir dilatación aórtica asociada86.
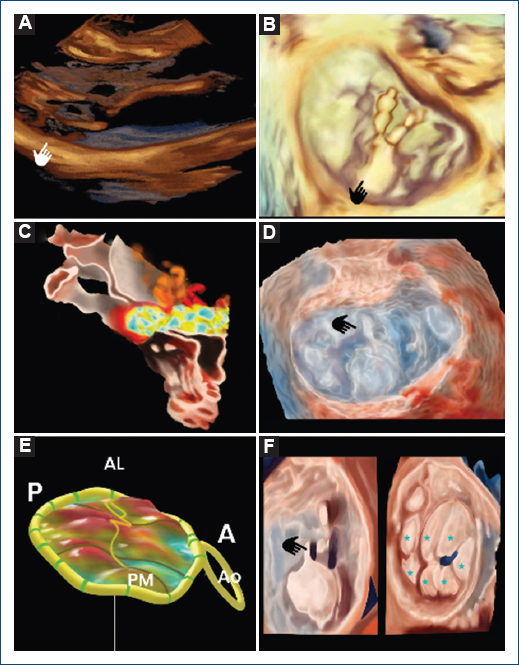
Figura 1 Ecocardiografía mitral en tercera dimensión (3D). A: ecocardiograma transtorácico 3D en el que se aprecia la disyunción del anillo mitral a nivel de la pared inferolateral del ventrículo izquierdo. B: ecocardiograma transesofágico 3D en el que se visualiza un prolapso de festón P2. C: insuficiencia mitral identificada por Doppler color con efecto de transparencia en el ecocardiograma transesofágico 3D. D: ecocardiograma transesofágico 3D con técnica de transparencia en el que se aprecia flail en P2 (señalado). E: modelo cuantitativo de la válvula mitral y su anillo en 3D que muestra un prolapso de múltiples festones en ambas valvas (enfermedad de Barlow). F: a la izquierda, imagen de ecocardiograma transesofágico 3D en la que se aprecia un prolapso del festón P2 (señalado) con función de transparencia; a la derecha, enfermedad de Barlow con múltiples festones prolapsados con función true view (estrellas). Ao: aorta; PM: posteromedial; AL: anterolateral, A: anterior; P: posterior
Resonancia magnética cardiaca
La resonancia magnética cardiaca es el método de referencia en la evaluación volumétrica y funcional ventricular87. La evaluación morfológica mediante imágenes de precesión libre en estado estacionario equilibrado diagnostica el PVM con una sensibilidad y una especificidad del 100% para la valva posterior y con valores menores para la anterior88. Con ella, la DAM presenta dos morfologías: pseudo-DAM (yuxtaposición valvar posterior) y verdadera DAM89, con un 50% de pacientes teniendo disyunción tricuspídea90. La hipertrofia basal inferolateral (índice > 1.5) coincide topográficamente con fibrosis sustitutiva y se correlaciona con el grado de DAM y con valores de curling > 3.5 mm91, y la función feature tracking demuestra un patrón bimodal asociado a fibrosis (p < 0.001)92. El realce tardío con gadolinio, presente en el 28-36.7% de los casos93,94, se asocia con AV y fibrosis histológica en el músculo papilar posteromedial (84-88%), la pared basal inferolateral (31.1-93%) y la pared basal inferior del ventrículo izquierdo (10.7%), exhibiendo patrones intramural (12.6%), parcheado (músculos papilares, 8.1%) o subendocárdico (0.8%)36,94. El 1.2-10% de la masa del ventrículo izquierdo puede presentarlo18,93, asociado con dilatación ventricular y correlacionado con el grado de IM (13% leve, 28% moderada, 37% grave)93, presagiando corrección quirúrgica94. Ante una DAM > 5 mm (30% de los pacientes con PVM) existe mayor realce tardío con gadolinio y peor carga arrítmica (p = 0.002)95. Un valor reducido en el mapeo T1 poscontraste (334 ± 52 ms) se correlaciona con dilatación ventricular y AV junto con tiempos T1 nativos globales elevados (1124.9 ± 97.5 ms) en la pared inferolateral basal/medial del ventrículo izquierdo, independientemente del grado de IM96,97. El volumen extracelular elevado (en el 87% de los pacientes con DAM y PVM, el 93% con realce tardío con gadolinio y el 81% con PVM y realce tardío con gadolinio ausente)98 se vincula a dilatación ventricular en pacientes asintomáticos con IM moderada/grave99. Existen valores anormales de T1, T2 y volumen extracelular en el 58%, el 25% y el 16%, respectivamente, de los pacientes con AV complejas100. Un volumen prolapsado > 15 ml contribuye al remodelado cardiaco (16% de los casos)93 actuando como una tercera cámara101.
Tomografía computarizada
La tomografía computarizada (sensibilidad del 92.6% y especificidad del 97.1%) para detectar PVM es limitada técnicamente por baja resolución temporal, radiación y poca sensibilidad para observar faldones prolapsados individuales (68.5%)102.
Prueba de esfuerzo
La prueba de esfuerzo desenmascara la AV por estimulación adrenérgica (grado de recomendación [R]: IC)1 incluso durante la fase de recuperación25, prediciendo mortalidad por causa cardiovascular incluyendo pacientes asintomáticos103.
Tomografía por emisión de positrones
A mayor cicatriz, los pacientes con AV complejas exhiben menor captación de 18F-fluorodesoxiglucosa detectada por tomografía con emisión de positrones/resonancia magnética cardiaca, respecto a formas simples (70 vs. 85%) en las que solo existe inflamación (focal o focal más difusa)104.
Estratificación del riesgo arrítmico
Existen dos fenotipos de PVMA: la IM degenerativa y el PVM grave (DAM más enfermedad de Barlow)1. La estratificación multidimensional es necesaria (R: IC)1 (Fig. 2). Los pacientes asintomáticos sin alteraciones estructurales ni electrocardiográficas requerirán un estudio Holter y ecocardiograma periódicos (R: IIa), priorizando ante palpitaciones/síncope (R: IC)1. En caso de TV de alto riesgo se colocará un DAI incluso en pacientes asintomáticos con o sin reparación mitral (R: IIa)1; si son de riesgo bajo o moderado, se colocará un grabador de asa implantable para detectar AV graves, y también en aquellos con una o más características fenotípicas o síncope arrítmico sugestivo (R: IIa)1. Ante una MSC abortada se colocará un DAI (R: IA)105, y si las AV persisten se realizará ablación con catéter con o sin fármacos antiarrítmicos (R: IC)1. La evaluación periódica es indispensable ante extrasístoles ventriculares frecuentes para identificar una miocardiopatía secundaria (R: IIa)105. La resonancia magnética cardiaca estará indicada con al menos un aspecto fenotípico presente (R: IIa)1, síncope inexplicable, TVNS, MSC o AV sostenidas antes de colocar un DAI (R: IC)1. Si durante el estudio electrofisiológico, indicado ante un síncope sospechoso o un hallazgo anómalo no invasivo, se detecta TVS monomórfica, esta será específica105. Sin embargo, por medio de estimulación ventricular programada, incluso con MSC documentada, los hallazgos son limitados (TVS monomórfica 5%, TVNS 23%, FV 18% y no inducibilidad 55%)20, por lo que no reemplaza al monitoreo electrocardiográfico106.
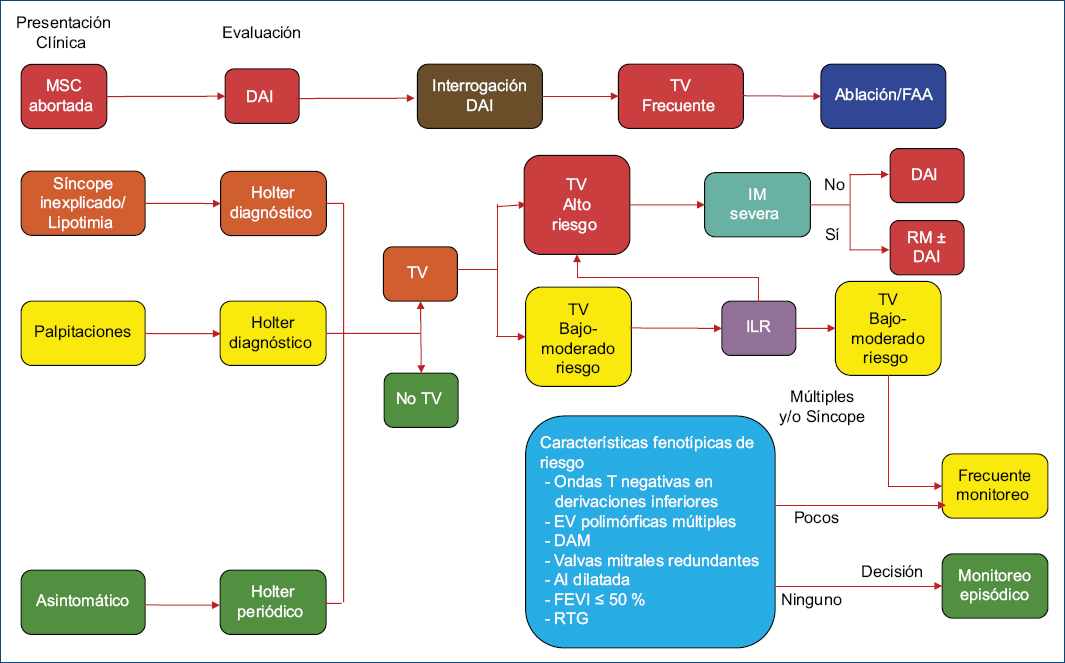
Figura 2 Algoritmo diagnóstico y terapéutico del paciente con prolapso valvular mitral o prolapso valvular mitral arrítmico. DAI: desfibrilador automático implantable; DAM: disyunción del anillo mitral; EV: extrasístoles ventriculares; FAA: fármacos antiarrítmicos; FEVI: fracción de expulsión del ventrículo izquierdo; ILR: implantable loop recorder (grabador de asa implantable); IM: insuficiencia mitral; MSC: muerte súbita cardiaca; RM: reparación mitral; RTG: realce tardío con gadolinio; TV: taquicardia ventricular.
Tratamiento médico
Los fármacos antiarrítmicos se emplearán ante sintomatología independientemente de la FEVI107. Los betabloqueantes reducen la contractilidad mitral y disminuyen la actividad simpática, y junto con los bloqueadores de los canales de calcio reducen moderadamente la carga extrasistólica (R: IC)105, siendo más efectivos al combinarse con fármacos antiarrítmicos de clase IC ante patología estructural ausente (R: IIa/C)105,108. La amiodarona reduce mejor las AV, empleándose como tercera línea (R: IIIC)105, sin disminuir totalmente el riesgo de MSC18. Los pacientes con IM grave no candidatos a cirugía ni a reparación percutánea deberán recibir tratamiento farmacológico óptimo para la insuficiencia cardiaca (R: IA)109. Ante una FEVI reducida y una carga de extrasístoles ventriculares ≥ 10%, donde la ablación es considerada de alto riesgo, no deseada o fallida, el uso de fármacos antiarrítmicos será apropiado (R: IIa/C)1,105.
Desfibrilador automático implantable
Los pacientes con un síncope arrítmico y TVS (R: IIa) o TVNS (R: IIb), o con AV persistentes tras ablación transoperatoria, se benefician del DAI1,3, así como en caso de IM con DSVI sin opciones correctivas y sin respuesta farmacológica (R: IA)109, otorgando terapias apropiadas a 42 meses en el 21.1% de los casos19, debiéndose mantener precaución al determinar sus algoritmos110.
Ablación con catéter
La ablación del foco arrítmico es factible independientemente del fenotipo de PVM111. La ablación intrapapilar (éxito inicial del 76% y a largo plazo del 75%; p = 0.001)112,113 es limitada por la mala estabilidad del catéter debido al movimiento enérgico de las cabezas papilares y la ubicación114. La ecocardiografía intracardiaca y otras técnicas intentan mejorar la interfaz catéter-tejido para entregar mejor la energía ablativa (R: IIa)1, donde la ablación en la base papilar evita complicaciones115. La crioablación alcanza un éxito de casi el 100%111, y realizada durante la reparación mitral reduce la carga extrasistólica > 90% (R: IIa)1,116. Existen recurrencias provenientes de focos arrítmicos ausentes en el momento del procedimiento inicial, requiriéndose vigilancia a largo plazo117.
Tratamiento quirúrgico
Las indicaciones quirúrgicas son ampliamente conocidas y la reparación mitral, recomendada (R: IB)118, disminuye la frecuencia de AV posoperatorias (p = 0.005)14. El respeto estructural es efectivo sin importar el antecedente de DAM, y en la enfermedad de Barlow podrá requerirse resección valvar119. La degeneración mixomatosa avanzada, la DAM, el prolapso multisegmentario, la calcificación anular grave y un elevado volumen prolapsado predicen independientemente fracaso quirúrgico120. Sin embargo, los resultados tempranos y tardíos son excelentes, con pérdida del impacto disyuntivo arrítmico (éxito del 87%)73. La reducción de AV ocurre al mejorar la repolarización y disminuir el volumen del ventrículo izquierdo, en los 6 meses a 3 años posoperatorios121, aunque su sola presencia aún no es una indicación quirúrgica. Ante un riesgo quirúrgico prohibitivo, estarían indicados abordajes percutáneos (R: IIb/B)118. Además, el Mitraclip® (Abbott Vascular, California, USA) aplicado en la enfermedad de Barlow es capaz de disminuir la carga arrítmica ventricular122.
Actividad física
Los pacientes asintomáticos con PVM e IM leve pueden participar en deportes competitivos (R: IC), pero no pueden hacerlo aquellos con antecedentes personales de MSC, síncope arrítmico o AV complejas, entre otras características123,124, independientemente del tratamiento recibido (R: IIIC)125, aun sin haberse determinado una asociación clara entre la dosis moderada de ejercicio y la aparición de AV graves126. Si se requiere un DAI, se implantará en el lado contralateral respecto al brazo dominante, y se esperará 3 meses para practicar ejercicio124; en aquellos sin bradicardia, un DAI subcutáneo es una opción (R: IIa/B)105 sin sustituir la restricción deportiva123.
Conclusiones
El hallazgo de PVM, pese a considerarse una característica anatómica sin repercusiones relevantes, ha sido implicado con MSC, y esto puede ser prevenido mediante el reconocimiento de un fenotipo particular. Con el máximo aprovechamiento de los estudios de gabinete cardiovascular será posible la estratificación del riesgo clínico-morfológico, y con ello aplicar todos los elementos terapéuticos y reduciendo la morbimortalidad de la manera más eficaz posible.











 nueva página del texto (beta)
nueva página del texto (beta)


