Servicios Personalizados
Revista
Articulo
Indicadores
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Agrociencia
versión On-line ISSN 2521-9766versión impresa ISSN 1405-3195
Agrociencia vol.42 no.3 Texcoco abr./may. 2008
Fitociencia
Composición del aceite esencial en germoplasma de Tagetes filifolia Lag. de la región centro–sur de México
Composition of essential oil in germplasm of Tagetes filifolia Lag. from central–south region of Mexico
Miguel Á. Serrato–Cruz1, Francisco Díaz–Cedillo2 y Juan S. Barajas–Pérez3
1 Metodología de Investigación. Departamento de Fitotecnia. Universidad Autónoma Chapingo. 56230. Chapingo, Estado de México. (serrato@correo.chapingo.mx).
2 Departamento de Química Orgánica. Escuela Nacional de Ciencias Biológicas. Instituto Politécnico Nacional. Prolongación Carpio y Plan de Ayala, Casco de Santo Tomás. 11340, México, D. F.
3 Centro de Desarrollo de Productos Bióticos. Instituto Politécnico Nacional. San Isidro Km 8.5 Carretera Yautepec–Jojutla. 62730. Yautepec, Morelos, México.
Recibido: Mayo, 2007.
Aprobado: Noviembre, 2007.
Resumen
Los aceites esenciales de Tagetes filifolia tienen potencial para controlar insectos biotransmisores de virus en plantas. El objetivo del presente estudio fue evaluar la composición del aceite esencial de 78 recolectas de T. filifolia de la región centro–sur de México, establecidas en Chapingo, México. Cuando las plantas presentaron floración se hizo la extracción de aceites esenciales por arrastre de vapor usando 500 g de tejido de la planta completa. La composición química del aceite se determinó con cromatografía de gases acoplada a masas. Los compuestos principales del aceite fueron 4–alilanisol y trans–anetol (4–propenilanisol), en forma individual o en mezcla: 1.3% de las recolectas sólo con anetol, 7.7% de las recolectas sólo con alilanisol y 91% de recolectas con mezcla. En las recolectas con mezcla de anetol y alilanisol, la proporción de estos compuestos químicos fue variable.
Palabras clave: Tagetes filifolia, aceites esenciales, composición química, germoplasma mexicano.
Abstract
The essential oils of Tagetes filifolia have potential for controlling insects that are biotransmitters of virus in plants. The objective of the present study was to evaluate the composition of the essential oil of 78 accessions of T. filifolia of the south–central region of México, established in Chapingo, México. When the plants presented flowering, the extraction of the essential oils was made by simple distrillation process using 500 g of tissue of the complete plant. The chemical composition of the oil was determined with gas chromatography coupled to masses. The principal components of the oil were 4–alilanisole and trans–anethole (4–propenilanisole), individually or in mixture: 1.3% of the accessions only with anethole, 7.7% of the accessions only with alilanisole and 91% of accessions with mixture. In the accessions with mixture of anethole and alilanisole, the proportion of these chemical compounds was variable.
Key words: Tagetes filifolia, essential oils, chemical composition, Mexican germplasm.
INTRODUCCIÓN
El empleo de aceites esenciales extraídos de plantas aromáticas es una opción importante para controlar insectos (Calmasur et al., 2006; Isman, 2006), hongos (Terblanche y Cornelius, 2000) y nemátodos (Perez et al., 2003) causantes de fuertes daños a la agricultura. El uso del aceite esencial de la especie aromática Tagetes filifolia Lag. tiene amplio potencial contra nemátodos e insectos biotransmisores de virus (Cubillo et al., 1999; Serrato, 2003; Serrato et al., 2005). Los bajos costos de producción del aceite esencial de esta especie (Serrato, 2003) y su origen orgánico, representan una opción económica y ecológica importante comparada con productos insecticidas de origen sintético, los cuales, además de ser fuente de contaminación ambiental y de daño a la salud humana, parcialmente son causa de incosteabilidad de los sistemas de producción agrícolas.
Los compuestos químicos anetol y alilanisol, del grupo fenilpropanoides, constituyen la mayor parte del aceite esencial de T. filifolia (Zygadlo et al., 1993; Feo et al., 1998; Vila et al., 2000). El anetol produce diferentes efectos biológicos como repelente, insecticida, fungicida, nematicida y bactericida y es un ingrediente activo del aceite esencial obtenido de las familias botánicas Lamiaceae y Apiaceae, especialmente de especies de los géneros Timbra, Satureja, Origanum, Corydothymus, Pimpinella y Foeniculum, las que contienen configuraciones químicas cis–anetol y trans–anetol (Tuzun y Yegen, 2000).
En la familia botánica Asteraceae la presencia de anetol es infrecuente, aunque en el género Tagetes, con centro de diversidad en México, las especies T. filifolia y T. mandonii contienen anetol en su aceite esencial. En T. mandonii, 12.7% del aceite corresponde a fenilpropanoides y sólo 9.2% corresponde a cisanetol (Senatore y Feo, 1999), composición muy pobre comparada con la de T. filifolia, donde los fenilpropanoides abundan y cuyas moléculas mayoritarias son anetol (33 a 68%) y alilanisol (13 a 61%) (Feo, 1998; Vila, 2000; Serrato et al., 2005).
En la literatura sobre la composición del aceite de T. filifolia se advierten algunas diferencias: 1) el número de sus compuestos reconocidos varía de 33 (Vila et al., 2000) a 57 (Feo et al., 1998); 2) se ha encontrado tanto cis–anetol (Feo et al., 1998) como trans–anetol (Zygaldo et al., 1993; Vila et al., 2000); 3) la cantidad de alilanisol y de anetol en la composición total del aceite esencial es 61.2% y 33.1% (Vila et al., 2000), a 21% y 79% (Serrato et al., 2005), o 13.7% y 68.3% (Feo et al., 1998). Esta variabilidad en la composición química del aceite esencial de T. filifolia se puede deber a diferencias ambientales entre los lugares de origen del material analizado, ya que esta especie se distribuye en forma silvestre desde el sur de EE.UU. hasta Argentina (Neher, 1965). En México, la especie se localiza en altitudes de 600 a 2600 m en diferentes climas y suelos (Neher, 1965; Turner, 1996; Villarreal, 2004). Para T. minuta se ha encontrado variación en el contenido del aceite esencial asociada con la diversidad de hábitats de origen de las muestras, y se ha confirmado la existencia de quimiotipos (Gil et al., 2000). Esta relación químico–ambiental también se ha encontrado en Artemisia (Putievsky et al., 1992) y en Mentha (Chou y Zhou, 1998).
El primer antecedente sobre la composición esencial de materiales mexicanos de T. filifolia es el de Serrato et al. (2005), quienes usaron muestras de una población silvestre recolectada en Tlalámac, Atlautla, México, localidad con clima transicional, altitud de 1720 m y suelo aluvial. Al cultivar estas plantas de Tlalámac pero en las condiciones de Chapingo, con clima templado subhúmedo, altitud de 2240 m y suelo franco arcilloso, se encontró la presencia de alilanisol 21 y transanetol 79%; este contenido fue constante durante diferentes fechas de cultivo de la especie.
El aceite esencial de T. filifolia constituye una importante fuente natural de anetol y alilanisol, pero se desconoce la variabilidad en la composición de su aceite esencial en función del origen geográfico. El conocimiento de la composición del aceite esencial de T. filifolia es fundamental para poder utilizarlo en la agricultura mexicana, especialmente para su uso en el control de insectos plaga (Serrato et al., 2003).
El Sistema Nacional de Recursos Fitogenéticos de la Secretaría de Agricultura Ganadería y Recursos de Pesca en México, aprobó un proyecto para la recolección y caracterización de T. filifolia, incluyendo la conformación de un Banco de Germoplasma Nacional con materiales de las regiones centro–sur, sur y norte de México. La caracterización morfológica preliminar de recolectas de la región centro–sur indica que es amplia la variabilidad de estos materiales, los cuales crecen en 27 variantes climáticas en altitudes de 750 a 2686 m (Serrato y Barajas, 2006). Los distintos aromas reconocidos cualitativamente en recolectas de esta región geográfica permiten suponer una composición química diferente (Serrato y Barajas, 2006). Con base en los planteamientos expuestos, el objetivo del presente trabajo fue evaluar la composición del aceite esencial en germoplasma de T. filifolia proveniente de la región centro–sur de México.
MATERIALES Y MÉTODOS
Procedencia de las recolectas
De septiembre a noviembre del 2004 se hizo la primera exploración botánica a localidades de varios Estados de la región centro–sur de México y se depositaron 104 accesiones de semillas en el Banco de Germoplasma Salvador Miranda Colín de la Universidad Autónoma Chapingo (Serrato y Barajas, 2006), pero sólo 78 de esas recolectas se incluyeron en el presente estudio (Cuadro 1) debido a distintos problemas para el establecimiento del total de recolectas.
Establecimiento de las recolectas
El 18 de junio de 2005 se sembraron 30 semillas de cada recolecta de la cosecha del 2004 en bandejas de poliestireno expandido para germinación, de 200 cavidades, que se mantuvieron en invernadero. Las plántulas se llevaron al Campo Agrícola Experimental del Departamento de Fitotecnia, en la Universidad Autónoma Chapingo; el trasplante fue el 20 de julio de 2005 a una distancia entre plantas de 30 cm, en surcos de 5 m de largo y distancia entre ellos de 85 cm. Se aplicaron riegos rodados según necesidad de las plantas y deshierbes manuales.
Extracción de aceite
Cuando las plantas se encontraban en plena floración, se prepararon muestras de toda la planta y se sometieron a un proceso de destilación simple. La extracción de aceite se inició el 18 de octubre de 2005 y duró una semana. Se empleó un equipo de destilación que consiste en fuente de energía, matraz de destilación (20 L) e intercambiador de calor. En el matraz de destilación se introdujo 0.5 kg de biomasa triturada (partículas 3–5 cm largo), se adicionaron 4 L de agua destilada calentada a punto de ebullición, se colocó el matraz en la fuente de energía (tela de asbesto cemento montada en una resistencia eléctrica) para una ebullición de 60 min (tiempo de destilación) y se recolectó el aceite de cada muestra con una probeta de 100 mL. De cada recolecta se realizaron tres extracciones.
Análisis del aceite
Muestras de aceite esencial puro (1 µL) de cada recolecta se diluyeron en 2 mL de cloruro de metileno y de esta solución se tomó una muestra la cual se inyectó a un cromatógrafo de gases modelo Finnigan Trace GC Ultra, mediante un inyector Split a 250 °C, usando una columna RTX–5MX, 5% difenil–95% dimetilpolisiloxano, de 30 m X 0.25 mm D X 0.25 µm, con detector de masas PolarizQ. Se usó un horno a temperatura inicial de 70 °C X 1 min, con rampa de 20 grados por min, hasta una temperatura final de 250 °C. Se usó inyector con temperatura de la línea de transferencia de 300 y con velocidad de flujo de 50 mL min–1; el tiempo de purga fue 1 min y se usó gas acarreador de He con presión de 100 kp; el volumen de la inyección fue 1 mL. El equipo de cromatografía se acopló al programa Xcalibur para realizar el proceso cuantitativo y obtener datos graficados.
La identificación y cuantificación de los compuestos se realizaron comparando los tiempos de retención cromatográficos, espectros de masas y de resonancia magnética nuclear de hidrógeno (RMN 1H), con los determinados a partir de patrones auténticos de alilanisol y de trans–anetol. En todas las muestras el porcentaje de cada compuesto de la mezcla se estableció relacionando el área bajo la curva del compuesto identificado con la de un estándar interno de trans–anetol o de alilanisol a una concentración de 15 mg mL–1. Todas las calibraciones de patrones y muestras fueron por triplicado (Zhang y Zuo, 2004).
RESULTADOS Y DISCUSIÓN
El cromatograma del aceite presentó dos señales principales con tiempos de retención a 5.50 y 6.20 min. Muestras de aceite con una sola señal se analizaron por RMN 1H; el análisis de estos espectros (desplazamiento químico, constantes de acoplamiento y multiplicidad de las señales) permitió identificar que el pico a 5.50 min corresponde a alilanisol (4–alilanisol) y el de 6.20 al trans–anetol (4–propenilanisol). Se inyectaron patrones de alilanisol y trans–anetol al cromatógrafo de gases–masas y se registraron tiempos de retención de 5.50 y 6.20 min, lo cual confirmó la identidad de los componentes del aceite (Figura 1).
La composición química del aceite esencial de las 78 recolectas indicó la presencia mayoritaria de alilanisol y de trans–anetol (Cuadro 2), compuestos principales identificados por Zygaldo et al. (1993) y Vila et al. (2000). De acuerdo con la composición de las 78 recolectas analizadas, parece que la molécula de trans–anetol es frecuente en el germoplasma mexicano y distinta del cisanetol que contiene T. filifolia en Sudamérica (Feo et al., 1998).
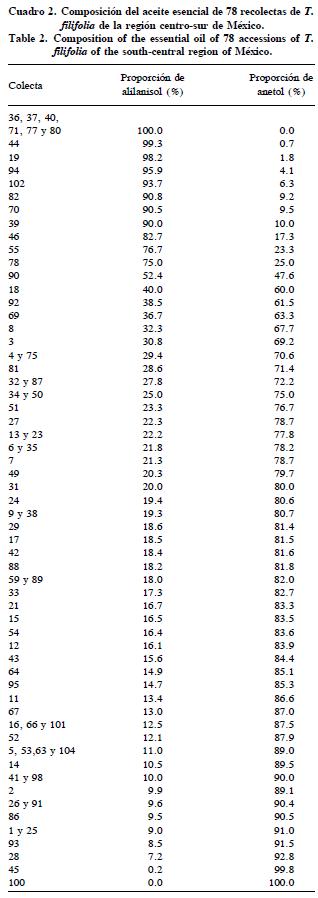
Lo novedoso de estos resultados es que las recolectas presentaron una composición específica de alilanisol y de anetol (Cuadro 2): 1.3% de recolectas sólo contenían anetol, 7.7% sólo alilanisol y 91 % contenían ambos compuestos, lo cual sugiere la posible existencia de quimiotipos. Antes sólo se había encontrado la mezcla de alilanisol y anetol en el aceite esencial de esta especie (Feo et al., 1998; Vila et al., 2000; Serrato et al., 2005).
En el grupo de recolectas con mezcla de compuestos (71 recolectas) se detectaron distintas tendencias en las proporciones de anetol y alilanisol en el aceite esencial (Cuadro 2): a) 12.6% de recolectas con más alilanisol que anetol, b) 1.2% de recolectas con cantidades parecidas de los compuestos, c) 86.2% de recolectas con menos alilanisol que anetol. Estos resultados amplían lo encontrado por Feo et al. (1998) y Vila et al. (2000), y en particular lo reportado por Serrato et al. (2005) para la recolecta 104 (79% de trans–anetol y 21% de alilanisol).
Las diferencias en la proporción de los compuestos químicos en el aceite esencial de T. filifolia en la región centro–sur de México se puede explicar por la interacción evolutiva entre las poblaciones silvestres y su ambiente, como se ha documentado para otras especies productoras de aceite (Putievsky et al., 1992; Chou y Zhou, 1998). En este sentido, los diferentes compuestos detectados, solos o en mezcla, se encontraron en las recolectas procedentes de diferentes pisos altitudinales, excepto para la recolecta que solamente presentó anetol (Cuadro 3). No obstante, las variaciones en la composición de aceites observadas en las 78 colectas evaluadas ocurrieron en un ambiente diferente (área de Chapingo) al de los sitios naturales donde se obtuvieron las muestras, por lo que sería importante corroborar estos datos con muestras in situ.
También se encontró variación en la composición química en materiales recolectados en el mismo sitio como en Yecapixtla (1558 m), Uruapan (1454 m) y Chilchota (1780 m) (Cuadros 1 y 2). Este resultado sugiere una posible variabilidad intrapoblacional, fenómeno que aún no se ha reportado en otras especies aromáticas; además, hay varios reportes sobre variabilidad de características morfológicas intrapoblacionales en especies de origen silvestre. Es probable que la naturaleza autógama de T. filifolia (Neher, 1965) podría predisponer la conservación de posibles variantes químicas. La abundancia de recolectas con compuestos mezclados, procedentes de altitudes entre 1600 y 2000 m (Cuadro 3), los cuales coinciden con los climas semicálidos A (C) y (A) C (Cuadro 1), sugiere que en esa altitud y climas pudieran ocurrir importantes procesos de evolución natural de T. filifolia. En general, las zonas de transición climática se asocian con diversidad de especies y con variabilidad genética (Harlan, 1975).
Como parte del trabajo sobre caracterización química de los aceites esenciales del germoplasma mexicano de T. filifolia, los autores del presente artículo están estudiando la composición del aceite esencial en cada órgano de la planta (raíz, tallo–hoja, flores) y la estabilidad de los compuestos al establecer las recolectas en ambientes contrastantes.
CONCLUSIONES
El germoplasma de T. filifolia de la región centro–sur de México contiene anetol y alilanisol como compuestos principales en el aceite esencial. Algunas muestras contienen anetol o alilanisol, pero la mayoría contiene ambos compuestos, cuya proporción presenta amplia variabilidad.
LITERATURA CITADA
Calmasur, O., I. Aslan, and F. Sahin. 2006. Insecticidal and acaricidal effect of three Lamiaceae plant essential oils against Tetranychus urticae Koch and Bemicia tabaci Genn. Indus. Crops Prod. 23 (2): 140–146. [ Links ]
Chou, G. X., and R. H. Zhou. 1998. The variation and chemotypes of the essential oil components in wild Mentha haplocalyx Briq. in China. J. Plant Resour. Environ. 7(3): 13–18. [ Links ]
Cubillo, D., G. Sanabria, and L. Hilje. 1999. Evaluación de la repelencia y mortalidad causada por insecticidas comerciales y extractos vegetales sobre Bemicia tabaci. Manejo Integrado de Plagas 53: 65–72. [ Links ]
Feo, V. de, G. della Porta, E. Soria U. F. Senatore. 1998. Composition of the essential oil of Tagetes filifolia Lag. Flav. Frag. J. 13 (3): 145–147. [ Links ]
García, E. 1981. Modificaciones al Sistema de Clasificación Climática de Köeppen. Instituto de Geografía. Universidad Nacional Autónoma de México. México D. F. 252 p. [ Links ]
Gil, A., C. M. Ghersa, and S. Leicach. 2000. Essential oil yield and composition of Tagetes minuta accessions from Argentina. Biochem. Syst. Ecol. 28 (3): 261–274. [ Links ]
Giorgi, A., M. Bononi, F. Tateo, and M. Cocucci. 2005. Yarrow (Achillea millefolium L.) growth at different altitudes in Central Italian alps: biomass yield, oil content and quality. J. Herb. Spic. Med. Plants 11 (3): 47–58. [ Links ]
Harlan, J. R. 1975. Crops and Man. American Society of Agronomy. Wisconsin, USA. 295 p. [ Links ]
Isman, M. B. 2006. Botanical insecticides, derrents, and repellents in modern agriculture and an increasingly regulated world. Ann. Rev. Entomol. 51: 45–66. [ Links ]
Muni, R. M., A. Gupta, A. Naqvi, and K. Sushil. 1997. Effect of planting time on the yield of essential oil and artemisinin in Artemisia annua under subtropical conditions. J. Essential Oil Res. 9 ( 2): 193–197. [ Links ]
Neher, R. T. 1965. Monograph of the genus Tagetes (Compositae). Ph. D. Dissertation. Indiana University. Bloomington, Indiana, USA. 306 p. [ Links ]
Pérez, M. P., J. A. Navas–Cortés, M. J. Pascual–Villalobos, and P. Castillo. 2003. Nematicidal activity of essential oils and amendments from Asteraceae against root–knot nematodes. Plant Pathol. 52: 395–401. [ Links ]
Putievsky, E., U. Ravid, N. Dudai, I. Katzir, D. Carmeli, and A. Eshel. 1992. Variations in the essential oil of Artemisia judaica L. chemotypes related to phenological and environmental factors. Flav. Fragr. J. 7 (5): 253–257. [ Links ]
Senatore, F., and V. De Feo. 1999. Chemical composition of the essential oil from Tagetes mandonii Sch. Bip. (Asteraceae). Flav. Fragr. J. 14(1): 3234. [ Links ]
Serrato C., M. A. 2003. Aspectos del cultivo de dos especies de Tagetes productoras de aceites esenciales. Rev. Naturaleza y Desarrollo 1 (1): 15–22. [ Links ]
Serrato C., M. A., B. Reyes T., L. Ortega A., L. Domingo G., N. Gómez S., M. A. López M., M. A. Sánchez, L. Carvajal V., 0. Jiménez R., A. Morgado G., E. Pérez M., J. Quiroz M., C. I .Vallejo G. 2003. Anisillo (Tagetes filifolia Lag.): recurso genético mexicano para controlar mosquita blanca (Bemicia sp. y Trialeurodes sp.). Rev. del Jardín Bot. Nacional 24 (1–2): 67–70. [ Links ]
Serrato–Cruz., M. A., F. Díaz–Cedillo, and J. S. Barajas–Pérez. 2005. Seasonal influence on phenology and essential oil content of Tagetes filifolia Lag. Annalen der Meteorologie 41 (1): 82–85. [ Links ]
Serrato–Cruz., M. A, y J. S. Barajas–Pérez. 2006. Poblaciones silvestres de Tagetes filifolia Lag. en el centro sur de México. Rev. Fitotec. Mex. (Número Especial 2): 1–11. [ Links ]
Terblanche, F. C., and G. Cornelius. 2000. A literature survey of the antifungal activity of essential oil constituents. J. Essential Oil Bearing Plants 3 (3): 139–156. [ Links ]
Turner, B. L. 1996. The Comps of Mexico–A systematic account of the family Asteraceae, Vol. 6, Tageteae and Anthemideae. Phytol. Memoirs 10: 1–93. [ Links ]
Tuzun, S., and O. Yegen. 2000. Essential Oils as Pesticides. PCT Int. Appl. New Jersey, USA. 89 p. [ Links ]
Vila, R., J. Iglesias, S. Canigueral, and J. F. Ciccio. 2000. Essential oil of Tagetes filifolia from Costa Rica. Ing. Ciencia Quím. 19 (1): 13–14. [ Links ]
Villarreal Q., J. A. 2003. Familia Compositae. Tribu Tageteae. Flora del Bajío y de Regiones Adyacentes. Fascículo 113. Instituto de Ecología A. C. Pátzcuaro, Michoacán. México. 85 p. [ Links ]
Zhang, K., and Y. Zuo. 2004. GC–MS Determination of flavonoids and phenolic and benzoic acids in human plasma after consumption of cranberry juice. J. Agr. Food Chem. 52: 222–227. [ Links ]
Zygadlo J., A., A. L. Lamarque, D. M. Maestri, C. A Guzmán, and N. R. Grosso. 1993. Composition of the inflorescence oils of some Tagetes species from Argentina. J. Essential Oil Res. 5 (6): 679–682. [ Links ]














