Introducción
La gangrena de Fournier fue descrita por primera vez por el venereólogo francés Jean-Alfred Fournier en 1883 al registrar un caso de gangrena idiopática de inicio súbito en un hombre joven previamente sano.
Es una enfermedad rara que representa < 0.02% del total de ingresos hospitalarios. De acuerdo con lo descrito por Auerbach y colaboradores, ocurre aproximadamente en 1.6 casos por 100,000 personas y en 0.25 mujeres por cada 100,000 personas por año. Esta condición afecta a ambos sexos, pero por lo regular se manifiesta en hombres, con una proporción de 10:1 con respecto a las mujeres. La razón de que se presente con menor frecuencia en mujeres es debido a que el drenaje venoso y linfático del periné se da por vía vaginal.
La edad promedio de presentación es de 50 años, pero se manifiesta en un rango muy amplio que va de 42 a 70 años de edad y el riesgo de presentación aumenta con la edad.1-3
Es considerada una emergencia médico-quirúrgica debido a su rápida progresión, de 2 a 3 cm por hora. Se caracteriza por ser una fascitis necrosante tipo 1 muy agresiva de la región perineal, genital y perianal, con una alta morbimortalidad que en la literatura se ha reportado hasta en 80% cuando no hay tratamiento oportuno. Durante un largo tiempo se consideró una condición idiopática; sin embargo, como describen Singh y colaboradores y Chernyadyev y su equipo, menos de una cuarta parte de los casos se clasifican de esta manera, ya que en la mayoría son causados por una infección subyacente que puede encontrarse en la región anorrectal de 30 a 50%, en la región urogenital de 20-40% y piel de genitales externos en 20%; también se ha descrito que traumatismos en estas áreas pueden ser una causa predisponente.4-7
Existen diversos factores predisponentes del desarrollo de la gangrena de Fournier, que tienen como causa subyacente una alteración del sistema inmunológico que crea un ambiente favorable para el desarrollo de infecciones como diabetes (más frecuente), alcoholismo crónico, desnutrición, inmunosupresión (quimioterapia, esteroides, malignidad), infección por virus de inmunodeficiencia humana, síndromes linfoproliferativos, entre otras.5,7
Es una patología que con frecuencia requiere ingreso a la unidad de cuidados intensivos (UCI), de múltiples intervenciones quirúrgicas e implica altos gastos económicos. Jiménez-Pacheco y colaboradores realizaron un cálculo del costo sanitario aproximado de forma global de un paciente con gangrena de Fournier en un hospital en Granada, España, concluyendo que es mayor de 25,108.67 euros, es decir, 627,716.75 pesos mexicanos, de acuerdo con el cambio actual.8
Etiología
La gangrena de Fournier es una infección polimicrobiana en 54 a 80% de los casos, de acuerdo con los estudios descritos por Luján y colaboradores y Gadler. Los microorganismos más comúnmente aislados son los que se encuentran en el periné y genitales externos, que son bacterias aerobias y anaerobias y que actúan de forma sinérgica causando necrosis del tejido (Tabla 1). La bacteria más reportada es Escherichia coli.9-13
Tabla 1: Microorganismos involucrados con más frecuencia en gangrena de Fournier.
| Según necesidad de oxígeno | Bacteria (%) |
|---|---|
| Bacteroides spp. (38.6) | |
| Streptococcus spp. (37.1) | |
| Anaerobios | Enterococcus spp. (27.1) |
| Staphylococcus spp. (25.7) | |
| Proteus spp. (18.6) | |
| Escherichia coli (40.0) | |
| Aerobios | Pseudomonas spp. (24.3) |
| Klebsiella pneumoniae (20.0) |
Existen diversos factores predisponentes que se han relacionado de forma importante con el desarrollo de la gangrena de Fournier, los cuales tienen como base común una alteración en el sistema inmunológico que crea un ambiente favorable para el desarrollo de infecciones; estos factores incluyen diabetes, hipertensión arterial sistémica, obesidad (IMC > 30), tabaquismo e inmunosupresión, principalmente.2,6,13,14
La diabetes es considerada la comorbilidad más prevalente en estos pacientes, se reporta hasta en 60%, según lo descrito por Voelzke y colaboradores, Vargas y su equipo y Hatipoglu y colegas.7,15-19
La gangrena de Fournier tiene un origen multifactorial, de los factores locales se incluyen patología urológica (cirugía, infección de tracto urinario, parafimosis, estenosis uretral, cateterización traumática), patología anorrectal (abscesos, cirugía, trauma rectal), dermatológicas (infecciones purulentas de la piel, reacciones alérgicas), proctológicas (absceso perirrectal, absceso perianal), celulitis o absceso escrotal o vulvar, hidradenitis, bartolinitis y úlceras por presión.17-19
Las infecciones necróticas de tejidos blandos se pueden categorizar en cuatro grupos dependiendo del agente microbiológico: tipo 1 (polimicrobiana), es el tipo más común y representa más de 50% de las infecciones. Hay acción sinérgica de bacterias aerobias, anaerobias y anaerobias facultativas. Por lo regular afecta a pacientes inmunocomprometidos o con comorbilidades severas, afecta tronco y periné; tipo 2 (monomicrobiana), puede ser más agresiva que el tipo 1 y es menos común; estreptococo ß hemolítico del grupo A es el agente más común y se presenta con más frecuencia con el antecedente de traumatismo o cirugía reciente; tipo 3 (mionecrosis clostridiana), responsable de menos de 5% de las infecciones, se relaciona con Clostridium perfringens y Aeromonas hydrophila, el Clostridium perfringens es la bacteria involucrada con más frecuencia en lesiones traumáticas. Un hallazgo clínico común en estos casos son las crepitaciones debido a la producción de gas de estas bacterias. Afecta extremidades, tronco y periné, se expande rápidamente resultando en falla orgánica múltiple y mortalidad en 24 horas sin tratamiento y tipo 4 (fúngica), que es secundaria a Candida spp. y Zygomycetes, por lo regular en pacientes inmunocomprometidos y posterior a un trauma, afecta extremidades, tronco y periné. Es agresiva y rápidamente progresiva.2,11,18
Fisiopatología
Una infección primaria localizada permite la entrada de bacterias comensales al periné provocando una reacción inflamatoria que causa endarteritis obliterativa en la zona afectada, lo que deriva en trombosis de pequeños vasos subcutáneos y necrosis del tejido afectado que posteriormente va a causar bajas concentraciones de oxígeno y crecimiento de bacterias anaerobias. Las bacterias aerobias y anaerobias actúan de forma sinérgica produciendo enzimas como colagenasa, heparinasa, hialuronidasa, estreptoquinasa y estreptodornasa, enzimas que destruyen el tejido afectado. La trombosis vascular y necrosis dérmica se deben a la actividad de la heparinasa y colagenasas producidas por los microorganismos aerobios. La actividad deteriorada de los leucocitos fagocitarios por la hipoxia en el tejido necrótico es responsable de la diseminación de la infección, ya que el oxígeno es necesario para la producción de sustancias antibacterianas por los leucocitos.5,19
Manifestaciones clínicas
La forma de presentación depende del estadio de la infección, las comorbilidades del paciente y su estado general de salud. Puede haber un periodo prodrómico con síntomas como malestar genital, prurito y fiebre durante días, a veces semanas previo al inicio de los síntomas más severos.
La enfermedad de Fournier tiene una evolución insidiosa, en la mayoría de los casos se presenta con dolor escrotal o vulvar que por lo general no corresponde con los hallazgos clínicos, edema, celulitis y eritema, que se pueden acompañar de olor fétido, crepitación y de datos sistémicos como fiebre, hipotensión y taquicardia; el prurito, dolor y malestar general usualmente empeoran de tres a cinco días antes de que los pacientes acudan al hospital, progresando a la formación de ampollas, isquemia y lesiones necróticas. Al inicio la piel superficial está intacta mientras el proceso necrosante se disemina en las fascias, dificultando el diagnóstico oportuno. La infección se disemina 2.5 cm por hora, sin mostrar cambios en la piel. Al paso de unas horas, se presenta hipertermia en genitales y comienza la necrosis del tejido. Y de acuerdo con lo descrito por Hernández y colaboradores la micción se vuelve dolorosa y difícil.20,21
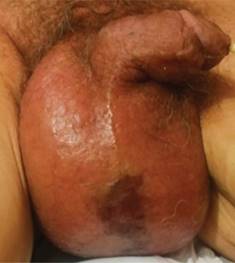
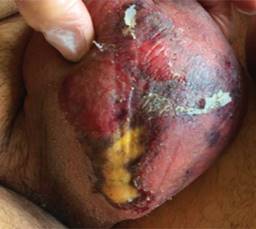
Posteriormente se caracteriza por necrosis de piel, tejido subcutáneo y músculos, pudiendo llegar a causar sepsis y falla multiorgánica que puede llevar al paciente a la muerte.10,19 La hipoxia local causa infarto de los nervios regionales, por lo que en un inicio hay dolor y posteriormente anestesia del área, como se muestra en las Figuras 1 y 2.6,18
La fascia superficial del periné o de Colles cubre a los músculos de la región, se continúa con la fascia de Dartos del pene y escroto en el hombre y de la vulva en la mujer y con la fascia de Scarpa del abdomen anterior. Estos planos fasciales están unidos y facilitan la diseminación rápida de la infección a través de éstos. En el hombre las fascias espermáticas interna y externa, y los vasos del retroperitoneo, independientes de los vasos de la región urogenital y anogenital, protegen los testículos de la infección. La fascia de Buck que recubre la uretra y el cuerpo cavernoso dan protección adicional a esta zona.18
Diagnóstico
El diagnóstico se basa en los datos clínicos de inflamación y necrosis de la zona afectada, crepitación, olor fétido y fiebre.12
En la radiografía simple se puede encontrar enfisema subcutáneo que se extiende del periné y genitales externos hacia la región inguinal, muslo y pared abdominal anterior. El ultrasonido muestra enfisema subcutáneo, áreas ecogénicas con “sombra sucia” en región escrotal o perineal, y en la tomografía axial computarizada (TC), también la presencia de aire subcutáneo, densidad heterogénea en la zona con la pared escrotal o vulvar engrosada y edematosa. Estos estudios ayudan a diferenciar una infección necrotizante de otras patologías. La resonancia magnética muestra enfisema subcutáneo, engrosamiento de la pared escrotal, acumulación de líquido y ayuda a determinar la extensión de la enfermedad. El ultrasonido o TC son suficientes como métodos diagnósticos.5,12,19
Los estudios de imagen pueden ser útiles para establecer la extensión del proceso necrótico, pero no deben retrasar el inicio del tratamiento, ya que éste se relaciona con mayor mortalidad.5
De los estudios de laboratorio, la biometría hemática evalúa el grado de respuesta inflamatoria sistémica e infección o anemia concomitante, trombocitopenia o trombocitosis; la química sanguínea es importante para evaluar la función renal, proteína C reactiva, hemocultivos y según lo reportado por Mehanic y colaboradores y Novoa-Parra y su equipo, la procalcitonina es de gran utilidad en la predicción de choque séptico en pacientes con gangrena de Fournier, e incluso ha demostrado ser un método más efectivo que las escalas utilizadas en la actualidad para su diagnóstico; un nivel bajo procalcitonina nos ayudaría a descartar de forma precoz su diagnóstico.6,10,22,23
El examen histológico revelará necrosis de las fascias superficiales y profundas, coagulación fibrinoide en el lumen vascular, infiltración de células polimorfonucleares en los tejidos y detritus necróticos. Es muy significativa la trombosis venosa de los tejidos afectados.6
Se han desarrollado sistemas de puntuación para el diagnóstico y pronóstico de la gangrena de Fournier como la escala LRINEC (Laboratory Risk Indicator for Necrotizing Fasciitis) que incluye variables que ayudarán a diferenciar una fascitis necrotizante de otras infecciones de tejidos blandos; los valores para diagnóstico van de 0-13 y de pronóstico: bajo riesgo igual o menor de cinco puntos, intermedio de seis a siete puntos, alto riesgo igual o mayor de ocho puntos, con probabilidad de infección necrotizante de tejidos blandos de < 50%, 50-75% y > 75% respectivamente (Tabla 2).24-26
Tabla 2: Escala LRINEC (Laboratory Risk Indicator for Necrotizing Fasciitis) para el diagnóstico y pronóstico de la gangrena de Fournier.
| Variable | Puntuación |
|---|---|
| Proteína C reactiva (mg/dl) | |
| < 15 | 0 |
| > 15 | 4 |
| Recuento leucocitario (por mm3) | |
| < 15,000 | 0 |
| 15,000-25,000 | 1 |
| > 25,000 | 2 |
| Hemoglobina (g/dl) | |
| > 13.5 | 0 |
| 11-13.5 | 1 |
| < 11 | 2 |
| Sodio (mmol/l) | |
| > 135 | 0 |
| < 135 | 2 |
| Creatinina (mg/dl) | |
| < 1.6 | 0 |
| > 1.6 | 2 |
| Glucosa (mg/dl) | |
| < 180 | 0 |
| > 180 | 1 |
Modificada de: Liao C et al.24
El índice de severidad de gangrena de Fournier (FGSI, por sus siglas en inglés) determina el riesgo de mortalidad; fue creado en 1995 por Laor y colaboradores y es la escala que más se utiliza, con sensibilidad de 65-88% y especificidad de 70-100% (Tabla 3). Este índice valora la temperatura corporal, frecuencia cardiaca, frecuencia respiratoria, sodio, potasio, creatinina, bicarbonato, leucocitos y hematocrito; un puntaje > nueve se asocia con 75% de probabilidad de muerte, igual o menor de nueve se asocia con 78% de probabilidad de supervivencia.12,13,20,27,28
Tabla 3: Índice de severidad de gangrena de Fournier.
| Variable | Valores anormales altos | Normal | Valores anormales bajos | ||||||
|---|---|---|---|---|---|---|---|---|---|
| Puntaje | +4 | +3 | +2 | +1 | 0 | +1 | +2 | +3 | +4 |
| Temperatura (oC) | > 41 | 39-40.9 | – | 38.5-39 | 36-38.4 | 34-35.9 | 32-33.9 | 30-31.9 | < 29 |
| Frecuencia cardiaca | > 180 | 140-179 | 110-139 | – | 70-109 | – | 55-69 | 40-54 | < 39 |
| Frecuencia respiratoria | > 50 | 35-49 | – | 25-34 | 12-24 | 10-11 | 6-9 | – | < 5 |
| Sodio sérico (mmol/l) | > 180 | 160-170 | 266-159 | 350-354 | 130-149 | – | 120-129 | 111-119 | < 110 |
| Potasio sérico (mmol/l) | > 7 | 6-6.9 | – | 5.5-5.9 | 3.5-5.4 | 3-3.4 | 2.5-2.9 | – | < 3.5 |
| Creatinina sérica (mg/100/ml × 2 por falla renal aguda) | > 3.5 | 2-3.4 | 1.5-1.9 | – | 0.6-1.4 | – | < 0.6 | – | – |
| Hematocrito | > 60 | – | 50-59.9 | 46-49.9 | 30-45.9 | – | 20-29.9 | – | < 20 |
| Leucocitos (total/mm3 × 1,000) | > 40 | – | 20-39.9 | 15-19.9 | 3-14.9 | – | 1-2.9 | – | < 1 |
| Bicarbonato sérico (venoso, mmol/l) | > 53 | 41-51.9 | – | 32-40.9 | 22-31.9 | – | 18-21.9 | 15-17.9 | < 15 |
Fuente: Laor E et al.27
Se debe hacer diagnóstico diferencial con patologías dermatológicas y sistémicas como pueden ser: celulitis escrotal, torsión o absceso testicular, epididimitis aguda, balanitis, hernia inguino-escrotal estrangulada, vasculitis, síndromes vasculares oclusivos, poliarteritis nodosa, eritema necrolítico migratorio, herpes simple y necrosis warfarínica.5,29
Tratamiento
La clave del tratamiento consiste en tres principios fundamentales: 1) estabilización hemodinámica (reanimación urgente con fluidos intravenosos, estabilización ácido-base y metabólica), 2) antibioticoterapia empírica de amplio espectro y 3) desbridamiento del tejido necrótico. Las metas del tratamiento son reducir la toxicidad sistémica, detener la progresión de la necrosis y eliminar el microorganismo causal.5,6
Todos los pacientes deben ser sometidos a desbridamiento quirúrgico en las primeras 12 horas de admisión, este paso es crucial para detener la progresión de la infección, de acuerdo con lo descrito por Singh y colaboradores un retraso de unas cuantas horas para iniciar los desbridamientos se ha asociado con un aumento significativo en la mortalidad de estos pacientes, por lo que se considera el factor más importante para la supervivencia.5,6,12,17,19,20 En promedio se requieren 3.5 procedimientos quirúrgicos por paciente para un control adecuado de la infección.5
Debe iniciarse antibioticoterapia empírica dirigida a los microorganismos involucrados con más frecuencia, según las recomendaciones de Carruyo y su equipo el manejo inicial debe hacerse con tres grupos de antibióticos: 1) cefalosporinas de tercera generación o aminoglucósidos para cubrir microorganismos aerobios Gram-negativos, 2) penicilina benzatínica o amoxicilina para cubrir microorganismos del tipo estreptococos y 3) metronidazol o clindamicina para cubrir microorganismos anaerobios; en contraste con Chennamsetty y colaboradores que al igual recomiendan un triple esquema de antibioticoterapia empírica, pero incluye: 1) penicilina o cefalosporinas de tercera generación, 2) aminoglucósidos y 3) metronidazol o clindamicina; además recomiendan agregar vancomicina en caso de sospechar infección por S. aureus resistente a meticilina.30)-(32 Se recomienda realizar cultivo y antibiograma de la lesión para modificar la antibioticoterapia o bien continuar con la establecida.
Los desbridamientos continúan hasta que se ha retirado todo el tejido necrótico y se establece tejido de granulación sano en la herida. Es crucial remover todo el tejido necrótico y desvitalizado lo más pronto posible, posponerlo aumenta el riesgo de muerte. Como característica durante el desbridamiento se observa ausencia de hemorragia secundaria a trombosis de los vasos sanguíneos, olor fétido, decoloración grisácea de los tejidos blandos por necrosis, fluido como “agua sucia”, pus y desprendimiento de los tejidos con la disección digital.5,6,12,17,19,20,30-32
La mortalidad general de la gangrena de Fournier ha sido descrita de 20-40% en la mayoría de los seguimientos, pero Sorensen la reportó en 88%.4 Caliskan y colaboradores refieren que un adecuado desbridamiento resulta en la reducción de la mortalidad hasta en 16%. Se recomienda una segunda cirugía second look a las 24 horas, en caso de deterioro del estado clínico del paciente debe realizarse antes.6,12,15,17,19
Métodos alternativos como la terapia VAC® (vacuum-assisted closure) o terapia con presión negativa recomendada de 50 a 125 mmHg, la cual se utiliza en el tratamiento de muchas heridas crónicas, ya que estimula el suministro sanguíneo en la región afectada y promueve la migración de células inflamatorias con la formación de tejido de granulación. Las terapias con oxígeno hiperbárico pueden servir para acelerar la velocidad de curación de la herida, la terapia con oxígeno reduce la disfunción de los leucocitos causada por la hipoxia y tiene un efecto antibacteriano directo contra anaerobios; se ha observado que ayuda a que algunos antibióticos penetren mejor en las bacterias.7,20,33 Según los hallazgos de la Dra. Devia y colaboradores, la terapia hiperbárica junto al sistema de presión negativa, demostró disminuir la mortalidad hasta 11.4%; sin embargo, Hatipoglu menciona que la terapia hiperbárica tiene alto riesgo de complicaciones cerebrales y pulmonares, además de altos costos, lo que limita su uso.33,34
La zona de desbridamiento por lo regular se encuentra en regiones cercanas al ano, por lo que se debe proteger la herida de la contaminación por heces fecales, derivando la materia fecal para mantener la herida limpia, por lo general la derivación fecal se realiza por medio de colostomía cuando las heridas se encuentran cerca de la región perianal, o por el sistema de manejo fecal Flexi-SealTM, un método alternativo que consiste en la colocación de un tubo rectal que permite la salida de la materia a través de éste a una bolsa colectora. Es una alternativa económica y cómoda para el paciente y con la que se puede evitar la colostomía.33,35











 nueva página del texto (beta)
nueva página del texto (beta)