Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Cirujano general
versión impresa ISSN 1405-0099
Cir. gen vol.34 no.1 Ciudad de México ene./mar. 2012
Artículos de investigación
Eficacia de la plastía dinámica en la reparación de grandes defectos de la pared abdominal con malla Proceed®, en el Hospital General
''Dr. Manuel Gea González''
Efficacy of dynamic plasty in repairing large defects of the abdominal wall with
Proceed™ mesh at the General Hospital ''Dr. Manuel Gea González''
Adriana Hernández López, Arianna López-Toledo González
Centro Médico ABC y Hospital General ''Dr. Manuel Gea González''
Cirugía General y Laparoscópica. Endoscopía Gastrointestinal. División de Cirugía. Centro Médico ABC.
Correspondencia: Dra. Adriana Hernández López
Hospital ABC. Observatorio. Sur Núm. 136 Consultorio 216, Col. Las Américas. 01170 México D.F.
Tel: (+52-55) 52.71.37.33 53.43.27.39.
Correo electrónico: ady_hdez_lopez@yahoo.com.mx
Recibido para publicación: 5 enero 2012 Aceptado para publicación: 25 febrero 2012
Resumen Objetivo: Comparar la eficacia y seguridad de la técnica de plastía dinámica de pared con malla intraperitoneal Proceed®, contra la malla de polipropileno de colocación supraaponeurótica.
Sede: Hospital General ''Dr. Manuel Gea González''.
Diseño: Observacional, longitudinal, comparativo con control histórico.
Análisis estadístico: Prueba de Chi cuadrada y medidas de asociación de razón de prevalencias, así como regresión lineal.
Material y métodos: Se incluyeron en el estudio 110 pacientes. El grupo control fue de 55 pacientes que se operaron con técnica ONLAY (localización supraaponeurótica) con malla de polipropileno. El grupo experimental fue de 55 pacientes que se operaron con la técnica IPOM con malla Proceed®. Las variables evaluadas fueron edad, género, tiempo quirúrgico, dehiscencia de la herida, infección de sitio quirúrgico, fístula, oclusión intestinal, seromas y tamaño del defecto.
Resultados: Ambos grupos fueron comparables en cuanto a edad y género. No existió diferencia en el tiempo quirúrgico promedio (80 vs 84 minutos, respectivamente, p > 0.05), ni en complicaciones totales (20 vs 32%, p > 0.05); tampoco en la dehiscencia de la herida, infección de sitio quirúrgico, fístula ni oclusión intestinal entre ambos grupos (p > 0.05). La ocurrencia de seromas se presentó con mayor frecuencia en el grupo de pacientes con técnica IPOM con malla Proceed®, con un riesgo relativo de 1.59 (p = 0.06). El IC (1.08-2.35) muestra una asociación entre la formación de seroma y el uso de la malla Proceed®. El tamaño del defecto de la pared abdominal fue significativamente mayor en el grupo de pacientes incluidos en el grupo de plastía IPOM con malla Proceed® que en el grupo de plastía ONLAY con malla de polipropileno (12 vs 6 cm, p < 0.05). La regresión lineal observó que sí existe una relación entre el tamaño del defecto y la ocurrencia de seroma en el grupo de pacientes con técnica IPOM con malla Proceed® (coeficiente de regresión 0.26, p < 0.05). La recidiva fue significativamente mayor en el grupo ONLAY con malla de polipropileno que en el grupo IPOM con malla Proceed® (18 vs 3%, respectivamente, p < 0.05) y el riesgo de recidiva en pacientes con comorbilidades asociadas es 2.5 veces mayor en el grupo ONLAY con malla de polipropileno con respecto al grupo IPOM con malla Proceed® (p < 0.05).
Conclusiones: Sugerimos el uso de malla Proceed® con técnica IPOM para este tipo de pacientes. La malla Proceed® ha demostrado ser eficaz y segura para la reparación de grandes defectos de la pared abdominal.
Palabras clave: Hernia, pared abdominal, plastía de pared.
Introducción Las hernias de la pared abdominal son una patología frecuente y una de las principales causas de atención médica en el medio hospitalario. Las hernias incisionales son las más frecuentes y ocurren hasta en el 2-10% de los pacientes sometidos a una laparotomía.1,2 Otros defectos de pared que se presentan con menor frecuencia, pero que requieren de una reparación son: las hernias umbilicales, las hernias de Spiegel y las hernias epigástricas.
El tratamiento quirúrgico para la reparación de las hernias ventrales sigue siendo un reto para el cirujano, por ello se han descrito múltiples técnicas con resultados variables, sin poder determinar hasta el momento cuál es o si existe una técnica ideal. El objetivo de la plastía de la pared abdominal para la reparación de hernias es evitar la eventración de las vísceras, restableciendo la funcionalidad de la pared sin tensión excesiva, permitiendo que mantenga sus características fisiológicas de distensibilidad y flexibilidad, idealmente con la aproximación y restablecimiento de la línea alba con fascia autóloga.
A lo largo de la historia se han descrito y utilizado diversas técnicas de plastía de pared para la reparación de los defectos abdominales.3-5 Se describen las plastías con tensión, primarias o anatómicas, en las cuales se utilizan sólo los tejidos mismos y suturas diversas para la reparación de las hernias de la pared abdominal, con resultados variables dependiendo de la técnica, con recidiva en un 18 a 62% de los casos.6,7 Se han considerado modificaciones a estas técnicas y recientemente se ha generalizado el uso de la técnica tradicional de separación de componentes, descrita por Ramírez y colaboradores, la cual permite el avance de tejido nativo hacia la línea media para realizar un cierre sin la necesidad de colocar material protésico. Esta técnica requiere de una disección subcutánea extensa para abordar la pared abdominal lateral con sección de los vasos perforantes, lo que permite un avance del tejido hasta de 10 cm de cada lado para el cierre utilizando la musculatura abdominal.
La recurrencia reportada va desde un respetable 5% hasta un inaceptable 30% dependiendo de la serie consultada. La principal complicación asociada a esta técnica es la morbilidad de la herida quirúrgica, con sepsis hasta en el 40% de los casos. Con la técnica laparoscópica de separación de componentes se logra un avance de los colgajos del 86% con respecto a la técnica abierta, sin requerir de una disección subcutánea extensa, pero se requieren estudios comparativos para evaluar los resultados definitivos entre ambos abordajes y concluir.8,9
En los últimos cuarenta años se introdujeron diversos tipos de materiales protésicos para llevar a cabo la reparación de los defectos de la pared abdominal sin tensión, con los cuales se ha logrado disminuir la recidiva de la hernia hasta el 1% (dependiendo de la serie consultada) y con mejores resultados a largo plazo.5,10-12 La recurrencia es la complicación más frecuente y puede presentarse posterior a cualquier tipo de reparación. La plastía primaria, utilizada antes de 1960, se asocia a un porcentaje de recurrencia que puede ser tan alto como el 60%. El material protésico para la reparación de hernias ventrales fue introducido por Usher a principios de los años 60 y su uso disminuyó significativamente la recidiva (5 al 20%), aunque con una mayor incidencia de otras complicaciones como son la formación de seromas, hematomas y necrosis de los tejidos en casos de disecciones extensas.
La plastía con malla puede realizarse con: 1. la colocación de la prótesis cubriendo el defecto más un perímetro de 3 a 5 cm de aponeurosis sana alrededor de este (ONLAY), 2. Como injerto aponeurótico cubriendo exclusivamente el defecto con la malla fijada a los bordes del mismo (INLAY), 3. De colocación intraperitoneal, con contacto visceral (IPOM) y 4. La técnica ''sándwich'' con colocación simultánea de una malla intraperitoneal y una segunda de localización supraaponeurótica.13
La mayor recurrencia ocurre cuando se utiliza la técnica ''INLAY'', por lo que no es recomendada. Algunas series se muestran optimistas en relación a la técnica de ''sándwich'' aún sin estudios concluyentes.
En relación a la fisiopatología de la recurrencia se han descrito varios mecanismos que, de acuerdo a la clasificación propuesta por Awad y colaboradores, se dividen en dos grupos: 1. El que incluye los factores asociados al paciente como la presión intraabdominal elevada y la calidad de los tejidos, y 2. El que considera los factores técnicos como la retracción lateral de la malla por fijación inadecuada o mala colocación y la falla en detectar la presencia de otra hernia en el campo quirúrgico.14 Otros autores identificaron como factores asociados a la recurrencia: el tamaño de la hernia, el tipo de cirugía (electiva o urgencia), la presencia de una malla colocada en un procedimiento previo y la infección del sitio quirúrgico.1,2
La infección de la herida quirúrgica es otra complicación que puede modificar la evolución del paciente y favorecer la recurrencia. Se define como infección superficial aquélla que afecta la piel o el tejido celular subcutáneo y, como profunda, la que afecta la fascia o el músculo. La incidencia reportada en la literatura es del 1 al 9% y los factores de riesgo identificados son: la presencia de infección de la herida en el preoperatorio, el tabaquismo, el uso crónico de esteroides, la insuficiencia cardiaca congestiva, la resección intestinal o enterotomía, un procedimiento de emergencia, el tiempo quirúrgico prolongado y la estancia intrahospitalaria. El uso de material protésico, aunque se ha considerado factor de riesgo para infección de la herida por algunos autores, no demostró en un análisis retrospectivo realizado en 1,505 pacientes ser un factor predictivo de infección del sitio quirúrgico.15 Otras complicaciones relacionadas con el uso de las mallas son la obstrucción intestinal y la formación de fístulas intestinales, unas de las más temidas por la alta morbilidad y mortalidad asociada.
Las mallas han sido ampliamente aceptadas desde su introducción aun para la reparación de defectos pequeños. Estudios publicados reportan mejores resultados cuando se utiliza una malla para cubrir defectos fasciales mayores de 2 cm.16 Los materiales protésicos se clasifican de varias formas; la primera, de acuerdo a las características propias de las mallas, siendo éstas macroporosas, microporosas o mixtas (de acuerdo al tamaño de su poro); la segunda, de acuerdo a los componentes del material que las cataloga como no absorbibles, con capas de material absorbible y mixtas (de acuerdo a las características de las fibras que le conforman); la tercera, de acuerdo a la cantidad final de material protésico que queda incluido dentro de la cicatriz (de alta y baja densidad) y características varias como maleabilidad, expansibilidad, entre otras.17
Cuando existen grandes defectos de la pared abdominal, primarios o secundarios a procedimientos previos (hernias incisionales), la reparación representa un gran reto, en especial en aquellos pacientes que han sido sometidos a múltiples cirugías abdominales e intentos de reparación, ya que en ocasiones es imposible separar el intestino de la malla previa.18,19 Esto ha generado múltiples intentos por encontrar el material protésico ideal, que no existe hasta ahora, lo que hace que en el mercado se disponga de varias mallas para la reparación de los defectos de la pared abdominal.
La malla Proceed® es un material protésico conformado por tres capas de las siguientes características:
1. Capa de polipropileno: Este es un monofilamento, el cual confiere durabilidad, fuerza y flexibilidad a la malla, además de una integración excelente del tejido a la misma, lo cual genera un reforzamiento de la pared abdominal.
2. Capa de celulosa oxidada regenerada que minimiza la adhesión a los tejidos. Es un material de origen no animal.
3. Polidioxanona absorbible, la cual crea una unión flexible y segura entre la malla y la capa de celulosa.
Las características de la malla Proceed® la convierten en un material protésico útil y seguro que puede colocarse de forma intraperitoneal para la reparación de los defectos de la pared abdominal. Además, permite realizar una plastía dinámica llevando a cabo el cierre de la pared abdominal con la tensión suficiente como cuando se tiene una línea media con características fisiológicas.20 Cualquier material extraño debe separarse de las vísceras abdominales para evitar las adherencias a la malla que pueden ser firmes y difíciles de disecar. Cuando se generan adherencias entre las vísceras y el material protésico se pueden generar erosión y fístula, y en algunos casos obstrucción intestinal, complicaciones que se relacionan con una considerable morbilidad y mortalidad.17-19 Estudios actuales en modelos animales han demostrado que las adherencias y las características de las mismas generadas por las mallas varían de acuerdo al material del cual están hechas. Se le ha nombrado índice de adhesión a la capacidad que tiene la malla para generar adherencias, reportándose en la literatura médica el más bajo índice para la malla Proceed®.
Kiudelis propone una escala tomando en cuenta cuatro parámetros. El primero es el área de la malla que se cubre de adherencias en porcentaje; el segundo, el grado de vascularización de las adherencias; el tercero es el grosor de las adherencias, y el último la fuerza de las adherencias. La sumatoria de los puntos indica el índice de adhesión, tomando el 0 como el valor mínimo y el 12 como valor máximo. Índice de adhesión (escala de 0-12)
Proceed® = 2.75
Mersilene® = 9.20
Vypro® = 9.70
Prolene® = 9.50
Las mallas de Mersilene® y Prolene® se cubren de adherencias hasta en un 75% de su superficie; estas adherencias suelen ser firmes y vascularizadas y requieren una disección mayor. La malla Proceed® se cubre de adherencias en el 1-25% de la superficie y se ha observado que el tipo de adherencias son no vascularizadas o poco vascularizadas y se separan con facilidad con una disección roma, manual.21-23 Esta bicapa es considerada como prótesis ligera, ya que contiene una menor cantidad de material extraño, pues la capa de celulosa se absorbe por completo de 7 a 14 días posteriores a su colocación, dejando únicamente el filamento de polipropileno peritonizado (ya que también las fibras de polidioxanona se absorben). Este esqueleto de fibras de monofilamento favorece un tejido de cicatrización flexible y, por lo tanto, una fuerte incorporación del mismo a los tejidos.
Otra característica de esta malla es que resiste la colonización bacteriana por tratarse de un material macroporoso que permite el flujo libre de líquidos a través de ella, incluyendo celularidad como los macrófagos para evitar o resistir la infección. Su maleabilidad permite que se adapte fácilmente a la anatomía y, una vez que se conoce la técnica quirúrgica, es de fácil colocación.23,24 La hernia de la pared abdominal es una patología frecuente que ocasiona dolor e incapacidad física y que puede ser causa de complicaciones que ponen en riesgo la vida. Es una de las principales causas de atención hospitalaria para su reparación como procedimiento electivo y también causa importante de atención en el Servicio de Urgencias, por complicaciones locales o sistémicas relacionadas. Las hernias primarias de la pared abdominal y las recidivantes son un problema de salud pública ya que representan una de las enfermedades más frecuentes en nuestro medio, que requieren días de hospitalización y consumo de recursos humanos y materiales. La reparación efectiva con un resultado óptimo inmediato y a largo plazo hace necesario que se disponga de una técnica quirúrgica depurada, con un material adecuado, que lleve a la resolución definitiva del problema.
Una cuidadosa y protocolizada técnica quirúrgica con el material protésico adecuado provee excelentes resultados con un riesgo mínimo de complicaciones asociadas, incluso en la reparación de los grandes defectos de la pared abdominal. Por tanto, el objetivo de este estudio fue comparar la eficacia y seguridad de la técnica de plastía dinámica con malla intraperitoneal Proceed® (IPOM) contra la plastía con malla de polipropileno de colocación supraaponeurótica (ONLAY), para la reparación de grandes defectos de la pared abdominal, en el Servicio de Cirugía General y Endoscópica del Hospital General ''Dr. Manuel Gea González'' en un periodo de dos años.
Material y métodos Se diseñó un estudio observacional, longitudinal, comparativo con control histórico. El universo de estudio fueron pacientes de la Clínica de Hernias, del Servicio de Cirugía General y Endoscópica del Hospital General ''Dr. Manuel Gea González''. Se calculó una muestra de 55 pacientes por grupo. Se tomó en cuenta una p = 0.01 para el grupo de los pacientes con un histórico de plastía de pared con malla de polipropileno supraaponeurótica que hayan cumplido dos años de postquirúrgico hasta el inicio del estudio y una p = 0.10 para el grupo de los pacientes de plastía dinámica con malla Proceed®, calculando un error tipo I de 0.05. Los pacientes fueron captados y seleccionados desde la consulta externa del Servicio de Cirugía General y Endoscópica. Se les explicó ampliamente sobre el padecimiento, tratamiento quirúrgico, preparación pre-hospitalaria y manejo postquirúrgico, así como sobre el seguimiento a largo plazo que deberán de llevar (controles clínicos y fotográficos). Una vez que aceptaron participar en el estudio se enviaron a la primera fotografía clínica para contar con imágenes preoperatorias controles de los defectos de la pared abdominal. En el postquirúrgico fueron citados nuevamente en la consulta externa para seguimiento a la semana, a dos semanas, a cuatro semanas, mes y medio y 3, 6, 12, 18 y 24 meses posteriores a la cirugía para revisión y nuevas fotografías clínicas.
El manejo hospitalario se llevó a cabo de la siguiente manera:
1. Todos los pacientes fueron enviados a laboratorio clínico para toma de estudios preoperatorios (biometría hemática, química sanguínea, tiempos de coagulación, examen general de orina), los cuales se revisaron en consulta externa antes de programar el procedimiento.
2. A los pacientes mayores de 50 años o menores pero con alguna comorbilidad, se les solicitó toma de electrocardiograma, rayos X de tórax y valoración cardiovascular por un médico internista y/o médico cardiólogo de la consulta externa.
3. Los pacientes con índice de masa corporal mayor a 40 fueron enviados a ecocardiograma y pruebas funcionales respiratorias.
4. Los pacientes con un tiempo simultáneo de restitución intestinal se enviaron a rayos X para secuencia de localización de estomas (tránsito intestinal, fistulografía, colon por enema y por estoma, tomografía computada de abdomen simple y contrastada), según se requirió. A estos pacientes se les incluyó además en su perfil de laboratorio parámetros nutricionales.
5. Todos los pacientes fueron enviados a valoración preanestésica antes de la cirugía.
6. Los pacientes con programación de restitución intestinal simultánea a la plastía de pared fueron internados uno o dos días previos al procedimiento para vigilancia y preparación intestinal con polietilenglicol oral (Nulitelly, 4 sobres), ceftriaxona 1 g IV cada 12 horas y metronidazol 500 mg IV cada 8 horas.
7. Todos los pacientes firmaron carta de consentimiento informado para el procedimiento.
Técnica quirúrgica Anestesia: regional o general de acuerdo a valoración por Servicio de Anestesiología. Asepsia y antisepsia de la pared abdominal con Duraprep® (solución antiséptica de yodo) y Lovan® (película auto adherente bacteriostática). Paso 1. Identificación de márgenes del defecto herniario. Incisión en línea media de espesor total y a lo largo de todo el defecto con resección de la cicatriz antigua.
Paso 2. Identificación del defecto herniario y disección más allá del tejido circundante.
Paso 3. Ingreso a la cavidad peritoneal y liberación de cualquier víscera o adherencia a la pared peritoneal.
Paso 4. Medición del tamaño del defecto y determinación del tamaño de la malla, dejando 3-5 cm más allá del borde del defecto.
Paso 5. Colocación intraabdominal (intraperitoneal, es decir, en contacto directo con las vísceras) de la malla Proceed®.
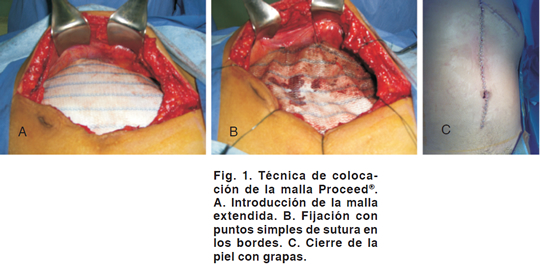
Paso 6. Colocación de la malla con las líneas azules (marcas del polipropileno) dirigidas hacia la superficie peritoneal. (Figura 1 a)
Paso 7. Corte de la malla a la medida y fijación con sutura absorbible Maxon™ (poligliconato del número 2-0) (Figura 1 b).
Paso 8. Colocación de la malla en forma de paracaídas invertido, dentro de la cavidad abdominal, traccionando las suturas y anudando. Se corroboró que la malla quedara completamente extendida para evitar que algún doblez pudiera condicionar contacto visceral con la cara de polipropileno.
Paso 9. La aponeurosis por arriba de la malla se cerró. ''Siempre debe dejarse un soporte aponeurótico a la malla.'' En algunos casos en que no fue posible el cierre primario aponeurótico, se efectuó rotación de colgajos o separación de componentes. A valorarse de acuerdo a la extensión de la disección, la colocación de un drenaje supraaponeurótico (casos seleccionados).
Paso 10. Se efectuó cierre de la piel con grapas metálicas (Figura 1 c).
Para el grupo control histórico (pacientes de plastía de pared con malla de polipropileno de colocación supraaponeurótica) se llevó a cabo la revisión de expedientes de pacientes operados en el periodo de 2000 al 2005 en este hospital. Se estableció un sistema de selección aleatorio para incluir a los 55 pacientes de este grupo control. Se realizó un cuestionario, vía telefónica, para determinar la existencia de recidiva o complicaciones y estado actual.
Los resultados se analizaron por medio de estadística descriptiva: medidas de tendencia central y dispersión: rango, media, mediana, moda o porcentajes.
Se utilizó estadística inferencial, prueba de Chi cuadrada y medidas de asociación de razón de prevalencias, así como regresión lineal para las variables significativas.
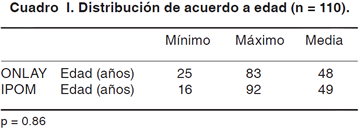
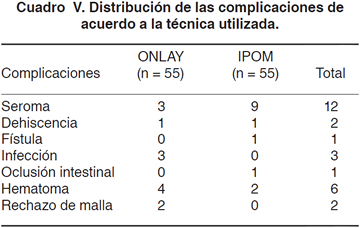
Resultados Fueron incluidos en el estudio 110 pacientes. El grupo control fue de 55 pacientes que se operaron con técnica ONLAY con malla de polipropileno. El grupo experimental fue de 55 pacientes que se operaron con la técnica IPOM con malla Proceed®. Ambos grupos son comparables en cuanto a edad y sexo (Cuadros I y II). No se reportó diferencia en el tiempo quirúrgico promedio (Cuadro III 80 vs 84 minutos, respectivamente, p > 0.05), ni en cuanto a complicaciones totales (Cuadro IV 20 vs 32%, p > 0.05). No se reportó diferencia en la incidencia de dehiscencia de la herida, infección de sitio quirúrgico, fístula ni oclusión intestinal entre ambos grupos (Cuadro V p > 0.05). La ocurrencia de seromas se presentó con mayor frecuencia en el grupo de pacientes con técnica IPOM con malla Proceed®, con un riesgo relativo de 1.59 (p = 0.06). El IC (1.08-2.35) muestra una asociación entre la formación de seroma y el uso de la malla Proceed® (Cuadros VI, VII y VIII). El tamaño del defecto de la pared abdominal fue significativamente mayor en el grupo de pacientes incluidos en el grupo de plastía IPOM con malla Proceed® que en el grupo de plastía ONLAY con malla de polipropileno (Cuadro IX, 6 vs 12 cm, p < 0.05). Al realizar la regresión lineal con las variables seroma y tamaño del defecto se observó que sí existe una relación entre el tamaño del defecto y la ocurrencia de seroma en el grupo de pacientes con técnica IPOM con malla Proceed® tuvo un coeficiente de regresión de 0.26, p < 0.05. Esto podría explicarse por el hecho de que los defectos de pared abdominal de grandes dimensiones requieren una disección más extensa sobre el plano aponeurótico. No se reportó diferencia en la estancia intrahospitalaria entre ambos grupos. La recidiva fue significativamente mayor en el grupo ONLAY con malla de polipropileno que en el grupo IPOM con malla Proceed® (18 vs 3%, respectivamente, p < 0.05) Cuadro X, y el riesgo de recidiva en pacientes con comorbilidades asociadas es 2.5 veces mayor en el grupo ONLAY con malla de polipropileno con respecto al grupo IPOM con malla Proceed® (p < 0.05) Cuadro XI, por lo que sugerimos el uso de malla Proceed® con técnica IPOM para este tipo de pacientes. La malla Proceed® ha demostrado ser eficaz y segura para la reparación de grandes defectos de la pared abdominal.





Discusión Sullivan y colaboradores publicaron su experiencia para reparación de hernias masivas con seis pacientes, con dimensiones máximas de 28 x 31 cm, requiriendo hasta tres tiempos quirúrgicos para lograr la reparación primaria con sólo avance de colgajos músculo-aponeuróticos, con resultados satisfactorios y sin recurrencia a 23 meses. La estancia intrahospitalaria fue en promedio de 22 días y sólo se presentaron complicaciones menores, reportándose infección superficial de la herida en el 16% y hematoma en el 16% de los casos.25 Es de esperarse, tarde o temprano, la recurrencia del defecto herniario, puesto que se ha demostrado que las reparaciones anatómicas se acompañan de un alto índice de recidiva.
Cuando es posible llevar a cabo una aproximación de los tejidos nativos protegiendo las asas intestinales (con epiplón, con saco herniario redundante o con cierre primario aponeurótico), se puede colocar de forma segura una malla supraaponeurótica como la de polipropileno, sin riesgo de complicaciones mayores como la erosión y fístulas intestinales. Cuando no es posible evitar el contacto con las vísceras se produce una respuesta inflamatoria local y necesariamente la formación de adherencias que pueden causar dolor crónico, infertilidad, obstrucción intestinal (1%) o fístulas (3-5%), además del riesgo quirúrgico elevado en caso de requerir a futuro otra cirugía abdominal.2
Las fístulas ocurren secundariamente a la erosión de las vísceras cuando se adhieren a la malla. Esta complicación es más común cuando la prótesis tiene contacto con órganos desprovistos de un recubrimiento de serosa, como el esófago distal, la vejiga y el intestino denudado, pero también se presenta aun en presencia de un intestino sano e íntegro.17 En la mayoría de los casos se asocia al uso de mallas no absorbibles como el Mersilene® y el polipropileno y se puede manifestar entre 4 y 18 meses posteriores al procedimiento e incluso se han reportado casos en los que los síntomas ocurren hasta 10 años después. La incidencia reportada de esta complicación es del 3 al 5% y la recomendación es retirar la malla y hacer una nueva reparación de la pared abdominal.26
En nuestro estudio solamente se reportó un caso de fístula colocutánea secundaria al contacto del colon con un segmento de la capa de polipropileno, de la malla Proceed® en el borde inferior, debido evidentemente a falla en la técnica quirúrgica. En este caso se retiró el fragmento de malla involucrada y la fístula cerró con manejo conservador. Doce meses después, el paciente permanece asintomático, sin evidencia de recurrencia de la hernia ni fístula.
Con el objetivo de minimizar las complicaciones y mejorar los resultados, varios grupos quirúrgicos han iniciado su experiencia con la colocación de aquellas mallas que pueden ser puestas de forma intraabdominal. Las mallas de colocación intraperitoneal, además de tener una cobertura temporal protectora para el contacto visceral mientras que se integran adecuadamente a la matriz tisular, tienen la ventaja teórica de disminuir la recurrencia de la hernia, puesto que los vectores de la presión intraabdominal y la contracción muscular se distribuyen radialmente sobre la pared abdominal y no directamente sobre los puntos de fijación de la malla.14 La plastía dinámica con este tipo de mallas permite la resolución de la patología en un solo tiempo quirúrgico. En casos de hernias de mayores dimensiones que requieren disecciones extensas existe mayor riesgo de complicaciones menores como seromas, hematomas y necrosis de los colgajos tisulares. Las complicaciones postoperatorias en general de la plastía de pared abdominal ocurren en el 18-34% de los casos. Las complicaciones relacionadas a la herida quirúrgica ocurren en el 15%. La infección superficial ocurre hasta en el 10% de los casos, la infección profunda en 3%, la infección de la malla en el 3 al 5% y la infección de la malla que amerita retiro de la misma en el 1%.17,27,28 En nuestra serie, la infección del sitio quirúrgico se presentó en el 5% de los pacientes del grupo de plastía IPOM con malla Proceed®. Todas fueron superficiales y se resolvieron con curaciones. En el caso de las plastías abdominales para hernias ventrales aún no se tienen estudios concluyentes en cuanto a la profilaxis antimicrobiana, por lo que permanece como tema de controversia.29,30 Con respecto al uso de mallas en cirugía contaminada existe debate pues la recomendación es no utilizar mallas en cirugía contaminada por el riesgo de infección; sin embargo, existen reportes de uso de material protésico y cirugía intestinal durante el mismo tiempo quirúrgico con resultados exitosos.13,31 En este estudio se incluyó una población de pacientes con potencial riesgo de contaminación con reparación simultánea de la hernia y restitución intestinal, por lo que en ellos fue preponderante la preparación formal del intestino para profilaxis de sepsis de área quirúrgica. Ante la eventualidad de lesión intestinal en el resto de los casos con antecedentes de cirugías abdominales previas, se estandarizó el uso de profilaxis antimicrobiana en todos los pacientes. En nuestra serie reportamos cinco casos de anastomosis intestinales con colocación de malla Proceed® como procedimientos simultáneos, electivos. Se reportó la ocurrencia de un seroma que resolvió espontáneamente, un caso de oclusión intestinal secundario a adherencias, que requirió retiro de la malla, y un caso de dehiscencia de anastomosis en el cual se decidió el retiro de la malla (cuerpo extraño) para el manejo conservador de la fístula. Excepto los dos últimos casos mencionados, el resto de los pacientes (3) se encuentran asintomáticos con un seguimiento de 12 meses. No se reportaron complicaciones infecciosas. La formación de seromas postoperatorios relacionados al uso de prótesis es causada por reacción inflamatoria al material extraño y el espacio muerto creado entre la malla y los tejidos, secundario a la extensa disección para la búsqueda de los bordes aponeuróticos sanos. Cuando se trata de una malla macroporosa que permite el flujo del líquido a través de ella o una que se integra satisfactoriamente a los tejidos por fibrosis acelerada eliminando el espacio muerto, es menos probable la formación del seroma. La incidencia de esta complicación se reporta entre el 1 y 9% y el riesgo del seroma se puede reducir considerablemente evitando el contacto del material protésico con el tejido subcutáneo adiposo, situación que sucede cuando la malla se coloca preperitoneal, retroaponeurótica o intraperitoneal como la malla Proceed®. Cuando se realizan disecciones extensas entre el plano aponeurótico y la grasa subcutánea será necesario entonces la colocación de drenajes para evitar la acumulación del líquido.17 En nuestro estudio, la ocurrencia de seromas se presentó con mayor frecuencia en el grupo de pacientes de técnica IPOM con malla Proceed® con un riesgo relativo de 1.59 con respecto al grupo control (ONLAY con polipropileno) con un valor de p > 0.05; en el análisis bivariado, el intervalo de confianza sí reveló asociación entre el uso de la malla Proceed® y la formación de seroma. Consideramos que esto se debe a que el tamaño del defecto aponeurótico fue significativamente mayor en el grupo IPOM con malla Proceed® que en el grupo control (p < 0.05) y, por lo tanto, se requirió una disección más extensa para crear un soporte aponeurótico que cubriera la bicapa para garantizar su integración a los tejidos. La formación de hematomas se reporta en la literatura en el 3% de los casos de plastías con malla y en 1.6% para reparaciones sin prótesis.32 A pesar de todo lo referido, el parámetro que califica el éxito en la reparación de un defecto de pared es el índice de recidiva. Está descrito que la recidiva para la técnica IPOM, INLAY y ONLAY es de 6, 35 y 11%, respectivamente; por lo tanto, la recurrencia varía dependiendo de la técnica utilizada. Se ha reportado una recurrencia acumulativa a 5 y 10 años de 4.2 y 12.5%, respectivamente, con la técnica de Rives-Stoppa.2 Esta técnica proporciona resultados satisfactorios, con la desventaja de que involucra una disección extensa retromuscular con colocación prefascial de una malla de grandes dimensiones.28 Este procedimiento es el más parecido a una técnica IPOM, con la ventaja de tener una cobertura peritoneal fisiológica íntegra, pues la malla se encuentra en posición retromuscular y, por lo tanto, una prótesis convencional sin cobertura especial puede ser utilizada. En la técnica IPOM, la cobertura especial de la malla (celulosa oxidada regenerada, colágeno, ácido hialurónico, etcétera), que permite el contacto con las vísceras, de alguna manera sustituye temporalmente la capa peritoneal. Ambas técnicas, al permitir la colocación de una malla subaponeurótica de grandes dimensiones que cubre la totalidad de la pared, permite que la presión intraabdominal y la fuerza de retracción muscular se distribuyan uniformemente, asegurando la fijación de material protésico. La recidiva a dos años reportada en nuestra serie fue del 3% para los pacientes del grupo IPOM con malla Proceed®, comparada con 18% en el grupo control ONLAY con polipropileno (p < 0.05). Este valor supera a lo reportado en la literatura para la técnica IPOM (6%). Para la colocación intraabdominal o intraperitoneal existen diversas mallas, entre ellas: e-PTFE (Dualmesh®), polipropileno-poliglecaprone (Ultrapro®), polipropileno-titanio (Timesh®), polipropileno con recubrimiento de carboximetilcelulosa y hialuronato (Sepramesh®), poliéster con colágena y recubrimiento de glicol-glicerol (Parietex Composite®), polipropileno con colágena y recubrimiento de glicol-glicerol (Parietene Composite®), polipropileno-polidioxanona con cubierta de celulosa oxidada (Proceed®) y pericardio bovino (Tutomesh®). Estudios experimentales realizados en ratas han demostrado que no existe diferencia en la incidencia de infección con los diferentes tipos de mallas y se documentó que las mallas que combinan un índice menor de adherencias con una incorporación máxima a los tejidos y fuerza tensil son la Parietex Composite®, Sepramesh® y Proceed®.20-22,33 Entre éstas se ha evidenciado superioridad en cuanto a menor formación de adherencias y mayor incorporación a los tejidos con la malla Proceed® y la Parietex Composite®. Esta última con mayor retracción y encogimiento en modelos experimentales.34 La plastía dinámica con colocación de malla intraperitoneal ha demostrado ser efectiva y segura, con la ventaja de que puede realizarse con técnica abierta o con técnica laparoscópica. Recientemente se ha cuestionado si la plastía de pared abierta es la técnica ideal ya que con la introducción de las técnicas de mínima invasión para diversos procedimientos se han obtenido resultados alentadores. Se han publicado varios reportes con resultados exitosos de plastías abdominales con colocación de material protésico totalmente laparoscópico. Las ventajas son todas aquellas que proporciona la mínima invasión, con una estancia intrahospitalaria corta, menor dolor postoperatorio y recuperación más rápida. Estudios publicados reportan una menor incidencia de complicaciones postoperatorias en los grupos laparoscópicos, incluyendo el número de infecciones superficiales y profundas y con una recurrencia tan baja de la hernia como el 4%. Los índices de conversión a cirugía abierta son bajos cuando el grupo quirúrgico tiene la experiencia.10,35-37 La reparación laparoscópica exitosa requiere de una adecuada superposición de tejido sano sobre la malla y fijación. Actualmente se acepta que los pacientes ideales para el abordaje laparoscópico son aquéllos en los que además de colocar una placa protésica también debe ser posible el cierre de la aponeurosis que permitirá darle soporte al material protésico. En nuestra experiencia, tres casos fueron resueltos por laparoscopia exitosamente a pesar de tratarse de pacientes con cirugías abdominales previas, con múltiples adherencias e incluso con colocación previa de material protésico en uno de los casos con un seguimiento de 12 meses sin complicaciones menores, mayores, ni recurrencia. Se han publicado estudios que analizan el costo-beneficio de la plastía abdominal laparoscópica con reportes de cortas estancias intrahospitalarias, con aumento en los costos por tiempo quirúrgico prolongado y material requerido pero con menos complicaciones a largo plazo, con resultados no concluyentes.10,37-39 En nuestra serie, la plastía abierta con técnica IPOM con malla Proceed® fue el procedimiento que se realizó con mayor frecuencia con resultados satisfactorios en cuanto a complicaciones (18%), estancia intrahospitalaria (EIH) (3 días), tiempo quirúrgico (media = 80 min) y recidiva (3%), que es comparable a lo descrito en la literatura. Al comparar las dos técnicas (ONLAY con polipropileno e IPOM con Proceed®), los resultados fueron similares en cuanto a complicaciones (11 vs 18%, p = 0.09), EIH (3 vs 3 días p = 0.16) y tiempo quirúrgico (80 vs 84 min. p = 0.70) incluso considerando los tiempos simultáneos de plastía con restitución intestinal; sin embargo, la recidiva disminuyó considerablemente de un 18% reportada con la técnica ONLAY a un 3% con la técnica IPOM (p = 0.01). Estos resultados son preliminares a 2 años de seguimiento del grupo experimental. La mortalidad en series grandes relacionada a riesgos generales se reporta de 1.8%. En nuestra serie la mortalidad fue de 0%. Finalmente, podemos afirmar que las hernias de la pared abdominal representan un problema de salud pública ya que son una patología frecuente. Son causa de discapacidad física, alteraciones respiratorias, posturales y dinámicas con el riesgo permanente de encarcelamiento, con necrosis intestinal subsecuente y las complicaciones derivadas de la misma que afectan la calidad de vida de los pacientes, además de afectar la estética. A pesar de ser un procedimiento que se realiza con frecuencia, la recurrencia y las complicaciones son considerables y el éxito de las plastías subsecuentes disminuye con el número de cirugías consecutivas previas. A lo largo de los años se ha intentado documentar cuál es el procedimiento ideal para la reparación definitiva de las hernias ventrales, en especial en aquellos pacientes que tienen grandes defectos o intentos previos por lo que es difícil la reconstrucción de la pared y separar las asas intestinales del material protésico colocado si se ha adherido. El objetivo de las plastías de pared es la restauración de la integridad de la pared abdominal con continuidad miofascial y sin tensión, recuperando las características fisiológicas de la pared, lo que permite al paciente la reincorporación a sus actividades con una adecuada calidad de vida. Aceptando que los mejores resultados se obtienen cuando se utiliza material protésico, existen diversos tipos de mallas que buscan cubrir los defectos aponeuróticos sin adherirse a los órganos intraabdominales, pero con adecuada integración a los tejidos de la pared. No existe aún el material ideal que cumpla con estas características, ya que aquellas que ofrecen una reducción en la formación de adherencias se asocian a una reducción en la incorporación. En estudios experimentales, los mejores resultados se obtienen con la colocación de la malla bicapa Proceed® pues tiene un menor índice de adherencias y se incorpora satisfactoriamente intentando cumplir los criterios de idoneidad. En nuestra experiencia, la malla Proceed® demostró ser eficaz y segura para la reparación de grandes defectos de la pared abdominal y los resultados son alentadores pues la recidiva reportada es solamente del 3%, comparada con la técnica ONLAY que utilizábamos previamente, en la cual es del 18% (p = 0.01). La incidencia de complicaciones es similar entre los dos grupos 20% vs 32%, p = 0.09, así como la estancia intrahospitalaria (m = 3 días) y el tiempo quirúrgico requeridos (m = 80 minutos). Se observa que el uso de la plastía ONLAY con malla de polipropileno tiene un mayor riesgo de recidiva en 1.8 veces con respecto a la plastía IPOM con malla Proceed®. Asimismo, la presencia de comorbilidades aumenta el riesgo de recidiva en 2.5 veces cuando se utiliza la técnica ONLAY, por lo que en ese tipo de pacientes recomendamos el uso de malla Proceed® intraperitoneal. Los grupos comparados son similares en cuanto a edad y género y se incluyeron 110 pacientes en total, 55 en cada grupo, todos con un defecto de la pared abdominal de más de 5 cm. El análisis estadístico demuestra que los pacientes incluidos en el grupo experimental (plastía con malla Proceed®) presentaban defectos significativamente mayores a los del grupo control (12 vs 6 cm, p = 0.00), los cuales se repararon exitosamente. La plastía dinámica con malla Proceed® para la reparación de grandes defectos de la pared abdominal es segura y eficaz.
REFERENCIAS
1. Espinosa MA, de la Aorre JI, Ahumada LA, Person DW, Rosenberg LZ, Vásconez LO. Reconstruction of the abdominal wall for incisional hernia repair. Am J Surg 2006; 191: 173-177. [ Links ]
2. Yaghoobi Notash A, Yaghoobi Notash A Jr, Seied Farchi J, Ahmadi Amoli H, Salimi J, Mamarabadi M. Outcomes of the Rives-Stoppa technique in incisional hernia repair: ten years of experience. Hernia 2007; 11: 25-29. [ Links ]
3. Hadi HI, Maw A, Samah S, Kumar P. Intraperitoneal tension-free repair of small midline ventral abdominal wall hernias with a Ventralex hernia patch: initial experience in 51 patients. Hernia 2006; 10: 409-413. [ Links ]
4. Alaedeen DI, Lipman J, Medalie D, Rosen MJ. The single-staged approach to the surgical management of abdominal wall hernias in contaminated fields. Hernia 2007; 11: 41-45. [ Links ]
5. Luijendijk RW, Hop WC, van den Tol MP, de Lange DC, Braaksma MM, IJzermans JN, et al. A comparison of suture repair with mesh repair for incisional hernia. N Engl J Med 2010; 343: 392-8. [ Links ]
6. Millikan KW, Baptista M, Amin B, Deziel DJ, Doolas A. Intraperitoneal underlay ventral hernia repair utilizing bilayer expanded polytetrafluoroethylene and polypropylene mesh. Am Surg 2003; 69: 287-292. [ Links ]
7. Trupka AW, Hallfeldt KK, Schmidbauer S, Schweiberer L. [Management of complicated incisional hernias with underlay-technique implanted polypropylene mesh. An effective technique in French hernia surgery]. Chirurg 1998; 69: 766-772. [ Links ]
8. Ronsen MJ, Williams C, Jin J, McGee MF, Schomisch S, Marks J, et al. Laparoscopic versus open-component separation: a comparative analysis in a porcine model. Am J Surg 2007; 194: 385-389. [ Links ]
9. Olmi S, Scaini A, Cesana GC, Erba L, Groce E. Laparoscopic versus open incisional hernia repair: an open randomized controlled study. Surg Endosc 2007; 21: 555-559. [ Links ]
10. Barbaros U, Asoglu O, Seven R, Erbil Y, Dinccag A, Deveci U, et al. The comparison of laparoscopic and open ventral hernia repairs: a prospective randomized study. Hernia 2007; 11: 51-56. [ Links ]
11. Catena F, Ansaloni L, Gazzotti F, Gagliardi S, Di Saverio S, D'Alessandro L, et al. Use of porcine dermal collagen graft (Permacol) for hernia repair in contaminated fields. Hernia 2007; 11: 57-60. [ Links ]
12. Bingener J, Buck L, Richards M, Michalek J, Schwesinger W, Sirinek K. Long-term outcomes in laparoscopic vs open ventral hernia repair. Arch Surg 2007; 142: 562-7. [ Links ]
13. Bleichrodt RP, Malyar AW, de ries Reilingh TS, Buyne O, Bonenkamp JJ, van H. The omentum-polypropylene sandwich technique: an attractive method to repair large abdominal-wall defects in the presence of contamination or infection. Hernia 2007; 11: 71-74. [ Links ]
14. Awad ZT, Puri V, LeBlanc K, Stoppa R, Fitzgibbons RJ Jr, Iqbal A, et al. Mechanisms of ventral hernia recurrence after mesh repair and new proposed classification. J Am Coll Surg 2005; 201: 132-140. [ Links ]
15. Finan KR, Vick CC, Kiefe CL, Neumayer L, Hawn MT. Predictors of wound infection in ventral hernia repair. Am J Surg 2005; 190: 676-681. [ Links ]
16. Alder AC, Alder SC, Livingston EH, Bellows CF. Current opinions about laparoscopic incisional hernia repair: a survey of practicing surgeons. Am J Surg 2007; 194: 659-662. [ Links ]
17. Amid PK. Classification of Biomaterials and their related complications in abdominal wall hernia surgery. Hernia 1997; 1: 15-21. [ Links ]
18. Kaufman Z, Engelberg M, Zager M. Fecal fistula: A late complication of Marlex mesh repair. Dis Colon Rectum 1981; 24: 543-544. [ Links ]
19. Leber GE, Garb JL, Alexander AI, Reed WP. Long-term complications associated with prosthetic repair of incisional hernias. Arch Surg 1998; 133: 378-382. [ Links ]
20. Hutchinson RW, et al. Pre-clinical abdominal adhesion studies with Proceed® surgical mesh. Business Briefing: Global Surgery 2004: 1-4. [ Links ]
21. Rasim ZM, Alzahrani MA, Sigman MH, Meakins JL, Fried GM. Comparison of adhesion formation and tensile strength after three laparoscopic herniorraphy techniques. Surg Laparosc Endosc 1997; 7: 133-136. [ Links ]
22. Kiudelis M, Jonciauskiene O. Effects of different kinds of meshes on postoperative adhesion formation in New Zealand White rabbit. Hernia 2007; 11: 19-23. [ Links ]
23. Baykal A, Onat D, Rasa K, Renda N, Sayek I. Effects of polyglycolic acid and polypropylene meshes on postoperative adhesion formation in mice. World J Surg 1997; 21: 579-583. [ Links ]
24. Kiudelis M, Jonciauskiene J, Deduchovas O, Radziunas A, Mickevicius A, Janciauskas D, et al. Effects of different kinds of meshes on postoperative adhesion formation in the New Zealand White rabbit. Hernia 2007; 11: 19-23. [ Links ]
25. Sullivan SR, Engrav LH, Anaya DA. Bulger EM, Foy HM. Bilateral anterior abdominal bipedicle flap with permanent prosthesis for massive abdominal skin-grafted hernia. Am J Surg 2007;193:651-655. [ Links ]
26. Ihedioha U, Leung E, Chung L, Burgess G, Hendry D, O'dwyer PJ. A complex fistula caused by eroding pelvic mesh sling. Hernia 2007; 11: 75-78. [ Links ]
27. Delikoukos S, Tzovaras G, Liakou P, Mantzos F, Hatzitheofilou C. Late-onset deep mesh infection after inguinal hernia repair. Hernia 2007; 11: 15-17. [ Links ]
28. Sakorafas G, Sarr MG. Repair of ventral and incisional hernias using modifications of the Rives-Stoppa technique. Prob Gen Surg 2002; 19: 51-58. [ Links ]
29. Aufenacker TJ, Keolemay MJ, Gourma DJ, Simons MP. Systematic review and meta-analysis of the effectiveness of antibiotic prophylaxis in prevention of wound infection after mesh repair of abdominal wall hernia. Br J Surg 2006; 93: 5-10. [ Links ]
30. Pérez AR, Roxas MF, Hilvano SS. A randomized, double blind, placebo-controlled trial to determine effectiveness of antibiotic prophylaxis for tension-free mesh herniorrhaphy. J Am Coll Surg 2005; 3: 393-397. [ Links ]
31. Hernández LA. Tratamiento simultáneo de plastía de pared con malla y cierre intestinal. Cir Gen 2004; 26: 242-247. [ Links ]
32. Stoppa RE. The treatment of complicated groin and incisional hernias. World J Surg 1989; 13: 545-554. [ Links ]
33. Burger JW, Halm JA, Wijsmuller AR, ten Raa S, Jeedel J. Evaluation of new prosthetic meshes for ventral hernia repair. Surg Endosc 2006; 20: 1320-1325. [ Links ]
34. Judge TW, Parker DM, Dinsmore RC. Abdominal wall hernia repair: a comparison of aepramesh and parietex composite mesh in a rabbit hernia model. Am Coll Surg 2007; 204: 276-281. [ Links ]
35. Lomanto D, Iyer SG, Shabbir A, Cheah WK. Laparoscopic versus open ventral hernia mesh repair: a prospective study. Surg Endosc 2006; 20: 1030-5. [ Links ]
36. McCormack K, Scott NW, Go PM, Ross S, Grant AM; EU Hernia Trialists Collaboration. Laparoscopic techniques versus open techniques for inguinal hernia repair. Cochrane Database Syst Rev 2003; CD001785. [ Links ]
37. Pierce RA, Spitler JA, Frisella MM, Matthews BD, Brunt LM. Pooled data analysis of laparoscopic vs open ventral hernia repair: 14 years of patient data accrual. Surg Endosc 2007; 21: 378-386. [ Links ]
38. Earle D, Seymour N, Fellinger E, Perez A. Laparoscopic versus open incisional hernia repair: a single institution analysis of hospital resource utilization for 884 consecutive cases. Surg Endosc 2006; 20: 71-75. [ Links ]
39. Beldi G, Ipaktchi R, Wagner M, Candinas BD. Laparoscopic ventral hernia repair is safe and cost effective. Surg Endosc 2006; 20: 92-95. [ Links ]














