Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista internacional de contaminación ambiental
versión impresa ISSN 0188-4999
Rev. Int. Contam. Ambient vol.28 no.1 Ciudad de México feb. 2012
Artículos
Metales pesados totales y arsénico en el agua para riego de Puebla y Veracruz, México
Total heavy metals and arsenic in irrigation water of Puebla and Veracruz, Mexico
Óscar Raúl MANCILLA–VILLA1*, Héctor Manuel ORTEGA–ESCOBAR1, Carlos RAMÍREZ–AYALA1, Ebandro USCANGA–MORTERA2, Rosalía RAMOS–BELLO3 y Amada Laura REYES–ORTIGOZA3
1 Postgrado de Hidrociencias, Colegio de Postgraduados, Campus Montecillo, carretera México Texcoco, km 36.5. C.P. 56230, Texcoco, México.
2 Botánica, Colegio de Postgraduados, Campus Montecillo, carretera México Texcoco, km 36.5. C.P. 56230, Texcoco, México. Correo electrónico: vios@colpos.mx
3 Departamento de Ecología y Recursos Naturales, Facultad de Ciencias, UNAM, área de biología. Correo electrónico: rorabe2003@hotmail.com
Recibido julio 2010,
aceptado noviembre 2011
RESUMEN
Los altos niveles de concentración de metales pesados en agua utilizada para riego representan un problema importante para la agricultura y la salud humana, así como para la biodiversidad, por tal motivo se realizó el presente trabajo con relación a la calidad del agua en los estados de Puebla y Veracruz, México. El estudio se llevó a cabo de noviembre de 2009 a marzo de 2010, se tomaron 91 muestras de agua duplicadas. Se analizaron el potencial hidrógeno (pH), la conductividad eléctrica (CE), As y metales pesados totales: Cd, Cr, Cu, Hg, Ni, Pb y Zn. Los metales pesados se determinaron mediante el uso de un ICP ("Inductively Coupled Plasma") Pekin Elmer Optima 5300, utilizándose la metodología recomendada por la EPA (Environmental Protection Agency) y APHA (American Public Health Association). Se comparó la calidad del agua superficial con los criterios de la NOM–001–ECOL–1996, de EPA (1986), de SEDUE (1989) y la modificación a la NOM–127–SSA1–1994. Los resultados mostraron valores bajos en la concentración de metales pesados en agua para riego agrícola y uso urbano, no así, para el criterio de consumo humano, pues 50 % de las muestras tomadas presentaron concentraciones por encima de los límites permisibles para Cd, 20 % para Hg y 2 % para Pb (SSA 2000). Se concluyó que el agua superficial no representa riesgos para riego agrícola. La mayor concentración y dispersión la presentó el As con valores de 0.0 a 0.78 mg L–1, mientras que la menor con 0.0 a 0.03 mg L–1, fue para el Hg. Las descargas de agua residual hacia los ríos, contaminan gravemente y llevan a sobrepasar los límites permisibles para Cd, Hg y Pb en agua para uso y consumo humano.
Palabras clave: metales pesados, agua superficial, límites permisibles.
ABSTRACT
High levels of heavy metal concentrations in water used for irrigation are a major concern for agriculture, human health and biodiversity. A study of surface water quality of rivers and springs of Puebla and Veracruz, Mexico was made. The study was conducted from November 2009 to March 2010. Sampling consisted of two repetitions. Parameters such as potential hydrogen (pH), electrical conductivity (EC), As and total heavy metals: Cd, Cr, Cu, Hg, Ni, Pb and Zn were analyzed. Heavy metals were determined using a Perkin Elmer Optima 5300 ICP ("Inductively Coupled Plasma"). The methods used were the recommended by the EPA (Environmental Protection Agency) and APHA (American Public Health Association). The surface water quality was compared with the criteria of NOM–001–ECOL–1996, EPA (1986), SEDUE (1989) and modification of NOM–127–SSA1–1994. It was observed the presence of low levels of heavy metals in water for agricultural irrigation and urban use. However the criterion for human consumption was exceeded because 50 % of the waters sampled had levels above maximum allowable limits for Cd, 20 % for Hg and 2 % for Pb (SSA 2000). It was concluded that surface waters sampled do not represent risks for agricultural irrigation. The highest concentration and dispersion was for As, with values from 0.0 to 0.078 mg L–1, while the lowest with 0.0 to 0.03 mg L–1, was for the Hg. Wastewater discharges on rivers, pollute to levels that exceed the permissible limits for Cd, Hg and Pb in drinking water.
Keywords: heavy metals, surface water, allowable limits.
INTRODUCCIÓN
La problemática de los metales pesados como plomo, níquel, cadmio y manganeso, presentes en el agua residual utilizada para riego, radica principalmente en que pueden ser acumulados en los suelos agrícolas. Resultan peligrosos por su carácter no biodegradable, la toxicidad que ejercen sobre los diferentes cultivos y su biodisponibilidad (Mahler, 2003, García y Dorronsoro 2005, Corinne et al. 2006), además de los mencionados incluyen: mercurio, arsénico y cromo (Lucho et al. 2005).
Los metales pesados y el As se encuentran generalmente como componentes naturales de la corteza terrestre, en forma de minerales, sales u otros compuestos, pueden ser absorbidos por las plantas y así incorporarse a las cadenas tróficas (Rooney et al. 2006, Zhao et al. 2006); pasar a la atmósfera por volatilización y movilizarse hacia el agua superficial o subterránea. No son degradados fácilmente de forma natural o biológica ya que no tienen funciones metabólicas específicas para los seres vivos (Abollino et al. 2002).
En lugares donde se ha utilizado agua residual para el riego agrícola, se reporta una tendencia creciente en las concentraciones de metales pesados, (García et al. 2000, Hettiarchchi y Pierzynski 2002). Existe una amplia investigación sobre el riesgo de los metales pesados en la salud y el ambiente (Spain et al. 2003).
Varios autores han mostrado el riesgo de contaminación por metales pesados en el agua (Yang et al. 1996, Ramos et al. 1999, Topalián et al. 1999, Santos et al. 2002, Taboada–Castro et al. 2002, Lee y Moon 2003, Montes–Botella y Tenorio 2003, Smolders et al. 2003, Lucho et al. 2005, Mapanda et al. 2005, Tahri et al. 2005, Malla et al. 2007, Prieto et al. 2007); en la acumulación de metales pesados en los suelos agrícolas (Fytianos et al. 2001, Ho y Egashira 2001, Moor et al. 2001, Ramos–Bello et al. 2001, Lin 2002, Moral et al. 2002, Davor 2003) y en el riesgo potencial para la salud humana debido a la acumulación de metales pesados en las plantas (Zhou et al. 2000, Long et al. 2003, Wang et al. 2003, Qi–Tang et al. 2004, Ismail et al. 2005).
En los valles agrícolas de Puebla y la zona centro–norte del estado de Veracruz, desde hace mas de 100 años se ha empleado para riego directo, agua superficial contaminada con agua residual, a consecuencia de esto, se han acumulado metales pesados en los suelos agrícolas irrigados con agua residual (Silva et al. 2002).
Algunos autores reportan presencia de Cd, Ni y Pb, en agua, suelo y en plantas (Ávila y Zarazúa 1993; Villanueva y Botello 1992, Prieto–Méndez et al. 2009). Se reportan estudios donde se analizaron los efectos de diferentes suelos que habían sido sometidos a riegos con agua–lodo residual y la influencia de éstos en el crecimiento vegetal y la biodisponibilidad de Ni, Cd y Pb (Perdomo 2005, Mahdy et al. 2007).
El presente estudio tuvo como objetivo fundamental conocer la concentración de metales pesados totales, Pb, Cd, Hg, Zn, Ni, Cu, Cr y As en el agua superficial de Puebla y Veracruz, así como definir el riesgo del uso de agua contaminada para riego agrícola y uso doméstico.
MATERIALES Y MÉTODOS
El área de estudio se encuentra en el estado de Puebla y la parte centro–norte del estado de Veracruz, México (Fig. 1). El agua muestreada es utilizada para riego agrícola, recreación y uso doméstico; los ríos, manantiales y embalses muestreados en Puebla fueron: Atoyac, Izúcar, Salado y Chiautla. En Veracruz: Blanco, San Miguel, Chocamam, Coscomatepec, Pescados, Alseseca, Tlapacoyan, Filobobos, Nautla, Tecolutla, Cazones, Tuxpan, Tempoal, Pánuco, Tampico, Nogales, Ojo de Agua, Puente de Dios, El Carmen y Pancho Pozas. Las coordenadas geográficas del cuadrante del área de estudio son: 22º 00' latitud norte y 97º 00' longitud oeste, hasta 18º 00' latitud norte y 99º 00' longitud oeste. Los sitios de muestreo se encuentran en altitudes desde 0 m hasta los 3 000 m.
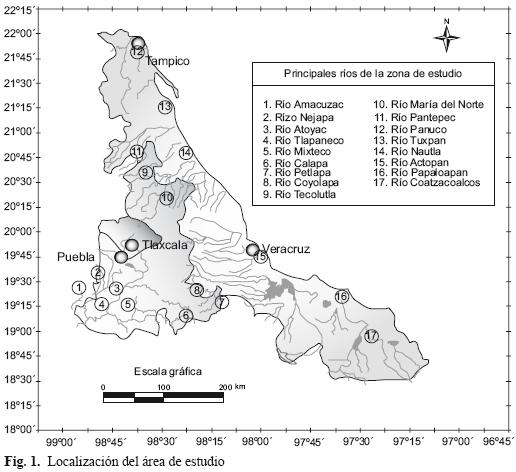
En la figura 1, se presenta la zona de estudio donde se realizó el recorrido de campo que se llevó a cabo para colectar las muestras de agua, dicha expedición se inició en los límites de Puebla con Tlaxcala, y continuó por la parte sur de Puebla, posteriormente se recorrió la parte centro–norte de Veracruz y finalmente se terminó en la Presa de Necaxa en Puebla.
La investigación de campo se realizó durante noviembre de 2009. Las estaciones de muestreo se establecieron en 91 sitios, en cada uno se colectaron 2 muestras duplicadas (182 en total) en recipientes de polietileno de alta densidad de 0.2 L, se les agregó ácido nítrico concentrado a pH<2, se colocaron en hieleras para transportarlas con base en los lineamientos de EPA (1983) y APHA (1995).
Los parámetros químicos que se midieron fueron: pH y CE al momento de tomar la muestra de acuerdo con APHA (1995), con el conductímetro/potenciómetro modelo: Excel 20/Phmetro–mV–Conductímetro. Los metales pesados totales se determinaron con la técnica de espectrometría de emisión atómica, mediante plasma de acoplamiento inductivo con el ICP, modelo Perkin Elmer 5300 Optima, en el laboratorio de Ciencias Ambientales del Colegio de Postgraduados, Campus Montecillo; los metales pesados analizados fueron Pb, Hg, Zn, Cd, Cu, Cr, Ni y As. Los límites de cuantificación fueron los siguientes: 5.0, 0.024, 8.0, 1.5, 3.0, 5.0, 15.0 y 0.05 (µg L–1), para los metales respectivos.
Los valores de recuperación obtenidos en las muestras fortificadas, en agua desionizada, para el análisis de los metales fueron los siguientes: As 109.1 %, Cr 99.46 %, Cu 99.25 %, Hg 106.15 %, Zn 98.21 %, Cd 100.35 %, Pb 96.93 % y Ni 98.24 %; dichos valores se encuentran dentro del rango recomendado y cercanos a 100 % (EPA, 1996).
Para evaluar la calidad del agua de los ríos, embalses y manantiales, se utilizaron los criterios de EPA, (1986), la NOM–001–ECOL–1996 (ECOL, 1997) y los criterios ecológicos de calidad de agua para diferentes usos (SEDUE 1989), que establecen los límites máximos permisibles para metales pesados contenidos en el agua para uso en riego agrícola y urbano (Cuadro I).
RESULTADOS Y DISCUSIÓN
En el Cuadro II, se presenta la ubicación geográfica, la altitud y los nombres de las estaciones de muestreo que fueron consideradas en la presente investigación. Es importante mencionar que las estaciones se localizan en un rango de altitud que va desde el nivel del mar hasta los 3000 m. Se consideraron los ríos y embalses que representan importancia para el riego agrícola y recreación en Puebla y Veracruz. La información de los resultados se manejó en conjunto para las 91 estaciones de muestreo, se resaltan las concentraciones de metales que sobrepasan los límites permisibles.
En la figura 2, se presenta el pH y la conductividad eléctrica medidos en los ríos, manantiales y embalses de Puebla y Veracruz, los valores de estos parámetros fueron corregidos por los factores de temperatura respectivos.

El pH de la solución tiene un efecto sobre la biodisponibilidad de la mayoría de los metales pesados al afectar el equilibrio entre la especiación metálica, solubilidad, adsorción e intercambio de iones en el suelo (Riechaman 2002). En soluciones ácidas se produce una competencia de los iones H+ con los cationes metálicos por los sitios de intercambio (Kheboian y Bauer 1987). Al aumentar el pH, los metales pesados son removidos de la solución del suelo y adsorbidos por los coloides disminuyendo su biodisponibilidad (Basta y Tabatabai 1992). Por lo tanto, en suelos agrícolas con cargas variables, la retención de los cationes metálicos aumenta en la medida que el pH sea más alto y se reduce al acidificarse el suelo o el agua.
En el agua analizada se encontraron valores de pH neutros y alcalinos, lo que sugiere que los metales pesados están menos disponibles, puesto que un porcentaje importante se ha precipitado como hidróxidos insolubles, carbonatos y complejos orgánicos (Silveira et al. 2003). Sin embargo, el Hg el Cd y el Pb que sobrepasaron los límites máximos permisibles en agua para consumo humano, posiblemente se encuentran asociados con partículas suspendidas del agua, que al igual que el As, Mo, Se y Cr, tienden a estar menos disponibles a pH alcalinos (Manzione and Merrill 1989).
En la figura 2, se observa que el 90 % de las muestras presentaron un pH entre 6.9 y 9, el rango de límites permisibles está entre 5 y 10 unidades para este parámetro, mientras que la conductividad eléctrica mostró, en el 85 % de las muestras, valores menores a 2000 µS cm–1, lo que indica que el agua analizada, bajo el criterio de estos dos parámetros y desde el punto de vista agrícola, es recomendable de acuerdo con Ayers y Westcot (1987), con algunas restricciones para el 15 % de las muestras que presentaron elevados valores de CE, debido a que proceden de agua influenciada por agua marina y agua subterránea salina.
En la figura 3 se presentan los resultados de la concentración de metales pesados en el agua muestreada.
Al comparar los valores obtenidos con los límites máximos permisibles establecidos por la NOM–001–ECOL–1996 (ECOL, 1997), sólo uno de los ocho metales pesados analizados, rebasa dichos límites, tal es el caso del mercurio. Para el promedio diario de los usos urbano y protección de vida acuática, 3 de las 91 muestras están por encima de 0.01 mg L–1. Para el criterio de EPA (1986), se encontró que 1, 30, 15 y 20 % de las muestras analizadas supera el límite permisible para As, Pb, Cd y Hg, respectivamente.
Las estaciones de muestreo que superaron los límites permisibles para uso urbano en la concentración de mercurio fueron, el Río Tepeyahualco con 0.0138 mg L–1, el Arroyo de Salinas Zapotitlán con 0.0180 mg L–1 y el Río Salado con 0.0318 mg L–1, por lo que el agua de estos sitios representa riesgo en el uso urbano.
Con respecto al agua para uso de riego, las concentraciones de As y los metales determinados, están por debajo de los límites máximos permisibles, por lo que el agua puede ser utilizada sin riesgo en el riego agrícola de acuerdo con la NOM–001–ECOL–1996 (ECOL, 1997). Sin embargo, de acuerdo con la EPA (1986), se debe tener restricción de uso para el agua que superó los límites de concentración de As, Pb, Cd y Hg. En cuanto al criterio de SEDUE (1989), para el uso en riego agrícola, 13 de las 91 muestras de agua superaron el límite de 0.01 mg L–1 de Cd. Mientras que las concentraciones para los otros metales se presentaron por debajo del límite máximo permisible, para riego, recreación y uso industrial.
Las concentraciones de As y Cu obtenidas, tanto para riego agrícola, para uso doméstico como para consumo humano, están por debajo del límite permisible que establece la modificación de la NOM–127–SSA1–1994 (SSA 2000), sin embargo, para el Hg cerca del 20% de las estaciones rebasan los 0.001 mg L–1; para el Cd prácticamente 50 % de las muestras analizadas excede los 0.005 mg L–1, que es el límite permisible para este elemento, en cuanto al Pb, sólo 2 % de los puntos de muestreo rebasa el límite permisible de 0.025 mg L–1.
Aunque el límite permisible para consumo humano no fue un objetivo fundamental de la investigación, es importante mencionarlo y tomar en cuenta los valores encontrados para los metales que superaron la concentración permitida, tanto para investigaciones futuras, como para la toma de decisiones en cuanto al uso que tenga el agua de los ríos que fueron analizados.
Gómez–Álvarez et al. (2004), encontraron valores superiores a los límites máximos permisibles para Pb en un afluente proveniente de una zona minera, aledaña al Río San Pedro, la concentración fue de 0.30 mg L–1, mientras que para el muestreo del presente estudio, el valor máximo de concentración para el mismo metal fue de 0.03 mg L–1. Esta gran diferencia de concentración se debe a que en zonas mineras los afluentes son contaminados con mayores cantidades de metales pesados por medio del agua residual, en contraste, la zona objeto de estudio no presenta actividad minera, pero sí, actividad agrícola, actividad industrial y urbanización.
La distribución del contenido de As y metales pesados en el agua, se presenta en la figura 4, donde se puede observar que el 75 % de las concentraciones de los iones determinados, mostraron valores por debajo de 0.01 mg L–1, por su parte 25 % de las concentraciones de As, Ni y Zn, fueron iguales o menores de 0.005 mg L–1.

El Hg presentó los valores más bajos, el límite superior fue de 0.03 mg L–1, por su parte el As mostró los más altos contenidos, así como la mayor dispersión en el agua para riego con valores de hasta 0.078 mg L–1. Además se reveló que la variación fue asimétrica en los diagramas de cajas, lo que se explica por la diversidad de los lugares donde se tomaron las muestras de agua.
Para los ríos, manantiales y embalses estudiados en el presente trabajo, aún no existen riesgos importantes que perjudiquen a la salud humana principalmente; excepto en algunos casos de exceso de As, Pb, Cd y Hg, encontrados en el agua de ríos cercanos a las descargas de agua residual.
La atribución de las concentraciones de metales pesados antes mencionadas, se le hace a la actividad agrícola principalmente de la zona cañera y a las descargas residuales de los ingenios azucareros, así como a las descargas de aguas urbano–industriales. Además del intemperismo de las rocas con las que está en contacto el agua, características similares fueron encontradas en el agua del Río Hondo en Quintana Roo, donde Buenfil–Rojas y Flores–Cuevas (2007) discutieron valores altos de 7 y 3.5 mg L–1, en la concentración de Cd y Hg, respectivamente. Concluyeron que el agua de dicho río excede los límites permisibles (EPA 1986), por lo que el nivel de contaminación afecta a los usuarios de este cuerpo de agua.
Por su parte, Pis–Ramírez (1999) realizó un estudio sobre metales pesados en el agua del embalse Palmarito en Cuba, donde encontró que las concentraciones de Pb fueron de 0.05 mg L–1, para Cd de 0.01 mg L–1 y el Hg no fue detectado. En el presente estudio, las concentraciones promedio de los metales respectivos fueron 0.008, 0.01 y 0.005 mg L–1, dichos valores constatan que el agua es recomendable para uso agrícola.
CONCLUSIONES
El pH y la conductividad eléctrica de la mayoría del agua analizada, no limitan su uso para riego agrícola o uso urbano, por lo que se recomienda su empleo, en cuanto a estos dos parámetros para 85 % de los cuerpos de agua y con restricciones para 15 % del agua estudiada.
El contenido de metales pesados en los ríos, embalses y manantiales de Puebla y Veracruz está por debajo de los límites máximos permisibles por la NOM–001–ECOL–1996. Con base en los resultados se recomienda su uso sin restricciones para riego agrícola y uso urbano, con excepción de 3.26 % de las muestras de agua que exceden la concentración de Hg de 0.01 mg L–1 y se restringe su uso para riego agrícola.
En cuanto al criterio de SEDUE (1989), no existe problema en el uso del agua muestreada para uso en recreación, como fuente de agua potable y en riego; excepto para 14.28 % de las muestras de agua que superan el límite permisible de Cd para el uso en riego agrícola.
De acuerdo a los límites permisibles de la EPA (1986), 1, 30, 15 y 20 % de los cuerpos de agua analizados exceden las concentraciones de As, Pb, Cd y Hg, respectivamente.
Por su parte 50, 20 y 2 % de las muestras analizadas rebasan los límites máximos permisibles para consumo humano, en cuanto al contenido de Cd, Hg y Pb, respectivamente
El Hg presentó las concentraciones y dispersiones de los datos más bajas, mientras que las más altas fueron para el As.
AGRADECIMIENTOS
Al Consejo Nacional de Ciencia y Tecnología (CONACyT), por la beca de posgrado que se le otorgó a Oscar Raúl Mancilla Villa, para hacer posible la realización del presente trabajo.
REFERENCIAS
Abollino O., Aceto M., Malandrino M., Mentaste E., Sarzanini C. y Barberis R. (2002). Distribution and mobility of metals in contaminated sites. Chemometric investigation of pollutant profiles. Environ. Pollut. 119–127. [ Links ]
APHA (1995). Standard methods for examination of water and wastewater. APHA (American Public Health Association), WWA (American Water Works Association), WPCF (Water Pollution Control Federation), Washington D.C., EUA. 1 100 p. [ Links ]
Ávila P.P. y Zarazúa O.G. (1993). Concentración de metales pesados en ostiones (Crassostrea virginica Gmelin), del canal El Chicol, Veracruz, México. Rev. Int. Contam. Ambient. 9, 53–64. [ Links ]
Ayers R.S. y Westcot D.W. (1987). La calidad del agua y su uso en la agricultura. Estudio FAO Riego y Drenaje 29 Rev. 1. Trad. al español por J. F. Alfaro de: Water quality and use in agriculture. 175 p. [ Links ]
Basta N.T. y Tabatabai M.A. (1992). Effect of cropping systems on adsorption of metals by soils: II. Effect of pH. Soil Sci. 153:195–204. [ Links ]
Buenfil–Rojas M. y Flores–Cuevas N. (2007). Determinación de metales pesados (As, Cd, Hg y Pb) presentes en el Río Hondo, Quintana Roo. VI Congreso Internacional y XII Nacional de Ciencias Ambientales, Chihuahua, México. 435–439 pp. [ Links ]
Corinne P.R., Fang–Jie Zhao y Steve McGrath P. (2006). Phytotoxicity of nickel in a range of European soils: Influence of soil properties, Ni solubility and speciation. Environ. Pollut. 145, 596–605. [ Links ]
Davor R. (2003). Heavy metals distribution in agricultural top soils in urban area. Environ. Geol. 43, 795–805. [ Links ]
ECOL (1997). Norma Oficial Mexicana NOM–OO1–ECOL–1996. Que establece los límites máximos permisibles de contaminantes en las descargas de aguas residuales en aguas y bienes nacionales. Secretaría de Medio Ambiente Recursos Naturales y Pesca. Diario Oficial de la Federación, México. [ Links ]
EPA (1983). Methods for chemical analysis of water and wastes (Environmental Protection Agency) Report No. EPA–600/4–79–020, EUA. 544 p. [ Links ]
EPA (1986). Gold Book of Quality Criteria for Water. (Environmental Protection Agency) EPA 440/5–86–001. EUA. 477 p. [ Links ]
EPA (1996). Method 6010B. Inductively Coupled Plasma–Atomic Emission Spectrometry. (Environmental Protection Agency) Las Vegas, Nevada. Revision 2. [ Links ]
Fytianos K., Katsianis G., Triantafyllou P. y Zachariadis G. (2001). Accumulation of heavy metals in vegetables grown in an industrial area in relation to soil. Bull. Env. Contam. Toxicol. 67, 423. [ Links ]
García J.C., Plaza C., Muñóz F. y Polo A. (2000). Evaluation of heavy metals pollution on barley crop by agricultural use of municipal solid waste compost. Centro de Ciencias Medioambientales, CSIC. Madrid. 3rd Internacional Symposium on Geotechnics related to the European Environment. Berlín, Alemania. (http://agrobioenmiendas.iespana.es). [ Links ]
García I. y Dorronsoro C. (2005). Contaminación por metales pesados. En Tecnología de Suelos. Universidad de Granada. Departamento de Edafología y Química Agrícola. http://edafologia.ugr.es. [ Links ]
Gómez–Álvarez A., Villalba A.A., Acosta R.G., Castañeda O.M. y Camp D. (2009). Metales pesados en el agua superficial del Río San Pedro durante 1997 y 1999. Rev. Int. Contam. Ambie. 20, 1–8. [ Links ]
Hettiarchchi G.M. y Pierzynski G.M. (2002). In situ stabilization of soil lead using phosphorus and manganese oxide: Influence of plant growth. J. Environ. Qual. 31, 564–573. [ Links ]
Ho T.L. y Egashira K. (2001). Solid–solution ratio on extraction of heavy metals by dilute acids from agricultural soils and river–sediments in Hanoi, Vietnam. Com. Soil Sci. Plant Anal. 32, 643–660. [ Links ]
Ismail I. B.S., Farihah K. y Khairiah J. (2005). Bioaccumulation of heavy metals in vegetables from selected agricultural areas. Bull. Environ. Contam. Toxicol. 74, 320–327. [ Links ]
Kheboian C. y Bouer C.F. (1987). Accuracy of selective extraction procedures for metal speciation in model aquatic sediments. Anal. Chem. 59, 1417–1423. [ Links ]
Lee S. y Moon H.S. (2003). Heavy metals in the bed and suspended sediments of Anyang River, Korea: implications for water quality. Environ. Geochem. Healt. 25, 433–452. [ Links ]
Lin Y.P. (2002). Multivariate geostatistical methods to identify and map spatial variations of soil heavy metals. Environ. Geol. 42, 1–10. [ Links ]
Long X.X., Yang X.E., Ni W.Z., Ye Z.Q., He Z.L., Calvert D.V. y Stoffella J.P. (2003). Assessing zinc thresholds for phytotoxicity and potential dietary toxicity in selected vegetable crops. Com. Soil Sci. Plant Anal. 34, 1421–1434. [ Links ]
Lucho C.A., Prieto F., Del Razo L.M., Rodríguez R. y Poggi H. (2005). Chemical fractionation of boron and heavy metals in soils irrigated with wastewater in central Mexico. Agric. Ecosyst. Environ. 108, 57–71. [ Links ]
Mahdy A.M., Elkhatib E.A. y Fathi N.O. (2007). Cadmium, copper, nickel, and lead availability in biosolids–amended alkaline soils. Australian J. Bas. App. Sci. 1, 354–363. [ Links ]
Mahler R.L. (2003). General overview of nutrition for field and container crops. En: National Proceeding: Forest and Conservation Nursery Associations. Riley, L. E., Dumroese R. K., Landis, T. D. Tech. Coords. June 9–12; Coeur d'Alene, ID; and 2003 July 14–17; Springfield, IL. Proc. RMRS–P–33. [ Links ]
Malla R., Tanaka Y. y Mori K.L. (2007). Shortterm effect of sewage irrigation on chemical build up in soils and vegetables. The Agricultural Engineering International: The CIGR Journal. Manuscript LW 07 006 Vol. IX, August, 2007. [ Links ]
Manzione M.A. y Merrill D.T. (1989). Trace metal removal by iron co–precipitation: Field evaluation. Electric Power Research Institute. Report GS–6438 (June, 1989). [ Links ]
Mapanda F., Mangwayana E.N., Nyamangara J. y Giller K.E. (2005). The effect of long–term irrigation using wastewater on heavy metal contents of soils under vegetables in Harare, Zimbabwe. Agric. Ecosyst. Environ. 107, 151–165. [ Links ]
Montes–Botella C. y Tenorio M.D. (2003). Water characterization and seasonal heavy metal distribution in the Odiel River (Huelva, Spain) by means of principal component analysis. Environ. Contam. Toxicol. 45, 436. [ Links ]
Moor C., Lymberopoulou T. y Dietrich V.J. (2001). Determination of heavy metals in soils, sediments and geological materials by ICP–AES and ICP–MS. Microchim. Acta. 136, 123–128. [ Links ]
Moral R., Gilkes R.J. y Moreno–Caselles J. (2002). A comparison of extractants for heavy metals in contaminated soils from Spain. Commun. Soil Sci. Plant An. 33, 2781–2791. [ Links ]
Perdomo C. (2005). Calidad de las aguas y su relación con los sistemas agrícolas. Ing. Agríc. 15, 87–95. [ Links ]
Pis–Ramírez M.A. (1999). Impacto de los metales contaminantes en la calidad de la Tilapia (Oreocromis aureus) cultivada en Cuba. Tesis de Maestría en Ciencias, Universidad de La Habana, Cuba. 57 p. [ Links ]
Prieto F., Lucho C.A., Poggi H., Acevedo O. y Barrado E. (2007). Caracterización fisicoquímica y extracción secuencial de metales y elementos trazas en suelos de la región Actopan–Ixmiquilpan del Distrito de Riego 03, Valle del Mezquital, Hidalgo, México. Ciencia Ergo Sum 14, 69–80. [ Links ]
Prieto M.J., González R. C.A., Román G. A.D. y Prieto G.F. (2009). Contaminación y fitotoxicidad en plantas por metales pesados provenientes de suelos y agua. Tropic. Subtropic. Agroecosyst. 10, 29–44. [ Links ]
Qi–Tang W.Z., Meng X.Q., Gerard E. y Morel J.L. (2004). Characterization of cadmium desorption in soils and its relationship to plant uptake and cadmium leaching. Plant S. 258, 217–226. [ Links ]
Ramos–Bello R., Cajuste L.J., Flores–Román, D. y García–Calderón N.E. (2001). Heavy metals, salts and sodium in Chinampa soils in Mexico. Agrociencia 35, 385–395. [ Links ]
Ramos L., Fernández M.A., González M.J. y Hernández L.M. (1999). Heavy metal pollution in water, sediments and earthworms from the Ebro River, Spain. Bull. Environ. Contam. Toxicol. 63, 305–311. [ Links ]
Riechaman M.S. (2002). The responses of plants to metal toxicity: A review focusing on copper, manganese and zin. Austral. Min. En. Environ. Found. 54 p. [ Links ]
Rooney C.P., Zhao F.J. y McGrath S.P. (2006). Soil factors controlling the expression of copper toxicity to plants in a wide range of European soils. Environ. Toxicol. Chem. 25, 726–732. [ Links ]
Santos A., Alonso E., Callejón M. y Jiménez J.C. (2002). Distribution of Zn, Cd, Pb and Cu Metals in groundwater of the Guadiamar River Basin. W. Air S. Pollut. 134, 273–283. [ Links ]
SEDUE (1989). Acuerdo por el que se establecen los Criterios Ecológicos de Calidad de Agua CE– CCA–001/89. Secretaría de Desarrollo Urbano y Ecología. Publicado en el Diario Oficial de la Federación del 2 de diciembre de 1989. Tomo CDXXX, No. 9. México, D.F. [ Links ]
Silva G.S., Muñoz O.A., De la Isla de Bauer M.L. e Infante G.S. (2002). Contaminación Ambiental en la región de Atlixco, Puebla. Terra 20, 243–251. [ Links ]
Silveira M. L.A., Alleonl L. R.F. y Guilherme L. R.G. (2003). Biosolids and heavy metals in soils. Sci. Agr, 60, 793–806. [ Links ]
Smolders A.J., Lock R.A., Van der Velde G., Medina R.I. y Roelofs J.G. (2003). Effects of mining activities on heavy metal concentrations in water, sediment, and macroinvertebrates, in different reaches of the Pilcomayo River, South America. Arch. Environ. Contam. Toxicol. 44, 314–323. [ Links ]
Spain A. (2003). Implications of microbial heavy metals tolerance in the environment. Reviews in Undergradate Research 2, 1–6. [ Links ]
SSA (2000). Modificación a la Norma Oficial Mexicana NOM–127–SSA1–1994. Salud Ambiental, Agua para Uso y Consumo humano– Límites permisibles de calidad y tratamientos a que debe someterse el agua para su potabilización, Estados Unidos Mexicanos, Secretaría de Salud. Diario Oficial de la Federación. [ Links ]
Taboada–Castro M.M., Diéguez–Villar A. y Taboada–Castro M.T. (2002). Effect of soil use and agricultural practices on heavy metal levels in surface waters. Com. Soil Sci. Plant Anal. 33, 2833–2849. [ Links ]
Tahri M., Benyaïch F. y Bounakhla M. (2005). Multivariate analysis of heavy metal contents in soils, sediments and water in the region of Meknes (central Morocco). Environ. Monit. Assess. 102, 405–417. [ Links ]
Topalián M.L., Castañé P.M., Rovedatti M.G. y Salibián A. (1999). Principal component analysis of dissolved heavy metals in water of the Reconquista River (Buenos Aires, Argentina). Bull. Environ. Cont. Toxicol. 63, 484. [ Links ]
Villanueva F.S. y Botello A.V. (1992). Metales pesados en la zona costera del Golfo de México y Caribe mexicano: Una revisión. Rev. Int. Contam. Ambient. 8, 47–61. [ Links ]
Wang Q.R., Cui Y.S., Liu X.M., Dong Y. T. y Christie P. (2003). Soil contamination and plant uptake of heavy metals polluted sites in China. J. Environ. Geochem. H. 38, 823–838. [ Links ]
Yang W., Yang L. y Zheng J. (1996). Effect of metal pollution on the water quality in Taihu Lake. Geo J. 40, 197–200. [ Links ]
Zhao F.J., Rooney C.P., Zhang H. y McGrath S.P. (2006). Comparison of soil solution speciation and diffusive gradients in thin–films measurement as an indicator of copper bioavailability to plants. Environ. Toxicol. Chem. 25, 733–742. [ Links ]
Zhou Z.Y., Fan Y. P. y Wang M.J. (2000). Heavy metal contamination in vegetables and their control in China. Environ. Cont. Toxicol. 16; 2, 239. [ Links ]














