ANTECEDENTES
La migraña es una de las enfermedades más frecuentes y discapacitantes en población económicamente activa (25-55 años), se encuentra entre las 10 enfermedades principales en la población general, su prevalencia general es de 14.7% con predominio en mujeres (17.6 vs 8%); según cálculos, afecta a más de 44 millones de personas en Estados Unidos y aproximadamente a 170 millones de personas en Europa.1 En Latinoamérica Morillo y colaboradores reportaron una prevalencia general de 8.5%, donde Brasil tuvo la cifra más alta con 12.6% y Argentina tuvo la más baja con 5%, mientras que en México se reportó en 8% (12.1% en mujeres y 3.9% en hombres).2 En el estudio de Arroyo y su grupo se evaluó la prevalencia en una cohorte de mujeres mexicanas (cohorte ESMaestras) que incluyó 77,885 participantes entre 2011 y 2013, con prevalencia de 19%.3
En el aspecto clínico la migraña puede identificarse con la mnemotecnia POUND que por su siglas en inglés hacen referencia a Pulsatil, One day, Unilateral, Nausea, Discapacity, que equivalen en español a pulsátil, duración de 4 a 72 horas, unilateral, asociada con náuseas-vómito y discapacidad, sin olvidar que frecuentemente se vincula también con foto-fonofobia y que su intensidad es de moderada a grave, asimismo, existe el cuestionario Migraine ID que analiza la existencia de náusea, fotofobia y discapacidad, puede establecerse el diagnóstico de migraña con la existencia de dos de tres de estas características con sensibilidad de 84% y especificidad de 76%.4
El tratamiento de la migraña puede ser en la fase aguda (abortivo) y profiláctico, este último reviste gran importancia porque incide directamente en la calidad de vida, en los días-trabajo perdidos por discapacidad y en las relaciones interpersonales, entre otros. Se ha calculado que entre 20 y 35% de los pacientes con migraña son aptos a recibir tratamiento profiláctico; sin embargo, hasta 66% de estos pacientes no lo reciben.5
Definiciones
De acuerdo con su frecuencia por mes, según la tercera clasificación internacional de cefaleas, la migraña puede definirse en dos tipos:6
Migraña episódica: con menos de 15 días de cefalea al mes, que representa 90% de los casos.
Migraña crónica: al menos 15 días de cefalea al mes de los que 8 o más cumplan los criterios de migraña con o sin aura, por más de tres meses. Representa 5 a 10%.
Fisiopatología
Existen múltiples factores implicados, como el genético, ambiental, metabólico, hormonal y fármacos exacerbantes, de igual forma, se han corroborado mecanismos que generan alteraciones en los circuitos tálamo-corticales, activación hipotalámica y de tallo cerebral, despolarización cortical, conectividad cerebral y liberación de péptidos moduladores del dolor central (PRGC-péptido relacionado con el gen de la calcitonina, polipéptido activador de la adenilato ciclasa hipofisaria, etc.).7
El PRGC es un neuropéptido de 37 aminoácidos, se halla en fase de estudio desde el decenio de 1990, se expresa en el sistema nervioso central y periférico, forma parte de una familia que incluye a la adrenomedulina, amilina y calcitonina, tiene un papel importante en la neurotransmisión del dolor y en la fisiopatología de la migraña, por lo que se ha convertido en un blanco terapéutico. Está aumentado en la circulación intracraneal en la fase aguda de la migraña y su administración intravenosa ha podido reproducir los síntomas en pacientes migrañosos, mas no en voluntarios sanos.8
El PRGC puede ejercer sus efectos a través de diferentes receptores, que incluyen: receptor del PRGC, receptor de la calcitonina, receptor de amilina y receptor de adrenomedulina, de los que la mayor afinidad es para el receptor del PRGC y al receptor de amilina. En términos funcionales, el receptor del PRGC se compone del receptor tipo calcitonina (RTC o CLR por sus siglas en inglés) y de la proteína 1 modificadora de la actividad del receptor (P1MAR o RAMP1 por sus siglas en inglés), que cuando se unen a la proteína componente del receptor (PCR o RCP por sus siglas en inglés) permiten la activación y transducción de la señal del dolor (Figura 1). De igual forma P1MAR puede unirse al receptor de calcitonina (RCT o CTR por sus siglas en inglés) para crear el receptor de amilina responsivo a PRGC. Otras combinaciones son RCT o RTC con P1MAR con lo que se crean receptores responsivos a los péptidos de la familia del PRGC. Al momento los detalles de la señalización de la vía del PRGC se desconocen; sin embargo, la vía que mejor se ha caracterizado es a través de la adenilato ciclasa, AMP cíclico y activación de la proteína-cinasa A.9
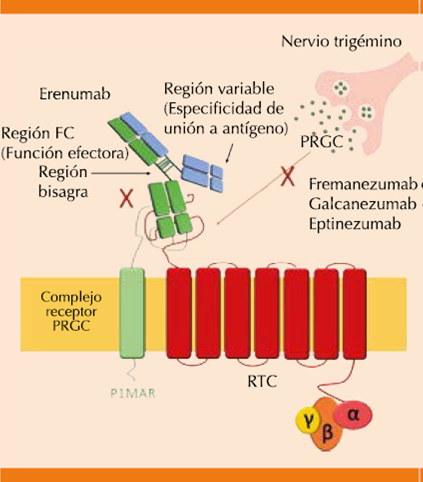
Adaptado de la referencia 9
Figura 1 Complejo del receptor del PRGC, donde se observan las vías de bloqueo con los anticuerpos monoclonales contra el receptor (erenumab) o contra el péptido propiamente (fremanezumab) galcanezumab y eptinezumab).
El sistema del PRGC (péptido y su receptor) se expresa ampliamente en el sistema nervioso central y periférico. En el sistema nervioso central se encuentra en neuronas corticales, hipocampo, cerebelo, tálamo, núcleo hipotalámico y núcleos de tallo cerebral. El PRGC se libera de los nervios trigéminos (expresado en 35 a 50% de las neuronas del ganglio trigémino) y se activan en el contexto de migraña, lo que lleva a vasodilatación no mediada por endotelio, inflamación neurogénica y sensibilización periférica, que conlleva a los procesos determinantes para la transmisión del dolor.10
Se han descrito cuatro fases de la migraña en su expresión clínica, que conviene identificar para efectos de clasificación y tratamiento, las cuales son:1
Fase premonitoria: precede a la cefalea, habitualmente por horas (< 72 horas). Se caracteriza por irritabilidad, fatiga, bostezos, dolor de cuello y fonofobia.
Fase de aura: ocurre en 30% de los pacientes con migraña, precede de forma inmediata (usualmente menos de una hora) o aparece durante la cefalea.
Fase cefalálgica: el episodio de dolor que cumple características clásicas y dura 4 a 72 horas, aunque si dura más de 72 horas habrá que considerarse estado migrañoso.
Fase posdrómica: posterior a la cefalea, usualmente alteraciones sensoriales y dura menos de 24 horas.
Tratamiento
Para el inicio del tratamiento es importante tomar en cuenta las características de la migraña (frecuencia, gravedad y efecto) y del paciente (necesidad, objetivos, comorbilidades, así como acceso a medicamentos y efectos adversos). En general, existen dos tipos de tratamiento: el abortivo (episodios agudos) y el preventivo (profiláctico) para disminuir la frecuencia e intensidad en los casos que se requiera:11
Siempre habrá que advertir de los posibles efectos adversos de los medicamentos y aconsejar al paciente para evitar el abuso de analgésicos.
Tratamiento agudo
Deben tomarse en cuenta los siguientes cuatro principios:11,12
Tratamiento temprano: se refiere que los episodios de dolor son más fácilmente controlados cuando el tratamiento se inicia en la fase de aura o de dolor inicial.
Vía de administración: en caso de vómito como síntoma asociado, los fármacos vía oral no son efectivos, por lo que en esa situación otras vías de administración serán más adecuadas.
Tratamiento coadyuvante: hace referencia a que incluso 60% de los pacientes tienen náusea y vómito, por lo que también son síntomas a tratar.
Rescate: se refiere a tener en cuenta el fármaco de segunda línea a prescribirse en caso de que no haya alivio del cuadro agudo, así como las indicaciones de tratamiento agudo en el contexto extra-hospitalario.
En el Cuadro 1 se enlistan los fármacos y dosis aprobadas para el tratamiento agudo de la migraña en orden de nivel de evidencia.
Cuadro 1 Tratamiento farmacológico en fase aguda de migraña y su nivel de evidencia
| Nivel A | Nivel B | Nivel C | Nivel U |
|---|---|---|---|
|
Analgésicos |
Antieméticos |
Antiepiléptico | AINES |
| Ergotamínicos | Ergotamínicos | Ergotamínico | Otros |
| AINEs | AINEs | AINEs | |
| Opioides | Opioides | ||
| Triptanos | Otros | Esteroides |
Nivel A: efectivo. Nivel B: probablemente efectivo. Nivel C: posiblemente efectivo. Nivel U: inadecuado o datos contradictorios.
En el tratamiento agudo habrá que evitar la administración de AINES y otros analgésicos no específicos por más de 15 días en administración simple o por más de 10 días en administración combinada, debido al riesgo de cefalea por abuso de medicamentos. Los triptanos pueden tener efecto vasoconstrictor, por lo que habrá que revisar sus dosis máximas y tener en cuenta que están contraindicados en: hipertensión arterial no tratada o descontrolada, enfermedad coronaria, enfermedad de Raynaud, antecedente de infarto cerebral, embarazo o lactancia, insuficiencia renal o hepática graves, edad mayor de 65 años, migraña hemipléjica y basilar.13
Tratamiento crónico o preventivo
Cuando se decida la administración de profilaxis es importante considerar su inicio paulatino, comorbilidades, efectos adversos, embarazo, contraindicaciones, expectativas del paciente y mantener el tratamiento al menos dos a seis meses de forma ininterrumpida.14
La profilaxis está indicada ante uno o más de los siguientes: ataques incapacitantes a pesar de tratamiento agudo adecuado, más de cuatro días al mes de migraña o más de ocho al mes de cefalea, sobre administración de fármacos de fase aguda o efecto adverso y otras causas especiales, como migraña hemipléjica, infarto migrañoso, migraña basilar y aura molesta.12,13
Se considera profilaxis exitosa cuando la frecuencia e intensidad de los episodios disminuye al menos 50%. En el Cuadro 2 se enlistan los fármacos con nivel de evidencia A y sus consideraciones.
Cuadro 2 Fármacos profilácticos nivel A
| Fármaco | Dosis efectiva | Efectos adversos | Contraindicaciones |
|---|---|---|---|
| Prooanolol | 80-240mg/d | Fatiga transtornos del sueño, depresión, poca tolerancia a ejercicio, ortostatismo, bracardía, impotencia sexual | Insuficiencia cardiaca , asma, diabetes con administración de insulina |
| Timolol | 10-15mg c/12h | ||
| Metoprolol | 50-200mg/d | ||
| Divalproato sódico | 500-1000 mg/d | Ganancia de peso, caída de cabello , heatotoxicidad, temblor | Mujeres en edad reproductiva |
| Topiamato | 100 mg/d (iniciando a 25g con aumento semanal) | Alteraciones de la conducta o cognitivas, aumento de la presión intraocular, perdida de peso , nefroiatisis , parestesias o estremecimiento de manos y pies | Mujeres en edad reproductiva |
| Toxina botulínica | 155 unidades cada 12 semanas | Dolor en el sitio de aplicación, dolor muscular, debilidad. | Enfermedad muscular o de la unión neuromuscular |
Nuevos tratamientos
Pequeñas moléculas antagonistas del PRGC gepantes
Actúan bloqueando al receptor del PRGC y amilina 1, no son vasoconstrictores, a diferencia de los triptanos y derivados de la ergotamina. Se ha reportado efectividad clínica en el contexto agudo de la migrada de siete moléculas de este grupo: telcagepant, BI44370TA, olcegepant, rimegepant, MK-3207, ubrogepant y atogepant; sin embargo, algunas mostraron hepatotoxicidad (telcagepant y BI44370TA), por lo que sus estudios se suspendieron.15
En un ensayo clínico fase 2B para tratamiento agudo de migraña, con ubrogepant y placebo, en el que se incluyeron 527 pacientes en el brazo de intervención con dosis de 1, 10, 25, 50 y 100 mg, se observó que el fármaco fue superior a placebo a dosis de 25, 50 y 100 mg en la obtención de estado libre de dolor, con efectos adversos similares a los del placebo (principalmente náuseas, mareo, boca seca, somnolencia y fatiga).16
Estudios clínicos de gepantes comparados con triptanos muestran para los gepantes eficacia clínica superior a placebo y similar a la de los triptanos con efectos adversos similares a los del grupo placebo.17
En la actualidad existen dos ensayos clínicos fase III con ubrogepant para el tratamiento agudo, que han terminado de reclutar pacientes, a la vez que atogepant se evalúa en un ensayo clínico fase II/ III para la prevención de la migraña episódica, que también ha completado su fase de reclutamiento de pacientes, por lo que es probable que pronto se publiquen los resultados.18-20
El ubrogepant, rimegepant y el atogepant, que son moléculas disponibles para administración oral, libres de hepatotoxicidad y con efectos adversos similares al placebo, continúan en estudio y resultan prometedores.
Anticuerpos monoclonales contra el receptor/ péptido relacionado con el gen de la calcitonina
Existen cuatro anticuerpos, uno contra el receptor (erenumab) y los otros tres (fremanezumab, galcanezumab y eptinezumab) contra el péptido relacionado con el gen de la calcitonina; hasta octubre de 2018 los ÚNICOS aprobados por la Dirección de Alimentos y Fármacos de Estados Unidos (FDA) eran erenumab, galcanezumab y fremanezumab. Al igual que los gepantes, éstos tienen menores efectos adversos sin efecto vasoconstrictor, este grupo se ha estudiado en el tratamiento preventivo (migraña episódica y crónica), a diferencia de los gepantes que están evaluados en el tratamiento agudo.21
Goadsby y colaboradores reportaron en 2017 los resultados del estudio STRIVE con erenumab en la prevención de migraña episódica, incluyeron 955 pacientes, de los que 317 recibieron 70 mg y 319, 140 mg de erenumab contra 319 en el grupo placebo; la administración fue mensual durante seis meses, la dosis de 140 mg mostró efecto significativo, reduciendo 1.9 días de migraña al mes al compararse con placebo (3.7 días entre el mes 4-6), 50% de los pacientes logró la meta de reducir ≥ 50% los días de migraña al mes, en comparación con 26.6% en el grupo placebo. Los efectos adversos más frecuentes fueron nasofaringitis, infección respiratoria alta, sinusitis, estreñimiento y artralgias.22
Un estudio clínico fase III en el tratamiento preventivo de la migraña crónica con fremanezumab incluyó 1130 pacientes distribuidos en tres grupos: fremanezumab trimestral y mensual vs grupo placebo. Los resultados reportaron disminución de los días de migraña al mes en 4.3 y 4.6 días con la administración trimestral y mensual, respectivamente, lo que representa disminución neta de 2.1 días al compararse con placebo. Con respecto a lograr disminución de 50% de los días de migraña al mes, esto se logró en 38% con la administración trimestral, 41% con la mensual y 28% en el grupo placebo (p < 0.0001). Los efectos adversos más frecuentes se asociaron con el sitio de inyección (dolor, induración y eritema), infección respiratoria alta-nasofaringitis y sólo 1% tuvo alteración de las pruebas de funcionamiento hepático, que se atribuyó a otra causa porque el metabolismo de fremanezumab no es esa vía.23
De igual forma se han reportado resultados positivos en estudios fase III con eptinezumab (PROMISE 1 y 2), así como un ensayo clínico fase 2B y III con galcanezumab (EVOLVE 1 y 2).24,25 En el Cuadro 3 se describen las características hasta ahora disponibles de estos anticuerpos.
Cuadro 3 Anticuerpos monoclonales en migraña
| Fármaco | Disminución días-migraña* (efecto máximo) | Administración | Dosis | Vida media | NNT | Efectos adversos (OR) | FDA |
|---|---|---|---|---|---|---|---|
| Eptinezumab | -1 (semana 5-8) | Trimestral IV | 300 mg | 31 días | 4.7 | 1.09 | - |
| Erenumab | -1.9 (semana 9-12) | Mensual SC | 70 o 140 mg | 21 días | 6.2 | 0.96 | Aprobado |
| Galcanezumab | -1.2 (semana 9-12) | Mensual SC | 240-120 mg | 28 días | 4 | 1.07 | Aprobado |
| Fremanezumab | -2.1 (semana 9-12) | Mensual/trimestral SC | 225/675 mg | 40-48 días | 4 | 1.05 | Aprobado |
* Días de reducción netos al compararse contra placebo.
NNT: número necesario a tratar; OR: razón de momios o probabilidad de un evento; FDA: Dirección de Alimentos y Fármacos de Estados Unidos; IV: intravenoso; SC: subcutáneo; - (guión): separa la dosis inicial de las dosis subsecuentes.
Aunque a la fecha no se han realizado estudios comparativos de estos anticuerpos vs el tratamiento actual preventivo (betabloqueadores o antiepilépticos) los datos sugieren que la eficacia podría ser comparable, lo que aunado a su perfil de seguridad y tolerabilidad, así como su administración mensual los hacen prometedores; sin embargo, su costo limitará su prescripción, por lo que habrá que definir a la población apta. aún está por determinarse lo referente a embarazo, lactancia y riesgo cardiovascular.
Agonista del receptor de serotonina1F ditanos
Los triptanos tienen su efecto farmacológico a través del agonismo del recepto 1B y 1D de serotonina, el receptor 1B tiene efecto vaso-constrictor y el 1D activa periféricamente a las fibras nerviosas además del tallo cerebral. Se ha descubierto que el agonismo del receptor 1F tiene efectos antinociceptivos sin los efectos vasoconstrictores de los triptanos o derivados de ergotamina.26,27
Lasmiditan es el primer fármaco del grupo de los ditanos que tiene como mecanismo el agonismo selectivo del receptor 1F en la vía trigeminal y como prospecto para el tratamiento agudo sin efecto vasoconstrictor asociado. Farkkila y colaboradores reportaron los resultados de un ensayo clínico fase II que incluyó 512 pacientes que se distribuyeron al azar para recibir dosis de 50, 100, 200 y 400 mg de lasmitidan o placebo. Se evaluó el alivio del dolor a las dos horas posdosis y se documentó alivio en 17.9, 38.2, 28.8 y 38.7% a las dosis comentadas, respectivamente; sin embargo, hubo también frecuencia alta de efectos adversos, como mareo, parestesias, náusea y vómito.28 Posteriormente se reportaron de forma preliminar dos ensayos clínicos fase III (SAMURAI y SPARTAN) donde se eligieron pacientes con tres a ocho ataques de migraña al mes con discapacidad moderada a grave, que recibieron dosis de 100 y 200 mg en SAMURAI y 50, 100 y 200 mg en SPARTAN, durante las primeras cuatro horas del episodio de migraña. A dos horas de la administración de la dosis de 200 mg 32.2% de los pacientes en SAMURAI y 38.8% en SPARTAN vs 15.3% en SAMURAI y 21.3% en SPARTAN con administración de placebo estuvieron libres de cefalea, lo que fue estadísticamente significativo, aunado a esto, los síntomas asociados, como náuseas, foto y fonofobia también disminuyeron y los efectos adversos más frecuentes (> 2%) fueron: mareo, parestesias, somnolencia, fatiga, náuseas y letargo.29,30 aún no lo ha aprobado la FDA; sin embargo, se planeaba su sometimiento para 2018.
Antagonistas de la orexina rexants
La orexina A y B son péptidos con participación nociceptiva, actúan mediante receptores OX1R (A) y OX2R (B). Chabi y colaboradores realizaron un estudio con filorexant (antagonista dual de los receptores de orexina), obtuvieron tendencia positiva; sin embargo, sin significación estadística y con mayor proporción de efectos adversos, principalmente somnolencia.31 Estudios posteriores reportaron que probablemente el receptor A sea antinociceptivo y el B pronociceptivo, por lo que los efectos de filorexant pudieron equilibrarse.
Inhibidores de óxido nítrico sintetasa
El óxido nítrico favorece la liberación del péptido relacionado con el gen de la calcitonina, por lo que la inhibición de éste mediante la inhibición de su sintetasa podría evitar la migraña, desgraciadamente los estudios en episodio agudo y en prevención no han mostrado efectividad.32,33
CONCLUSIONES
Existe alta proporción de pacientes aptos para recibir tratamiento profiláctico; sin embargo, pocos lo reciben debido a múltiples factores, como falta de prescripción por parte del médico, la cronicidad y forma de posología, así como a los efectos adversos. Existen nuevos tratamientos prometedores, como los gepantes y los ditanos (lasmiditan) en el tratamiento agudo y los anticuerpos monoclonales dirigidos al PRGC en la profilaxis, de los que debemos tener conocimiento previo a su incorporación en el mercado. Aunque a la fecha no se han publicado estudios comparativos con los tratamientos actualmente disponibles, los datos sugieren que la eficacia clínica podría ser similar; sin embargo, la ventaja de los anticuerpos residiría en la facilidad de su administración (mensual o trimestral), la menor proporción de efectos adversos y la ausencia de efecto vasoconstrictor, con la desventaja de los costos económicos, por lo que habrá que valorar cuidadosamente a los posibles pacientes susceptibles de recibir estas terapias.











 nueva página del texto (beta)
nueva página del texto (beta)


