Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Salud mental
versión impresa ISSN 0185-3325
Salud Ment vol.36 no.3 México may./jun. 2013
Artículo original
Nuevas vacunas contra la morfina/heroína
Novel Vaccines against morphine/heroin
Alberto Salazar-Juárez,1 Susana Barbosa Méndez,1 Martha Ivone Feregrino Alonso,1 Ricardo Hernández Miramontes,1 Elisabet Ramos Ochoa,1 Edgar Bonilla Reyes,1 Salomón Jacinto Gutiérrez,1 Paul Pentel,2 Benito Antón1
1 Laboratorio de Neurobiología Molecular y Neuroquímica de las Adicciones. Subdirección de Investigaciones Clínicas. Instituto Nacional de Psiquiatría Ramón de la Fuente Muñiz.
2 Minneapolis Medical Research Foundation, University of Minnesota.
Correspondencia: Dr. Benito Antón Palma.
Laboratorio de Neurobiología Molecular y Neuroquímica de las Adicciones.
Subdirección de Investigaciones Clínicas. Instituto Nacional de Psiquiatría Ramón de la Fuente Muñiz.
Calz. México-Xochimilco 1 01, Col. San Lorenzo Huipulco, Tlalpan, 1 4370 México DF.
Tel. (52-55) 4160-5093. Fax. (52-55) 5513-3722. E-mail: bapags@gmail.com
ABSTRACT
Drug addiction is one of the most important health problems in the world. This psychiatry disease results in the death of about 500 000 individuals annually in the world. Despite this scenario, the development of effective drug therapies against this disease has been slow and not very successful. In recent years, new alternative pharmacological strategies against drug addiction have been designed and validated. Among them are vaccines against drugs like nicotine, morphine or cocaine and their subsequent use in immunotherapeutic pharmacological procedures for the treatment of addictive behaviors of drug consumption, both in animal models and in humans.
These strategies are based on the experimental design and synthesis of various structural formulations of therapeutic vaccines against drugs of abuse. When dosed in active immunization schedules, they induce the production of specific antibodies, which recognize and bind these substances in the intravascular space and prevent the drug permeability through the blood brain barrier, resulting in decreased effects of drugs into the brain.
In 2006, our research group at the National Institute of Psychiatry Ramón de la Fuente Muñiz (INPRFM) achieved and consolidated the design, synthesis, application and validation of immunoprotective therapeutic effects against relapse to morphine/heroin addiction in a rodent animal model, a model vaccine for potential human use against addiction to morphine/heroin. This model shows immunogenic capacities (high and sustained titers of highly specific antibodies) and immunoprotection (attenuates the effect up to 15mg/kg sc morphine) that the structural vaccine models competing have not been matched, which makes it the leading vaccine model against the addictive effects of heroin and morphine.
Key words: Addiction, morphine/heroin, vaccines, immunotherapy, active and passive immunization.
RESUMEN
La adicción a una droga de abuso representa uno de los problemas sanitarios más importantes ya que esta patología genera la muerte de cerca de 500 000 sujetos anualmente en el mundo. A pesar de este panorama, el desarrollo de terapias farmacológicas efectivas contra esta enfermedad es lento y poco exitoso. En los últimos años se han diseñado y validado nuevas estrategias farmacológicas alternativas contra la adicción a drogas de abuso, como las vacunas y su uso en procedimientos farmacológicos inmunoterapéuticos para el tratamiento de esas conductas tanto en modelos de animales como en el humano.
Estas nuevas estrategias experimentales están basadas en el diseño y síntesis de diversas formulaciones estructurales de vacunas terapéuticas contra las sustancias de abuso las cuales, al ser dosificadas en esquemas de inmunización activa, inducen la producción de anticuerpos séricos específicos que reconocen y se unen a estas sustancias en el espacio intravascular sistémico e impiden que crucen la barrera hematoencefálica, con lo cual disminuyen sus efectos en el cerebro.
En el año 2006 nuestro grupo de trabajo en el Instituto Nacional de Psiquiatría Ramón de la Fuente Muñiz (INPRFM) logró y consolidó el diseño, síntesis, aplicación y validación de efectos terapéuticos inmunoprotectores contra recaídas al consumo adictivo de morfina/heroína, en un modelo animal con roedores y su escalamiento potencial para uso humano contra la adicción a esas sustancias. Este modelo muestra capacidades inmunogénicas (títulos altos y sostenidos de anticuerpos altamente específicos) y de inmunoprotección (atenúa el efecto de hasta 15mg/Kg sc de morfina) que los modelos estructurales de vacuna desarrollados por otros grupos de investigadores no han podido igualar. Esto lo convierte en un modelo líder de vacuna contra los efectos adictivos de la heroína y morfina.
Palabras clave: Adicciones, morfina/heroína, vacunas, inmunoterapéutica, inmunización activa y pasiva.
INTRODUCCIÓN
La adicción a una droga de abuso representa uno de los problemas médicos más importantes en el mundo. La adicción a la nicotina y al alcohol, por ejemplo, genera en la población mundial la muerte de cerca de 440 000 y 80 000 sujetos al año, respectivamente. En los Estados Unidos el abuso y la adicción a drogas ilícitas generan a la sociedad un costo de cerca de $180.9 billones* de dólares por año, sin mencionar las complicaciones sociales y familiares que están relacionadas a este problema.
A pesar de este difícil panorama y de que cada día los sujetos dependientes tienen más acceso y consumen múltiples drogas de abuso fácilmente, el desarrollo de terapias farmacológicas efectivas contra esta enfermedad no ha producido los resultados esperados. A lo largo de las tres últimas décadas, diversos centros de investigación y empresas farmacéuticas a nivel mundial han sintetizado y validado una amplia variedad de fármacos encaminados a desintoxicar, disminuir los síntomas afectivos observados durante la abstinencia, reducir la apetencia o craving y/o a prevenir las recaídas del consumo adictivo en sujetos adictos a opiáceos y psicoestimulantes.1
Sin embargo, a pesar de que la oficina estadunidense para el control de medicamentos y alimentos o FDA (Food and Drug Administration) ha certificado el uso de una gran variedad de estos fármacos, su efecto en tratamientos clínicos anti-adictivos no ha sido exitoso. El procedimiento terapéutico inicial en el tratamiento de un sujeto dependiente o adicto a cualquier droga de abuso es el empleo de tratamientos de desintoxicación aguda, encaminados principalmente a reducir y/o bloquear los signos y síntomas de la abstinencia. El uso de estos tratamientos es fácil y de bajo costo, sin embargo a la fecha actual no existe una evidencia sólida de resultados eficaces a largo plazo en el mantenimiento de la abstinencia en los sujetos sometidos a tratamientos de desintoxicación.
Es probable que el fracaso de estos tratamientos de desintoxicación en mantener la abstinencia por largos periodos de tiempo se deba a la imposibilidad de revertir y/o modular las alteraciones neuroplásticas que el consumo crónico generó sobre los diferentes sistemas de neurotransmisión y vías de reforzamiento placentero.1-3 Adicionalmente, la gran mayoría de estas terapéuticas producen importantes efectos colaterales tóxicos a mediano y largo plazo, lo cual podría explicar el poco apego que el sujeto adicto muestra a estos tratamientos.1
En la actualidad se tiene el concepto de que los tratamientos farmacológicos que buscan reducir los síntomas de abstinencia y el craving durante una adicción crónica, y finalmente mantener un estado de abstinencia por largos periodos de tiempo, requieren de periodos de tratamiento a muy largo plazo (vg., de meses a años)y que por lo general son mayores a los utilizados en la desintoxicación.4,5 Además deben ser aplicados en combinación con psicoterapia, terapias de apoyo, de expresión y de desarrollo motivacional, así como terapias cognitivo-conductuales, entre otras, para así prolongar el periodo de abstinencia y prevenir al máximo las recaídas al consumo a largo plazo.6
En la actualidad se conocen mejor los cambios neuroadaptativos del cerebro que a nivel celular y molecular inducen las drogas adictivas. Así también se ha definido con mayor precisión el papel central que tiene el sistema dopaminérgico como mediador de las respuestas de recompensa. Esto les ha permitido a diversos laboratorios desarrollar nuevas estrategias farmacológicas centradas en el bloqueo de los efectos farmacodinámicos cerebrales de las drogas de abuso.
En la última década, el Instituto Nacional de los Estados Unidos para las Adicciones (NIDA) ha estado involucrado en el desarrollo de programas internacionales relacionados con el diseño de nuevos medicamentos para controlar y contrarrestar la adicción a psicoestimulantes y opioides en sujetos adictos.1,7,8 Actualmente existe un gran número de fármacos en proceso de ser aprobados por la FDA para el tratamiento de la adicción a estas drogas de abuso. Sin embargo, todas estas sustancias de la farmacopea, en conjunto, han demostrado tener una pobre capacidad terapéutica, tanto a corto como a largo plazo, en el proceso anti-adictivo.7,8
En resumen, en la actualidad, desde el punto de vista terapéutico, la mayoría de los tratamientos farmacológicos clásicos anti-adictivos contra la adicción a diversas drogas, como la cocaína o la morfina, no han mostrado eficacia significativa. La mayoría de estos fármacos presentan importantes efectos tóxicos colaterales, por lo que la mayoría de los sujetos en tratamiento abandonan tempranamente su dosificación.7,8 Por estas desventajas se han diseñado estrategias alternativas. Un ejemplo notable de estas nuevas estrategias son las vacunas y su uso en procedimientos farmacológicos inmunoterapéuticos para el tratamiento de conductas de consumo adictivo, tanto en modelos animales como en el humano.9
INMUNOFARMACOTERAPIAS
Estas nuevas estrategias experimentales están basadas en el diseño y síntesis de diversas formulaciones estructurales de vacunas terapéuticas contra la adicción a cocaína,10-13 nicotina14-16 y heroína/morfina,17-20 las cuales, al ser dosificadas en esquemas de inmunización activa en modelos animales como el roedor o en el humano, inducen la producción de anticuerpos séricos específicos que reconocen y se unen a estas sustancias en el espacio intravascular sistémico. Estos anticuerpos anti-droga poseen la capacidad de secuestrar al compuesto adictivo circulante en el torrente sanguíneo ya que los anticuerpos son macromoléculas (≈150 kD) que normalmente no permean la barrera hematoencefálica, formando así complejos moleculares anticuerpo-droga de alto peso molecular, que "secuestran" e impiden el paso de la droga a través de la barrera hematoencefálica.21,22 Así, por lo tanto, en esta condición de alteración farmacocinética de la droga, existe una disminución muy significativa de la fracción de "droga libre" plasmática que se difunde al espacio extracelular del tejido nervioso cerebral y, por ende, que estaría disponible para la unión y/o bloqueo funcional de los mecanismos moleculares a través de los cuales llevan a cabo su efecto (aumento en la liberación de dopamina).21,22 Así, al reducirse la concentración sináptica de este neurotransmisor por el consumo de la droga ya no se desarrollará el reforzamiento placentero de re-consumo con patrón adictivo en el sujeto vacunado activamente e inmune a la misma sustancia.21,22 Como resultado de esta alteración significativa de "antagonismo farmacológico de permeación hematoencefálica de la droga", el valor reforzante placentero que ésta induce disminuye notablemente, lo cual reduce el porcentaje de recaídas al consumo21,22 (figura 1).
Esta estrategia farmacológica experimental de naturaleza "inmunoprotectora" ha demostrado ser un tratamiento con eficacia terapéutica para atenuar significativamente y/o inhibir las conductas de búsqueda y consumo adictivo a la cocaína, la nicotina y la morfina/heroína, tanto al nivel pre-clínico en el roedor23-32 como en el humano.33,34
Además es importante resaltar que dada la naturaleza del mecanismo farmacocinético antes descrito, relacionado con los efectos de la droga, al disminuirse significativamente la permeación de la droga hacia el tejido cerebral se bloquean los efectos reforzadores que induce la droga a nivel central, y además no se producen los efectos secundarios tóxicos colaterales generados a menudo con los fármacos clásicos empleados comúnmente contra los procesos de adicción.33-36
Las inmunoterapias diseñadas (tanto al nivel pre-clínico como clínico) que han sido evaluadas actualmente contra la adicción pueden dividirse en forma general, en términos de los paradigmas en que están basados, en procesos de "vacunación activa" (los de mayor índice de estudios reportados) y, adicionalmente, algunos otros de menor frecuencia de aplicación y uso, centrados en la "vacunación pasiva".
La vacunación activa es el método tradicional de inmunización contra diferentes enfermedades. En este caso por medio de la administración de formulaciones de agentes infecciosos (v.g., virus, bacterias, parásitos), químicamente atenuados en su virulencia o inclusive muertos o mecánicamente fragmentados. Confieren defensa humoral y/o celular, con memoria a largo plazo. Este procedimiento genera anticuerpos con una enorme capacidad de reconocimiento amplio y específico a antígenos o determinantes antigénicos específicos que invaden el organismo.21,35-37 Sin embargo, el sistema inmune también muestra la capacidad de "no reconocimiento antígénico" a numerosas moléculas de baja masa (v.g., < 100-300 daltones) y complejidad estructural, denominadas haptenos, que por sí mismas no tienen la capacidad de generar una respuesta de activación (inmunogenicidad) de la respuesta inmune humoral (anticuerpos específicos) eficiente. En este contexto, las drogas de abuso adictivo pueden ser incluidas dentro de este grupo de compuestos químicos dado que su masa molecular nominal es de alrededor de 300 daltones y de escasa complejidad molecular.21,35,36 Una de las ventajas de la inmunización activa por medio de la dosificación de una vacuna o preparación inmunogénica es que la vida media de los anticuerpos generados es de larga duración (usualmente entre 30 y 90 días), permitiendo que el efecto inmunoprotector mediado por los anticuerpos específicos circulantes se extienda también por largos periodos de tiempo (usualmente entre 2 y 6 meses).21,22,35,36 Otra ventaja es que las propiedades farmacocinéticas de la droga (como su metabolismo y depuración plasmática) no se alteran por los procedimientos de la inmunización activa contra la misma droga.21,22,35,36
Para lograr que el sistema inmune sea capaz de reconocer eficientemente como moléculas extrañas (antígenos) a haptenos como la cocaína o la morfina, se requiere de condensarla covalentemente a sistemas acarreadores proteicos de alta masa y complejidad estructural (conjugado-droga-proteína acarreadora=vacuna), los cuales tienen la capacidad de presentar estructuralmente a la droga como una molécula antigénica o "extraña" al sistema inmune, y que éste genere una intensa respuesta de inmunoglobulinas circulantes específicas contra la droga.21,22,35,36 El grado de eficacia farmacológica de una formulación de conjugado molecular (vacuna) de droga adictiva-proteína acarreadora para estimular su correspondiente respuesta inmune humoral se denomina "capacidad inmunogénica" de la vacuna.21,22,35,36
Es importante mencionar que a pesar de que a la fecha se han reportado diversos trabajos científicos que han demostrado que la vacunación activa es un procedimiento experimental eficaz, con capacidad de generar concentraciones elevadas de anticuerpos séricos específicos contra drogas adictivas como la morfina/heroína,17,18,38 la nicotina39,40 y la cocaína,23-28 a nivel clínico los resultados no han sido muy alentadores. Ahora se sabe que el éxito de esta estrategia inmunoterapéutica se basa principalmente en tres parámetros: la magnitud de la concentración de anticuerpos, denominada título; la afinidad y especificidad de los anticuerpos hacia una cierta estructura molecular (hapteno) y la capacidad de generar anticuerpos específicos a la droga de manera constitutiva (sostenimiento del título a largo plazo). Es importante mencionar que la presencia de estos tres parámetros depende exclusivamente de los elementos que conforman al modelo estructural del inmunoconjugado.
La magnitud de la respuesta inmunogénica, medida como concentración de anticuerpos, es el resultado del tipo de proteína acarreadora usada, a la cual se une el hapteno, así como al tipo de adyuvante usado en la formulación antigénica final.13,35-37,41,42 Otra característica muy importante que le concede el tipo de proteína acarreadora usada es la capacidad de estimular receptores del tipo TOLL, lo cual le van a permitir la activación de células B que producen anticuerpos específicos para la droga a largo plazo (memoria). Por otro lado, la afinidad y especificidad de los anticuerpos a un hapteno están directamente relacionados a una presentación inmunogénica exitosa, la cual es el resultado de un buen diseño molecular de conjugado inmunogénico (diseño: hapteno-largo y tipo del brazo espaciador-sitio de unión del hapteno a la proteína acarreadora).
VACUNAS CONTRA MORFINA/HEROÍNA
Los reportes de inmunoterapias para la adicción a opioides son escasos. Muchos de ellos usan protocolos de vacunación con diferentes modelos estructurales empleando diferentes tipos de reacciones para la obtención del hapteno, acoplando al hapteno en diferentes posiciones de la molécula. Si bien la mayoría usan básicamente a la morfina para la generación del hapteno, éste es acoplado covalentemente a diferentes proteínas acarreadoras inmunogénicas43-47 lo cual, en conjunto, dificulta el análisis de los efectos de los mismos.
Las primeras aproximaciones experimentales se realizaron desde hace 42 años y estuvieron enfocadas principalmente a la generación de anticuerpos policlonales contra la morfina (cuadro 1). Sin embargo, en ninguno de estos reportes se evaluó la cantidad de anticuerpo generado por el procedimiento de vacunación, ni el antagonismo farmacológico basado en anticuerpos encaminado a atenuar los efectos conductuales de las drogas opioides. No obstante, proporcionaron la suficiente información para el desarrollo de nuevos conjugados inmunogénicos encaminados a atenuar el efecto de diferentes dosis de morfina, heroína y sus metabolitos.
En conjunto, sus datos sugieren que si la reacción une el hapteno a la posición 3' de la morfina, lo que se produce es una respuesta inmune capaz de unir preferentemente moléculas estructuralmente relacionadas como la codeína. En cambio si se une el hapteno a la posición 6' los anticuerpos muestran una especificidad equivalente tanto para la heroína como para la morfina o la codeína. Finalmente, si se une el hapteno a la posición 2' de la morfina se genera la respuesta inmune con mayor especificidad a la morfina.17-20
En el año 2006 nuestro grupo de trabajo, encabezado por el doctor Benito Antón, logró en el INPRFM el diseño y la síntesis de un modelo de vacuna, para potencial uso humano, contra la adicción a la morfina/heroína.17,18 El objetivo inicial fue lograr que su mecanismo fuera válido y aplicable para producir efectos terapéuticos inmunoprotectores contra recaídas al consumo adictivo de morfina/heroína en un modelo animal con roedores (fase pre-clínica). Una de las grandes ventajas de este modelo estructural de vacuna bivalente morfina/heroína (M-TT) es que los elementos que la conforman están certificados por la FDA para uso humano, lo cual le permite ser usada rápidamente en protocolos clínicos. La proteína acarreadora que se utiliza es el toxoide tetánico que es una proteína de alta masa y complejidad estructural, lo que le confiere la capacidad de ser una proteína muy antigénica. Esta proteína acarreadora es una de las más usadas en protocolos de vacunación activa en humanos para prevenir la enfermedad del tétanos con mínimos efectos tóxicos secundarios. Al ser el toxoide tetánico una proteína muy antigénica le confiere al modelo de vacuna M-TT la capacidad de estimular fuertemente al sistema inmune, generando una gran cantidad de anticuerpos (títulos de anticuerpos muy altos). Otra característica muy importante es que le confiere la complejidad estructural requerida para estimular receptores del tipo TOLL; esto ocurre gracias a que la proteína acarreadora, al ser una molécula de enorme masa molecular compuesta de un patrón estructural de subunidades polipeptídicas de multi-repetición, permite estimular a estos receptores, los cuales inducen la liberación de citocinas de los linfocitos T, que a su vez estimulan y activan a células B, productoras de anticuerpos específicos para la droga a largo plazo (memoria). Estos anticuerpos tienen la característica de que no disminuyen significativamente con el tiempo, lo que constituye una característica única en el área de generación de vacunas adictivas. El hapteno de la vacuna M-TT es la morfina-6-henisuccinato. Este hapteno se acopla a la proteína acarreadora en la posición 6' de la molécula de la morfina, la cual, como se había reportado previamente, genera anticuerpos con una especificidad equivalente tanto para la heroína como para la morfina.
Nuestro grupo ha publicado varios trabajos que muestran que un programa de vacunación en la rata y el ratón genera una respuesta humoral intensa. En estos ensayos pre-clínicos la vacuna M-TT fue dosificada entre 50-200 µg/Kg, y se usó hidróxido de aluminio como adyuvante. Los títulos máximos, generados por este procedimiento, fueron de 1:250000, produciendo 0.8 ± 0.2 mg/ ml de inmunoglobuli-nas específicas, en suero, después de la cuarta inmunización. Adicionalmente, el título de anticuerpo se mantuvo prácticamente inalterado por un periodo de aproximadamente de seis a ocho meses. Posteriormente hay un progresivo decaimiento de los anticuerpos anti-morfina/heroína, llegando a niveles no detectables de 10 a 12 meses después de su última inmunización. Esto sugiere que la vacuna M-TT no sólo es efectiva en generar grandes cantidades de anticuerpos sino también es capaz de activar a largo plazo la memoria inmunológica humoral contra estos opioides17,18,48 (figura 2).
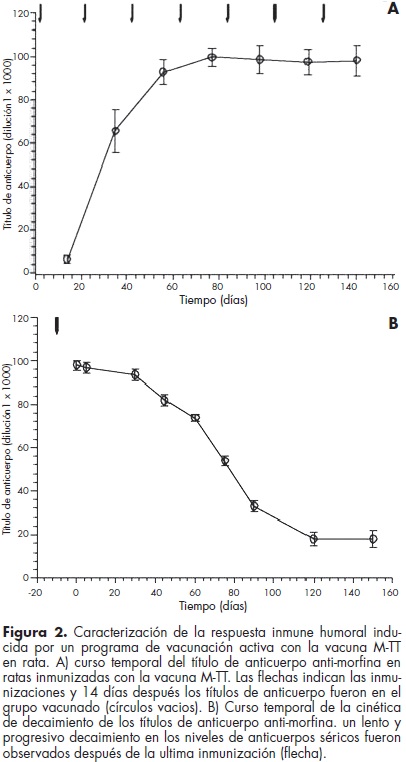
Recientemente Li et al., Raleigh et al. y Stowe et al. reportaron el desarrollo de nuevos modelos de vacuna contra la morfina/heroína,19,20,49,50 la KLH-morfina, la M-KLH y la Vacuna dinámica, respectivamente. La inmunización con estos nuevos modelos de vacuna generó títulos de anticuerpos de 1:100000 para la KLH-Morfina, 1:100000 para la M-KLH y de 1:160000 para la morfina y de 1:120000 para la heroína, en el caso de la Vacuna dinámica, después de la cuarta inmunización, respectivamente.
Para la vacuna KLH-Morfina, el título de anticuerpo disminuye rápidamente después de la última inmunización. Entre los 8 a 10 días después de la última inmunización los títulos de anticuerpo son indetectables. En el caso de la M-KLH y la vacuna dinámica, los títulos para ambas fueron de 1:50000 a los 21 días después de la última inmunización.17,18,49,50
Como se había mencionado anteriormente, la magnitud de la respuesta inmunogénica es el resultado del tipo de proteína acarreadora utilizada así como del tipo de adyuvante usado en la formulación antigénica final. Si tomamos en cuenta la proteína acarreadora usada por cada tipo de vacuna, entonces la vacuna KLH-Morfina, la M-KLH y la dinámica deberían generar títulos de anticuerpos superiores a la vacuna M-TT ya que usan como proteína acarreadora a moléculas de KLH (hemocianina de molusco marino), las cuales son proteínas con una masa y complejidad estructural significativamente mayor. Sin embargo, a pesar de esa diferencia notable en el tamaño y complejidad de la proteína acarreadora, los títulos son similares entre los tres modelos de vacunas (cuadro 2). Esto, a pesar de que las vacunas KLH-Morfina y M-KLH fueron administradas utilizando el adyuvante de Freund's19,20,49,50 que es un potente potenciador de la respuesta inmune. Es importante mencionar que una propiedad que diferencia notablemente a la vacuna M-TT de las otras es la capacidad de generar títulos de anticuerpo de manera persistente. En el caso de los modelos evaluados por Li et al., Raleigh et al. y Stowe et al., los títulos disminuyeron significativamente entre los 10 a 20 días después de la última inmunización, a diferencia de los 6 a 8 meses que tardan los títulos en disminuir en animales inmunizados con la vacuna M-TT.19,20,49,50 Esta respuesta inmunológica diferencia notablemente a la vacuna M-TT de los demás modelos de vacuna.
Como se había mencionado anteriormente, una propiedad muy importante que debe cumplir un nuevo modelo de vacuna es la capacidad de generar anticuerpos altamente específicos a la droga, lo cual depende del hapteno y de la adecuada presentación inmunogénica del mismo. En la vacuna M-TT a la proteína acarreadora se le acopló el hapteno y la morfina-6-hemisuccinato en la posición 6' de la molécula de la morfina. Esto permite que los anticuerpos que genera sean altamente específicos para la morfina y la heroína, con una indetectable reacción cruzada con otros componentes como la codeína, la hidromorfona, la hidrocodona y la oxicodona. Esto le confiere que muestren una nula especificidad de reconocimiento a análogos sintéticos de la morfina como la metadona, la buprenorfina, la nalorfina, la naloxona y la naltrexona. Otra característica muy importante de los anticuerpos generados por esta vacuna es que muestran una especificidad equivalente no sólo para la morfina/heroína sino también para sus metabolitos, los cuales son 10 veces más bioactivos que ambas drogas.17,18 Una diferencia muy importante entre la vacuna M-TT y las vacunas KLH-Morfina y dinámica es que los anticuerpos generados por estas últimas no fueron evaluados en su especificidad contra los metabolitos de la morfina, lo cual podría limitar su uso.19,20,49,50
Los cuatro modelos de vacuna comparten el sitio en el cual se acopla el hapteno a la proteína acarreadora (posición 6' de la molécula de la morfina), la diferencia entre ellos radica en el hapteno y en el largo del brazo espaciador que une al hapteno a la proteína acarreadora. En el caso de la vacuna KLH-Morfina, los anticuerpos comparten la especificidad a la morfina, heroína y moléculas relacionadas a ellas como lo muestran los anticuerpos generados por la vacuna M-TT. Aunque el hapteno es diferente, ambas vacunas comparten un brazo espaciador de longitud similar. En cambio la vacuna dinámica comparte el mismo hapteno pero el brazo espaciador es mucho más corto, lo cual reduce la especificidad de los anticuerpos a la morfina y a la heroína. Por otro lado, dado que los anticuerpos generados por la vacuna M-TT carecen de especificidad para los agentes opioides farmacológicos-terapéuticos, como la naltrexona, la metadona y la buprenorfina, su aplicación podría coadyuvar a las terapias de mantenimiento de abstinencia.17,18
A nivel de inmunoprotección contra las conductas adictivas inducidas por morfina/heroína, en 1974 Bonese et al., realizaron el primer estudio para evaluar la capacidad de inmunoprotección del conjugado inmunogénico (BSA- morfina-6-hemisuccinil [M-6-H]) en el modelo animal del primate (Macacus Rhesus), previamente entrenado para auto-administrarse por vía intravenosa, tanto heroína como cocaína. Estos autores demostraron que la inmunización activa con la preparación inmunogénica BSA-M-6-H era capaz de generar anticuerpos específicos anti-morfina/heroína capaces de bloquear y extinguir la conducta de auto-administración de heroína pero no de cocaína en el primate.38 Posteriormente, Antón y Leff, en el 2006, reportaron que los títulos de anticuerpos específicos contra la morfina y la heroína generados por la M-TT (1:250000) eran suficientes para bloquear el restablecimiento de la conducta de búsqueda y consumo de heroína (0.06 mg/Kg) y morfina (0.6 mg/Kg) en un modelo de auto-administración en la rata (figura 3). Stowe et al., en el 2011, reportaron con la vacuna dinámica títulos de anticuerpos de 1:160000 para la morfina y de 1:120000 para la heroína, capaces de atenuar la adquisición de la autoadministración de heroína (0.06 mg/Kg); a su vez, Li et al. (2011) reportaron que la vacuna morfina-KLH generaba títulos de anticuerpos de 1:100000, capaces de prevenir el restablecimiento de la conducta de búsqueda de la heroína (0.5 mg/Kg) en un modelo de auto-administración.17-20,49,50
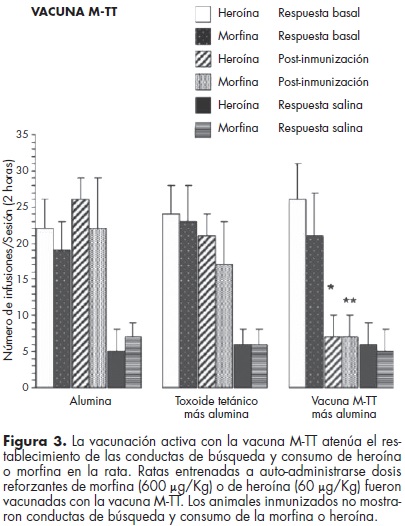
Li et al. (2011) reportaron el uso de dosis de morfina más altas que las dosis que se utilizan en protocolos de autoadministración para inducir reforzamiento o euforia. Estos autores reportaron que los títulos de anticuerpos generados por la vacuna morfina-KLH eran capaces de disminuir la actividad locomotora inducida por 10mg/Kg sc de morfina. A su vez, Stowe et al. (2011) y Raleigh et al. (2013) reportaron que la vacuna M-KLH y la vacuna dinámica eran capaces de bloquear el efecto antinociceptivo de 1 mg/Kg sc de heroína.19,20,49,50
Nuestro grupo de trabajo reportó recientemente que los anticuerpos generados por la M-TT (1:250000) fueron suficientes para atenuar, durante 60 minutos, el efecto antinociceptivo de 1 y 3mg/Kg de morfina administrados intraperitonealmente y de hasta 15mg/Kg de morfina cuando la droga era administrada subcutáneamente, en el modelo de tail-flick.48
CONCLUSIONES
Es indudable que el campo del desarrollo de las vacunas antiadictivas es una opción potencialmente eficaz para el control de este grave problema de salud mundial. Los esfuerzos de diversos grupos de investigación muestran la necesidad de buscar nuevas y mejores alternativas de tratamiento para el reto complejo que representan las adicciones.
Los datos expuestos en este trabajo sugieren que el modelo estructural de vacuna bivalente contra la morfina y la heroína muestra capacidades inmunogénicas (altos y sostenidos títulos de anticuerpos altamente específicos) y de inmunoprotección (atenúa el efecto de hasta 15mg/Kg sc de morfina) que los modelos estructurales de vacuna competidoras no han podido igualar, lo cual lo convierte en el modelo líder de vacuna contra los efectos adictivos de la heroína y la morfina. Sin embargo, aún queda mucho por avanzar. Nuestros resultados requerirán someterse a pruebas toxicológicas, y una vez superadas, a las primeras pruebas en humanos.
AGRADECIMIENTOS
Esta investigación fue apoyada por los proyectos: Fundación Gonzalo Río Arronte, INP-2040, SEP-CONACYT 2009-I0003-106549, NIDA-1R01DA030715-01 e ICyT PINV11-26.
REFERENCIAS
1. O'Brien CP. Anticraving medications for relapse prevention: a possible new class of psychoactive medications. Am J Psychiatry 2005;162:1423-31. [ Links ]
2. Lawental E. Ultra rapid opiate detoxification as compared to a 30-day inpatient detoxification program — a retrospective follow-up study. J Subst Abuse 2000;11:173-181. [ Links ]
3. Gerra G, Zaimovic A, Giusti F, Di Gennaro C et al. Lofexidine versus clonidine in rapid opiate detoxification. J Subst Abuse Treat 2001;21:11-17. [ Links ]
4. McLellan AT, Lewis DC, O'Brien CP, Kleber HD. Drug dependence, a chronic medical illness: implications for treatment, insurance, and outcomes evaluation. JAMA 2000;284:1689-1695. [ Links ]
5. Volpicelli JR, Pettinati HM, McLellan AT, O'Brien CP (eds). Combining medication and psychosocial treatments for addiction—the brenda approach. New York: Guilford; 2001. [ Links ]
6. Karno MP, Longabaugh R. An examination of how therapist directive-ness interacts with patient anger and reactance to predict alcohol use. J Stud Alcohol 2005;66:825-832. [ Links ]
7. Vocci FJ, Elkashef A. Pharmacotherapy and other treatments for cocaine abuse and dependence. Curr Opin Psychiatry 2005;18:265-270. [ Links ]
8. Vocci FJ, Acri J, Elkashef A. Medication development for addictive disorders: the state of the science. Am J Psychiatry 2005;162:1432-1440. [ Links ]
9. Montoya ID, Vocci F. Novel medications to treat addictive disorders. Curr Psychiatry Rep 2008; 10:392-398. [ Links ]
10. Shen X, Kosten TR. Immunotherapy for drug abuse. CNS Neurol Disord Drug Targets. 2011;10:876-879. [ Links ]
11. Shorter D, Kosten TR. Novel pharmacotherapeutic treatments for cocaine addiction. BMC Med 2011;9:119. [ Links ]
12. Kinsey BM, Kosten TR, Orson FM. Anti-cocaine vaccine development. Expert Rev Vaccines 2010;9:1109-1114. [ Links ]
13. Kinsey BM, Kosten TR, Orson FM. Active immunotherapy for the Treatment of Cocaine Dependence. Drugs Future 2010;35:301-306. [ Links ]
14. Raupach T, Hoogsteder PH, Onno van Schayck CP. Nicotine vaccines to assist with smoking cessation: current status of research. Drugs 2012;72:e1-e16. [ Links ]
15. Kitchens CM, Foster SL. Nicotine conjugate vaccines: A novel approach in smoking cessation. J Am Pharm Assoc 2012;52:116-118. [ Links ]
16. Fahim RE, Kessler PD, Fuller SA, Kalnik MW. Nicotine vaccines. CNS Neurol Disord Drug Targets 2011;10:905-915. [ Links ]
17. Anton B, Leff P. A novel bivalent morphine/heroin vaccine that prevents relapse to heroin addiction in rodents. Vaccine 2006;24:3232-3240. [ Links ]
18. Anton B, Salazar A, Flores A, Matus M et al. Vaccines against morphine/heroin and its use as effective medication for preventing relapse to opiate addictive behaviors. Hum Vaccine 2009;5:214-229. [ Links ]
19. Stowe GN, Schlosburg JE, Vendruscolo LF, Edwards S et al. Developing a vaccine against multiple psychoactive targets: a case study of heroin. CNS Neurol Disord Drug Targets 2011; 10:865-875. [ Links ]
20. Stowe GN, Vendruscolo LF, Edwards S, Schlosburg JE et al. A vaccine strategy that induces protective immunity against heroin. J Med Chem 2011;54:5195-204. [ Links ]
21. Carrera MR, Meijler MM, Janda KD. Cocaine pharmacology and current pharmacotherapies for its abuse. Bioorg Med Chem 2004;12:5019-5030. [ Links ]
22. Haney M, Kosten TR. Therapeutic vaccines for substance dependence. Expert Rev Vaccines 2004;3:11-18. [ Links ]
23. Bagasra O, Forman LJ, Howeedy A, Whittle P. A potential vaccine for cocaine abuse prophylaxis. Immunopharmacology 1992;23:173-179. [ Links ]
24. Carrera MR, Ashley JA, Parsons LH, Wirsching P et al. Koob Suppression of psychoactive effects of cocaine by active immunization. Nature 1995;378:727-730. [ Links ]
25. Carrera MR, Ashley JA, Zhou B, Wirsching P et al. Cocaine vaccines: antibody protection against relapse in a rat model. Proc Natl Acad Sci USA 2000;97:6202-6206. [ Links ]
26. Carrera MR, Ashley JA, Wirsching P, Koob GF et al. A second-generation vaccine protects against the psychoactive effects of cocaine. Proc Natl Acad Sci USA 2001;98:1988-1992. [ Links ]
27. Carrera MR, Kaufmann GF, Mee JM, Meijler MM et al. Treating cocaine addiction with viruses. Proc Natl Acad Sci USA 2004;101:10416-10421. [ Links ]
28. Carrera MR, Ashley JA, Hoffman TZ, Isomura S et al. Investigations using immunization to attenuate the psychoactive effects of nicotine. Bioorg Med Chem 2004;12:563-570. [ Links ]
29. Ettinger RH, Ettinger WF, Harless WE. Active immunization with cocaine-protein conjugate attenuates cocaine effects. Pharmacol Biochem Behav 1997;58:215-220. [ Links ]
30. Fox BS, Kantak KM, Edwards MA, Black KM et al. Efficacy of a therapeutic cocaine vaccine in rodent models. Nat Med 1996;2:1129-1132. [ Links ]
31. Kantak KM, Collins SL, Bond J, Fox BS. Time course of changes in cocaine self-administration behavior in rats during immunization with the cocaine vaccine IPC-1010. Psychopharmacology (Berl) 2001;153:334-340. [ Links ]
32. Kantak KM. Anti-cocaine vaccines: antibody protection against relapse. Expert Opin Pharmacother 2003;4:213-218. [ Links ]
33. Kosten TR, Rosen M, Bond J, Settles M et al. Human therapeutic cocaine vaccine: safety and immunogenicity. Vaccine 2002;20:1196-1204. [ Links ]
34. Martell BA, Mitchell E, Poling J, Gonsai K et al. Vaccine pharmaco-therapy for the treatment of cocaine dependence. Biol Psychiatry 2005;58:158-164. [ Links ]
35. Orson FM, Kinsey BM, Singh RA, Wu Y et al. Vaccines for cocaine abuse. Hum Vaccine 2009;5(4):194-199. [ Links ]
36. Orson FM, Kinsey BM, Singh RA, Wu Y et al. Substance abuse vaccines. Ann N Y Acad Sci 2008;1141:257-269. [ Links ]
37. Moreno AY, Janda KD. Immunopharmacotherapy: vaccination strategies as a treatment for drug abuse and dependence. Pharmacol Biochem Behav 2009;92:199-205. [ Links ]
38. Bonese KF, Wainer BH, Fitch FW, Rothberg RM et al. Changes in heroin self-administration by a rhesus monkey after morphine immunisation. Nature 1974;252:708-710. [ Links ]
39. Cerny EH, Cerny T. Anti-nicotine abuse vaccines in the pipeline: an update. Expert Opin Investig Drugs 2008;17:691-696. [ Links ]
40. Cerny EH, Cerny T. Vaccines against nicotine. Hum Vaccin 2009;5:200-205. [ Links ]
41. Kinsey BM, Jackson DC, Orson FM. Anti-drug vaccines to treat substance abuse. Immunol Cell Biol 2009;87:309-314. [ Links ]
42. Montoya I. Immunotherapies for drug addictions. Adicciones 2008;20:111-115. [ Links ]
43. Wainer BH, Fitch FW, Rothberg RM, Fried J. Morphine-3-succinyl-bovine serum albumin: an immunogenic hapten-protein conjugate. Science 1972;176:1143-1145. [ Links ]
44. Wainer BH, Fitch FW, Rothberg RM, Fried J. The structure of morphine monohemisuccinate. Science 1972;178:647-648. [ Links ]
45. Wainer BH, Fitch FW, Fried J, Rothberg RM. A measurement of the specificities of antibodies to morphine-6-succinyl-BSA by competitive inhibition of 14 C-morphine binding. J Immunol 1973;110:667-673. [ Links ]
46. Wainer BH, Fitch FW, Rothberg RM, Schuster CR. In vitro morphine antagonism by antibodies. Nature 1973;241:537-538. [ Links ]
47. Akbarzadeh A, Mehraby M, Zarbakhsh M, Farzaneh H. Design and synthesis of a morphine-6-succinyl-bovine serum albumin hapten for vaccine development. Biotechnol Appl Biochem 1999;30:139-146. [ Links ]
48. Salazar-Juárez A, Feregrino Alonso MA, Barbosa Méndez S, Hernández Miramontes R et al. Morphin/heroin vaccine attenuates analgesic effects of different doses of morphine in rats. Addiction Biology 2013 (enviado). [ Links ]
49. Li QQ, Luo YX, Sun CY, Xue YX et al. A morphine/heroin vaccine with new hapten design attenuates behavioral effects in rats. J Neurochem 2011;119:1271-1281. [ Links ]
50. Raleigh MD, Pravetoni M, Harris AC, Birnbaum AK et al. Selective effects of a morphine conjugate vaccine on heroin and metabolite distribution and heroin-induced behaviors in rats. J Pharmacol Exp Ther 2013;344:397-406. [ Links ]
* Para los norteamericanos un billón equivale a mil millones.














