Introducción
Las infecciones virales mixtas en plantas, también conocidas como coinfecciones, son un fenómeno complejo y común en plantas. Anteriormente se estimaba que las infecciones mixtas eran escasas y se restringían a áreas geográficas complejas. Sin embargo, un análisis reciente del “viroma” en cultivos hortícolas mediante secuenciación de nueva generación ha proporcionado evidencia de la frecuencia de las coinfecciones por múltiples agentes virales (Moreno y López-Moya, 2020). Esto ha contribuido a comprender las coinfecciones virales, las relaciones virusplanta y los mecanismos para el establecimiento de la infección, el desarrollo de enfermedades, y la propagación de virus. A diferencia de la monoinfección, las coinfecciones tienen algunas características distintivas, tales como la presencia de vectores virales asociados a múltiples hospedantes (Syller, 2014), la aparición repentina y el aumento de los síntomas, y la progresión de la enfermedad (Jacobson et al., 2018). Las coinfecciones resultarán en interrelaciones virus-virus beneficiosas, neutrales o contraproducentes.
Los efectos sinérgicos son frecuentes entre virus que pertenecen a diferentes especies (de diferentes géneros o del mismo género) (Miranda-Campaña et al., 2024; Kwon et al., 2023; Takeshita et al., 2012), pero también entre virus que comparten un vector, tales como aquellos que se transmiten por insectos como las moscas blancas, pulgones, trips, saltahojas y escarabajos. La especie de virus dentro de los géneros Crinivirus, Potyvirus y Begomovirus son los caos más reportados de interacciones sinérgicas en cultivos hortícolas (Wintermantel et al., 2008; Lucía-Sanz y Manrubia, 2017; Escobedo Garcia-Medrano et al., 2022; Tamborindeguy et al., 2023).
El antagonismo ha sido reportado en especies relacionadas de virus e implica una infección mixta en la que dos elementos virales compiten para establecer una infección en la planta (Mascia y Gallitelli, 2016), lo que resulta en un virus con mayor aptitud que el otro. Este rasgo causa que el virus menos favorecido rápidamente reduzca sus títulos. Desde un punto de vista adaptativo, está la activación de las respuestas de defensa del hospedante que previenen una posterior infección por un virus secundario (Singhal et al., 2021). La hipótesis de la competencia por recursos del hospedante es la más aceptada y que explica, en parte, por qué la mayoría de las interacciones virus‒virus resultan en una monoinfección (Singhal et al., 2021), como en las infecciones mixtas de begomovirus (Silva et al., 2014).
La exclusión de superinfección (SIE) es un tipo de antagonismo que es específico a virus de la misma especie, virus leves o cepas de viroides que protegen a la planta de enfermedades resultantes de un encuentro posterior con una cepa severa del mismo virus (Ziebell y Carr, 2010). En este fenómeno, el primer virus bloquea la infección de un segundo virus y causa una patogenicidad y severidad por debajo de la inicial, proporcionando así una protección oculta solo contra virus y cepas de virus relacionados (Cwick et al., 2022; Tsuda et al., 2007). Cuando se usa SIE como práctica agrícola se llama protección cruzada, la cual está establecida como una estrategia de manejo ampliamente usada para reducir las pérdidas de cultivos causadas por algunas enfermedades virales (Xu et al., 2022; Lecoq y Katis, 2014; Zhou et al., 2019). Así, la protección cruzada es específica a las cepas del mismo virus, en comparación con el antagonismo, donde se consideran dos virus diferentes en el proceso de infección (Pal y Gardener, 2006).
Finalmente, la coinfección neutra ocurre cuando la especie viral coinfecta, causa daño a la planta (Vinodhini et al., 2021) y sus títulos permanecen intactos. Se sugiere que este tipo de interacción es poco estudiado porque los síntomas causados por un virus enmascaran los síntomas del otro agente (Singhal et al., 2021). Las infecciones antagonistas y neutrales son escasamente reportadas y no se han analizado a profundidad en comparación con el sinergismo. Sin embargo, la diversidad fenotípica siempre emerge, lo cual mejora nuestra comprensión de la patogénesis viral (Syller y Grupa, 2016).
En este trabajo hemos limitado nuestro análisis a hortalizas de interés agroindustrial, tales como Capsicum spp., Solanum lycopersicum, y otras Cucurbitáceas. Si bien las infecciones virales mixtas empezaron a ser publicadas en la década de 1970, en este trabajo hemos descrito informes actuales de infecciones virales mixtas en cultivos de hortalizas reportadas en los últimos diez años (Cuadro 1). Las herramientas genómicas han ayudado a comprender su naturaleza y han conducido a avances significativos en la identificación de este tipo de infección. Este análisis explora los aspectos bioquímicos y moleculares de las infecciones virales mixtas en plantas agronómicas, con el enfoque puesto en tres aspectos fundamentales que posibilitan las infecciones mixtas. Primero, los componentes vegetales involucrados en las infecciones virales mixtas; segundo, el sistema de ARN de interferencia, y por último, los componentes virales reportados en infecciones mixtas.
Componentes vegetales involucrados en infecciones virales mixtas
Las infecciones mono y mixtas pueden ser difíciles de detectar, ya que el daño es causado en diversas partes de las plantas, como brotes, hojas, flores y frutos, y pueden confundirse con una falta de nutrientes o con daños causados por herbicidas (Gergerich y Dolja, 2006). Otro aspecto importante es la afinidad de cada virus involucrado por ciertos componentes de la planta. Además, ciertos componentes de la célula hospedante asisten a los virus para entrar, moverse y translocarse de una célula a otra o de un tejido a otro. Por lo tanto, la determinación de los componentes de las plantas involucrados en las infecciones mixtas virales es un tema de gran importancia.
Los plasmodesmos (PD) son canales de comunicación citoplásmica entre las células de las plantas que permiten el transporte simplástico de macromoléculas vitales para el crecimiento y desarrollo de las plantas (Figura 2). Sin embargo, los virus de las plantas usan este espacio para moverse durante el proceso de infección. La proteína localizada en los plasmodesmos-5 (PDLP5) actúa como inhibidor del tráfico de los PD (Lee et al., 2011). Para elucidar las características de esta proteína,
Cuadro 1 Infecciones virales mixtas reportadas para cultivos de vegetales en los últimos 10 años.
| Recurso/ Tipo de infección mixta | Género perteneciente | Virus/ Síntomas | Relevancia | País y referencia |
|---|---|---|---|---|
| Tomate/ Sinergismo | Potexvirus, Potyvirus y Amalgavirus | Potato virus Y (PVY), Pepino mosaic virus (PepMV), y STV / Clorosis, deformación, y manchas de color oscuro en las hojas. PVY y Tomato spotted wilt virus (TSWV) / Enanismo, clorosis foliar, moteado y rizado. PaMMV y TBRFV / Lesiones locales necróticas en las hojas. TYLCV, Tomato leaf curl betasatellite (ToLCB), y Mungbean yellow mosaic Indian virus (MYMIV) / Síntomas de coloración amarillenta, curvatura y retraso del crecimiento. TYLCV y ToCV / Datos no mostrados. Tomato golden mottle virus (TGMV) y Tomato severe leaf curl virus (ToSLCV) / Crecimiento reducido, mosaico y clorosis. Cucurbit leaf crumple virus (CuLCrV), Cucurbit yellow stunting disorder virus (CYSDV), y TYLCV / Arrugamiento severo y curvatura hacia abajo de las hojas. TBRFV y PepMV / Frutos inmaduros abiertos o con cicatrices, junto con hojas estrechas, con parches amarillos, y hojas en forma de cordón. TYLCV, Tomato yellow leaf curl Kanchanaburi virus (TYLCKaV), y Pepper yellow leaf curl Indonesia virus (PepYLCIV) / Amarillamiento leve, rizado y atrofiado de las hojas. ToCV y TYLCV / Disminución de la altura y peso de los tallos. Tomato yellow spot virus (ToYSV), Tomato yellow spot alphasatellite (ToYSA), Euphorbia yellow mosaic virus (EuYMV), y Euphorbia yellow mosaic alphasatellite (EuYMA)/ Mosaico severo, deformación de hojas, rizado y enanismo. | Hubo un incremento en la severidad de los síntomas en las plantas coinfectadas en comparación con las plantas infectadas únicamente con PepMV. Hubo una alta tasa de transmisión de STV y asociación con los síntomas del tomate. | Italia Iacono et al. (2015) |
| Capsicum sp./ Sinergismo | Orthotospovirus y Potyvirus | Alta incidencia de infecciones virales mixtas asociadas con Frankliniella occidentalis y Myzus persicae. | Zimbabue Karavina et al. (2016) | |
| Tomate/ Sinergismo | Tobamovirus | Aceleración de los síntomas y la infección. Ambos virus interfieren con la respuesta hipersensible. | Israel Luria et al. (2018) | |
| Tomate/ Sinergismo | Begomovirus | Los Begomovirus no suelen infectar los tomates; pero, MYMIV, podría transmitirse como pasajero del TYLCV en los tomates. | Oman Shahid et al. (2019) | |
| Tomate / Sinergismo | Begomovirus y Crinivirus | La coinfección por TYLCV y ToCV indujo cambios en la expresión de genes implicados en el transporte y el metabolismo energético. | China Ding et al. (2019) | |
| Tomate / Sinergismo | Begomovirus | Altas poblaciones de B. tabaci se asociaron con infecciones de diferentes especies de begomovirus, pero en este estudio el número de moscas blancas fue bajo. | México Zuñiga-Romano et al. (2019) | |
| Calabaza y tomate / Sinergismo | Begomovirus y Crinivirus | Efecto de la adquisición de TYLCV y CuLCrV por parte de la mosca blanca sobre la carga viral y examinación de la preferencia y aptitud de la mosca blanca. | Estados Unidos Gautam et al. (2020) | |
| Tomate/ Sinergismo | Tobamovirus y Potexvirus (ver síntomas en la Figura 3). | Las infecciones leves por PepMV precedidas por TBRFV pueden inducir síntomas característicos de cepas agresivas de PepMV. | Israel Klap et al. (2020) | |
| Tomate/ Sinergismo | Begomovirus | Falta de efectividad de los genes de resistencia Ty contra infecciones mono y mixtas de distintos begomovirus locales del sudeste asiático. | Japón Koeda et al. (2020) | |
| Tomate/ Sinergismo | Crinivirus y Begomovirus | TYLCV presentó tropismo por el follaje superior en contraste con ToCV, que estuvo presente principalmente en las hojas inferiores. | China Li et al. (2021) | |
| Tomate/ Sinergismo | Begomovirus | Algunos begomovirus pueden aumentar la gravedad de los síntomas y promover o restringir la acumulación de otros virus en el huésped. | Brasil Nogueira et al. (2021) | |
| Tomate/ Sinergismo | Begomovirus (ver síntomas en la Figura 1). | Tomato yellow mottle virus (ToYMoV), Tomato yellow mottle disease (ToYMoD), y Tomato leaf curl Sinaloa virus (ToLCSiV) / Aclaramiento de venas, arrugamiento, mosaico amarillo y hojas atrofiadas. TYLCV y ToCV / Encrispamiento severo y coloración amarillenta extensa en las hojas superiores, necrosis de las hojas recién emergentes. PepYLCIV, TYLCKaV, y ToLCNDV / Mosaico amarillo, bandas venosas, ahuecamientos hacia arriba, curvatura y tamaño reducido de las hojas. Retraso del crecimiento de la planta TBRFV y PepMV / Necrosis y clorosis STV, Cucumber mosaic virus (CMV), y PepMV / Fuerte deformación de las hojas, síntomas severos de mosaico, diferencias de altura y peso respecto a los controles. TYLCV y Tomato mottle virus (ToMoV) / Síntomas de curvatura, amarillamiento y mosaico de las hojas. ToSRV y ToRMV/ Mosaico amarillo y distorsión de las hojas. CMV, Capsicum chlorosis virus (CaCV), y Groundnut bud necrosis virus (GBNV) / Manchas y anillos cloróticos concéntricos, necrosis junto con mosaico y malformación de las hojas. TYLCV, Cotton leaf curl Gezira virus (CLCuGeV), Okra yellow crinkle Cameroon alphasatellite (OYCrCMA), y Okra leaf curl Oman betasatellite (OLCuOMB) / Síntomas de curvatura, amarillamiento y mosaico de las hojas. CaCV, Chilli veinal mottle virus (ChiVMV), Large cardamom chirke virus (LCCV), CMV, PMMoV, y Chilli leaf curl virus (ChiLCV) / Moteado de mosaico amarillo, enrollamiento de las hojas, manchas cloróticas y necróticas. ToMV, Tomato golden mosaic virus (ToGMoV), y Pepper huasteco yellow vein virus (PHYVV) / Necrosis foliar, moteado amarillo, bandas venosas verdes, ampollas, curvatura hacia arriba y hacia abajo, malformación de las hojas y clorosis. | La interacción sinérgica de los begomovirus conducirá a una mayor gravedad de la enfermedad. | Costa Rica Maliano et al. (2022) |
| Tomate/ Sinergismo | Begomovirus y Crinivirus | Se sugiere que el antagonismo y el sinergismo ocurren en las etapas temprana y tardía, respectivamente. | España Ontiveros et al. (2022) | |
| Pimientos/ Sinergismo | Begomovirus | La monoinfección grave causada por PepYLCIV provocó infecciones mixtas con TYLCKaV. PepYLCIV y TYLCKaV infectaron variedades resistentes de plantas de pimiento sin mostrar síntomas de infección. | Indonesia Wahyono et al. (2023) | |
| Tomate/ Sinergismo | Tobamovirus y Potexvirus | Presencia de PepMV y TBRFV en tomates importados en supermercados de Florida. | Estados Unidos Yilmaz y Batuman (2023) | |
| Tomate/ Sinergismo y antagonismo | Amalgavirus, Cucumovirus y Potexvirus | STV aumentó el título viral e indujo síntomas por CMV en las primeras etapas de la infección, mientras que el título de PepMV no cambió a pesar de que PepMV exacerbó los síntomas. | España Elvira-González et al. (2021) | |
| Tomate/ Antagonismo | Begomovirus vs Tobamovirus | TYLCV produjo un efecto antagónico sobre la infección sistémica por ToMoV. | Estados Unidos McLaughlin et al. (2022) | |
| Tomate/ Antagonismo | Begomovirus vs Begomovirus | Los genes involucrados en la replicación (CR) son responsables del antagonismo. | Brasil Nogueira et al. (2023) | |
| Capsicum sp. / Neutral | Cucumovirus y Potyvirus | La sustitución de aminoácidos de Ser129 por Pro129 de la CP del CMV es necesaria para la infección mixta. | India Vinodhini et al. (2021) | |
| Tomate y melón / Neutral | Begomovirus | Primer informe de infección mixta de begomovirus bipartitos y monopartitos asociados con satélites de ADN de tomate y melón. | Arabia Saudita AlHudaib et al. (2022) | |
| Chile /No disponible | Orthotospovirus, Potyvirus, Macluravirus, Cucumovirus, Tobamovirus y Begomovirus | Aparición generalizada de infecciones mixtas. Primer informe de la detección de seis virus en chile. | India Devi et al. (2022) | |
| Tomate/ Sinergismo | Tobamovirus y begomovirus | La coinfección de ToMV con begomovirus resultó en una mayor gravedad de la enfermedad, una reducción del crecimiento de las plantas y una mayor acumulación viral. ToMV exhibió una alta tasa de mutación. | México Gonzalez-Perez et al. (2024) |

Figura 1 Transición de síntomas en las hojas inferiores, medias y superiores de plantas de tomate agroinoculadas con los componentes de ADN-A y DNA-B de clones infecciosos de aislados de TYLCV (ToYMoV-[CR:Gre:GR1:90]), y Tomato leaf curl Sinaloa virus (ToLCSiV-[CR:Lib:L1:02]) de Costa Rica y un clon infeccioso del ADN genómico de TYLCV de la República Dominicana (TYLCV-[DO]) de forma individual o en todas las combinaciones. (A) TYLCV; (B) planta de tomate no inoculada; (C) ToYMoV y ToLCSiV; (D) ToYMoV y TYLCV; (E) ToLCSiV y TYLCV; (F) ToYMoV, ToLCSiV y TYLCV. Las plantas fueron fotografiadas 21 días después de la agroinoculación (con el permiso de Maliano et al., 2022).
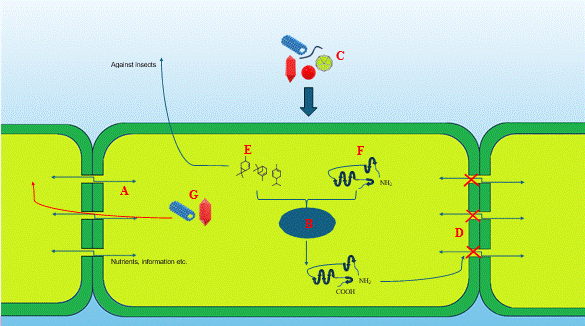
Figura 2 Componentes vegetales involucrados en las infecciones virales mixtas. El proceso normal de comunicación entre las células vegetales de las plantas implica la interrelación de estructuras tales como los plasmodesmos (A) y el núcleo (B); los primeros se encuentran en las paredes celulares que permiten el pasaje de moléculas en el citoplasma. En presencia de una infección viral (C), la célula contrarresta la acción mediante vías bioquímicas bien definidas, como la inhibición de la función de los plasmodesmos y el tráfico intracelular (D), la producción de metabolitos de respuesta específica (que pueden ocurrir antes o durante el desarrollo de la infección viral), (E) o el aumento en la producción de proteínas involucradas en los procesos de desintoxicación (F). Por otro lado, después de una internalización exitosa por dos virus, ocurre un efecto sinérgico de la infección viral mixta (G).
Kutsher et al. (2021) investigaron plantas de tomate y tabaco infectadas con virus y, a través del ensayo con Proteína Verde Fluorescente (GFP) se determinaron la ubicación, cuantificación y efecto de PDLP5 sobre los PD. En hojas de tabaco, el Tobacco mosaic virus (TMV) y el Tomato brown rugose fruit virus (TBRFV) aumentaron los niveles de PDLP5-GFP en PD en comparación con el testigo, mientras que se observaron diferencias significativas en las hojas del tomate. En cambio, la infección con el Tomato yellow leaf curl virus (TYLCV) redujo la acumulación de PDLP5-GFP en el PD de hojas del tomate en comparación con el testigo, sin efectos significativos sobre el PD de la hoja de tabaco. Si bien las inoculaciones y los efectos virales fueron evaluados por separado y no en una infección viral mixta, la investigación evidenció claras diferencias en los mecanismos moleculares involucrados en los diferentes tipos de infección. La infección por parte de la especie del Tobamovirus condujo a un aumento en la expresión de una proteína específica,
PDLP5, mientras que los virus pertenecientes al género Begomovirus inhibieron su expresión, estableciendo que la actividad en los PD depende en gran medida del tipo de virus. Así, sería interesante saber cuál sería el papel de PDLP5 en relación con la infección mixta con diferentes géneros virales.
Los metabolitos vegetales abarcan un vasto número de compuestos orgánicos de diferentes naturalezas químicas, importancia y funciones. Participan en el desarrollo de procesos celulares, reproducción, protección, maduración y senescencia de plantas (Figura 1). Existen escasos informes sobre la síntesis y funcionalidad de metabolitos vegetales cuando ocurren las coninfecciones; se han observado cambios en el tipo y los patrones de acumulación de fitoquímicos (Zaynab et al., 2018). Fereres et al. (2016) investigaron las alteraciones en el patrón de producción de compuestos volátiles en tomates infectados por un virus circulativo como Tomato severe rugose virus (ToSRV) y un virus no circulativo como Tomato chlorosis virus (ToCV). Un análisis de los compuestos individuales mostró que las plantas testigo de tomates emitieron cantidades significativamente mayores de los terpenos α-pineno, 4-careno, α-felandreno, terpineno y β-felandreno que las plantas infectadas con ToSRV, lo que indicó que la infección con ToSRV promueve la supresión de algunos terpenos volátiles. Además, las moscas blancas presentaron una clara preferencia por plantas no infectadas, favoreciendo la dispersión de la enfermedad. Estos resultados sugirieron la habilidad de ciertos virus de coevolucionar con su hospedante, aumentando su propagación por medio de la modificación de los patrones de síntesis de compuestos volátiles en plantas de tomate. Sería interesante discernir si existe una conexión en la síntesis de terpenos como mecanismo de defensa contra insectos vectores, especialmente para Bemisia tabaci (B. tabaci).
Sin embargo, la reducción en la concentración de los terpenos no se asoció con una
mayor atracción del vector hacia plantas infectadas con ToSRV.
Posteriormente, De et al. (2018) describieron que la infección sinérgica de N. benthamiana por Potato virus X (PVX) y por Potato virus A (PVA) que aumentó la expresión del Componente Ayudante de Proteasa (HCPro), una proteína que causa alteraciones en el ciclo de la metionina en la célula huésped. En este experimento, a través del silenciamiento génico de enzimas vegetales clave, como S-adenosill-metionina sintetasa (SAMS) y S-adenosil-l-homocisteína hidrolasa (SAHH), se encontró una reducción significativa en la glutatión reductasa (GSH), un antioxidante importante en las células vegetales, y por ende, la deficiencia de GSH puede explicar los síntomas observados durante la infección mixta PVX-PVA.
Un estudio reciente publicado por Pollari et al. (2022) encontró que cuando N. benthamiana es infectado por potivirus y potexvirus, la respuesta metabólica del hospedero difiere de forma significativa, según si es una infección mixta o una monoinfección. En las infecciones mixtas se encontró un aumento en metabolitos relacionados con defensas, y se sugirió un bajo potencial de metilación del material genético. Finalmente, se concluye que el estrés oxidativo asociado a la infección se controla con éxito, pero no en infecciones sinérgicas.
Das et al. (2019) reportaron un conjunto de metabolitos secundarios (terpenoides e isoprenoides tales como clorofila, carotenoides, filoquinonas, giberelinas, y ácido abscísico), producidos por N. benthamiana después de la infección con TMV durante la infección cruzada. Mediante la técnica de las Etiquetas Isobáricas para la Cuantificación Relativa y Absoluta (iTRAQ) durante una infección mixta fue posible demostrar que un TMV-43A (una mutante en la que se reemplazaron 43 nt de poli(A)) pudo proteger de forma cruzada a las plantas de N. benthamiana contra una cepa silvestre de TMV. En plantas protegidas de forma cruzada, se observó un aumento en la biosíntesis de aminoácidos y las actividades fotosintéticas, apoyadas por un aumento en la acumulación de las enzimas 1-desoxi-D-xilulosa-5-fosfato reductoisomerasa (DXR) y geranilgeranil difosfato sintasa (GGPS), fundamentales para la biosíntesis de la clorofila. También se encontró un aumento en la abundancia de enzimas relacionadas con el manejo de especies reactivas de oxígeno (ROS) y la homeostasis redox, tales como las tiorredoxinas y la L-ascorbato peroxidasa.
Los PD y la síntesis de metabolitos son modificados por la presencia de virus,
aunque los componentes vegetales relacionados con las infecciones mixtas son escasos, otros sitios importantes para el crecimiento, como el mecanismo de ubiquitinación podría ser viable para su estudio y establecer el papel de estos componentes en infecciones virales mixtas.
Sistema de ARN de interferencia
El silenciamiento con base en el ARN es un sistema cuya función principal es la del mantenimiento de la integridad genómica, pero las plantas han adaptado este sistema como un mecanismo de protección, especialmente contra los virus. La defensa por medio del silenciamiento con base en el ARN permite la supresión de la expresión génica mediante interacciones específicas de secuencia que son mediadas por moléculas de ARN de entre 21 y 24 nucleótidos de longitud (Figura 3), (Moissiard y Voinnet, 2004; Cisneros y Carbonell, 2020). Bajo la premisa de que las secuencias del ARN están dirigidas a objetivos virales específicos, sería útil saber si los virus con secuencias similares pueden ser el objetivo de estos microARNs (Kwon et al., 2020) y cuál es el impacto de las estrategias de silenciamiento de los genes contra las infecciones virales mixtas y su efecto sobre la protección cruzada (Mohamed et al., 2022; Leonetti et al., 2021). Turco et al. (2018) caracterizaron la defensa antiviral de plantas solanáceas cultivadas y con infecciones mixtas. En este experimento (Turco et al., 2018), plantas de tomate resistentes a la cepa chilena del PepMV (CH2) ejercieron, de forma indirecta, un efecto de resistencia a la infección por el genotipo peruano (cepa LP) del mismo virus. La exposición de la cepa LP a plantas de tomate preinfectadas con la cepa PepMV CH2 promovió alteraciones de las secuencias genómicas de consenso en las especies virales, lo cual indica un amplio potencial para la protección cruzada (Turco et al., 2018). Asimismo, encontraron una amplia asociación de pequeños ARN de interferencia (ARNsi) con componentes catalíticos del silenciamiento génico, tales como AGO 1, AGO 2, y AGO 3, involucrados con el ARN de interferencia (ARNi) en la escisión de secuencias virales (Figura 2). Los autores señalaron que las cuasiespecies LP (variantes genotípicas) experimentan una rápida evolución dentro de una planta infectada mediante la aparición y fijación de mutaciones puntuales.
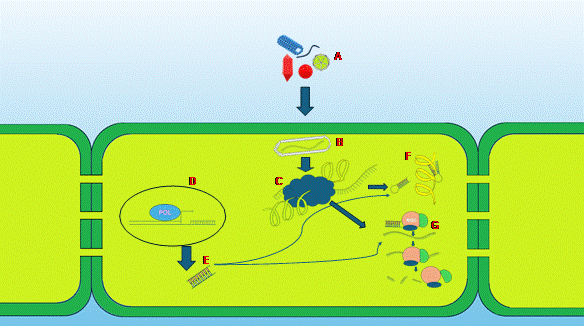
Figura 3 Silenciamiento génico a través del ARN de interferencia pequeño en células vegetales. La internalización del virus ocurre (A), el ARN viral está protegido por una cápside viral (B), el virus usa la maquinaria de transcripción celular para la síntesis de proteínas virales (C). La replicación del ADN vegetal tiene lugar en el núcleo (D) y se sintetiza un ARN de interferencia pequeño, que posteriormente madura y se exporta el citosol donde, después de algunas modificaciones, se produce un ARN de horquilla corta (E). El ARN pequeño puede actuar de varias maneras, tales como interferir con proteínas virales específicas (F), o unirse al ARN viral y a través del Complejo de Silenciamiento Inducido por el ARN (RISC, por sus siglas en inglés), que interfiere con la expresión de genes virales (G).
Además, se encontró que las cuasiespecies CH2 evolucionan rápidamente, lo cual, en el largo plazo, puede crear variantes genéticas agresivas con síntomas severos de enfermedades y la estabilidad genética es considerada importante para la protección cruzada contra cepas virales específicas (Ziebell y Carr, 2010). La efectividad de las secuencias génicas que median la resistencia de plantas contra las coinfecciones virales ha sido abordada. Wen et al. (2013) destacaron el papel crucial del gen TOM1 en el proceso de replicación del Hibiscus latent Singapore virus (HLSV) y del TMV. En un estudio realizado en N. benthamiana, la planta presentó síntomas leves en lugar de necrosis sistémica severa, y se demostró la protección cruzada contra infecciones mixtas. Aunque el mecanismo detrás de la doble protección viral todavía se desconoce, se establece que los genes TOM juegan un papel crucial en la multiplicación del Tobamovirus.
Posteriormente, Moreno-Pérez et al. (2016) reportaron que el Pepper mild mottle virus (PMMoV) con mutaciones en los aminoácidos M138N, T43K + D50G, L13F + G66V, M138N, T43K D50G y A87G en la Proteína de Cubierta (CP) puede superar la resistencia mediada en plantas, produciendo efectos pleiotrópicos e impactando la expansión del rango del hospedante. En este experimento, los fenotipos sensibles y resistentes al gen L del pimiento se evaluaron en una prueba de habilidad y se encontró que los efectos que rompen la resistencia de la planta dependen de la mutación específica, el genotipo del huésped susceptible y el tipo de infección (monoinfección o infección mixta). En consecuencia, los efectos pleiotrópicos pueden ser negativos, positivos o ausentes, según la naturaleza del virus.
Wang et al. (2021) reportaron avances en la comprensión de la activación de ARNi durante la infección viral. Los experimentos realizados en N. benthamiana demostraron que las heridas activaron el Factor de Transcripción de Unión a Calmodulina-3 (CAMTA3) y la Nucleasa Bifuncional 2 (BN2) por medio de la cascada de señalización asociada al ion Ca++ (Toyota et al., 2018). Este conjunto de proteínas es responsable de ensamblar y estabilizar el ARN mensajero (mARN) que codifica para componentes clave de la maquinaria de interferencia por ARNi. Los autores mencionan que ARGONAUTE1 y DICER-LIKE1 juegan un rol central en la degradación de microARNs. CAMTA3 o plantas knockout BN2 presentaron una mayor susceptibilidad a las infecciones por Begomovirus y Potyvirus, y en particular, la proteína V2 presente en los geminivirus interrumpe la interacción calmodulina-CAMTA3 para contrarrestar la defensa por ARNi. Estos hallazgos asocian la señalización de Ca++ con el inicio de la defensa mediada por ARNi y revelan la versatilidad de la defensa antiviral. Elvira-González et al. (2021) reportaron el perfil de pequeños ARN interferentes (siARNs) obtenidos de S. lycopersicum sometidos a infección mixta con virus no relacionados. En el experimento, se inocularon las plantas de tomate con CMV, PepMV, y Southern tomato virus (STV), y se encontró que hasta 47 siARNs se expresaron diferencialmente en plantas infectadas con estos virus en comparación con las plantas control inoculadas. Finalmente, los ARNsi con expresión diferencial encontrados en este trabajo estaban involucrados, sobre todo en procesos fundamentales de la planta, como el desarrollo, metabolismo, estrés biótico, abiótico, pero las frecuencias de los ARNsi no fueron uniformes, ni presentaron señales de influencia por el tipo de virus. Este es uno de los primeros reportes que establecen las características de la defensa de la planta mediada por el silenciamiento de ARNi cuando una planta enfrenta una infección mixta.En plantas, la defensa antiviral mediada por el ARNi es mediada por la complementariedad con secuencias foráneas (secuencias virales). Las características sinérgicas debidas a las infecciones mixtas suscitan interrogantes amplias y robustas sobre la especificidad y la cobertura de la acción de las secuencias ARNi contra virus involucrados en las coinfecciones. De hecho, pocos indicadores evidencian diferencias de forma tan clara con el ARNi producido por la planta para tratar con la monoinfección vs. infecciones mixtas.
Componentes de las proteínas virales involucradas en las infecciones mixtas
La continuidad del linaje viral al infectar una planta puede ser considerado el propósito común de los virus en plantas. Bajo esta premisa, un virus tiene una serie de proteínas responsables de llevar a cabo tres situaciones fundamentales. Primero, la adhesión a la célula hospedante, seguida de la internalización mediada de varias formas (enmascaramiento, mimetismo de proteínas, etc.) y finalmente, la réplica del genoma. La probabilidad de éxito de todas las etapas dependerá de factores que no son típicos de virus (el sistema de defensa mediado por proteínas y material genético vegetal) y en sus propias características. Luego, analizamos las proteínas y discernimos los complejos procesos que superan para lograr su objetivo. Enfatizamos que las estructuras descritas en esta sección se basan en características observadas en la monoinfección, ya que los estudios que evalúan las características de estas proteínas en infecciones mixtas son escasos.
La CP juega un papel fundamental en el ensamblaje de partículas virales y se ha establecido como meta para el desarrollo de moléculas contra virus en plantas (Wu et al., 2022). Basu et al. (2021) reportaron que en los begomovirus Tomato leaf curl New Delhi virus (ToLCNDV) y Tomato leaf curl Gujarat virus (ToLCGuV), las proteínas AV-2 (pre-CP) y AC-2 (proteína activadora transcripcional) han funcionado como moduladoras del proceso de coinfección viral del proceso de coinfección viral en el tomate y N. benthamiana. Ambos virus presentaron sinergia en una prueba in vitro en plantas de tomate y N. benthamiana, promovieron la aparición de síntomas extremos de infección. Los autores sugieren que AC2 y AV2 de ToLCGuV aumentan la acumulación asimétrica de ToLCNDV y que la presencia de este tipo de proteína viral favorece la supresión del silenciamiento de genes en plantas de
N. benthamiana y de tomate. Por medio de una prueba reversión de silenciamiento génico acoplado a GFP, (brevemente, las plantas transgénicas que expresaron AC2 y AV2 fueron validadas mediante la prueba GFP; posteriormente, las plantas fueron infiltradas con A. tumefaciens con los constructos deseados) se obtuvo la actividad supresora de las proteínas virales codificadas con los aislamientos de ARNsi a los 6 días post-infección. Los autores sugirieron que la actividad supresora de AV2 se debe al bloqueo de la propagación de las señales de silenciamiento del ARN en las hojas y concluyeron que las proteínas codificadas por ToLCGuV promueven la replicación eficiente de ToLCNDV por medio de la vía de silenciamiento antiviral. En algunos géneros de virus vegetales, CP es esencial para el proceso de infección, ya que recluta e interactúa con varias estructuras celulares (Bennett Agbandje-McKenna, 2020). Mochizuki et al. (2014) demostraron que la mutación de CP en P129 redujo la expresión de los genes relacionados con la función de los cloroplastos y la fotosíntesis en plantas de tabaco infectadas con CMV. Otras proteínas del proceso de replicado, tales como el complemento 2b de la virulencia, también se asociaron con fenotipos asintomáticos y títulos virales bajos. Los autores concluyeron que el efecto de la mutación aumentó la capacidad de patogenicidad, debido a que el CMV adquirió virulencia a través de mutaciones en los aminoácidos de la CP, lo que condujo a anomalías estructurales en los cloroplastos. Posteriormente, Zhang et al. (2017) reportaron que la mutación E96 de CP del Cucumber green mottle mosaic virus (CGMMV) es importante para el proceso de patogénesis del desarrollo. Pruebas in vitro con mutantes de N. benthamiana E96 CGMMV produjeron una infección exitosa y este estudio indicó que las modificaciones en el sitio de ensamblaje en las células pueden ser afectadas por mutaciones en el aminoácido crucial E96. Por este motivo, otros mutantes realizados en este estudio, tales como E96A y E96K, y tres mutantes dobles, V94A-E96K, V97-E96K, y T104A-E96K, presentaron solo rasgos sistémicos tardíos de infección en N. benthamiana, destacando el papel del residuo de E96 en el proceso de infección.
Shi et al. (2023) reportaron que en el género de Tobamovirus, CP y MP presentan la capacidad de interactuar para facilitar el movimiento viral a través de PD. Se determinó in vitro que la región de la proteína MP entre los residuos 78 y 128 era importante para el movimiento viral. Específicamente, el residuo de treonina en la posición 107 en MP (T107MP) es crucial para la interacción CP-MP interacción y la sustitución de T107A retrasa la infección sistémica de CGMMV en N. benthamiana. Mutaciones en otros residuos evaluados, tales como F17AMP y D97AMP inhibieron la infección de CGMMV, lo que sugiere que estos últimos no juegan ningún papel en la interacción, pero regulan la función de MP, independiente de CP. Además, se encontró que la coexpresión de MP y CP de CGMMV en N. benthamiana aumenta la acumulación de CP y que la interacción de ambas proteínas inhibe la respuesta de defensa mediada por el ácido salicílico en las primeras etapas de infección. Finalmente, los autores concluyeron que la supresión de la defensa antiviral del hospedante, activado por la interacción CP-MP facilita le infección sistémica.
Comprender el papel de CP en el proceso de infección ha permitido realizar
avances notables que podrían aplicarse en el futuro para el control de infecciones virales en plantas. Liu et al. (2020) reportaron que las cepas mutantes de CGMMV
presentaron características útiles para el control de virus específicos mediante la protección cruzada. A través de la mutagénesis dirigida, se obtuvo mutantes de CPCGMMV que después fueron inoculados en N. benthamiana hasta que se observaron síntomas. Específicamente, la mutación de CP en el residuo D89 (D89A) redujo los síntomas de la infección por CGMMV en hojas y venas. Los clones mutantes de obtenidos mostraron una característica importante para la regulación de la virulencia de CGMMV y se pueden desarrollar como un modelo exitoso para la contención de cepas virulentas de este tipo específico de virus. Sharma et al. (2020) también sugirieron la gran utilidad de CPTMV como un modelo para generar mutantes que confieran resistencia viral a futuras infecciones y desarrollen protección cruzada. Específicamente, los mutantes CPTMV T42W y E50Q exhibieron la presencia de varillas no helicoidales y altamente estables que interfieren con la acumulación de MP y promueven el desensamblaje molecular de TMV en la célula hospedante. Dado que la protección cruzada se considera dentro de las infecciones virales mixtas, los resultados indican que este tipo de metodología podría brindar una protección adecuada contra la infección por TMV.
Ya hemos descrito anteriormente las características de las proteínas reportadas
durante el proceso de infección viral. Aunque las funciones han sido establecidas, se requiere más investigación para comprender lo que sucede cuando interactúan proteínas ortólogas de diferentes especies de virus en una infección mixta y por qué no estimar el grado en el que una interacción proteínaproteína favorece el sinergismo viral o la protección cruzada, o incluso si tal interacción pudiera desencadenar el desarrollo de un antagonismo viral.
Perspectivas y conclusión
Las estrategias de control viral dependen, en buena parte, de la comprensión de los fenómenos naturales, incluyendo la patogénesis viral y sus aspectos, tales como las monoinfecciones y coinfecciones. La investigación preliminar en este campo podría ser, en el futuro, la base para la implementación de programas para el control de infecciones virales mixtas en hortalizas de interés agronómico. Una de las teorías más aceptadas acerca de infecciones mixtas de los virus relacionados es que, debido a que tienen mecanismos de entrada a las células huésped y comparten el arsenal de proteínas involucradas en el proceso de infección, las probabilidades de desarrollar una coinfección aumentan (Ng y Falk, 2006; Tamborindeguy et al., 2023). Si bien este proceso es posible y comprobable en virus multipartitos de las familias de Closteroviridae, Geminiviridae, Nanoviridae, Potyviridae y Rhabdoviridae (Lucía-Sanz y Manrubia, 2017), no funciona de la misma manera para otros virus. La Figura 4 presenta una infección mixta de tobamovirus con potexvirus, con un efecto sinérgico sobre el fenotipo. Sin embargo, para el género del tobamovirus, donde algunas especies presentan semejanza genética (por ejemplo, Tomato mottle mosaic virus (ToMMV) y Tomato mosaic virus (ToMV)), no hay reportes de infecciones mixtas (Tettey et al., 2022).

Figura 4 Desarrollo de síntomas en hojas de tomate (cv. Macizo) infectadas con TBRFV y PepMV en infecciones mono y mixta (sinergia) a 21 días post-inoculación, (fotografía donada por el grupo Dr. Tovar-Pedraza, CIAD Culiacán, México).
Syller y Grupa (2016) destacan que, por lo general, las infecciones virales relacionadas producen antagonismos. En este contexto, estudios realizados sobre el Turnip crinkle virus (TCV) establecen que virus de ARN de sentido positivo (+), por medio de una función viral que todavía se desconoce, “niega” a los virus producidos la posibilidad de replicar sus genomas en células de sus “progenitores”, lo cual conduce a la generación de virus altamente homólogos superinfecciosos que son indistinguibles de la progenie (Tatineni and French, 2016). En la actualidad, SIE explica la forma en que los virus son seleccionados de forma evolutiva al mantener una frecuencia óptima de error en los genomas de la progenie. Aunque se basa principalmente en observaciones realizadas en TCV, este nuevo modelo podría aplicarse a otros viruses para entender cómo SIE influye en la función codificada por virus y evolutivamente conservada que minimiza la proliferación de errores en la replicación. Así, SIE se establece como un mecanismo molecular que promueve el antagonismo y debe ser fortalecido en plantas solanáceas y cucurbitáceas modelo (Yin et al., 2022; Zhou et al., 2019).
Las tecnologías de Secuenciación de Alto Rendimiento (HTS) hacen posible el discernimiento de los orígenes de infecciones mixtas de forma más precisa y rápida. Específicamente, las tecnologías como Oxford Nanopore Technologies (ONT), basadas en lecturas largas, presentan la suficiente sensibilidad como para detectar agentes virales relacionados, según reportes de autores anteriores (Abou Kubaa et al., 2023; Lee et al., 2022; van Rengs et al., 2022). Además, el ARNi se convierte en una alternativa versátil y ecológica para la protección de cultivos de interés económico (Bharathi et al., 2023). El Silenciamiento Génico Inducido por el Hospedador (HIGS, por sus siglas en inglés) y el Silenciamiento Génico Inducido por Pulverización (SIGS, por sus siglas en inglés) son tendencias en las tecnologías de aplicación de ARNi. Estas metodologías hacen uso de la encapsulación para mejorar la efectividad del silenciamiento génico por parte del ARNi; además, confiere protección y estabilidad al ARN, evitando que experimente modificaciones enzimáticas o de pH (Mitter et al., 2017). Sin embargo, el mayor desafío de estos procedimientos yace en lograr la estabilidad y evitar la degradación prematura de ARNi en el ambiente. La mayor parte de la investigación actual sobre ARNi encapsulado se centra principalmente en la administración oral para controlar insectos mediante el silenciamiento de genes esenciales (Hernández-Soto y Chacón-Cerdas, 2021). Existe una investigación incipiente sobre la aplicación de ARNi para el mejoramiento de las características de cultivos de interés, según lo reporta Termolino, (2021) pero no hay reportes de que esta tecnología se esté usando para contrarrestar infecciones virales mixtas. Sin embargo, la primera evidencia de su uso y su efectividad contra virus que infectan cultivos de interés comercial ya ha sido establecida en informes previos (Worrall et al., 2019).
Gracias a la aplicación de nuevas tecnologías de secuenciación, se ha elucidado
la relación virus-huésped. La sinergia viral es la confección más estudiada y su objetivo es aumentar los recursos duales para lograr la infección. En comparación, el antagonismo o la coinfección neutral es una forma de que los virus proliferen mientras compiten con otros organismos, reduciendo la probabilidad de que estos últimos se establezcan. Se están estableciendo nuevos nichos ecológicos, hospedantes, vectores y modos de transmisión de virus que infectan a las plantas en la naturaleza.











 texto en
texto en 


