Introducción
Durante el embarazo, la prevalencia de síntomas de reflujo (pirosis y regurgitación) es elevada, pues va del 30% al 80%.1,2 El embarazo es uno de los factores que predispone a la aparición de enfermedad por reflujo gastroesofágico (ERGE), entre otros como el tabaquismo, el consumo de ciertas bebidas y alimentos, el sobrepeso y la obesidad.1,3
Epidemiología
En el embarazo, la pirosis se puede presentar hasta en el 50% de los casos durante los dos primeros trimestres, y se incrementa hasta el 80% en el tercer trimestre. La incidencia de síntomas de reflujo durante el embarazo es del 25%, con un aumento en la frecuencia y la gravedad de los síntomas al final del embarazo. Afortunadamente, las complicaciones relacionadas con el reflujo durante el embarazo son poco frecuentes.2,4
Fisiopatología
La ERGE durante el embarazo es multifactorial e involucra factores hormonales y mecánicos, favorecida además por la disminución progresiva de la presión del esfínter esofágico inferior (EEI) debido al incremento de estrógenos y progesterona.2,5 Otros factores que contribuyen son el aumento de la presión intragástrica, secundario al útero gestante, y los cambios en la motilidad gastrointestinal, como una motilidad esofágica inefectiva y un retraso en el aclaramiento esofágico.2
Nagler y Spiro5 describieron que el 55% las mujeres sintomáticas y el 20% de las asintomáticas presentan disminución progresiva de la presión del EEI al mismo tiempo que el embarazo progresa, con retorno a los niveles basales de presión del EEI posterior al parto. También observaron que un 15% de las embarazadas tenían un segmento intraabdominal del EEI, el cual se reubicaba en su mayoría posterior al parto.5
Van-Thiel et al.6 evaluaron, durante el embarazo y posterior al parto, la presión basal del EEI, el pH esofágico y el pH basal gástrico, y los niveles séricos de gastrina, estrona, estradiol y progesterona. Los resultados mostraron que existe una disminución progresiva de la presión del EEI, con el punto más bajo a las 36 semanas de gestación, con una presión normal al término del embarazo. Todas las pacientes tuvieron reflujo ácido en la semana 36 de gestación. Los niveles de pH gástrico y de gastrina sérica fueron similares en el embarazo y en el posparto. Los niveles de estrona, estradiol y progesterona incrementaron durante el embarazo y regresaron a valores normales en el posparto.6
Fisher et al.7 estudiaron a ocho mujeres embarazadas programadas para aborto electivo. Midieron la presión basal del EEI entre las semanas 14 y 19 del embarazo, y 6 semanas posterior al aborto electivo. No hubo diferencia en la presión basal del EEI; sin embargo, demostraron inhibición significativa del EEI a la pentagastrina, al edrofonio y a la metacolina, y una respuesta menor del EEI tras la ingesta de alimentos altos en proteína.7
Un estudio en zarigüeyas encontró que la exposición a estrógenos y progesterona, solos o en combinación, disminuyó la respuesta del EEI a la acetilcolina, la gastrina y la norepinefrina.8
Ulmsten y Sundström9 evaluaron la presión intraesofágica e intragástrica en 12 mujeres, seis de ellas embarazadas y las otras seis no embarazadas, y reportaron que las mujeres embarazadas presentaban una presión intraesofágica baja y una presión intragástrica alta, comparadas con las no embarazadas; asimismo, observaron que la peristalsis esofágica tenía una velocidad de onda y una amplitud menores durante el embarazo.
Wald et al.10 evaluaron el tránsito gastrointestinal durante el tercer trimestre del embarazo y a la semana 4-6 posparto. Midieron el tiempo de tránsito intestinal, con prueba en aliento con hidrógeno, y los niveles de progesterona y estradiol. Los resultados evidenciaron que los tiempos de tránsito gastrointestinal eran significativamente más prolongados durante el tercer trimestre del embarazo, cuando los niveles de progesterona y estradiol estaban aumentados, en comparación con el periodo posparto.10
Otro parámetro evaluado ha sido el vaciamiento gástrico durante los tres trimestres del embarazo, sin demostrar un retraso significativo.11
Presentación clínica
La presentación clínica es similar en embarazadas y no embarazadas, siendo pirosis y regurgitación las manifestaciones más frecuentes. Aproximadamente el 17% de las embarazadas presentan pirosis y regurgitación simultáneamente. Otros síntomas son náusea, vómito, plenitud posprandial, epigastralgia, estreñimiento y cambios en el apetito. Los síntomas se pueden exacerbar con las comidas copiosas, con la ingesta de alimentos grasos o irritantes, y durante el decúbito. La mayoría de las embarazadas presentan los síntomas de reflujo al final del primer trimestre, y a medida que avanza el embarazo, los síntomas se incrementan en intensidad y frecuencia.4
Diagnóstico
El diagnóstico de ERGE durante el embarazo debe ser clínico, basándose únicamente en los síntomas. La presencia de pirosis y regurgitación tiene una sensibilidad del 78% y una especificidad del 60% para el diagnóstico de ERGE; ante la presencia de estos dos síntomas típicos, no es necesario realizar pruebas complementarias.12-14
La manometría esofágica y la monitorización del pH esofágico pueden realizarse de forma segura, pero rara vez son necesarias.14
En caso de síntomas de reflujo intratables, complicaciones o datos de alarma, se debe realizar una panendoscopia de manera segura con monitorización fetal, uso razonado de sedación y monitorización estrecha de la presión arterial y de la oxigenación, idealmente después del primer trimestre del embarazo.4,14
En caso de presentar datos de alarma (hemorragia, vómito persistente, disfagia, dolor torácico o pérdida de peso involuntaria), la mujer embarazada debe ser enviada a valoración por un gastroenterólogo.4,15
Tratamiento
El tratamiento de la ERGE durante el embarazo es un reto, pues pretende aliviar los síntomas y no provocar daño al binomio. Se propone una terapia escalonada, inicialmente con cambios en el estilo de vida y, si no hay respuesta o persisten los síntomas molestos, pasar al tratamiento farmacológico (Figura 1).
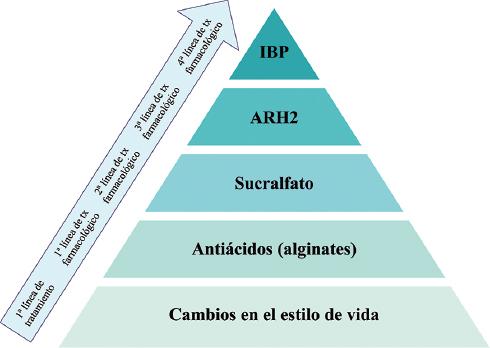
Figura 1 Recomendaciones de tratamiento médico escalonado para la enfermedad por reflujo gastroesofágico en el embarazo. ARH2: antagonista de los receptores de histamina 2; IBP: inhibidor de la bomba de protones.
Cambios en el estilo de vida
Los cambios en la dieta y el estilo de vida es la primera línea de tratamiento, debido a su seguridad y efectividad (recomendación de grado B).15-18 Estos cambios incluyen:
– Dieta fraccionada en porciones pequeñas (realizar cinco a siete comidas al día).
– Elevar la cabecera de la cama.
– Acostarse en decúbito lateral izquierdo.
– Reducir o evitar alimentos que pueden precipitar los síntomas: grasas, especias, picantes, cítricos, bebidas carbonatadas, alcohol, etc.
– Cenar 3 horas antes de acostarse.
– No fumar.
– No beber alcohol.
La elevación de la cabecera de la cama, en promedio 25 cm (se recomienda que sea entre 20 y 28 cm) (Figura 2A), o colocando una almohada en cuña con un angulación de 20 a 22° (Figura 2B), es una medida eficaz para el control del reflujo. Kaltenbach et al.19 realizaron una revisión sistemática de 100 artículos, incluyendo 16 ensayos clínicos, que evaluaron el impacto del estilo de vida en la ERGE. Los resultados muestran que la elevación de la cabecera de la cama y la posición de decúbito lateral izquierdo mejoran el tiempo total en que el pH esofágico es < 4,0 (evidencia B). La pérdida de peso mejoró los perfiles de pH y los síntomas (evidencia B). Se concluye que la disminución de peso y la elevación de la cabecera de la cama son intervenciones eficaces para control de la ERGE; sin embargo, durante el embarazo no se recomienda la disminución de peso.19,20
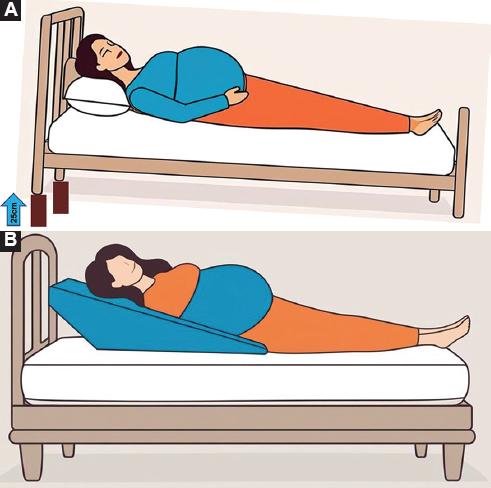
Figura 2 A: elevación correcta de la cabecera de la cama, en promedio 25 cm (se recomienda que sea entre 20 y 28 cm). Arte editorial: ©maindart a través de Canva.com. B: colocación correcta de una almohada en cuña, con angulación de 20 a 22°, para mantener una posición recta del tórax y el abdomen. Arte editorial: ©maindart a través de Canva.com.
En adultos se ha reportado que la posición de decúbito lateral izquierdo se asocia con un tiempo de exposición al ácido esofágico nocturno significativamente más corto y una depuración del ácido esofágico más rápida.20
Se recomienda una ingesta baja de alimentos grasos, realizar cinco a siete comidas al día, comer porciones pequeñas de alimento y evitar las comidas copiosas antes de dormir o acostarse. Con estos cambios se obtienen buenos resultados, pero no existen estudios que respalden estas recomendaciones. También se recomienda evitar el tabaco, la cafeína y el alcohol.16
Las terapias alternativas durante el embarazo, como la acupuntura, han demostrado que pueden mejorar la capacidad para comer y dormir, aunque con bajo nivel de evidencia (evidencia D).21
Tratamiento farmacológico
Debido a los problemas éticos de realizar ensayos con intervención farmacológica durante el embarazo, muchas de las recomendaciones sobre la seguridad de los fármacos se basan en reportes de casos, estudios de cohortes retrospectivas o estudios en animales.4
Actualmente están disponibles diversos fármacos para el control de la ERGE; sin embargo, existe un potencial riesgo para la mujer, el feto o el recién nacido, que debe ser informado a las pacientes. El periodo teratogénico crítico durante la gestación abarca los días 31 a 71 posteriores a la fecha de la última menstruación, en una mujer con ciclos regulares.22 La exposición a un potencial teratógeno durante este periodo puede provocar un efecto de «todo o nada», ya sea muerte fetal o supervivencia sin anomalías; por lo tanto, cualquier fármaco que no sea absolutamente necesario debe retrasarse hasta después del periodo posible de teratogenicidad.
La Food and Drug Administration (FDA) clasifica los fármacos, de acuerdo al grado de riesgo durante el embarazo, en seis categorías (Tabla 1).
Tabla 1 Clasificación de la Food and Drug Administration para fármacos durante el embarazo
| Clase | Comentarios |
|---|---|
| Categoría A | Estudios con diseño bien controlado en humanos no muestran riesgo fetal |
| Categoría B | Estudios en animales muestran que no hay riesgo, pero en humanos los estudios son inadecuados, o los estudios en animales muestran algún riesgo, pero no se respalda en estudios en humanos |
| Categoría C | Los estudios en animales muestran riesgos, pero los estudios en humanos son inadecuados o inexistentes, o no existen estudios en humanos o animales |
| Categoría D | Se han reportado anormalidades fetales en estudios en humanos, pero los beneficios potenciales superan el riesgo |
| Categoría X | Contraindicado en el embarazo por anomalías fetales en animales o humanos; los riesgos superan el beneficio |
| Categoría N | El fármaco no ha sido clasificado |
ANTIÁCIDOS
Su mecanismo de acción es neutralizando el ácido gástrico después de ser secretado.
Los antiácidos son la primera línea de tratamiento farmacológico para la ERGE durante el embarazo (Tabla 2). Aproximadamente el 30-50% de las embarazadas logran el control de los síntomas solo con antiácidos; proporcionan un alivio rápido y eficaz, aunque temporal, de la pirosis, y son seguros durante el embarazo y la lactancia.4
Tabla 2 Antiácidos en el embarazo
| Fármacos | Clase de la FDA | Comentarios |
|---|---|---|
| Antiácidos elaborados con aluminio, calcio o magnesio | Ninguna | Son los más recomendados para aliviar la pirosis o como rescate para el alivio inmediato de los síntomas de reflujo. Los que tienen calcio han demostrado un efecto en la prevención de la hipertensión y la preeclampsia. Los que tienen sulfato de magnesio reducen un 50% el riesgo de eclampsia |
| Trisilicato de magnesio | Ninguna | No se recomienda. Su uso prolongado se asocia con dificultad respiratoria fetal, hipotonía, afección cardiovascular y nefrolitiasis |
| Bicarbonato de sodio | Ninguna | No se recomienda. Se relaciona con alcalosis metabólica fetal y materna, y con sobrecarga hídrica |
FDA: Food and Drug Administration.
En el embarazo se recomienda utilizar antiácidos que contengan calcio, aluminio y magnesio, para aliviar la pirosis o como rescate para el alivio inmediato de los síntomas de reflujo.17
Los antiácidos que contienen calcio, en las dosis recomendadas, tienen un efecto en la prevención de la hipertensión y la preeclamsia (recomendación de grado A), aunado a que incrementan la suplementación de calcio. Tienen efectos adversos limitados, pero la ingesta excesiva de carbonato de calcio puede provocar el síndrome de leche-álcali en dosis mayores de 1.4 g/día de calcio elemental, con baja probabilidad de tener un efecto significativo en el recién nacido.23
Durante el embarazo se ha estudiado el efecto del hidróxido de aluminio y magnesio, el cual demostró lograr mayor control de la pirosis contra un placebo, pero no mejoró la náusea ni la regurgitación.24 El hidróxido de aluminio y magnesio con dimeticona mejora la pirosis en el 93% de las embarazadas.25 Los antiácidos con sulfato de magnesio reducen hasta un 50% el riesgo de eclampsia y, por lo tanto, disminuyen la incidencia de mortalidad materna.26
No se recomienda el uso de antiácidos que contengan bicarbonato o trisilicato de magnesio (recomendación de grado C). Los antiácidos con bicarbonato se relacionan con alcalosis metabólica fetal y materna, y sobrecarga hídrica.4 El uso prolongado y en dosis altas de trisilicato de magnesio se asocia con dificultad respiratoria fetal, hipotonía, afección cardiovascular y nefrolitiasis.27
ALGINATOS
Pertenecen a la familia de los antiácidos. Son polisacáridos aniónicos que se encuentran naturalmente en algas pardas. Actúan desplazando la bolsa de ácido gástrico posprandial, e impiden el re-reflujo de ácido. Al entrar en contacto con el ácido gástrico crean una barrera mecánica al precipitarse en forma de gel que protege el estómago proximal. Son seguros y eficaces en el embarazo.26,27
Lindow et al.26 evaluaron el efecto de un alginato bajo en sodio (Gaviscon Advance) en 146 embarazadas, y reportaron un adecuado control de los síntomas a los 10 minutos de tomar el antiácido en el 90% de ellas. Su uso a largo plazo mostró eventos adversos en la madre: hipertensión, náusea y diarrea. La tasa de eventos adversos en el feto y el neonato fue similar a la reportada en población general, por lo que fueron clasificados como probables o posibles.26
Los estudios realizados con Gaviscon líquido reportan que es efectivo y seguro durante el segundo y el tercer trimestres del embarazo, con mejoría de los síntomas en el 98% de las embarazadas, con disminución en la frecuencia, la intensidad y la duración de los síntomas de reflujo. Ningún estudio demostró eventos adversos para la madre o el neonato.28,29
SUCRALFATO
Es la segunda línea de tratamiento farmacológico, ante la persistencia de síntomas con el uso de antiácidos. Es un fármaco compuesto por un disacárido sulfatado y sales de aluminio. Es pobremente absorbido, lo que brinda seguridad en el embarazo y la lactancia (categoría B).
Su mecanismo de acción consiste en que la fracción disacárido sulfatado, en el estómago, reacciona con el ácido clorhídrico y forma una sustancia viscosa que se une a la mucosa lesionada, inactiva la pepsina y previene el desarrollo de úlceras. Puede estimular los mecanismos reparadores, como el aumento de la concentración de prostaglandinas en la mucosa.30
Ranchet et al.31 realizaron un ensayo clínico y evaluaron el efecto de sucralfato, comparado con cambios en estilo de vida, para el control de la pirosis y la regurgitación. Reportaron que el 90% de las embarazadas presentaron mejoría de los síntomas con sucralfato, frente a solo el 43% con los cambios en el estilo de vida, al mes de tratamiento.
No se han informado eventos adversos maternos ni fetales, y los estudios en animales demostraron su seguridad, sin efectos teratógenos.32
ANTAGONISTAS DE LOS RECEPTORES DE LA HISTAMINA (ARH2)
Se consideran la tercera línea de tratamiento para la ERGE durante el embarazo (categoría B).
La famotidina y la nizatidina se pueden combinar con antiácidos (recomendación grado B).
Los ARH2 inhiben competitivamente la unión de la histamina a los receptores de histamina 2, inhibiendo la secreción de ácido gástrico y la producción de pepsina y gastrina.33
El inicio del alivio de síntomas ocurre en aproximadamente 60 minutos, con una duración de 4 a 10 horas, lo que los hace útiles para el tratamiento a libre demanda. Se deben administrar antes de acostarse, en dosis única. En caso de uso a libre demanda, se tomarán 30 a 60 minutos antes del alimento desencadenante.34
Un metaanálisis comparó 2398 embarazadas expuestas a ARH2 en el primer trimestre con 119.892 embarazadas no expuestas. La odds ratio (OR) de malformación congénita fue de 1.14 (intervalo de confianza del 95% [IC95%]: 0.89-1.45). No hubo diferencias estadísticamente significativas en el riesgo de aborto espontáneo, menor tamaño para la edad gestacional o parto prematuro entre mujeres expuestas y no expuestas.35
La cimetidina puede ocasionar un efecto antiandrogénico en animales, con reducción de los testículos, la glándula prostática y las vesículas seminales.
La ranitidina demostró eficacia y seguridad en el embarazo, pero en 2018 fue descontinuada por la FDA.33
La famotidina no tiene estudios en animales que revelen toxicidad fetal o teratogenicidad.
La nizatidina, en estudios en conejos, causó más abortos espontáneos, menor peso fetal y menos fetos vivos. Estos hallazgos no se replicaron en estudios con ratones.36,37 Se reclasificó de categoría C a categoría B en el año 2000, con la recomendación de utilizarla solo en caso de clara necesidad.
INHIBIDORES DE LA BOMBA DE PROTONES (IBP)
Son la cuarta línea de tratamiento para la ERGE durante el embarazo (Tabla 3). Cuando los antiácidos y los ARH2 no son suficientes para el control de los síntomas, se recomienda usar IBP mas antiácidos como rescate (recomendación de grado C).
Tabla 3 Inhibidores de la bomba de protones en el embarazo
| Fármacos | Clase de la FDA | Comentarios |
|---|---|---|
| Omeprazol | C | Toxicidad fetal en animales. Reportes en humanos mencionan hallazgos similares |
| Lansoprazol | B | No se relaciona con toxicidad fetal o infertilidad. En animales se ha reportado bajo peso fetal |
| Pantoprazol | B | No se relaciona con toxicidad fetal o infertilidad. Reportes en humanos no han demostrado toxicidad fetal durante el primer trimestre |
| Esomeprazol | B | No se relaciona con toxicidad fetal o infertilidad. En humanos se sugiere que el riesgo de anomalías estructurales es bajo |
| Dexlansoprazol | B | No se relaciona con toxicidad fetal o infertilidad. La información es limitada. |
FDA: Food and Drug Administration.
Actúan suprimiendo la secreción de ácido gástrico mediante inhibición directa sobre la célula parietal gástrica. Las formulaciones disponibles se muestran en la tabla 3.
En términos de seguridad, la FDA clasifica al omeprazol como categoría C debido a su posible toxicidad fetal, con evidencia de estudios en animales; todos los demás son de categoría B.38 Todos son cancerígenos en ratones y ratas, pero no hay datos de daño fetal.
No hay evidencia procedente de ensayos clínicos aleatorizados o de estudios prospectivos sobre la eficacia de los IBP para el control de la pirosis o la regurgitación durante el embarazo ni durante la lactancia, y por lo tanto, los datos sobre su seguridad durante el embarazo son limitados.
Las recomendaciones de los expertos sugieren a los IBP para síntomas intratables o más preocupantes que no se controlan con las medidas anteriores.30,39
En un metaanálisis que incluyó 1530 embarazadas expuestas a IBP al menos en el primer trimestre, en comparación con 133,410 embarazadas no expuestas, la OR de malformación congénita fue de 1.12 (IC95%: 0.86-1.45). No hubo diferencias estadísticamente significativas en el riesgo de malformaciones importantes, aborto espontáneo o parto prematuro.40,41
Pasternak y Hviid, en un estudio de cohorte danés, analizaron más de 840,000 casos, entre enero de 1996 y septiembre de 2008. El estudio incluyó en el análisis a 5,082 embarazadas que estuvieron expuestas a IBP 4 semanas antes de la concepción y hacia el final del primer trimestre del embarazo. Se compararon con 21,811 embarazadas sin exposición a IBP. El riesgo para incidencia de malformaciones congénitas después de la exposición intrauterina fue bajo (OR de 1.1; IC95%, 0.91 – 1.34).42
En un metaanálisis se reportó un aumento estadísticamente significativo (p < 0.001) en el riesgo de asma en niños nacidos de madres que usaron IBP o ARH2 durante el embarazo.43
Dehlink et al.,44 en un estudio de cohorte, en un periodo de 10 años (1995-2004), evaluaron a 585,716 niños y encontraron que los expuestos a fármacos inhibidores del ácido (IBP, ARH2 y prostaglandinas) durante el embarazo, independientemente del tipo de supresor de ácido o del tiempo de exposición, tuvieron una OR para desarrollar alergias de 1,43 (IC95%: 1.29-1.59) y para desarrollar asma infantil de 1,51 (IC95%: 1.35-1.69).
El lansoprazol no ha demostrado toxicidad fetal o infertilidad; se ha reportado que en animales puede causar bajo peso fetal. La información sobre su uso durante el embarazo en humanos es limitada.
El pantoprazol no ha demostrado deterioro en la fertilidad ni daño fetal en animales. En humanos, no ha demostrado un incremento de malformaciones fetales durante su uso en el primer trimestre del embarazo.42,43
El esomeprazol, en estudios en animales, no ha demostrado alteraciones en la fertilidad ni daño fetal. Como no hay evidencia de una relación causal entre uso de esomeprazol durante el embarazo y malformaciones congénitas, especialmente en el primer trimestre, se sugiere que el riesgo de toxicidad en el desarrollo, incluidas anomalías estructurales, es bajo con esomeprazol. Sin embargo, se recomienda su uso con precaución hasta no contar con estudios bien controlados que confirmen esta suposición.42
El dexlansoprazol no ha demostrado tener un riesgo incrementado de malformaciones, pero hay muy pocos datos que sustenten su uso en el embarazo.
Existe un nuevo grupo de fármacos altamente eficaces para el tratamiento de la ERGE, llamados bloqueadores ácidos competitivos de potasio (vonoprazan, tegoprazan y fexuprazan); sin embargo, la ficha técnica de estos fármacos menciona que está contraindicado su uso durante el embarazo y la lactancia.1,45
En la tabla 4 se resumen los fármacos seguros durante el embarazo.
Tabla 4 Fármacos seguros para el tratamiento de la enfermedad por reflujo gastroesofágico durante el embarazo
| Fármacos | Dosis | Clase de la FDA |
|---|---|---|
| Antiácidos | ||
| Hidróxido de aluminio y magnesio | 5-10 ml, tomar 3-4 veces al día, administrar 1 h después del alimento. Dosis máxima 40 ml/día | Ninguna |
| Carbonato de calcio | 1-2 tabletas masticables de 500 mg, 3-4 veces al día, administrar 1-2 h después del alimento. Dosis máxima 12 tabletas al día | Ninguna |
| Alginatos | ||
| Gaviscon líquido | 10-20 ml, vía oral, 3 veces al día, administrar después del alimentos y al acostarse | Ninguna |
| Sucralfato | 1 g, vía oral, 3 veces al día, administrar 1 h antes del alimento | B |
| Antagonistas de los receptores de histamina 2 | ||
| Famotidina | 40 mg, vía oral, administrar cada 24 h antes de acostarse | B |
| Inhibidores de la bomba de protones | Administrar 30-60 min antes del desayuno | |
| Omeprazol | 20 mg cada 24 h, vía oral | C |
| Lansoprazol | 30 mg cada 24 h, vía oral | B |
| Pantoprazol | 40 mg cada 24 h, vía oral | B |
| Esomeprazol | 20 mg cada 24 h, vía oral | B |
| Dexlansoprazol | 60 mg cada 24 h, vía oral | B |
FDA: Food and Drug Administration.











 nueva página del texto (beta)
nueva página del texto (beta)


