Introducción
Los pacientes críticamente enfermos padecen dolor de moderada a severa intensidad, tanto en reposo como durante la realización de procedimientos habituales, es por eso que la sedación y la analgesia son parte integral en el manejo y cuidado de los pacientes en las Unidades de Cuidados Intensivos (UCI).1
La Asociación Internacional para el Estudio del Dolor define al dolor como «una experiencia sensorial y emocional desagradable asociada con un daño tisular real o potencial, o descrita en términos de daño».2
Diversos estudios muestran que la adecuada monitorización de la sedación y de la analgesia permite reducir el tiempo de ventilación mecánica, la estancia en la UCI, el número de infecciones nosocomiales, especialmente neumonía asociada a la ventilación mecánica e incluso reducción de la mortalidad;3-8 por lo tanto, la evaluación del dolor es fundamental en los pacientes críticamente enfermos.
La dificultad para comunicarse por el nivel alterado de conciencia, la sedación y la ventilación mecánica de los pacientes en las UCI complican la identificación del dolor,9 por lo que existen herramientas clínicas que han demostrado ser válidas y confiables para evaluar el dolor en este grupo de pacientes. Sin embargo, existen situaciones en las que estas escalas no son aplicables, por ejemplo, con Richmond Agitation Sedation Scale (RASS) ≤ -4.10 Se debe entonces explorar tecnologías que evalúen el dolor de manera objetiva.
La Escala de Comportamientos Asociados al Dolor (BPS, del inglés Behavioral Pain Scale) desarrollada por Payen,11 tiene una sensibilidad de 52.4% y una especificidad de 87.5% según un estudio realizado por Chen y colaboradores,12 con una puntuación mínima de 3, ausencia de dolor, a 12, dolor intenso. Por otro lado, la herramienta de observación del dolor en pacientes críticos (CPOT, del inglés Critical-Care Pain Observation Tool) desarrollada por Gélinas,13 tiene una sensibilidad de 86% y una especificidad de 78% para detectar dolor postquirúrgico severo cuando es > 2.14
Una herramienta de aparición relativamente reciente es el llamado índice de nocicepción analgesia (ANI, del inglés Analgesia Nociception Index), que mide la variabilidad de la frecuencia cardiaca a partir de la monitorización del electrocardiograma del paciente,15 generando un algoritmo que convierte la nocicepción en un valor absoluto entre 0 y 100 a través del análisis espectral.16,17 Este número es una estimación del equilibrio entre el sistema nervioso simpático y el parasimpático: ANI inferior a 50 corresponde a mayor actividad simpática (nivel de estrés alto, nocicepción alta); mientras que un ANI superior a 70 corresponde a mayor actividad parasimpática (nivel de estrés bajo y nocicepción baja).18,19 Por lo tanto, los valores meta del ANI se sitúan entre 50 y 70.
Consideramos que esta herramienta no ha sido completamente explorada en Medicina Crítica, pues ANI no se ha evaluado en pacientes de UCI ligeramente sedados, como se recomienda en las guías actuales para el manejo del dolor y la sedación, en quienes la evaluación del dolor puede representar un desafío. Por lo tanto, realizamos un estudio de exactitud diagnóstica para determinar si ANI puede predecir dolor en pacientes de UCI no comatosos e incapaces de reportar dolor, de acuerdo a las escalas clínicas que han demostrado ser válidas y confiables para evaluar el dolor: BPS y CPOT.
Material y métodos
Se realizó un estudio observacional, transversal, analítico, en una UCI de Tercer Nivel durante el periodo comprendido del 01 de Julio al 30 de Septiembre de 2021. Se incluyeron todos los pacientes con edad ≥ 18 años, ventilados mecánicamente y que se encontraban con sedación y/o analgesia; se seleccionaron los pacientes con RASS de -3 a -1 con incapacidad de comunicar la presencia o ausencia de dolor. Se excluyeron los pacientes con uso de fármacos que tengan efecto sobre la actividad del nodo sinusal (atropina, dopamina, dobutamina), presencia de arritmia cardiaca, frecuencia respiratoria menor a 9 ciclos por minuto, presencia de marcapasos y/o circulación extracorpórea.
El protocolo fue aprobado por el Departamento de Investigación del Hospital Español.
Procedimiento para la obtención de los datos
La medición del dolor se llevó a cabo de dos maneras distintas y de forma simultánea: clínicamente, utilizando las herramientas BPS y CPOT realizado por dos observadores diferentes: médico y enfermera; electrofisiológicamente por un tercer observador, utilizando el ANI registrado continuamente por el monitor ANI V2 rev 2.2.2.0® (MDoloris Medical Systems, Lille, Francia). Los observadores que utilizaron las escalas BPS y CPOT, y el observador del ANI desconocían las mediciones de los otros. Para fines del estudio se analizó el valor de ANI inmediato, que es un promedio calculado por el monitor, en un periodo de tiempo de 64 segundos. Las evaluaciones del dolor en cada paciente se realizaron en cuatro momentos distintos (Figura 1): minuto 0, minuto 4, minuto 8 y minuto 12, es decir, un total de cuatro mediciones por evaluación. Se tomaron en cuenta las tres condiciones en las que se pudo encontrar el paciente al momento de la evaluación: antes de cualquier procedimiento, durante el procedimiento de atención en UCI (no planeado previamente) y después del procedimiento, registrando cada dato en una hoja de trabajo previamente diseñada.
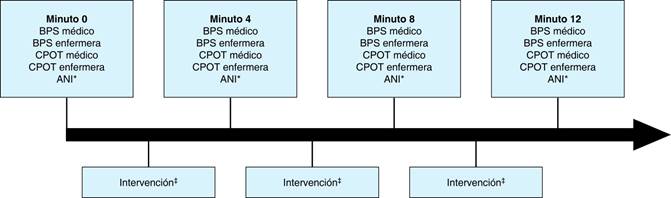
* ANI inmediato: calculado en un periodo de tiempo de 64 segundos.
‡ Procedimiento realizado: aspiración de secreciones por cánula orotraqueal o traqueostomía, colocación de sonda nasogástrica o nasoyeyunal, movilización en cama, aseo de cavidad oral, colocación de termómetro esofágico, broncoscopia, endoscopia.
BPS = escala de comportamientos asociados al dolor, CPOT = herramienta de observación del dolor en pacientes críticos, ANI = índice de nocicepción y analgesia.
Figura 1: Distribución de las evaluaciones clínicas y electrofisiológicas del dolor realizadas en los pacientes en cuatro momentos distintos.
Análisis estadístico. Se utilizó la prueba de Shapiro-Wilk para determinar la normalidad de las variables cuantitativas. En caso de no tener una distribución normal, se resumieron a través de mediana y rango intercuartil. Los datos cualitativos se expresan en frecuencias y porcentajes.
Se determinó la capacidad discriminativa de ANI para detectar dolor a través del área por debajo de curvas ROC (Característica Operativa de Receptor) y se analizaron las diferencias entre ellas aceptando como significante una «p» menor de 0.05. Para este análisis se evaluó el desempeño de ANI para detectar el dolor definido por una calificación BPS > 3 o CPOT > 2, medidos por personal médico y de enfermería, lo cual dio como resultado cuatro curvas ROC. Se identificó también el punto de corte que mejor se desempeña en cada una de ellas.
La sensibilidad, la especificidad, el valor predictivo positivo, el valor predictivo negativo, la razón de verosimilitud positiva y razón de verosimilitud negativa se calcularon de acuerdo con definiciones estándar. Para lo anterior, se dicotomizaron tanto la calificación de ANI (menos de 50 puntos identifica dolor) como las calificaciones de BPS y CPOT (> de 3 puntos y > 2 puntos identifican dolor, respectivamente).
Para el recuento y el análisis estadístico se utilizó el programa XLSTAT 23.1.1
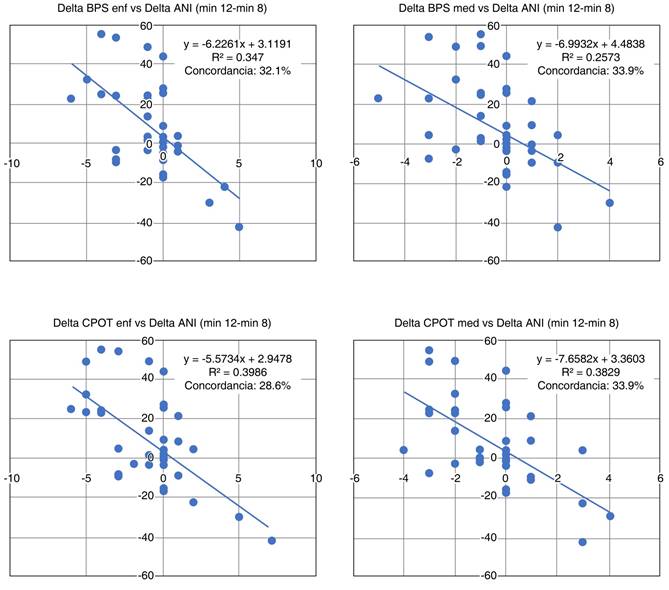
Análisis post hoc. Se realizó un análisis post hoc para determinar la concordancia entre los cambios observados por BPS y CPOT y los cambios registrados por ANI antes y después de las intervenciones realizadas a los pacientes en el momento de la evaluación, dichas intervenciones fueron desde procedimientos habituales de una UCI, tales como aspiración de secreciones por cánula orotraqueal o traqueostomía, movilización en cama, aseo de cavidad oral, colocación de sonda nasogástrica, hasta procedimientos como una broncoscopia o panendoscopia.
Para este análisis se identificaron los cambios simultáneos concordantes, definidos como descensos de ANI e incremento de la calificación de las escalas clínicas o como ascensos de ANI y decremento de la calificación de las escalas clínicas. El total de cambios concordantes se dividió entre el total de cambios registrados y se expresó en valores porcentuales. Estos cambios se analizaron en tres momentos distintos durante los 12 minutos que duró cada sesión. Por ejemplo, al valor de ANI registrado después del procedimiento, se le restó el valor de ANI registrado antes del procedimiento; lo mismo se hizo con las calificaciones de BPS y CPOT registrados tanto por la enfermera como por el médico. A la diferencia le denominamos Delta y se acompaña de la especificación de los tiempos y del personal que hizo la evaluación. Así, «Delta BPS 4-0 enf» significa que se calculó el cambio de BPS registrado entre el minuto 4 y el minuto 0, medido por una enfermera y se comparó con el cambio de ANI en ese periodo de tiempo. Para este análisis se describen 12 combinaciones posibles (Anexos 1 a 4). Además, se analizó la correlación entre los cambios a través del coeficiente de correlación de Pearson.
Resultados
Se realizaron en total 56 evaluaciones, con duración de 12 minutos, cada una con 4 mediciones. Se obtuvo un total de 224 mediciones del dolor en 23 pacientes, con un mínimo de 2 y un máximo de 4 mediciones por paciente. En la Tabla 1 se resumen las características demográficas y clínicas de los pacientes.
Tabla 1: Características demográficas y clínicas de los pacientes.
| Por número de pacientes | N = 23 |
|---|---|
| Edad* | 66 (49-73) |
| Mujeres, n (%) | 8 (29.6) |
| Índice de masa corporal (kg/m2)* | 25 (23.0 - 28.5) |
| Tipo de diagnóstico, n (%) | |
| Quirúrgicos | 6 (26) |
| No quirúrgico | 17 (74) |
| Diagnósticos, n (%) | |
| Insuficiencia respiratoria aguda | 14 (60) |
| Choque séptico | 4 (17) |
| Hemorragia de tubo digestivo | 2 (8.7) |
| Gran quemado | 1 (4.3) |
| Resección de tumor neuroendocrino | 1 (4.3) |
| Esofagectomía | 1 (4.3) |
| Neumonía por SARS-CoV-2 | 11 (47.8) |
| RASS‡ | -3 (-3 , -2) |
| Gravedad SAPS 3* ,§ | 58 (50.7 - 70.0) |
| Riesgo de morir por SAPS 3 (%)* | 29 (18 - 56) |
| Por número de evaluaciones, n (%) | N = 56 |
| Modalidad de ventilación mecánica | |
| Asistida/controlada por presión | 15 (26.79) |
| Asistida/controlada por volumen | 20 (35.71) |
| Presión soporte | 16 (28.57) |
| ASV¶ | 5 (8.93) |
| Fármacos usados para la sedación y analgesia, n (%) | |
| Propofol | 35 (62.00) |
| Midazolam | 3 (5.36) |
| Lorazepam | 4 (7.14) |
| Dexmedetomidina | 39 (69.64) |
| Fentanilo | 49 (87.50) |
| Sulfentanilo | 3 (5.36) |
| Paracetamol | 10 (17.86) |
* Las variables cuantitativas se expresan en mediana y rango intercuartil.
‡ Escala de sedación Richmond Agitation-Sedation Scale.
§ Modelo de gravedad Simplified Acute Physiologic Score.
¶ Modalidad de ventilación asistida adaptable.
La capacidad discriminativa de ANI evaluada por curvas de Característica Operativa del Receptor (ROC) para cada escala clínica y cada tipo de profesional se presenta en la Figura 2. El mejor desempeño se observa cuando ANI predice el dolor medido por las enfermeras con la escala CPOT (AUC 0.817, IC del 95%: 0.743 a 0.892); sin embargo, esta área no es estadísticamente diferente del área de la predicción del dolor medido por médicos con la escala CPOT (AUC 0.800 (IC de 95%: 0.724 a 0.876) ni por médicos con la escala BPS (0.802, IC de 95%: 0.738 a 0.866); sin embargo, sí fue estadísticamente diferente compararla con el área que predice la presencia de dolor con la escala BPS aplicada por enfermeras (AUC 0.779, IC de 95%: 0.712 a 0.846, p = 0.034).
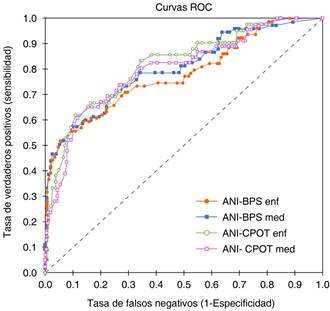
ANI-BPS enf AUC = 0.779 (IC 95%: 0.712-0.846); p < 0.0001
ANI-BPS med AUC = 0.802 (IC 95%: 0.738-0.866); p < 0.0001
ANI-CPOT enf AUC = 0.817 (IC 95%: 0.743-0.892); p < 0.0001
ANI-CPOT med AUC = 0.800 (IC 95%: 0.729-0.876); p < 0.0001
Figura 2: Capacidad discriminativa de ANI para detectar dolor estimado por BPS >3 y CPOT >2.
ANI = índice de nocicepción y analgesia, BPS = escala de comportamientos asociados al dolor, CPOT = herramienta de observación del dolor en pacientes críticos, enf = enfermera, med = médico. IC95% = intervalo de confianza de 95%. AUC = área por debajo de la curva ROC. La significancia estadística descarta la hipótesis de que el AUC es de 0.5. El AUC de ANI-CPOT enf y de ANI-BPS enf, son estadísticamente diferentes (p = 0.034).
Los mejores puntos de corte para las cuatro curvas, oscilaron entre 52 y 55 puntos, con una sensibilidad que osciló entre 51.9 y 65.2% y una especificidad que osciló entre 84.3 y 94.5%.
En la Tabla 2 se presentan los parámetros de prueba diagnóstica de ANI para la presencia de dolor medido con cada una de las escalas clínicas y por médicos y enfermeras. Es notoria la baja sensibilidad y alta especificidad de ANI en las cuatro estimaciones. El valor predictivo positivo y la razón de verosimilitudes positiva fueron mayores para BPS medido tanto por médicos como enfermeras.
Tabla 2: Parámetros de rendimiento de prueba diagnóstica.
| Prueba | Estándar | Sen | Esp | TFP | TFN | VPP | VPN | RV+ | RV- |
|---|---|---|---|---|---|---|---|---|---|
| ANI < 50 | BPS médico > 3 | 0.440 | 0.980 | 0.020 | 0.560 | 0.917 | 0.777 | 22.00 | 0.57 |
| ANI < 50 | BPS enfermera > 3 | 0.418 | 0.979 | 0.021 | 0.582 | 0.917 | 0.755 | 19.90 | 0.59 |
| ANI < 50 | CPOT médico > 2 | 0.478 | 0.921 | 0.079 | 0.522 | 0.611 | 0.872 | 6.05 | 0.57 |
| ANI < 50 | CPOT enfermera > 2 | 0.524 | 0.923 | 0.077 | 0.476 | 0.611 | 0.894 | 6.81 | 0.52 |
ANI = índice de nocicepción y analgesia (un valor menor de 50 predice la presencia de dolor); BPS = escala de comportamientos asociados al dolor (un valor mayor de 3 se asocia a la presencia de dolor); CPOT = herramienta de observación del dolor en pacientes críticos (un valor mayor de 2 se asocia a la presencia de dolor); Sen = sensibilidad; Esp: especificidad; TFP = tasa de falsos positivos; TFN = tasa de falsos negativos; VPP = valor predictivo positivo; VPN = valor predictivo negativo; RV+ = razón de verosimilitud positivo: RV- = valor de verosimilitud negativo.
La concordancia entre los cambios registrados por ANI y los registrados con cada escala clínica, osciló entre 28 y 41%. El coeficiente de correlación osciló entre 0.507 y 0.715. El coeficiente de determinación osciló entre 0.257 y 0.511 (Anexos 1 a 4).
Discusión
Los pacientes adultos internados en UCI por afecciones médicas, quirúrgicas o por trauma suelen padecer dolor, tanto en reposo como durante intervenciones propias del cuidado habitual; además, la realización de procedimientos suele generar aún más dolor.10 De hecho, el dolor intenso asociado a procedimientos se asocia con complicaciones graves (por ej., taquicardia, bradicardia, hipertensión, hipotensión, desaturación, bradipnea y mala adaptación a la ventilación mecánica),20 que podrían prevenirse con la evaluación adecuada del dolor y la utilización de analgesia preventiva.
Cuando existe la imposibilidad de medir dolor en pacientes que no pueden comunicarlo, las guías de práctica clínica para el manejo del dolor, la agitación, sedación, el delirium, la inmovilidad y las alteraciones del sueño en pacientes adultos en la UCI del 2018 (PADIS 2018),10 recomiendan que: se deben explorar otras tecnologías que puedan ser útiles para la evaluación del dolor. La tecnología que evalúa la variabilidad en la frecuencia cardiaca (por ej., el índice de analgesia nocicepción, puede ser relevante).
ANI es una tecnología emergente, por eso existen pocos estudios prospectivos que lo validen. Broucqsault-Dédrie y su equipo17 realizaron un estudio observacional prospectivo en dos Unidades de Cuidados Intensivos, donde incluyeron 41 pacientes con ventilación mecánica invasiva y sedación profunda. En este estudio, ANI fue significativamente menor durante un estímulo doloroso (mediana de 69, RIC: 55-78), en comparación con el estado de reposo (mediana de 85, RIC: 67-96), «p» < 0.0001, sin encontrarse correlación significativa entre ANI y BPS durante el estímulo doloroso (r2 = 0.221, p = 0.165). La ausencia de correlación puede explicarse porque ANI es una medida indirecta que detecta el estrés, sin diferenciar que se deba a dolor, ansiedad y/o miedo.
Por otro lado, Chanques G y colaboradores15 realizaron un estudio similar al nuestro, donde compararon ANI con BPS antes, durante y después de los procedimientos de atención de rutina en pacientes no comatosos en estado crítico. ANI inmediato fue la medición de dolor con más capacidad discriminativa; se correlacionó significativamente con BPS (r2 - 0.30; IC de 95% -0.37 a -0.25; p < 0.001). Para un punto de corte de ANI inmediato de 42.5, la sensibilidad, la especificidad y los valores predictivos positivos y negativos fueron 61.4, 77.4, 37.0 y 90.4%, respectivamente. Ellos concluyen que a pesar de la baja sensibilidad y especificidad, ANI inmediato > 43 tuvo un valor predictivo negativo de 90%, por lo tanto, es de mayor beneficio para excluir el dolor significativo.
Chanques15 determina la presencia de dolor con BPS mayor a 4 puntos y en enfermos con RASS de -3 a más de 0; mientras que en nuestro trabajo el puntaje de BPS fue de más de 3 puntos y los enfermos tenían un RASS de -3 a -1. Estas diferencias pueden explicar el hecho de que nuestro mejor punto de corte de ANI fue más alto y que utilizando el punto de corte de 50, ANI tuvo una sensibilidad baja y una especificidad muy alta, lo cual le confiere un valor predictivo positivo y una razón de verosimilitud positiva muy altos, utilizando BPS como estándar. En nuestro estudio también se explora el desempeño de ANI con otra escala clínica (CPOT) y las diferencias en los resultados cuando son aplicadas por profesionales diferentes; el rendimiento de ANI utilizando CPOT como estándar fue inferior que cuando utilizamos BPS y no hubo diferencias entre profesionales.
Además, analizamos la concordancia de los cambios inducidos por procedimientos que podían generar dolor, observando que la concordancia es muy baja (de 28 a 41%) al comparar los cambios de ANI con los cambios de BPS o de CPOT. El coeficiente de determinación identifica que de 26 a 51% de las variaciones de ANI son explicadas por las variaciones de BPS y CPOT (Anexos 1 a 4); lo cual orienta a pensar que ANI se modifica por otras variables que afectan el equilibrio entre el sistema nervioso simpático y el parasimpático y no solamente el dolor.
Conclusiones
El índice de nocicepción analgesia (ANI) tiene buena capacidad discriminativa para detectar dolor en el enfermo crítico bajo ventilación mecánica y sedación (RASS de -3 a -1).
Nuestros resultados identifican un punto de corte óptimo más alto que el publicado para determinar la presencia de dolor.
Un punto de corte > 50 de ANI para detectar dolor es altamente específico y tiene un buen desempeño como prueba diagnóstica positiva (alto VPP y alta RV+).
La concordancia y la correlación entre los cambios de ANI y los de las escalas clínicas son bajas. Esto nos orienta a pensar que el dolor no fue la única variable que explica los cambios en ANI; seguramente otros factores influyeron en modificar el equilibrio entre el simpático y el parasimpático.
Es importante reconocer las limitaciones en este trabajo, pues fue un estudio unicéntrico, con un número pequeño de pacientes, los casos no fueron consecutivos y las mediciones donde se detectó dolor fueron relativamente escasas. Otra limitación fue la curva de aprendizaje en la aplicación de BPS y CPOT, que podría afectar la precisión en el diagnóstico del dolor.
Los resultados identifican una tecnología con potencial para su utilización en el enfermo crítico. Son necesarios más estudios que corroboren nuestros resultados y aclaren los puntos de corte a utilizar en la práctica clínica.











 nova página do texto(beta)
nova página do texto(beta)