Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Boletín médico del Hospital Infantil de México
versão impressa ISSN 1665-1146
Bol. Med. Hosp. Infant. Mex. vol.66 no.4 México Jul./Ago. 2009
Caso clínico patológico
Adolescente con síndrome de inmunodeficiencia adquirida de transmisión perinatal
Adolescent with AIDS of perinatal transmission
Y. Rocío Peña-Alonso1, Luis Romano-Mazzotti2, Aarón Pacheco-Ríos3
1 Departamento de Patología Clínica y Experimental, Hospital infantil de México Federico Gómez, México, D. F., México.
2 Departamento de Infectología, Hospital infantil de México Federico Gómez, México, D. F., México.
3 Subdirección de Enseñanza, Hospital infantil de México Federico Gómez, México, D. F., México.
Autor de correspondencia:
Dra. Yolanda Rocío Peña Alonso.
Correo electrónico: rociopena@hotmail.com
Fecha de recepción: 31-01-2009.
Fecha de aprobación: 10-03-2009.
Resumen de la historia clínica
Caso A-2004-02
Adolescente masculino de 14 años de edad quien fue referido al hospital de una organización no gubernamental cuatro días antes de su muerte por presentar dificultad respiratoria.
Entre sus antecedentes se refiere que el padre falleció a los 24 años de edad por virus de inmunodeficiencia humana/síndrome de inmunodeficiencia adquirida (VIH/SIDA) y la madre, de 18 años de edad, abandonó al paciente cuando tenía seis meses de vida. La madre adoptiva tenía 52 años, escolaridad primaria y no padecía ninguna enfermedad; se ignoraba el parentesco con el paciente. Se desconocen otros antecedentes heredofamiliares.
Originario y residente de Tlalnepantla, estado de México, vivía en casa habitación prestada con todos los servicios, convivía con un perro. Baño y cambio de ropa diario.
La madre adoptiva refirió que fue producto de gesta I y que nació por parto eutócico; desconocía otros datos del período prenatal y perinatal. No conocía los datos de la alimentación previa, pero inició la ablactación a los seis meses de edad con papillas de frutas y verduras, y se integró a la dieta familiar al año de edad. Aunque no mostró la cartilla de vacunación, refirió que se le habían aplicado todas las vacunas. A los seis meses fijó la mirada, tenía sostén cefálico y sonrisa social; a los ocho meses se sentó y a los 10 meses comenzó a caminar; tuvo control de esfínteres a los tres años de edad. Un año antes de su ingreso asistía a primer año de secundaria; sin embargo, su aprovechamiento era deficiente, por lo que abandonó los estudios debido a su enfermedad.
Entre sus antecedentes patológicos se refirió que a los seis meses de edad la prueba de ELISA fue positiva, se repitió al año de edad resultando negativa. A los ocho años padeció varicela y a los 13 años presentó una dermatitis por herpes, acudió a un médico particular, quien solicitó nuevamente ELISA que fue positiva para VIH. No se refirió el haber realizado prueba confirmatoria. Nunca recibió tratamiento con antirretrovirales y, como dato importante, refirió pérdida de peso de 12 kg en los últimos dos meses. Antecedentes alérgicos, quirúrgicos y transfusionales negativos.
Inició su padecimiento final cuatro días antes de ingresar al hospital con tos disneizante, cianozante y emetizante, de predominio nocturno, dificultad respiratoria progresiva de tres días de evolución manifestada por tiraje intercostal y posteriormente aleteo nasal; tenía además dolor abdominal en hipocondrio izquierdo de intensidad moderada, que remitía con paracetamol, asociado a los accesos de tos. Había sido tratado con ranitidina a dosis no especificada. Fue referido a este hospital de un albergue para niños.
Exploración física: peso 15 kg, talla 140 cm, perímetro cefálico 49 cm, perímetro abdominal 49 cm, frecuencia cardiaca 120 x minuto, frecuencia respiratoria 46 x minuto, tensión arterial 80/ 50 mm Hg, temperatura 36.5 °C, llenado capilar menor a tres segundos. Se encontró íntegro, caquéctico, en mal estado de hidratación, con ojos hundidos, pupilas isocóricas normorefléxicas, ambas membranas timpánicas hiperémicas, lengua saburral, lesiones blanquecinas en mucosa oral y úlcera en amígdala derecha. Cuello con ganglios sub mandibulares, tórax simétrico con tiros intercostales, aleteo nasal, estertores crepitantes enambas bases pulmonares, ruidos cardiacos sin alteraciones, abdomen plano, hígado palpable a 2-2-2 cm del borde costal sobre líneas convencionales, peristalsis normal, genitales externos hipotróficos (Tanner I). Extremidades torácicas y pélvicas con disminución acentuada de tejido celular subcutáneo y masa muscular. Valoración de Glasgow 15/15, reflejos osteotendinosos normales. Los exámenes de laboratorio se muestran en el cuadro 1. La radiografía del tórax mostró infiltrado basal izquierdo. Se manejó con ayuno, soluciones de base a requerimientos normales, trimeto-prim con sulfametoxazol, ceftazidima, amikacina y ranitidina. Fue valorado por el Servicio de Infectología y se sustituyó ceftazidima por ceftriaxona. Los exámenes reportaron: urea de 239 mg/dL, creatinina 5.9 mg/dL, glucosa 76 mg/dL, cloro 85 mEq/L, sodio 130 mEq/L, potasio 1.5 mEq/L; por lo que se inició corrección de potasio. Fue valorado por el Servicio de Nefrología debido a insuficiencia renal. Presentó deterioro respiratorio por lo que fue necesario intubarlo. Al día siguiente de su hospitalización continuaba inestable a pesar del manejo con aminas y cargas de cristaloides. Se le transfundió concentrado de eritrocitos sin que se observaran cambios hemodinámicos. Se inició tratamiento antirretroviral con lopinavir/ritonavir, zidovudina y lamivudina. Fue valorado por oftalmología y se le diagnosticó retinopatía isquémica y hemorragia del vitreo en el ojo izquierdo. Se agregó anfotericina B al tratamiento y se transfundió concentrado de eritrocitos debido a inestabilidad hemodinámica e hipotensión.
Al segundo día de internamiento estaba afebril pero inestable, sin datos de sangrado, con pupilas anisocóricas con respuesta a la luz del lado derecho, Glasgow 6/15 a expensas de apertura ocular y función verbal. La radiografía de tórax mostró desviación del mediastino hacia la izquierda; clínicamente presentaba hipoventilación por lo que se diagnosticó atelectasia izquierda (Cuadro 2).
La tomografía axial computada de cráneo mostró atrofia cortical y edema cerebral leve sin hipertensión intracraneal. Presentó sangrado en la cavidad oral por lo que se transfundió plasma fresco congelado sin complicaciones. Al tercer día de hospitalización presentaba hipotensión persistente por lo que se incrementaron las aminas, sin mejoría; tenía una frecuencia cardiaca de 40 x minuto, sin embargo, a pesar del manejo presentó paro cardiorrespiratorio irreversible a maniobras de reanimación.
Discusión del caso
El día de hoy discutiremos el caso de un adolescente de 14 años de edad que ingresó a nuestro hospital el 13 de enero de 2004 y falleció tres días después.
Existen dos datos clínicos en la historia de este paciente que llaman poderosamente nuestra atención: el peso de 15 kg que presentaba al ingreso y los antecedentes heredo familiares, donde se refiere que el padre murió por infección por VIH/SIDA a los 24 años y que el paciente fue abandonado a los seis meses por la madre.
De forma retrospectiva, es fácil determinar que el paciente murió por complicaciones secundarias a la infección por VIH, pero el análisis de su historia desde el nacimiento nos da la oportunidad de revisar varios conceptos sobre esta enfermedad.
El antecedente de un padre con infección por VIH y abandono por la madre, de la cual no conocemos más datos, son la primera "bandera roja" sobre el riesgo que tenía este paciente al haber sido expuesto verticalmente al VIH y la obligación de su pediatra de diagnosticar oportunamente esta infección.
Las guías de diagnóstico y manejo de VIH en pediatría de los Institutos Nacionales de Salud de los Estados Unidos de Norteamérica, así como las emitidas por CONASIDA en nuestro país, establecen que el diagnóstico en niños con sospecha de exposición vertical al VIH debe hacerse utilizando métodos dirigidos a la identificación del virus y no de anticuerpos, ya que existe la posibilidad de encontrar anticuerpos anti-VIH de origen materno en lactantes no infectados, así como la posibilidad de un resultado falso-negativo secundario a la pobre producción de anticuerpos por el sistema inmunológico inmaduro del lactante.1,3
Para diagnosticar la infección por VIH en un lactante menor de 18 meses se requieren dos pruebas virológicas (PCR-DNA o PCR-RNA) positivas en dos muestras separadas.1
En el año 2004, cuando ingresó este paciente al hospital, el consenso internacional para diagnóstico de infección por VIH recomendaba no utilizar la determinación de anticuerpos anti-VIH (ELISA) en menores de 18 meses de edad. Actualmente se recomienda el uso de pruebas tanto virológicas como serológicas después de los seis meses para descartar la infección por VIH en lactantes menores de 18 meses de edad.1
En el caso de nuestro paciente, se realizaron dos pruebas buscando anticuerpos anti-VIH antes de los 18 meses. La primera fue positiva y la segunda fue negativa. En el momento del resultado positivo del primer ELISA, se debió haber realizado una prueba virológica para establecer el diagnóstico de infección por VIH. Es difícil interpretar el resultado negativo del segundo ELISA y debemos tomar en cuenta la calidad del laboratorio que hizo este reporte.
Suponemos que este paciente adquirió la infección por VIH de la madre. El riesgo de transmisión vertical del VIH de una madre infectada al recién nacido es de 13-40% por parto natural. La administración de antirretrovirales pre, trans y postparto, el nacimiento por cesárea, así como evitar la lactancia materna, han logrado disminuir el riesgo de infección en el recién nacido a menos de 2%. Es importante subrayar que entre 33 y 50% de casos de VIH de transmisión vertical ocurre por lactancia materna.4
En nuestro paciente se refiere un peso de 15 kg a su ingreso, lo cual significa un déficit ponderal de 70%. El síndrome de desgaste es una complicación frecuente de la infección por VIH, además de ser una condición definitoria de SIDA y de estadio clínico C.5 La pérdida de peso que caracteriza a este síndrome comprende una desregulación del metabolismo secundaria a varios factores: 1. La propia infección por VIH; 2. Las infecciones oportunistas, que además comprometen la tolerancia a la vía oral como la candidiasis esofágica, o impiden la adecuada absorción de nutrientes como en la diarrea causada por bacterias y parásitos; y 3. El catabolismo secundario a neoplasias asociadas al VIH.68
El manejo del síndrome de desgaste asociado a VIH debe incluir control de la replicación viral, tratamiento y prevención de infecciones oportunistas y una nutrición adecuada.89
El síndrome de desgaste se define como una pérdida de más de 10% del peso basal asociado a diarrea crónica, historia de fiebre o debilidad por más de 30 días en ausencia de otra explicación que no sea la infección por VIH. Antes del desarrollo de la terapia antirretroviral altamente activa (TARAA), el síndrome de desgaste se encontraba entre las cuatro condiciones definitorias de SIDA más frecuentes junto con neumonía por Pneumocystis jirovecii, infección por micobacterias del complejo avium (MAC) y candidiasis esofágica.6,11
En países industrializados, la incidencia de este síndrome ha disminuido gracias al diagnóstico e inicio temprano de la TARAA para controlar la infección.
El último reporte de UNAIDS estima que en el mundo viven 33 millones de personas con VIH; durante el año 2007, se registraron 2.7 millones de casos nuevos y de éstos, 370 000 pertenecieron al grupo de menores de 15 años.12 En México, CENSIDA registró 59 casos nuevos de SIDA y 40 con infección por VIH en menores de 15 años durante las primeras 46 semanas del año 2008.13
Los avances médicos en el tratamiento del VIH en los últimos 25 años, han permitido que actualmente la supervivencia de un paciente con infección por VIH que recibe tratamiento oportuno, en países desarrollados, sea mayor a 40 años. 14,15
Desafortunadamente, estos logros no se han traducido en una disminución en la incidencia de nuevos casos a nivel mundial (uno de los objetivos del Milenio de la Organización de las Naciones Unidas), y la principal razón de esto sigue siendo la desinformación de la población y la pobre preparación de los trabajadores de salud en los países en vías de desarrollo.12
En nuestro caso, durante los tres días que el paciente estuvo hospitalizado, se documentó una neumonía adquirida en la comunidad, candidiasis oral y desequilibrio hidroelectrolítico.
Es importante considerar que el diagnóstico de desequilibrio hidrolectrolítico sea debido al estado de homeorrexis secundario al síndrome de desgaste y que más que un desequilibrio, se trate de la adaptación del organismo a este estado de desnutrición de tercer grado.
Por las condiciones del paciente a su ingreso, se iniciaron antibióticos de amplio espectro, así como trimetoprim sulfametoxazol para cubrir P. jirovecii, y anfotericina B para cubrir hongos. Llama la atención que en la historia clínica no se reporta la cuenta de linfocitos CD4+ ni la carga viral. Se inició manejo antirretroviral con zidovudina, lamivudina y ritonavir/lopinavir. Es importante señalar que el inicio inmediato de terapia antirretroviral, aún en pacientes graves, sigue siendo un tema controversial. A pesar de estas medidas el paciente se deterioró rápidamente, requiriendo intubación endotraqueal y apoyo con aminas; finalmente presentó falla orgánica múltiple y falleció.
Este caso es interesante por varios factores poco comunes en el VIH/SIDA pediátrico de transmisión vertical:
La mayoría de los pacientes con infección vertical por VIH presenta datos de inmunocompromiso importante de forma temprana y si no reciben tratamiento antirretroviral fallecen antes de los cinco años de edad. Las manifestaciones clínicas más comunes en estos pacientes incluyen: retardo en el desarrollo psicomotor, bajo peso o pérdida de peso, candidiasis oral/esofágica y neumonía.4,16
Existe un grupo de pacientes conocidos como progresores lentos, en los que la replicación viral es mínima, lo cual retarda el daño al sistema inmune por varios años, logrando llegar hasta la adolescencia con pocos síntomas.
Se han analizado las características virales e inmunológicas que expliquen la lenta progresión en estos pacientes. Los pacientes con mutación homocigota del gen que codifica el correceptor CCR5 (CCR5-delta32) de los linfocitos CD4 presentan inmunidad total a la infección por VIH, mientras que los pacientes con mutación en un solo alelo de esta región se comportan como progresores lentos. También se han identificado fenotipos virales asociados a una progresión más lenta a la inmunosupresión. A pesar de estos factores, en la mayoría de pacientes pediátricos que se comportan como progresores lentos no es posible encontrar una razón que explique este fenómeno.16-21
Sería interesante conocer el estatus de CCR-delta32 del paciente para poder explicar la ausencia de síntomas durante sus primeros 10 años de vida, además de conocer un poco más sobre el cuadro de varicela que presentó a los ocho años, ya que pudiera darnos una idea sobre su estado inmunológico a esa edad; aunque aparentemente se trató de un episodio autolimitado sin mayores complicaciones. En cambio, a los 13 años se refiere una infección por herpes virus, que hizo sospechar la infección por VIH y, a pesar de que no contamos con más datos de este episodio, en el caso de haberse tratado de un cuadro de zoster, podemos asumir que el paciente ya estaba con un grado de inmunosupresión importante.
Para concluir, los diagnósticos de este paciente son:
1. SIDA, estadio clínico C y estadio inmunológico probablemente 3, aunque no se tiene cuenta de linfocitos CD4+.
2. Candidiasis mucocutánea.
3. Síndrome de desgaste.
4. Desequilibrio hidroelectrolítico.
5. Atrofia cerebral.
6. Insuficiencia renal.
7. Neumonía.
8. Choque séptico.
Causa directa de muerte: choque séptico con foco pulmonar.
Este paciente representa la desinformación que aún existe sobre la infección del VIH, que si bien es una enfermedad incurable, los esquemas antirretrovirales actuales permiten que los pacientes puedan gozar de una buena calidad de vida por períodos cada vez mayores.14,15
Además, el paciente discutido ilustra de manera dramática la historia natural de la infección por VIH de transmisión vertical. Dramática porque fallamos como sistema médico al ignorar varias oportunidades de intervenir y mejorar el pronóstico del paciente. La muerte de este niño debe servir para recordarnos que el VIH no es una enfermedad restringida a personas con conductas de alto riesgo y que afecta a pacientes de todas las edades, origen étnico, ocupaciones, preferencias sexuales y estrato socioeconómico.
Pregunta: en los hallazgos radiológicos se mencionó la presencia de atrofia cerebral. ¿Esta alteración es frecuente en pacientes con VIH?
Respuesta: así es, en un estudio realizado por los servicios de la Clínica de Inmunodeficiencias/VIH (CLINDI) y Neurología de nuestro Hospital, y publicado en el Boletín Médico del Hospital Infantil de México en enero de 2008, se describen las alteraciones neurológicas encontradas en 127 pacientes pediátricos con infección por VIH. La atrofia cerebral (cortical o central) se documentó en 42.5% de los pacientes, lo cual es un hallazgo frecuente en esta población.22
Hallazgos anatomopatológicos
La autopsia se hizo tres horas después de la muerte. Se tomaron cultivos de líquido cefalorraquídeo, pulmones, bazo, hígado y sangre que fueron negativos; del intestino grueso se aisló Escherichia coli y del intestino delgado, levaduras.
Lo más llamativo de este caso era el grado de desnutrición que mostraba el cuerpo de este adolescente; el desarrollo era armónico y la edad aparente menor a la cronológica; el tejido subcutáneo y muscular eran escasos, los genitales externos estaban poco desarrollados y no había vello en el pubis ni en las axilas. La piel presentaba petequias en todo el cuerpo, equimosis en los talones, cicatrices irregulares en la pared lateral izquierda del tórax y escaras sobre la columna lumbar que en conjunto medían aproximadamente 1.5 cm2.
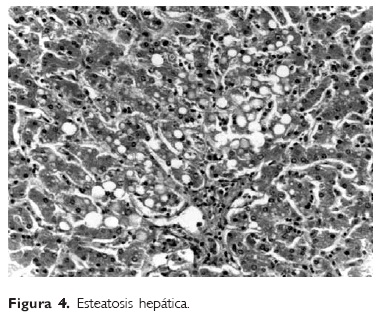
A la apertura de las cavidades se encontró escaso líquido cetrino en la cavidad abdominal. La mucosa de la tráquea y bronquios mostraba congestión, los pulmones presentaban adherencias, y en el pulmón izquierdo la pleura era blanco-amarillenta y estaba engrosada (Fig. 1); ambos pulmones estaban aumentados de consistencia y peso (derecho 310 vs 210 g, izquierdo 350 vs 190 g); al corte mostraban zonas de hemorragia y consolidación. Los cortes histológicos mostraron: paquipleuritis del pulmón izquierdo, hemorragia intralveolar y bronconeumonía bilateral (Fig. 2). Con excepción del esófago, que presentaba úlceras colonizadas por hifas y levaduras (Fig. 3), en el resto del aparato digestivo no había alteraciones. El hígado pesaba 350 vs 210 g y mostraba esteatosis, que es un hallazgo en pacientes con desnutrición (Fig. 4). El páncreas, vesícula biliar y vías biliares no mostraban alteraciones.



Los riñones mostraron puntilleo hemorragia) en la médula y los cortes histológicos revelaron glomeruloesclerosis segmentaria y focal, así como nefritis túbulo intersticial (Fig. 5); estas alteraciones son frecuentes en los pacientes infectados con VIH. En las glándulas suprarrenales había adrenalitis focal y algunas células mostraban alteraciones compatibles con infección viral; sin embargo, no se observaron inclusiones. La médula ósea mostraba hipoplasia leve de las tres series, y los testículos mostraban atrofia de los túbulos seminíferos y fibrosis intersticial.
El cerebro mostraba atrofia supratentorial leve (peso 1 150 vs 1 351 g) y al corte, hemorragias puntiformes, principalmente en la sustancia blanca (Fig. 6). Los cortes histológicos mostraron nodulos de microglía, más aparentes en los núcleos básales y mesencéfalo (Fig. 7), así como infiltrado inflamatorio perivascular en algunos vasos sanguíneos y focos de ependimitis; estas alteraciones son características de las encefalitis virales. Había, además, microcalcificaciones perivasculares en núcleos básales (Fig. 8). Todos estos hallazgos son compatibles con una encefalitis viral. La presencia de adrenalitis y encefalitis permiten sospechar una infección por citomegalovirus; sin embargo, la presencia de microcalcificaciones en los núcleos basales son muy sugestivas de que las lesiones cerebrales posiblemente fueron causadas por el VIH.



Los diagnósticos finales en este caso son:
1. SIDA de transmisión vertical.
2. Desnutrición grado III (síndrome de desgaste),
a. Esteatosis hepática.
3. Bronconeumonía por germen no identificado.
4. Paquipleuritis del pulmón izquierdo.
5. Hemorragia pulmonar bilateral.
6. Esofagitis aguda ulcerada con levaduras e hifas de Candida sp.
7. Glomeruloesclerosis segmentaria y focal.
8. Nefritis túbulo intersticial.
9. Atrofia cerebral supratentorial leve.
10. Encefalitis y ependimitis compatible con encefalitis viral.
11. Retardo del desarrollo sexual.
12. Atrofia testicular.
13. Datos anatómicos de choque,
a. Necrosis tubular aguda.
Se atribuye la causa inmediata de la muerte a choque séptico secundario a neumonía de la comunidad.
Referencias
1. Working Group on Antiretroviral Therapy and Medical Management of HIV-Infected Children (U.S.), United States. Health Resources and Services Administration. National Institutes of Health (U.S.). Guidelines for the use of antiretroviral agents in pediatric HIV infection; 2008 Junio Bethesda, MD: National Institutes of Health; 2008. [ Links ]
2. WHO case definitions of HIV for surveillance and revised clinical staging and immunological classification of HIV-related disease in adults and children. Geneva: WHO Press; 2007. [ Links ]
3. Guia de Manejo Antirretroviral de las Personas con VIH. Mexico, D.F.: Secretaria de Salud; 2007. [ Links ]
4. American Academy of Pediatrics. Human immunodeficiency virus infection. En: Pickering LK, Baker CJ, Long SS, Mc Millan JA, editores. Red Book: 206 Report of Committe on Infections Diseases. 27th ed. Elk Grove Village, III: American Academy of Pediatrics; 2006. p. 378-401. [ Links ]
5. 1993 revised classification system for HIV infection and expanded surveillance case definition for AIDS among adolescents and adults. MMWR Recomm Rep. 1992; 41: 1-19. [ Links ]
6. Shikuma CM, Valcour VG, Ratto-Kim S, et al. HIV-associated wasting in the era of highly active antiretroviral therapy: a syndrome of residual HIV infection in monocytes and macrophages? Clin Infect Dis. 2005; 40: 1846-8. [ Links ]
7. Kotler D, Wanke C. Management of HIV wasting syndrome: a consensus conference. J Acquir Immune Defic Syndr. 2004; 37 Suppl 5: S261. [ Links ]
8. Grinspoon S, Mulligan K. Weight loss and wasting in patients infected with human immunodeficiency virus. Clin Infect Dis. 2003; 36: S69-78. [ Links ]
9. Corcoran C, Grinspoon S. Treatments for wasting in patients with the acquired immunodeficiency syndrome. N Engl J Med. 1999; 340: 1740-50. [ Links ]
10. Wanke CA, Silva M, Ganda A, et al. Role of acquired immune deficiency syndrome-defining conditions in human immunodeficiency virus-associated wasting. Clin Infeet Dis. 2003; 37 Suppl 2: S81-4. [ Links ]
11. Dworkin MS, Williamson JM. AIDS wasting syndrome: trends, influence on opportunistic infections, and survival. J Acquir Immune Defic Syndr. 2003; 33: 267-73. [ Links ]
12. UNAIDS. Report on the global HIV/AIDS epidemic 2008: executive summary. Geneva: Joint United Nations Programme on HIV/AIDS (UNAIDS); 2008. [ Links ]
13. El VIH/SIDA en México. 2008. Available from: http://www.censida.salud.gob.mx/interior/cifras.html [ Links ]
14. Bhaskaran K, Hamouda O, Sannes M, et al. Changes in the risk of death after HIV seroconversion compared with mortality in the general population. JAMA. 2008; 300: 51-9. [ Links ]
15. Life expectancy of individuals on combination antiretroviral therapy in high-income countries: a collaborative analysis of 14 cohort studies. Lancet. 2008; 372: 293-9. [ Links ]
16. Ofori-Mante JA, Kaul A, Rigaud M, et al. Natural history of HIV infected pediatric long-term or slow progressor population after the first decade of life. Pediatr Infect Dis J. 2007; 26: 217-20. [ Links ]
17. De Angelis DS, Freiré WS, Pannuti CS, Succi RC, Machado DM. CCR5 genotypes and progression to HIV disease in perinatally infected children. Braz J Infect Dis. 2007; 11: 196-8. [ Links ]
18. Mikhail M, Wang B, Saksena NK. Mechanisms involved in non-progressive HIV disease. AIDS Rev. 2003; 5: 230-44. [ Links ]
19. Ioannidis JP, Contopoulos-loannidis DG, Rosenberg PS, et al. Effects of CCR5-delta32 and CCR2-641 alíeles on disease progression of perinatally HIV-1-infected children: an international meta-analysis. AIDS. 2003; 17: 1631-8. [ Links ]
20. Contopoulos-Ioannidis DG, O'Brien TR, Goedert JJ, Rosenberg PS, loannidis JP. Effect of CCR5-delta32 heterozygosity on the risk of perinatal HIV-1 infection: a meta-analysis. J Acquir Immune Defic Syndr. 2003; 32: 70-6. [ Links ]
21. Ometto L, Bertorelle R, Mainardi M, et al. Polymorphisms in the CCR5 promoter region influence disease progression in perinatally human immunodeficiency virus type I-infected children. J Infect Dis. 2001; 183: 814-8. [ Links ]
22. Capristo-Gonzalez F, Barragán-Pérez E, Pavía-Ruz N, et al. Manifestaciones neurológicas en pacientes pediátricos y adolescentes mexicanos infectados con VIH/SIDA. Experiencia del Hospital Infantil de México Federico Gómez. Bol Med Hosp Infant Mex. 2008; 65: 6-12. [ Links ]














