ANTECEDENTES
Según datos de la Federación Internacional de Diabetes (IDF) 8.3% de la población mundial padece diabetes mellitus y se espera que el número de individuos con la enfermedad se incremente a más de 592 millones en los próximos 25 años. Sudamérica y Centroamérica aportan 24 millones.1 En Colombia se describen tres estudios con prevalencias variables según los criterios de inclusión, la Encuesta Nacional de Salud 2007 encontró prevalencia de 3.5%, posteriormente en 2008 se creó la Cuenta de Alto Costo donde Antioquia aportó 16% y se reportó prevalencia de 2.2 en mujeres y 1.4 en hombres. La Encuesta Nacional de Demografía y Salud de 2010 encontró prevalencia de 11.2%.2-4 Según Aschner y colaboradores, en Colombia 7 a 9% de la población mayor de 20 años tiene diabetes mellitus tipo 2 con prevalencia cinco veces menor en áreas rurales.5 El control de la diabetes mellitus debe ser temprano y efectivo con el objetivo de prevenir complicaciones crónicas y evitar el efecto nocivo de la memoria metabólica (efecto legado).6 El uso de un objetivo de HbA1c de 6.5% para el diagnóstico de diabetes y como meta terapéutica se basa en estudios que siguen vigentes (United Kingdom Prospective Diabetes Study 1998), donde se demostró que la diabetes mellitus tipo 2 adecuadamente controlada reduce la incidencia de complicaciones crónicas atribuidas a la hiperglucemia crónica (retinopatía, nefropatía y neuropatía).7,8 En los pacientes con terapia dual que continúen con HA1c fuera de metas después de tres meses las guías de tratamiento de la diabetes mellitus tipo 2 recomiendan considerar triple terapia.9 Las terapias tradicionales generalmente actúan en la célula beta o en la función de la insulina. Asimismo, los terapias de nueva generación, como los inhibidores de dipeptidil peptidasa 4 (iDPP4), los agonistas del péptido similar al glucagón tipo 1 (AGLP1) y los inhibidores del cotransportador de sodio-glucosa tipo 2 (iSGLT2) actúan en la célula alfa o en la liberación del glucagón.10 Las guías de práctica clínica AACE/ACE 2017 no se oponen a la combinación de un AGLP-1 y iSGLT2 como tratamiento doble o triple9 y en la actualización de la Asociación Americana de Diabetes (ADA) y la Asociación Europea para el Estudio de la Diabetes (EASD) de 2017 no pudo hacerse una recomendación basada en evidencia para la administración de esta combinación debido a la falta de datos disponibles que apoyan esta práctica.11
Metodología
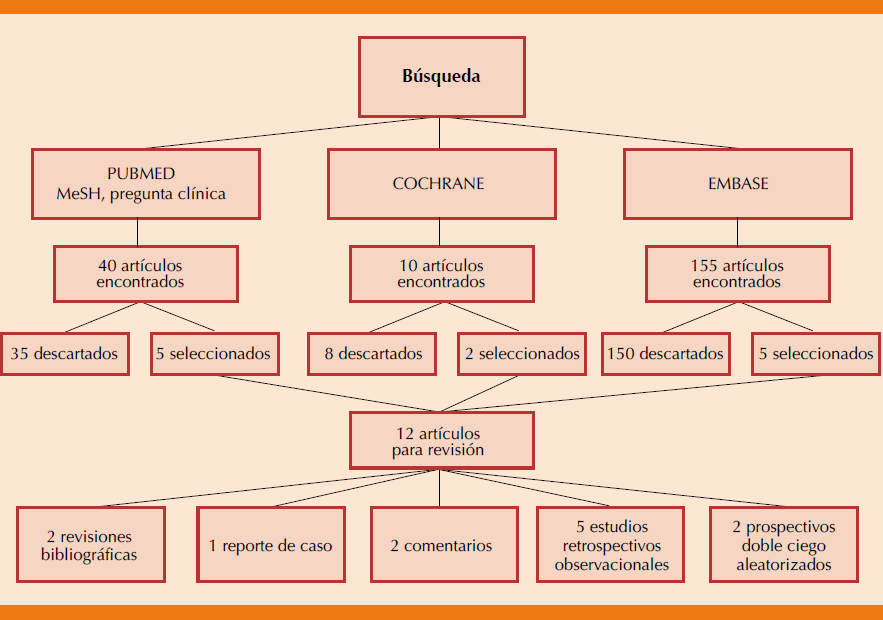
La revisión bibliográfica requirió el desarrollo de criterios para los tipos de estudios que se incluirían en el análisis. Se identificaron los descriptores o términos MeSH equivalentes al lenguaje documental o controlado. De la misma manera se hizo referencia a las siglas y variantes derivadas del tema central, para estructurar la estrategia de búsqueda bibliográfica, acudiendo a los mecanismos de recuperación de información de bibliografía relevante y pertinente que ofrece la base de datos PubMed sobre el tema de análisis. De la anterior búsqueda se obtuvieron 40 resultados de los que se descartaron 35 y se incluyeron 5. En Cochrane se obtuvieron 10 resultados de los que dos cumplieron criterios. En Embase se obtuvieron 155 resultados de los que cinco cumplieron criterios. En total se seleccionaron 12 artículos de los que dos son revisiones bibliográficas, un reporte de caso, dos comentarios, cinco estudios observacionales retrospectivos y dos estudios prospectivos doble ciego con distribución al azar (Figura 1).
Fisiopatología y mecanismos de acción
En pacientes normoglucémicos hay equilibrio entre células alfa (glucagón) y células beta (insulina) para lograr la homeostasia de glucosa óptima, pero en los pacientes con diabetes mellitus tipo 2 existe resistencia basal a la insulina que lleva a hiperinsulinemia, generando a largo plazo tolerancia a concentraciones altas de glucosa con déficit de insulina por pérdida progresiva de células beta, así como por desdiferenciación.12,13 El aumento en el número de las células alfa pancreáticas altera la homeostasia en el islote con el posterior aumento del glucagón posprandial y de la producción de glucosa endógena.13
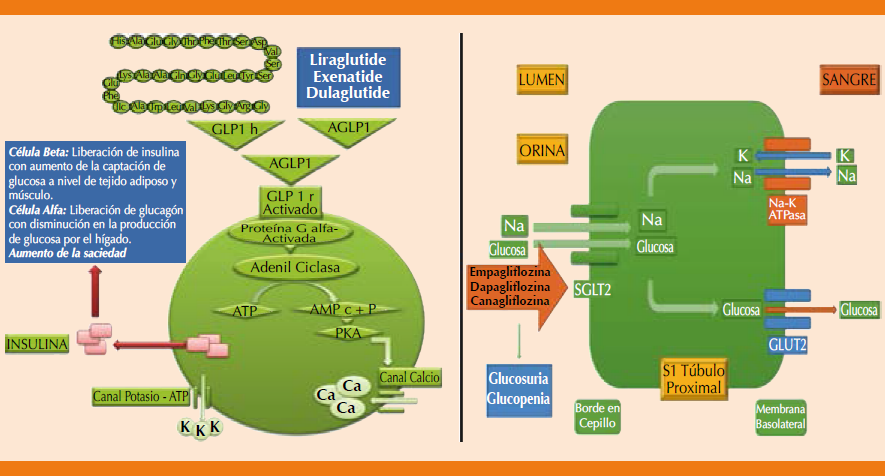
Normalmente el péptido similar al glucagón tipo 1 (GLP-1) es secretado tras la ingestión de comida, sintetizado por las células L localizadas predominantemente en la mucosa intestinal de íleon y el colon.14 Su vida media es de dos minutos15,16 y su acción es disminuir la glucemia estimulando la secreción de insulina y reduciendo la secreción de glucagón por las células pancreáticas.17 Este efecto parece estar disminuido en pacientes con diabetes mellitus tipo 2 en comparación con sujetos sanos, pero conserva algún nivel de respuesta glucémica a la acción del AGLP1.18 Los primeros AGLP-1 (lixisenatida y exenatida) derivaron de la exendina 4, péptido de 39 aminoácidos descubierto en la saliva de Heloderma suspectum (monstruo de Gila) con homología de 53% con el GLP-1 humano.19 Posteriormente se desarrollaron AGLP1 con homología estructural al GLP-1 nativo y aumentaron su vida media mediante modificaciones en su molécula, como la adición de un ácido graso (liraglutida), una molécula de albúmina (albiglutida) o la fracción Fc de la inmunoglobulina G (dulaglutida).20-22 Figura 2
En individuos sanos el riñón filtra aproximadamente 180 gramos de glucosa/día en los túbulos proximales. Normalmente 90% de la glucosa filtrada es reabsorbida en el primer segmento (S1) del túbulo por el transportador de alta capacidad y baja afinidad (SGLT2), difundiéndola posteriormente en la membrana basolateral a través del GLUT2. El resto es reabsorbido en el segmento distal (S3) del túbulo por el transportador de baja capacidad y alta afinidad SGLT1, difundiendo la glucosa en la membrana basolateral a través del GLUT1.25 Algunos estudios sugieren que la hiperglucemia crónica genera regulación a la alta en la actividad y la expresión del transporte SGLT2 y GLUT2.26,27 Rossetti y colaboradores publicaron desde 1987 los resultados con florizina, glucósido extraído de la corteza del manzano, que redujo la glucemia en ratas pancreatectomizadas y bloqueaba SGLT1 y SGLT2.25 Sin embargo, la florizina no tuvo utilidad clínica por su degradación intestinal y su inhibición simultánea de SGLT1 a nivel gástrico. Por ello se desarrollaron inhibidores selectivos de SGLT2,28 de administración oral con una sustitución en su estructura molecular que los hizo resistentes a la inactivación intestinal. Su vida media varía entre 10.6 y 17.8 horas, por lo que se pueden administrar una vez al día.29 Los iSGLT2 eliminan 60-80 gramos de glucosa al día por orina y este efecto es independiente de la función de la célula beta y del tiempo de evolución de la diabetes mellitus tipo 2, por lo que pueden prescribirse en cualquier momento de la enfermedad (Figura 2).30
La terapia con insulina produce aumento de peso generando más necesidad de la misma en un esquema repetitivo.31,32 Los estudios clínicos ya han demostrado que la adición de iSGLT2 a los iDPP4 mejora las concentraciones de glucosa con pérdida significativa de peso,33,34 y al tener en cuenta que los pacientes con diabetes mellitus tipo 2 tienen de base aumento del glucagón y de la gluconeogénesis hepática,35-39 se ven beneficiados con la administración de AGLP1.29,40 Asimismo, los iSGLT2 también producen aumento del glucagón, gluconeogénesis hepática29,41 y riesgo de cetoacidosis euglucémica, efectos que podrían contrarrestarse con los AGLP1, dando soporte fisiológico a su combinación.
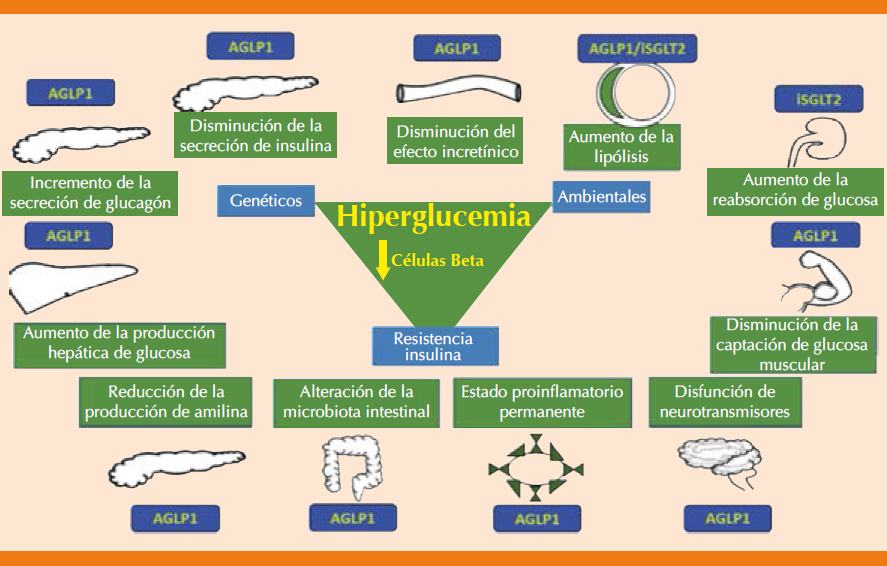
Lo primero que se podría decir en relación con la combinación de iSGLT2 (acción independiente de insulina) más AGLP1 (acción dependiente de insulina) es que tiene un soporte en los tiempos de sus mecanismos de acción, debido a que los iSGLT2 proporcionan sus efectos protectores cardiovasculares a través de mecanismos más hemodinámicos a corto plazo: 3-6 meses EMPA REG,42 mientras que los AGLP1 los proporcionan teóricamente más a través de acción antiaterogénica y antiinflamatoria a largo plazo: 12 meses LEADER43 y SUSTAIN,44 lo que hace que esta combinación produzca protección cardiovascular a corto y largo plazos. Lo segundo que debe resaltarse es propuesto por DeFronzo en una publicación reciente, teniendo en consideración que la combinación de los AGLP1 y los iSGLT2 comparten un número de acciones metabólicas, cardiovasculares y renales, propone que el sinergismo de ambas moléculas podría corregir, en teoría, al menos siete de los ocho componentes del octeto ominoso.45 Los AGLP1 mejoran la liberación de insulina,46-48 estimulan la transcripción/biosíntesis de insulina, regulan a la alta el GLUT 2 y mejoran la transcripción/actividad de la glucocinasa,49-52 inhibiendo la secreción de glucagón.53 Además, reducen la producción de gluconeogénesis hepática y ejercen un efecto en el sistema nervioso central suprimiendo el apetito en el núcleo hipotalámico;54 también corrigen el defecto incretínico, promueven la pérdida de peso55 que indirectamente disminuye la resistencia y, por tanto, aumenta la sensibilidad en 25-30% en el tejido muscular y hepático.56 Los iSGLT2, por otro lado, generan glucosuria57-59 con posterior disminución de la glucemia y de la glucotoxicidad.41,60 Teóricamente el único componente del octeto ominoso que no se interviene directamente es la resistencia a la insulina en el adipocito; sin embargo, podría considerarse un efecto indirecto por la acción positiva de los AGLP1 y los iSGLT2 en el perfil lipídico acentuado con la pérdida de peso y la disminución de la resistencia a la insulina.61 Se ha planteado un nuevo concepto que tiene en cuenta otras variables en relación con la fisiopatología de la diabetes. Shwartz y colaboradores proponen el llamado “onceno atroz” (Figura 3) que pone como principal elemento la anormalidad de la célula beta más disminución en su número, con un esquema donde hay interacción de predisposición genética, resistencia a la insulina, elementos ambientales, estilo de vida y respuesta inmuno/inflamatoria alterada. Este esquema reconoce tres vías adicionales que generan hiperglucemia: cambios en la microbiota intestinal, reducción en la producción de amilina por la alteración de la célula beta (vaciamiento gástrico acelerado con aumento en la absorción de glucosa en el intestino y aumento de la glucemia posprandial) y un estado inflamatorio que genera aumento en la demanda de insulina, todos ellos teóricamente cubiertos con los AGLP1.62,63
En tercer lugar podría plantearse la combinación fundamentada en sus mecanismos de acción y los estudios disponibles en relación con las variables de interés. Por ejemplo, en cuanto al control glucémico representado en HbA1c, los AGLP1 redujeron 1.2-1.4% en pacientes con diabetes mellitus tipo 2 iniciando en 8-8.2%43 y, por otro lado, los iSGLT2 redujeron HbA1c 0.8-1.0% en pacientes con diabetes mellitus tipo 2 iniciando en 8-8.2%.64 Al evaluar la pérdida de peso los iSGLT2 repercutieron a través de la pérdida de calorías por la orina65,66 y los AGLP1 a través de la disminución del apetito y el retraso del vaciamiento gástrico.67
Si se evalúa el tejido graso también encontramos efecto. Los iSGLT2 en pacientes con diabetes mellitus tipo 2 mal controlados redujeron el peso corporal total expresado en masa de grasa, tejido adiposo visceral y subcutáneo al medirse por absorciometria dual de rayos X y resonancia magnética.68 La liraglutida en pacientes con diabetes mellitus tipo 2 repercute en este mismo aspecto69 y, además, a nivel hepático con reducción del hígado graso.70,71 La presión arterial también es foco de estudio, los iSGLT2 repecutieron a través de la natiuresis con reducción del volumen intravascular72,73 y los AGLP1 produjeron un efecto leve repercutiendo a través de su acción vasodilatadora y por natriuresis leve.74,75 Si tenemos en cuenta el efecto en la célula beta, los AGLP1 mejoran su función a las 8 horas e incluso se demostró efecto después de tres años,47,48,76-79 también estimula su neogénesis y modula su apoptosis80,81 y, por otro lado, los iSGLT2, al revertir la glucotoxicidad, mejoran la función de la célula beta.82 En cuanto a protección renal, ya se ha demostrado que la empagliflozina y la liraglitida redujeron la filtración glomerular, la progresión a macroalbuminuria y la necesidad de terapia de reemplazo renal en pacientes con diabetes mellitus tipo 2.65,67 En relación con las hipoglucemias la combinación de estas terapias tiene muy baja probabilidad de producirla. En los estudios grandes de empagliflozina (EMPA REG),42 liraglutida (LEADER)43 y semaglutida (SUSTAIN-6)44 las hipoglucemias fueron similares e incluso menores que en los grupos placebo.
Estudios de la combinación
Las publicaciones en relación con la combinación son limitadas. El estudio CANVAS, que incluyó 4330 pacientes, doble ciego, con distribución al azar, se realizó para evaluar a la semana 18 la eficacia y seguridad de la canagliflozina en pacientes con diabetes mellitus tipo 2 que ya recibían otros tratamientos. De este estudio se analizó un subgrupo de 95 pacientes que tenían AGLP1 de base y se concluyó que la adición de canagliflozina 100 y 300 mg mejora la HbA1c 1 y 1.06%, respectivamente, el índice de masa corporal y la presión arterial (7.1 y 2.6 mmHg, respectivamente) en comparación con un grupo placebo.83 Aunque fue una muestra limitada con seguimiento corto, tuvo un diseño cerca de lo ideal con una combinación secuencial. Se encontró también el reporte de un paciente de 52 años de edad con diabetes mellitus tipo 2 mal controlada (HA1c 9.7%) con evolución de 20 años y complicaciones microvasculares. Lo particular del paciente era que tenía obesidad mórbida y recibía dosis altas de insulina, peso de 209.5 kg e índice de masa corporal de 61.2. Tenía, además, presión arterial de 225/110 mmHg y apnea del sueño. Se indicó dapagliflozina más liraglutida con lo que se redujo el valor de HA1c hasta 5.4% con pérdida de peso de 73.5 kg y mejoría de las cifras tensionales con alivio de los síntomas de apnea del sueño,84 lo que apoya posiblemente esta respuesta particular en variables genéticas en receptores GLP1 (hiperrespondedores).85
En relación con los estudios retrospectivos se revisaron cuatro. El primero a mencionar se realizó en 14 pacientes con diabetes mellitus tipo 2, con mal control metabólico, el grupo tenía edad media de 54 años con tiempo de evolución de la enfermedad de 18.5 años, HbA1c promedio de 10.1% y peso de 113.3 kg. Se adicionó inicialmente AGLP1 durante 20 semanas con reducción de HA1C 2.9% y 4.9 kg; posteriormente dapagliflozina para evaluar el efecto en HbA1c y el peso, alcanzando a las 20 semanas efecto en HbA1C 4.5% y en el peso 2.6 kg. Por último, a las 48 semanas la disminución de la HbA1c fue de 4.4% y en el peso de 5.4 kg, resultados estadísticamente significativos.86 El segundo estudio para mencionar se realizó en Escocia, con una cohorte de 85 pacientes que recibían tratamiento con AGLP1 y posteriormente con dapagliflozina durante un promedio de 3-18 meses. El tiempo de evolución de la diabetes mellitus tipo 2 fue, en promedio, de 13 años con edad media de 57 años. De los pacientes evaluados, 74 tomaban liraglutida y 11 exenatida, sin especificarse el tiempo de administración; comenzaron con una HbA1c media de 9.1%. Se evaluó HbA1c a las 12 semanas de 8% (p < 0.001). La presión arterial, el peso, el perfil lipídico, las transaminasas y la tasa de filtración glomerular de base con medición posteriormente a las 12 semanas no tuvieron diferencias significativas.87 Saroka y colaboradores realizaron otro estudio en Nueva York con 75 pacientes, en su mayoría estadounidenses obesos, de edad media (49-67 años) con duración media de diabetes mellitus tipo 2 de 8-20 años. Los pacientes recibían tratamiento con AGLP1 en intervalo de 12 a 106 meses previo a la adición de canagliflozina en pacientes distribuidos así: 62.7% liraglutida, 25.3% exenatida semanal (LAR) y 12% exenatida cada 12 horas con HbA1c basal promedio de 7.94%. Se adicionó canagliflozina en un intervalo de duración de 7.8-13.6 meses a dosis de 300 mg/día en una tercera parte y 100 mg en dos terceras partes. La HbA1c y el peso disminuyeron significativamente: 0.39% y 4.6 kg, respectivamente. También hubo disminución significativa en la presión arterial sistólica y aumento de HDL no significativo.88
El último estudio retrospectivo a mencionar se realizó en Madrid, España, con dos cohortes en el “mundo real”. El objetivo principal fue evaluar la efectividad y la seguridad en la reducción de peso y HbA1c en pacientes con diabetes mellitus tipo 2 con múltiples tratamientos de base más la combinación de dapagliflozina, durante al menos 12 meses, y AGLP1. Se evaluó a las 24 y 52 semanas. El objetivo secundario fue comparar las diferencia de la HbA1c, el peso, la presión arterial, el perfil lipídico, la filtración glomerular y los efectos secundarios entre esta cohorte de 109 pacientes con otro grupo de 104 pacientes tratados con dapagliflozina, pero sin AGLP1 de base. El grupo con AGLP1; liraglutida 72.5%, exenatida semanal (LAR) 20.2%, exenatida diario 2.8% y lixisenatida 4.6% redujeron HbA1c y peso antes del inicio de dapagliflozina, mientras que el grupo sin AGLP1 aumentaron HbA1c y peso. Al iniciar dapagliflozina hubo una reducción significativa de HbA1c en ambas cohortes, con disminución significativamente mayor en el grupo sin AGLP1 al hacer análisis incluso multivariado y al considerar los pacientes con HbA1c mayor a 7% (p < 0.0001 en ambos grupos). En cuanto al peso, hubo disminución significativa en ambos grupos a las 24 y 52 semanas, pero el grupo sin AGLP1 perdió más peso, 2.3 vs 3.9 kg a las 24 semanas y 2.4 vs 4.8 kg a las 52 semanas. El comportamiento en esta variable se debió probablemente a los múltiples mecanismos neuronales/hormonales y periféricos implicados en el equilibrio de la ingesta y regulación de la energía, reforzando otras vías implicadas en ese equilibrio y limitando la pérdida de peso con otros medicamentos. Se demostró que la adición secuencial (mundo real) de dapagliflozina en pacientes con diabetes mellitus tipo 2 que tenían de base AGLP1 reduce significativamente HbA1c, el peso y la presión arterial sistólica a las 52 semanas.89,90
Un estudio multicéntrico prospectivo de 52 semanas hecho en Japón con 62 pacientes mayores de 20 años y HA1c de 7-10.5% tuvo como objetivo evaluar la eficacia y seguridad de un inhibidor de SGLT2 (luseogliflozina), adicionada a pacientes con diabetes mellitus tipo 2 considerados con mal control metabólico a pesar de dieta, ejercicio y tratamiento de base con liraglutida. Se encontró disminución en HbA1c de 0.58-0.78%, glucemia en ayunas de 28.5-35.7 mg/dL, glucemia posprandial de 61.9-51.1 mg/dL y peso 2.47-2.95 kg a la semana 52 con p < 0.0001. Además, Seino y colaboradores encontraron incremento de la sensibilidad a la insulina usando el índice de Matsuda, disminución de la grasa corporal a través de análisis de impedancia bioeléctrica, disminución de la presión arterial y de la frecuencia cardiaca.91,92
El estudio DURATION 8 con seguimiento de 28 semanas efectuado en 109 centros de 6 países, se realizó doble ciego y con distribución al azar. Se distribuyeron al azar 611 pacientes con diabetes mellitus tipo 2 con antecedente de enfermedad de 7.6 años, HbA1c basal promedio de 9.3% y tratamiento con metformina al menos durante ocho semanas para recibir exenatida semanal (LAR) más dapagliflozina en inicio simultáneo, exenatida LAR o dapagliflozina. El objetivo primario fue evaluar los cambios en HA1c y los secundarios fueron los cambios en glucemia en ayunas, glucemias poscarga 2 horas, pacientes con HbA1c < 7% y cambios en el peso, entre otros. El grupo que combinó exenatida LAR/dapagliflozina tuvo mayor efecto en la presión arterial (4.1 mmHg), HbA1c (-2% IC95%: -2.1 a -1.8) y fue significativamente superior a cualquiera de los dos medicamentos independientes en relación con los objetivos secundarios. Se concluyó que el inicio simultáneo de exenatida LAR más dapagliflozina mejoró las mediciones glucémicas y disminuyó los factores tradicionales de riesgo cardiovascular. La combinación fue bien tolerada con similares eventos adversos en los grupos y no se reportaron hipoglucemias. La combinación no tuvo efectos aditivos en el control glucémico y 45% de los pacientes con la combinación logró la meta de HbA1c < 7%, con la observación que la combinación fue simultánea y no secuencial. Sí hubo efectos aditivos en el peso, presión arterial sistólica y triglicéridos, lo que sugiere mecanismos de acción independientes en relación con estas variables.93
En la actualidad está en curso un estudio por DeFronzo y colaboradores que pretende comparar y evaluar el efecto de la combinación de liraglutida más canagliflozina con ambos tratamientos en monoterapia, teniendo en cuenta variables como la producción de glucosa hepática, glucosa plasmática, HbA1c, peso, hígado graso y grasa visceral.94 El estudio AWARD-10, con distribución al azar, de brazos paralelos, controlado con placebo y doble ciego (fase 3B), evaluará la reducción de las concentraciones de HbA1c y la seguridad de la combinación de dulaglutida más iSGLT2 en pacientes con diabetes mellitus tipo 2 con o sin metformina en su tratamiento con duración de 24 semanas en modalidad secuencial.95
CONCLUSIONES
La diabetes mellitus tipo 2 es una afección compleja de naturaleza progresiva y con múltiples perfiles en relación con los diferentes mecanismos por los que los pacientes pueden producir hiperglucemia. Este contexto nos obliga a buscar alternativas y combinaciones con tratamientos dobles y triples con el objetivo de lograr metas metabólicas y de otras variables, como presión arterial, perfil lipídico, peso, protección renal y desenlaces cardiovasculares. Las nuevas moléculas disponibles en el mercado (AGLP1 e iSGLT2) han demostrado de manera individual efecto en esas variables aparentemente por mecanismos de acción diferentes y complementarios; entonces, al considerar que los AGLP1 disminuyen las concentraciones de glucagón y la producción endógena de glucosa, en contraste con los iSGLT2 que producen efectos contrarios, su combinación es atractiva en búsqueda de un sinergismo pragmático. Los estudios de naturaleza retrospectiva tienen poco poder estadístico no sólo por su metodología, sino, además, por el número limitado de pacientes y los tiempos de seguimiento. El estudio DURATION 8 es el único estudio con distribución al azar, controlado, realizado en pacientes con diabetes mellitus tipo 2 que evaluó la combinación de manera simultánea, pero sin demostrar efectos aditivos. Aunque en la actualidad la combinación con inicio simultáneo es un escenario poco probable en el mundo real, no es claro que los resultados obtenidos sean mejores que el inicio secuencial; por su parte, ese estudio determinó que el inicio simultáneo de exenatida LAR más dapagliflozina mejoró las mediciones glucémicas y disminuyó los factores tradicionales de riesgo cardiovasculares. Con base en esta revisión de la bibliografía, deberían hacerse más estudios clínicos con la combinación de AGLP1 más iSGLT2 en el contexto de pacientes con diabetes mellitus tipo 2 con mal control metabólico y obesidad a pesar de tratamientos duales y triples. Serían ideales los estudios doble ciego, controlados, con distribución al azar, con número significativo de pacientes que comparen la combinación simultánea, secuencial o ambas para evaluar si los efectos son similares y teniendo en cuenta iSGLT (específicos y duales) y AGLP1 de acción larga, corta o ambas. Asimismo, en el paciente con alto riesgo cardiovascular sería conveniente considerar escenarios de terapia puente, en combinación o ambas, teniendo en cuenta que el efecto en la mortalidad con empagliflozina fue a los 6 meses de iniciado el tratamiento (efectos más hemodinámicos) y con liraglutida fue a los 12 meses de iniciado el tratamiento (efecto más vascular).











 nova página do texto(beta)
nova página do texto(beta)