Introducción
La integración es uno de los grandes problemas que tienen los estudiantes durante la licenciatura y que no han podido solucionarse del todo. Uno de los eventos que favorecen esta disociación es que cada sección se imparte, no sólo de manera separada, sino desarticulada. En el caso de bioquímica, los eventos metabólicos que se dan quedan suspendidos en el espacio, ya que éstos no se refieren a la función de los organitos celulares que se revisan en otra asignatura.
En la sección o en los cursos de Biología Celular en los que se revisa la estructura y parte de la función de la célula y sus componentes, con frecuencia se hace referencia a una célula que tienen prácticamente todos los organitos, y en ella se realizan varias -si no es que todas- de las vías metabólicas que se revisan en el curso de bioquímica. Esta célula es el hepatocito, así que analizaremos sus características morfológicas y las rutas metabólicas, que ubicaremos en los organitos que identificaremos.
Descripción histológica
El hígado es la glándula más grande del cuerpo y en él se identifican dos estructuras de manera general: el parénquima y el estroma.
El estroma es el tejido de sostén. El hígado está cubierto por una gruesa cápsula de tejido conjuntivo denso que se llama cápsula de Glisson. Esta glándula tiene una región cóncava, que es el hilio. A través del hilio ingresan al hígado los elementos vasculares (arteria hepática y vena porta), y lo abandonan los conductos biliares, la vena hepáticas y vasos linfáticos. Los elementos vasculares y los conductos viajan en el parénquima hepático rodeados por tejido conectivo, y forman a las tríadas portales o espacios porta.
El sostén fino de las células que se encuentran en el hígado, está conformado por la fina red de fibras reticulares (constituidas por colágena III) que se encuentran alrededor de las placas de hepatocitos y de los elementos vasculares. Este órgano está irrigado por capilares de tipo sinusoide, que son capilares de luz amplia y de pared delgada, y por ello, son los más permeables.
El parénquima del hígado está formado por tres tipos celulares principales, que en orden de abundancia son: hepatocitos, células de Kupffer (macrófagos) y células de Ito (lipocitos). Existen otras células menos conocidas: las células troncales, que se ubican en los espacios porta y de Hering, como se refiere en este número de la revista1.
Para formar el parénquima hepático, las células se ordenan de la siguiente manera: los hepatocitos forman placas o muros que están flanqueados por sinusoides que drenan en las venas centrales. El espacio que queda entre la pared de los hepatocitos y la pared del sinusoide se llama espacio perisinusoidal (de Dissé), y las células de Kupffer y las de Ito se alojan en ese espacio (Figuras 1 y 2).
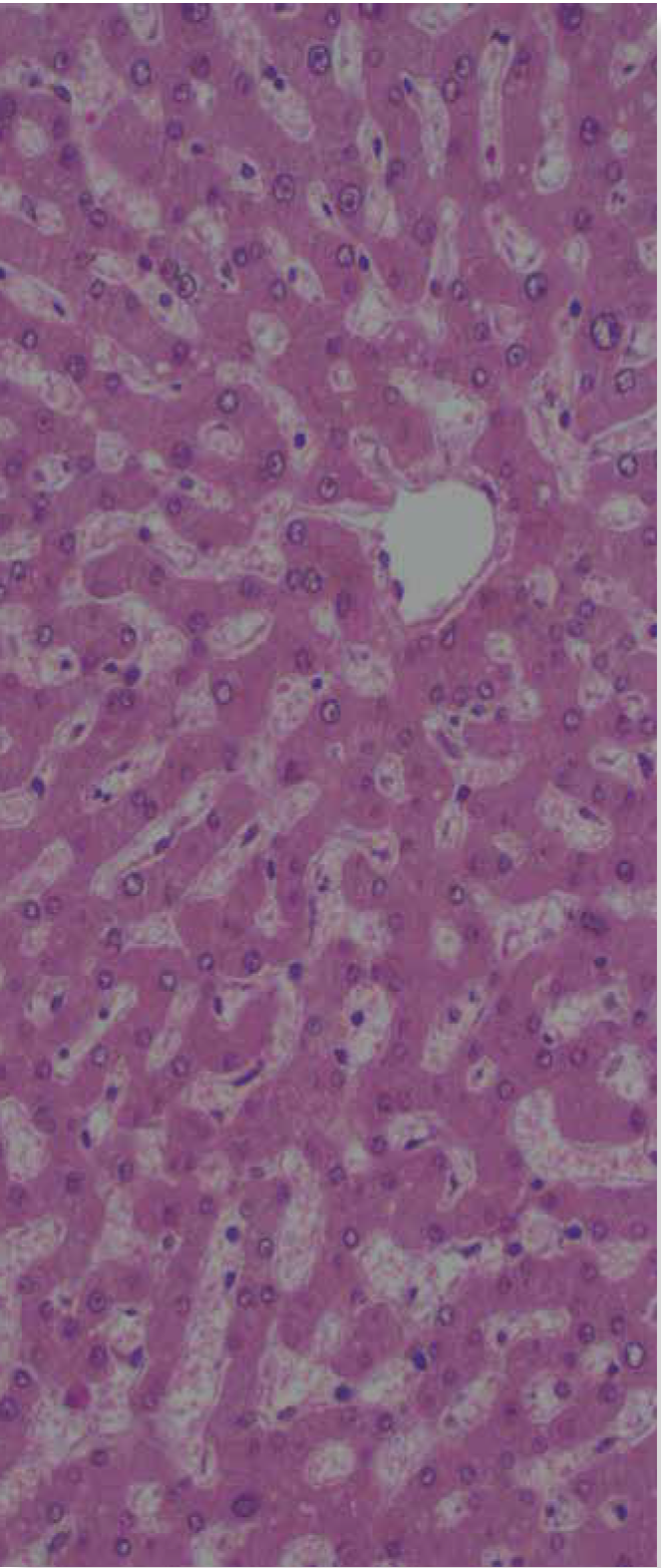
Fotos: Autores
Figura 1 Corte histológico de hígado teñido con hematoxilinaeosina. Los espacios pálidos entre las placas de hepatocitos corresponde a los capilares sinusoidales.
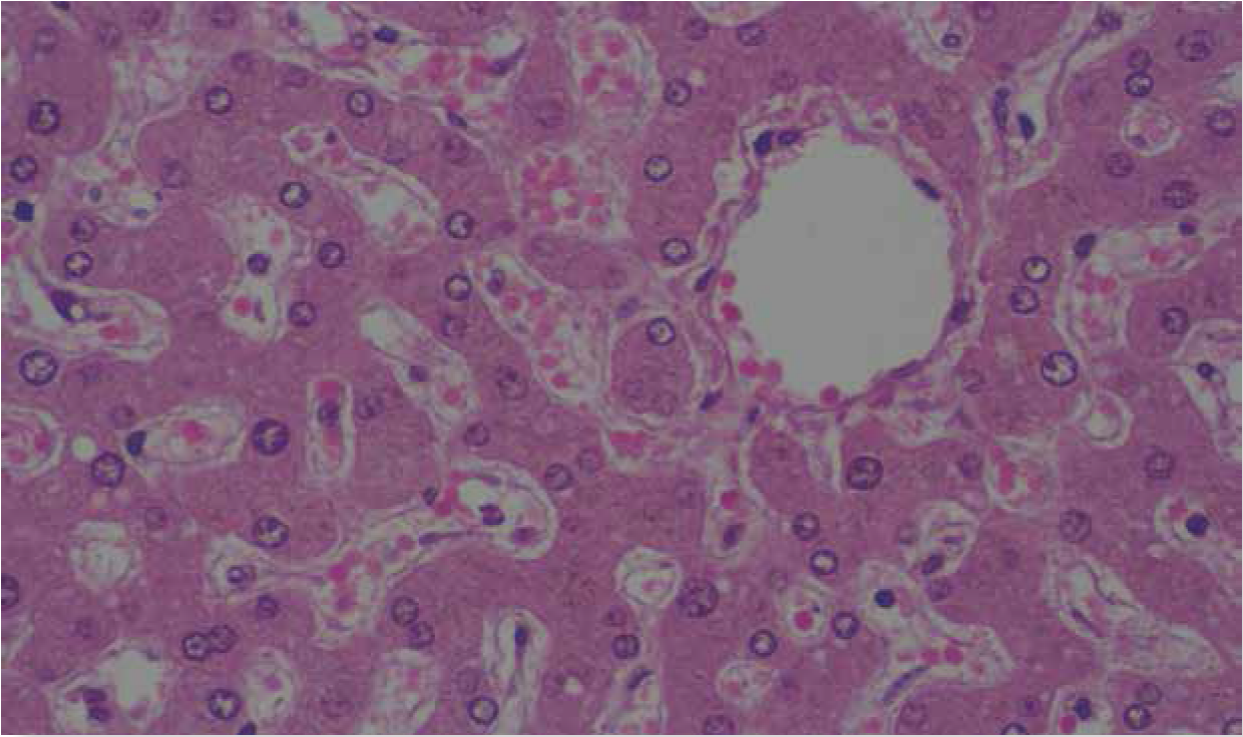
Figura 2 En esta imagen observamos a las placas de hepatocitos flanqueadas por los sinusoides. El espacio entre la pared de los sinusoides y los hepatocitos es el espacio perisinusoidal. También se aprecia la vena central del lobulillo. Tinción HE.
Las células de Kupffer son los macrófagos del hígado y son muy activos, debido a que dentro de las funciones de este órgano se encuentra la de eliminar elementos formes de la sangre que están viejos o gastados. Todos los detritos celulares son eliminados por estas células.
Las células de Ito o estelares se encargan de almacenar vitamina A, por ello, en el citoplasma se observan pequeñas gotitas lipídicas.
Los hepatocitos son células poliédricas que se organizan en placas o cordones. Pueden ser uni o binucleados, con predominio de eucromatina que delata la intensa actividad transcripcional (y por tanto, metabólica) que presentan estas células. Su citoplasma es abundante, con grumos acidófilos y basófilos.
La células pit constituyen una población de células NK (natural killer) específicas del hígado. Se encuentran en los sinusoides hepáticos y su tamaño se encuentra entre el de un linfocito y el de un granulocito. Su forma es variable e irregular. Se ubican adheridas a las células endoteliales por pequeñas microvellosidades. No están en el espacio de Dissé, suelen ser vecinas de las células de Kupffer y lo que las caracteriza son sus pequeños granulos, que al parecer corresponden a lisosomas. En condiciones normales, las células pit se mantienen estables, pero cuando se realiza una hepatectomía parcial, éstas entran en división celular en el parénquima restante2.
Los colangiocitos cubren la superficie interna del árbol biliar y varían en tamaño de acuerdo al sitio en el que los estudiemos: cúbicos en los duetos pequeños, cilindricos en los más grandes; ambos con microvellosidades y su cilio primario. Unidos entre sí por uniones herméticas. El cilio primario es 9 + O, y de acuerdo con estudios recientes, éstos funcionan como sensores osmóticos, químicos y mecánicos. Cuando hay daño hepático, los colangiocitos proliferan -en condiciones normales se mantienen quiescentes-, ya que estos colangiocitos pueden servir como células que pueden regenerar a otras células hepáticas, en especial las células positivas para la citoqueratina 19, que se ubican en los conductos de Hering3.
¿Qué funciones realizan los hepatocitos?
Cada hepatocito cumple con cientos de funciones, tanto endocrinas como exocrinas, entre ellas:
• Almacena glucógeno.
-
• Sintetiza hormonas, como:
• Trombopoyetina.
• Eritropoyetina.
-
• Somatomedinas.
• Desintoxica al sistema.
• Sintetiza proteínas:
• Albúmina.
• Transferrina.
• Fibrinógeno y otros factores de la coagulación.
• Lipoproteinas.
• Proteínas de fase aguda.
• Sintetiza a la bilis.
• Oxida ácidos grasos.
• Sintetiza colesterol, ácidos biliares y algunos lípidos utilizados en la síntesis de mielina.
• Desamina aminoácidos (para la producción de urea).
Por supuesto, no es posible ahondar en todas las funciones de los hepatocitos, así que situaremos algunas de las rutas metabólicas principales en los organelos en los que tienen lugar.
Almacén de glucógeno
Dentro de los hepatocitos se pueden observar inclusiones de glucógeno. En la Figura 3 se observa una imagen de hígado teñido con ácido peryodico schiff (PAS), con esa tinción el glucógeno se observa en rojo magenta.
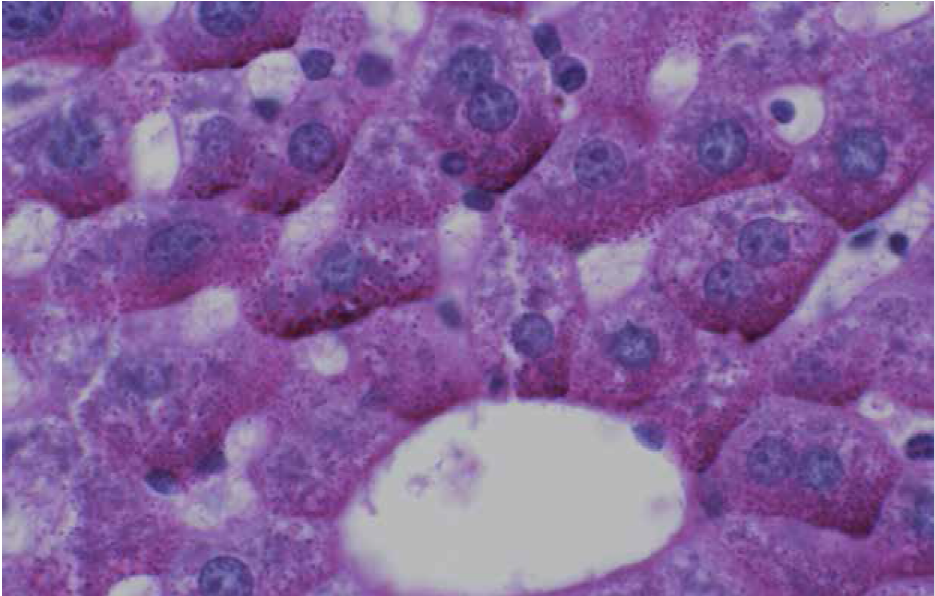
Figura 3 En un artístico arreglo, con la tinción de PAS se aprecian los cúmulos de glucógeno en los hepatocitos.
¿Cómo sintetiza glucógeno el hepatocito?
El glucógeno se va a sintetizar cuando los requerimientos energéticos de la célula se encuentren cubiertos y todavía exista un exceso de glucosa. La glucosa dentro del hepatocito es fosforilada, queda en la forma de glucosa-6-fosfato, y como se ha descrito, este metabolito funciona como un intermediario para la glucólisis, la via de las pentosas y glucogénesis.
La síntesis de glucógeno está regulada por la secreción de insulina, primero porque permite la captación de glucosa hacia el hepatocito y después activa a la proteína fosfatasa-1 que es la enzima que se encarga de la desfosforilación y activación de la glucógeno sintasa, mediante este mecanismo se permite que se vayan colocando sobre la cadena las unidades de glucosa, lo que permite que la cadena crezca para que posteriormente la enzima ramificante, como su nombre 10 indica, forme las diferentes ramas de glucosa, lo que facilita que se pueda almacenar mayor cantidad de glucosa4(Figura 3).
Una vez cubiertos los depósitos de glucógeno, ¿qué pasa con el exceso de glucosa u otros carbohidratos que se consumen? El hepatocito tiene la capacidad de metabolizar y transformar los esqueletos carbonados en ácidos grasos, ya que un exceso de acetil CoA hace que el ciclo de Krebs se sature y permita al citrato salir de la mitocondria, lo que tiene como consecuencia que se active la lipogénesis.
El citrato va a transformarse en oxaloacetato, y posteriromente en malato. Lavia que se encarga de llevar a cabo la síntesis de ácidos grasos se denomina beta-reducción, se lleva a cabo en el citoplasma y requiere un complejo multienzimático llamado proteina transportadora de acilos y la activación de malato en malonil CoA, así como de acetil CoA. La beta-reducción tiene como producto final la biosíntesis de ácido palmítico (16C), el cual puede enlongarse para generar ácidos grasos de cadena más larga.
Pero a diferencia de lo que el hígado puede hacer con el glucógeno, en las mismas condiciones de exceso, éste no tiene la capacidad de almacenar a los ácidos grasos; estos son esterificados en una molécula de glicerol formando triacilgliceroles que son empaquetados en las lipoproteinas de muy baja densidad (very low density lipoprotein) y así son transportadas al tejido adiposo para su almacenamiento. En condiciones patológicas el hígado empieza a almacenar lípidos y ocurre lo que se conoce como hígado graso, lo que hace que pierda algunas de sus funciones5.
Síntesis de lipoproteinas
Como se hace referencia en el párrafo anterior, otras proteínas vitales para el organismo son las lipoproteínas ya que cumplen con la función de transportar la grasa que se absorbe a partir de la dieta, así como los lípidos sintetizados por el hígado y el tejido adiposo. Debido a que los lípidos son insolubles en el agua, el hígado sintetiza este tipo de compuestos al asociar lípidos no polares (triacilglicerol y colesteril esteres) con lípidos (fosfolípidos y colesterol)6. Se han identificado cuatro grupos principales de lipo-proteínas que tienen importancia fisiológica y en el diagnóstico clínico: 1) quilomicrones derivados de la absorción intestinal de triacilglicerol y otros lípidos; 2) lipoproteinas de muy baja densidad (VLDL) derivadas del hígado para la exportación de triacilglicerol; 3) lipoproteinas de baja densidad (LDL) que representan una etapa final en el catabolismo de VLDL, y 4) lipoproteinas de alta densidad (HDL) comprometidas en el transporte del colesterol de los tejidos periféricos al hígado, y en el metabolismo de LDL y de quilomicrones. El triacilglicerol es el lipido predominante en los quilomicrones y VLDL, mientras que el colesterol y los fosfolípidos son los lípidos predominantes en LDL y HDL, respectivamente6,7. A pesar de que coloquialmente se conoce al LDL como el "colesterol malo" y al HDL como "colesterol bueno", ambos cumplen con funciones muy importantes y cualquier alteración que aumente o disminuya la concentración de alguna de ellas puede desencadenar alteraciones metabólicas importantes, entre ellas las famosas dislipidemias (hipercolesterolemia, hipertrigliceridiemia)8.
Desintoxicación
En el retículo endopásmico liso se encuentran las enzimas necesarias para el metabolismo de diversos agentes, tanto tóxicos como de fármacos. Ahí se encuentran enzimas que modificarán a estos agentes para transformarlos y hacerlos más hidrosolubles. Los fármacos y los agentes tóxicos pasan por procesos de oxidación y conjugación, y así se eliminan por el riñon. En estos procesos de desintoxicación el hígado se encarga de la eliminación de la bili-rrubina, producto de la degradación de los grupos hemo que formará parte de la bilis9.
Síntesis de proteínas plasmáticas
El hepatocito se encarga de sintetizar y secretar proteínas muy importantes como la albúmina (la proteina plasmática más abundante), que es la encargada de mantener la presión oncótica (coloidosmótica). Como es una proteína de secreción, se sintetiza por la vía retículo endoplásmático rugoso y el aparato de Golgi. Además, las proteínas del sistema de coagulación, también se sintetizan en el hepatocito y siguen una vía semejante a la de la albúmina.
Modificación de hormonas
En el hígado se modifica la hormona secretada por la glándula tiroides, conocida como T4 (tertrayo-dotiroxina) y se transforma en su forma activa o T3 (triyodotiroxina). La actividad de la hormona de crecimiento se estimula por la liberación del factor de crecimiento semejante a la insulina (IGF-1). De igual forma, las hormonas esteroideas que pasan a la circulación general y que se distribuyen por todos los tejidos corporales, son desconjugados y eliminados por el hígado. En resumen, varias alteraciones hormonales pueden ser consecuencia de una mala función hepática y no necesariamente de la glándula productora de dicha hormona.
Síntesis de bilis
La bilis está compuesta principalmente por agua (82%), sales biliares (12%), fosfolípidos (4%), colesterol (1%), bilirrubina, inmunoglobulina A, sales inorgánicas, y pueden encontrarse otras sustancias como fármacos y hormonas esteroideas. El hepatocito produce, a partir de colesterol, los ácidos biliares primarios; aunque también son reutilizados los ácidos biliares obtenidos de la circulación entero-hepática. El hepatocito conjuga los ácidos biliares con glicina o taurina y les añade sales de sodio y potasio, formando así sales biliares. Éstas son secretadas hacia los canalículos biliares, y durante su paso por los conductos biliares, los colangiocitos añaden bicarbonato y agua. En la vesícula biliar, la bilis se concentra, se modifican las concentraciones de iones (aumentan Ca2+ y K+; disminuyen Na+, Сl- y bicarbonato) y aumenta la concentración de las sales biliares. El 95% de las sales biliares se reabsorbe en el íleon y 5% (por acción de la microbiota intestinal) se deconjugan e hidroxilan en el colon para formar a los ácidos biliares secundarios, una parte de éstos se reabsorbe y otra es eliminada por las heces10.
Algunas alteraciones en los hepatocitos
Una las alteraciones más frecuente en el hepatocito es el exceso de triglicéridos acumulados en su citoplasma, lo que se conoce como esteatosis. Esta patología se asocia con el consumo elevado de carbohidratos, grasas y alcohol, lo que provoca un aumento en la biosintesis de los lípidos, y generalmente se observa en personas con sobrepeso y obesidad. La esteatosis hepática puede ser de dos tipos: microvesicular, que se refiere a múltiples gotas pequeñas que no desplazan el núcleo a la periferia, y macrovesicular, que consiste en una gota grande simple que desplaza el núcleo a la periferia. Es importante mencionar que la esteatosis puede conducir a la muerte del hepatocito. Por otra parte, de manera fisiológica se pueden observar hepatocitos binucleados, que son células que no han completado el proceso de citocinesis. Estas células binucleadas son la evidencia de la gran capacidad de regeneración hepática, por lo tanto, si el daño al parénquima hepático aumenta, el número de estos hepatocitos binucleados también se incrementará, acompañado de otros cambios en la histología normal hepática, como el engrosamiento de las trabéculas con cierto desarreglo en su simetría11(Figuras 3y4).
Conclusión
El hepatocito es una célula metabòlicamente muy activa y es, quizá, la más versátil de nuestro organismo. Todos y cada uno de los hepatocitos que conforman al hígado, cumplen íntegramente con las funciones que se describieron (y con otras muchas más), lo que implica una alta relevancia en la homeostasis del cuerpo humano. Es importante mencionar que el hígado tiene una gran capacidad regenerativa, solamente superada en la placenta, pero esto no llega a ser suficiente ya que, cuando es agredido constantemente y de forma crónica, como sucede con la ingesta de alcohol, infecciones virales o enfermedades autoinmunes, progresa a un daño hepático irreversible. Por lo que su patología representa una de las principales causas de muerte en nuestro país12, y su conocimiento por parte del estudiante de medicina y de los profesionales de la salud es de vital importancia.











 nova página do texto(beta)
nova página do texto(beta)



