Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Boletín médico del Hospital Infantil de México
versión impresa ISSN 1665-1146
Bol. Med. Hosp. Infant. Mex. vol.70 no.6 México nov./dic. 2013
ARTÍCULO DE INVESTIGACIÓN
Aparición de la osteopenia en recién nacidos de pretérmino en un servicio de neonatología
Time of onset of osteopenia in preterm newborn in a neonatology service
Carlos Antonio Tapia-Rombo,1 Karla Paola Villalobos-Granja,1 Jorge Ramírez-Pérez,2 Herminia Uscanga-Carrasco,1 Luis Alfonso Robles-Espinosa3
1 Servicio de Neonatología, Unidad Médica de Alta Especialidad, Hospital General Dr. Gaudencio González Garza, Centro Médico Nacional La Raza Instituto Mexicano del Seguro Social, México D.F., México
2 Servicio de Radiología e Imagen, Unidad Médica de Alta Especialidad, Hospital General Dr. Gaudencio González Garza, Centro Médico Nacional La Raza Instituto Mexicano del Seguro Social, México D.F., México.
3 Laboratorio Central de Análisis Clínicos, Unidad Médica de Alta Especialidad, Hospital General Dr. Gaudencio González Garza, Centro Médico Nacional La Raza Instituto Mexicano del Seguro Social, México D.F., México.
Autor de correspondencia:
Dr. Carlos Antonio Tapia-Rombo
Correo electrónico: tapiachar@yahoo.com.mx
Fecha de recepción: 10-06-13
Fecha de aceptación: 24-09-13
Resumen
Introducción. La osteopenia es la disminución de la densidad ósea secundaria a menor mineralización del hueso, y puede presentarse como raquitismo, osteomalacia y osteoporosis. El objetivo del estudio fue detectar el momento en que se presenta la osteopenia en prematuros de un servicio de neonatología.
Métodos. Se realizó un estudio observacional, prospectivo, comparativo y clínico. Se incluyeron 30 recién nacidos de pretérmino (RNPT) que ingresaron de noviembre del 2010 a agosto del 2011 y cumplieron con los criterios de inclusión. En todos los pacientes se determinaron los niveles séricos de Ca, P y fosfatasa alcalina, y radiografías de huesos largos a las dos, cuatro, seis y ocho semanas a partir del ingreso. Para el análisis de los datos se utilizó estadística descriptiva e inferencial. Se consideró significación cuando p <0.05.
Resultados. La población estudiada estuvo conformada por 30 RNPT con una mediana de edad gestacional de 29 semanas. La mediana de peso al nacimiento fue de 1,055 g. En todos los pacientes se manejó nutrición mixta. Los cambios radiológicos sugestivos de osteopenia fueron reportados en 83.3% de los pacientes durante las primeras dos semanas de estudio. Al final del estudio, 86.7% de los pacientes la presentaron (n =26). La mediana de la edad de detección de la osteopenia fue de 19 días de vida extrauterina.
Conclusiones. La osteopenia del prematuro se presenta alrededor de la tercera semana de vida extrauterina. Estos resultados dan un panorama diferente a lo reportado en la literatura. Por ello, la prevención de la desmineralización ósea debe realizarse más tempranamente.
Palabras clave: recién nacido pretérmino, osteopenia, aparición.
Abstract
Introduction. Osteopenia is a decrease in bone density secondary to low bone mineralization and can present as rickets, osteomalacia and osteoporosis. The aim of this study is to detect when osteopenia is presented in preterm newborns (PNB) of a neonatal ward.
Methods. We carried out an observational, prospective, comparative clinical trial (study cohort) that included 30 PNB admitted from November 2010 to August 2011 and who met the criteria selection. Alkaline phosphatase levels were considered elevated from 280 IU/L. All patients were determined Ca, P, alkaline phosphatase serum. X-rays of long bones at 2, 4, 6 and 8 weeks after admission were taken. Statistical analysis was performed using descriptive and inferential statistics. Significance levels were set at p <0.05.
Results. The study population consisted of 30 PNB with a median gestational age of 29 weeks and median birth weight of 1055 g. Parenteral and enteral nutrition (mixed) was managed in all patients. Radiological changes suggestive of osteopenia were reported in 83.3% of patients during the first 2 weeks of study and at the end of the study in 86.7% of patients (n =26). The median age of detection of osteopenia was 19 days of life.
Conclusions. Osteopenia of prematurity occurs at approximately the third week after birth. These results present a different picture to that reported in the literature since the time of reporting these data. Preventing bone disease should be done early.
Key words: preterm infants, osteopenia, appearance.
INTRODUCCIÓN
La osteopenia o enfermedad ósea metabólica (EOM) del prematuro es la disminución de la densidad ósea secundaria a una menor mineralización del hueso. Es multifactorial y se presenta como raquitismo, osteomalacia y osteoporosis. Cualquiera de los anteriores puede presentarse en el recién nacido de pretérmino (RNPT). En el raquitismo, los niveles séricos de Ca, de P o de ambos se encuentran disminuidos y el nivel de fosfatasa alcalina (FA) aumentado. Existen cambios en la unión cartílagodiafisiaria, como el aumento de la anchura del cartílago de crecimiento, el abultamiento de este en forma de copa y signos de deshilachamiento. La osteomalacia se caracteriza por los mismos cambios bioquímicos que el raquitismo, incluyendo la osteopenia y escaso o ningún crecimiento lineal, pero carece de los rasgos de raquitismo en la unión cartílago-diafisiaria. La osteoporosis se define como la disminución de la masa ósea por unidad de volumen con una proporción normal de mineral respecto a la matriz ósea; es decir, todo está reducido, y no puede distinguirse radiográficamente de la osteomalacia porque ambas se caracterizan por osteopenia. Sin embargo, los pacientes con osteoporosis tienen concentraciones séricas de Ca, P y FA normales. A veces, la osteoporosis y la osteomalacia se asocian.1
La incidencia de la osteopenia varía según los diferentes centros hospitalarios. Se ha reportado en 30% de los prematuros menores de 1,500 g y en 50% de los menores de 1,000 g de peso.2
El desarrollo perinatal del hueso se lleva a cabo por medio de dos procesos que están relacionados entre sí: el intramembranoso y el endocondral. El intramembranoso se lleva a cabo en el primer hueso donde comienza la osificación y origina la diferenciación de células del mesénquima para producir preosteoblastos y luego osteoblastos, con la formación subsecuente de matriz ósea; elaboran trabéculas óseas que se fusionan después y forman la capa esponjosa primaria. Los osteoblastos cubren la superficie de la capa esponjosa y depositan nuevas capas de matriz ósea, mientras que el hueso sobrante nuevo es eliminado de otras superficies por los osteoclastos. Por otra parte, durante la osificación endocondral existe un reemplazo óseo progresivo del precursor cartilaginoso. Las sales de Ca comienzan a precipitarse en diversas porciones de la matriz ósea.3,4
La etiología de la osteopenia es multifactorial. Se han mencionado diferentes factores de riesgo para su desarrollo, como la prematurez que es el más importante. Se sabe que los depósitos de Ca y P incrementan sustancialmente desde la semana 24 de gestación en adelante. Durante este período, el feto aumenta alrededor de 30 g al día, lo que representa un consumo de 310 mg/día de Ca y 170 mg/día de P. Las dos terceras partes de estos requerimientos se adquieren durante ese período.3,5 El uso prolongado de nutrición parenteral (NP) es una de las causas más frecuentes de osteopenia, porque la solubilidad de Ca y P limita el aporte ideal de estos minerales, sobre todo cuando el prematuro requiere restricción de líquidos.5,6 Otro factor asociado es la displasia broncopulmonar (DBP) por el uso prolongado de diuréticos, principalmente, y el tratamiento con metilxantinas (ambos aumentan la pérdida de minerales en orina). También, el uso de corticosteroides ha influido en la función osteoblástica al disminuir la absorción de Ca y P.7 La carencia de estimulación mecánica y la falta de movimiento de las extremidades, así como el reposo prolongado favorecen el incremento de la actividad de los osteoclastos8-12 y la sepsis neonatal. Estas patologías son frecuentes en los servicios de neonatología, y están relacionadas con el estado catabólico del paciente.12 También, la osteopenia se ha relacionado con una pobre transferencia transplacentaria de Ca y P, que ocurre de forma frecuente en embarazos complicados con preeclampsia.
La mayoría de las veces el raquitismo se presenta en el RNPT por la deficiencia de sustrato mineral óseo más que por una deficiencia de vitamina D. Es más común en los RNPT que son alimentados solamente con seno materno.13-15
La osteopenia o EOM —con o sin evidencia radiológica de raquitismo— se presenta entre la tercera y la décimo segunda semanas de edad en los RNPT y, generalmente, se asocia también con el bajo peso al nacimiento.1 Usualmente, la osteopenia es subclínica y posterior a la presencia de fracturas. En diversas ocasiones, esta es la causa por la que se diagnostica.12,16-18
Otro marcador de disminución del sustrato mineral ósea, es la FA, enzima derivada de las vesículas matrices que se encuentra localizada en la membrana de los osteoblastos, y que se eleva en la osteopenia secundaria a raquitismo o a osteomalacia en los RNPT. También se ha asociado con el crecimiento lineal hasta la edad de 12 semanas (en pequeños grupos de RNPT).15,19-22 En un estudio se encontró que el punto de corte era ≥1,200 UI de FA, con una alta incidencia de concentraciones bajas de P sérico y concentraciones urinarias altas del mismo elemento y elevación sérica de Ca entre los RNPT con y sin EOM. Esto sugirió la asociación de la deficiencia de P con retardo en el crecimiento.22 También se apreció que los RNPT que tomaron leche materna (que contiene menor cantidad de Ca y P con respecto a la industrializada) tenían niveles más elevados de FA que aquellos alimentados con fórmula industrializada para prematuros durante las primeras nueve semanas de vida extrauterina. En el grupo de FA ≥1,200 UI, la ganancia de peso, talla y perímetro cefálico estaban disminuidos en el período neonatal, y a la edad de 9 a 18 meses solamente la talla y el peso con respecto al grupo con menor actividad de la FA.21
Kovar y colaboradores introdujeron el uso de la FA sérica para la detección de fracturas en el RNPT.20 En contraste, Faerk y colaboradores no encontraron relación entre el incremento de FA y los cambios óseos observados por absorbiometría.23
Los lactantes con osteopenia pueden presentar una fontanela anterior amplia, craneotabes (signo de "pelota de ping-pong"), anchura de las muñecas, rosario condrocostal, fracturas de costillas o huesos largos y, con el tiempo, detención del crecimiento lineal, dependiendo del tipo de osteopenia. Radiológicamente, todos presentan disminución de la densidad ósea. Miller refiere que 10% de prematuros <1,000 g de peso, a la edad promedio de 76 días, presentan fracturas.15 Brooke y Lucas encontraron que 57% de los prematuros <1,200 g presentan fracturas, y la principal causa son los aportes bajos de Ca y P.3
El uso de vitamina D para el tratamiento de la osteopenia no está probado. La cantidad de 400 UI diarias no mejora la absorción de Ca y P, y una cantidad mayor a 800 UI puede producir hipervitaminosis y no se recomienda. El suplemento mineral, después de iniciado, debería de continuarse hasta que exista una evidencia de mejora radiológica.4 En general, en literatura médica se habla del diagnóstico y tratamiento cuando ocurre la osteopenia y no en qué momento debe prevenirse.2,4,11,16,18
En el Servicio de Neonatología de la Unidad Médica de Alta Especialidad Hospital General Dr. Gaudencio González Garza (UMAE HG Dr. GGG) del Centro Médico Nacional La Raza (CMNR) se atiende un gran número de RN; aproximadamente, 380 al año. De ellos, más de 60% son prematuros y, prácticamente, 100% se maneja con NP. En la literatura se habla de la presencia de osteopenia desde la tercera o cuarta semana de vida extrauterina o, incluso, después.1,6 Sin embargo, empíricamente se ha observado con mayor frecuencia cerca de la tercera semana. Por ello surgió la necesidad de este estudio, para reportar la experiencia en el UMAE HG Dr. GGG de CMNR. De acuerdo con los resultados, se podrían sentar bases y criterios más precisos para el inicio del manejo de minerales —como Ca, P u otros— para, en lo posible, prevenir la aparición de esta patología.
El objetivo de este estudio fue detectar el momento en el que surge la osteopenia en el prematuro (raquitismo, osteomalacia u osteoporosis), en el Servicio de Neonatología de la UMAE HG Dr. GGG del CMNR.
MÉTODOS
Se realizó un estudio observacional, prospectivo, comparativo y clínico (cohorte). Se incluyeron 30 RNPT del Servicio de Neonatología de la UMAE HG Dr. GGG del CMNR, que ingresaron consecutivamente de noviembre del 2010 a agosto del 2011 y cumplieron con los criterios de selección.
Se incluyeron todos RNPT <34 semanas de edad gestacional corroborada al ingreso del servicio en las primeras 72 horas de vida extrauterina con el método de Ballard expandido para RN extremadamente prematuros; en caso de duda, también se utilizó este método aún con mayor edad extrauterina que la mencionada.24 Con o sin ventilación mecánica, NP o ayuno, o que recibieron alimentación al seno materno o fórmula especial para prematuros (desde el primer día de nacidos hasta una edad extrauterina máxima de dos semanas), con presencia o no de DBP, con o sin antecedentes de enterocolitis necrosante y que los padres o tutores hayan estado de acuerdo con el ingreso de sus hijos al estudio.
Se excluyeron RNPT con malformaciones congénitas mayores, tales como trastornos de la migración neuronal, cardiopatías congénitas complejas, atresia esofágica, hipo o hiperparatiroidismo congénito, congénito, anemia (Hb <8 g/dl), cualquier tipo de hepatopatía. Lo anterior cuando se detectara en cualquier momento de su evolución o cuando los familiares decidieran retirar al paciente del estudio.
El diagnóstico de osteopenia se realizó con base en la disminución de la densidad ósea radiológica del húmero o fémur asociado o no a otros cambios radiológicos, como anchura del cartílago de crecimiento, el abultamiento de este en forma de copa y signos de deshilachamiento, además de niveles séricos de Ca bajos o normales, con niveles de P séricos bajos o normales y un incremento de la FA (raquitismo y osteomalacia).
Se consideró hipocalcemia cuando los niveles de Ca sérico reportados fueron <7 mg/dl. Se consideró hipofosfatemia cuando los niveles de P sérico fueron <3.7 mg/dl e hiperfosfatemia con niveles de P sérico > 8.2 mg/dl. Los niveles séricos de FA se consideraron elevados por encima de 280 UI/l.
El Ca por vía parenteral se proporcionó en forma de gluconato de Ca al l0%; el P, como fosfato de potasio y ambos se administraron por vía enteral a través de los aportes de minerales referidos en las fórmulas especiales para prematuros.
A todos los pacientes incluidos en el estudio se les determinaron los niveles de Ca, P y FA séricos a las dos, cuatro, seis y ocho semanas a partir de la fecha de ingreso al Servicio. Las radiografías de huesos largos (fémur y húmero) se tomaron en las mismas semanas con un aparato móvil de rayos X (Siemens, Polymobil III, modelo 4564 100 X0381, España). Las valoraciones las realizó un médico radiólogo experto.
El Ca sérico y el P sérico se determinaron por análisis dicromático por punto final. El Ca presente en la muestra se liga al complexón de ocresolftaleína para formar un complejo color púrpura en solución salina. Los valores normales para el RNPT son de 7 a 10.8 mg/dl. Para el P, el método refiere qué cantidad del complejo fosfomolibdato no reducido es proporcional a la cantidad de P inorgánico en la muestra. Los valores normales en el RNPT van de 3.7 a 8.2 mg/dl. La FA en suero se determinó por la metodología propuesta inicialmente por Bowers y McComb — utilizando p–nitrofenilfosfato como sustrato— y optimizado por Tietz, con la inclusión de un buffer para proveer un ión metálico y un buffer 2-amino, 2-metil, 1-propanolol. Los valores de referencia en esta determinación para nuestros pacientes son de 150 a 280 UI/l.
Se consideró la edad de aparición de la osteopenia a partir del día en el que se diagnosticó por primera vez en cada paciente.
Se detrminaron también el peso, talla y perímetro cefálico durante el estudio. Los datos obtenidos se registraron en un formato especial de recolección de datos.
El análisis de los resultados se realizó a través de estadística descriptiva (mediana y rango intercuartil en las variables que no tenían distribución normal y en las que la tenían, media y desviación estándar, frecuencias). La inferencial se realizó por medio de la Prueba de Friedman y, en caso de distribución normal, el análisis de muestras repetidas. Cuando se indique, se realizó la prueba de rangos de Wilcoxon. La significación se consideró con p <0.05.
Para el análisis estadístico se utilizó el programa SPSS, v. 15 (Chicago, IL, USA). Este trabajo fue aprobado por el Comité de Educación e Investigación Médica y por el Comité de Bioética, ambos de la UMAE Dr. GGG del CMNR.
RESULTADOS
La población estudiada estuvo conformada por 30 RNPT que cumplieron con los criterios de selección. Se les dio un seguimiento de 8 semanas. El 60% (n =18) fueron del sexo masculino (Cuadro 1).
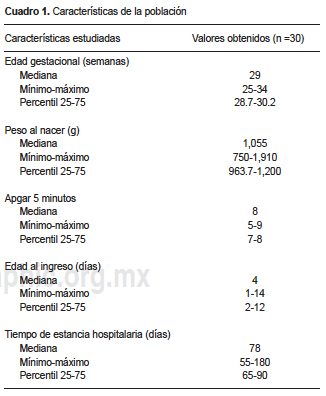
Dentro de los diagnósticos de motivo de ingreso, la sepsis ocupó el primer lugar con 9 pacientes (30%); en segundo, el síndrome de dificultad respiratoria con 8 pacientes (26.7%); con menor frecuencia, persistencia del conducto arterioso, neumonía, retraso en el crecimiento intrauterino y prematurez para manejo preciso de NP.
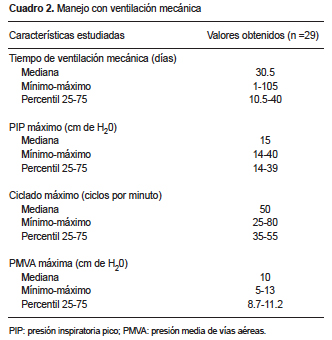
De los 30 pacientes estudiados, solamente 5 recibieron esteroides prenatales (16.7%), aunque 20 fueron hijos de madres con preeclampsia (66.6%). De los 30 pacientes, 29 se manejaron con asistencia mecánica a la ventilación (96.7%), con una duración de 1 a 105 días y una mediana de 30.5 días (Cuadro 2).
Todos los pacientes recibieron NP, iniciada dentro de las primeras 48 horas posteriores al ingreso (Cuadro 3). Se puede observar que los aportes de Ca fueron aumentando conforme pasaron los días de estancia hospitalaria, con diferencia significativa. No así los de P.
Los aportes de vitamina D menores a 400 UI por día se reportaron en 10 pacientes (33.3%); el resto (n =20) tuvo un aporte mayor de 400 UI (66.7%).
Se manejó en todos los pacientes alimentación mixta (parenteral y enteral) con diferente tiempo de duración (Cuadro 4).
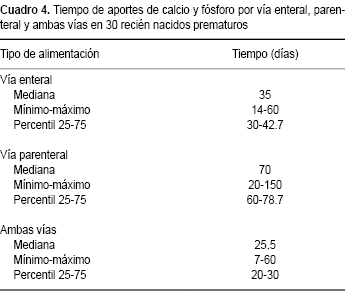
El 60 % de los pacientes recibieron alimentación con leche Pre NAN® (n =18) y el 40% con Enfamil para prematuros (n =12). El 73% de los pacientes recibieron leche materna combinada con alguna de las fórmulas mencionadas.
Las medianas del peso durante las semanas de estudio mostraron diferencia significativa. Lo mismo se apreció con la talla y el perímetro cefálico (Cuadro 5).
Para la detección de la osteopenia, se tomaron en cuenta los valores de Ca, P y FA séricos, así como las radiografías de huesos largos. Dichos estudios fueron realizados cada dos semanas durante ocho semanas. Hubo incremento en los valores de FA del ingreso (de 95 UI/l a 879 UI/l, mediana de 350 UI/l) con respecto a los reportados durante las dos últimas de seguimiento (de 101 a 969 UI/l, mediana de 393 UI/l) pero sin diferencia significativa (prueba de rangos de Wilcoxon con p =0.09) (Cuadro 6). Al realizar la prueba de Friedman, se puede observar una diferencia significativa en los niveles de Ca sérico, pero no en los de P sérico ni de FA (p >0.05).
Los cambios radiológicos sugestivos de osteopenia fueron reportados en 83.3% de los pacientes durante las primeras dos semanas del estudio. Se observaron en 76.7% durante la tercera y cuarta semanas, ya que fueron los pacientes los que lograron mejoría con los aportes de Ca, P y vitamina D. Sin embargo, durante la quinta y sexta semanas nuevamente 83.3% de los pacientes (n =25) reportaron osteopenia. Al final del estudio, 86.7% de los pacientes presentaron osteopenia (n =26), y solamente cuatro pacientes no la presentaron (13.3%). En esta población predominó el raquitismo (n =18) y, con menor frecuencia, la osteomalacia (n =8). En 33.3% (n =10) se detectaron datos clínicos como rosario costal y ensanchamiento de muñecas.
El diagnóstico de osteopenia se presentó en el día 16 (como mínimo) y en el día 57 (como máximo) de vida extrauterina, con una mediana de 19 días (percentil 25-75 de 16 a 25.7 días). Las fracturas patológicas, en el día 48 (mínimo) y en el 85 (máximo), con una mediana de 69 días, sólo en cuatro pacientes.
Con relación al uso de diuréticos, los más utilizados fueron el furosemide y la espironolactona, ambos en 23 pacientes (77%). Las xantinas y los esteroides también se utilizaron, ambos en 26 pacientes y cada uno en 86.7%. El ultrasonido transfontanelar se realizó en todos los pacientes. Este reportó 10 pacientes (33.3%) con hemorragia intraperiventricular (cuatro con grado I y seis con grado III, de acuerdo con Papille y colaboradores).25 A otros 10 pacientes (33.3%) se les diagnosticó leucomalacia periventricular. En los demás, no se reportaron alteraciones.
El tiempo de estancia hospitalaria fue de 55 a 180 días, con una mediana de 78 días.
Cinco pacientes fallecieron. La causa más frecuente fue choque séptico. Las patologías presentes al fi nal del estudio fueron DBP, reportada en 26 pacientes (86.7%) pacientes; la edad de detección fue entre los 30 y 48 días, con una mediana de 33 días. La sepsis neonatal, en 25 pacientes (83.3%); el retardo en el crecimiento intrauterino en nueve pacientes (30%), la persistencia del conducto arterioso en cinco pacientes (16.7%) y las fracturas patológicas en cuatro (13.3%). Algunos presentaron combinación de patologías.
DISCUSIÓN
Este es el primer estudio realizado en la Unidad de Cuidados Intensivos Neonatales (UCIN) de la UMAE HG Dr. GGG del CMNR. Se encontró que la frecuencia de osteopenia fue de 86.7%, cifras mayores a las reportadas en la literatura.2 Es un panorama inicial para conocer la cantidad de pacientes que presentan la enfermedad, y resulta elevado.
Es importante mencionar que, en este estudio, el aporte promedio de Ca y P por vía enteral, parenteral o ambas al ingreso fue bajo, comparado con el recomendado por la Academia Americana de Pediatría. Al final del estudio, los aportes de Ca en la mayoría de pacientes fueron adecuados, aunque no los de P. Estos últimos continuaron bajos, por lo que no se logró una relación adecuada entre Ca y P (1.7: 1) para mantener un óptimo crecimiento extrauterino —similar al intrauterino— condicionándose así la desmineralización ósea.5 Steichen y colaboradores realizaron un estudio en prematuros con aportes de Ca que fueron de 220 a 250 mg/kg/día, de P de 110 a 125 mg/kg/día y de vitamina D de 260 a 400 UI al día. Compararon dos grupos, uno alimentado con fórmula para prematuros y otro control alimentado exclusivamente con leche materna. Concluyeron que los RN que recibieron únicamente leche materna tenían mayor riesgo de presentar desmineralización ósea.16 En este estudio, los aportes de Ca fueron similares a lo ideal en la mayoría de los pacientes; sin embargo, los de P fueron menores.
La mayoría de los pacientes presentaron DBP, y ameritaron manejo con diuréticos como furosemide, metilxantinas y esteroides. Estos fármacos aumentan la pérdida de minerales por la orina. Shrivastava y colaboradores demostraron que los pacientes con DBP que recibieron esteroides por más de tres semanas presentaron disminución de la velocidad de crecimiento, de la absorción de Ca y retención de Ca y P, favoreciendo así alteraciones en la mineralización ósea.7 La DBP se presentó en gran parte de la población estudiada. La frecuencia del uso de diuréticos fue de 77%, y de metilxantinas y de esteroides de 86.7%. Se sabe que estos fármacos son factores que pueden favorecer la presencia de osteopenia.
La falta de estimulación mecánica y de movimiento en las extremidades así como el reposo prolongado favorece el incremento de la desmineralización ósea.8-11 Moyer y colaboradores demostraron que realizar movimientos pasivos en las cuatro extremidades durante 5 a l0 minutos promueve la ganancia ponderal y aumenta la masa ósea.8 Todos los pacientes permanecieron en reposo prolongado, y no recibieron manejo de rehabilitación.
La sepsis neonatal se ha relacionado con el incremento del catabolismo, condicionando depleción ósea aumentada en prematuros.12 Este diagnóstico se encontró en 30% de los RNPT al ingreso y en 83.3% al final del estudio.
Los aportes de vitamina D no influyeron en la presencia de osteopenia. La principal causa es el insuficiente aporte de minerales.1,2,13,16,26 Solamente 33.3% de los prematuros no alcanzaron a recibir 400 UI de vitamina D al día, lo que hace que no sea factor importante para la presentación de osteopenia.
El diagnóstico de osteopenia se realizó tomando en cuenta niveles altos de FA >280 UI/l (en el raquitismo y osteomalacia), niveles bajos o normales de Ca, P y cambios radiológicos, tales como disminución de la densidad ósea, aunada o no al aumento en la anchura de la placa de crecimiento, el abultamiento de esta en forma de copa y signos de deshilachamiento. Algunos autores mencionan que el punto de corte para hablar de actividad osteoclástica es cuando la FA está por encima de 1,000 UI/l.27 Otros,2 cuando está por arriba de 700 UI/l, y algunos más mencionan valores alrededor de 400 UI/l.28 Efectivamente, en este estudio se observó un aumento de la FA desde las dos primeras semanas del estudio sin significación estadística entre todas las semanas que duró. También se obtuvo evidencia clínica-radiológica de osteopenia. Alrededor de la tercera semana de vida extrauterina, ya con una mediana más elevada, por arriba de 400 UI/l. Así permaneció hasta prácticamente la finalización del estudio. Esto sugiere que el problema de osteopenia se presentó más tempranamente del promedio de lo que se ha reportado en la literatura médica.2,16-18 En muchos pacientes con alteraciones bioquímicas y evidencia radiológica de osteopenia no se presentan datos clínicos como fontanela anterior amplia, craneotabes, anchura de las muñecas, rosario condrocostal, hasta que ya hay fracturas de costillas o huesos largos.1 Miller refiere que 10% de prematuros menores de 1000 g de peso a la edad promedio de 76 días presentan fracturas patológicas.15 Brooke y colaboradores encontraron que 57% de los prematuros de 1,200 g las presentan.3 Aquí se encontró la presencia de fracturas en aproximadamente 13% de los prematuros. La edad de detección fue desde 48 hasta 85 días. Solamente en el 33.3% de los pacientes se detectaron datos clínicos como rosario costal y ensanchamiento de muñecas. La osteopenia con o sin evidencia de raquitismo se presentó entre la semana tres y la semana 12 de vida extrauterina.2,16-18 Al valorar las radiografías de esta investigación, 83.3% de los pacientes presentaron datos de osteopenia durante las primeras dos semanas del estudio (alrededor de la tercera semana de vida extrauterina) y 86.7% al final. En la población estudiada solo se presentó raquitismo y osteomalacia. La edad extrauterina de los prematuros al diagnóstico de osteopenia fue desde 16 a 57 días con una mediana de 19 días y, con estos resultados, se demostró que la osteopenia se puede detectar alrededor de la tercera semana de vida extrauterina.
En este trabajo se encontró un incremento de la FA sérica final con respecto a la de ingreso (aunque sin diferencia estadística), a pesar de haber mayor ingreso de Ca al final del estudio, con ingreso de P similar durante toda la investigación, sin que se reflejaran cambios en el P sérico inicial ni final. Lo anterior puede estar relacionado con el incremento de la frecuencia de cambios radiológicos reportados en las semanas siete y ocho.
Son las propias complicaciones de la prematurez, como la DBP, que llevan al uso de esteroides, diuréticos y metilxantinas, las que producen pérdidas urinarias excesivas de minerales. No se incluyó la medición urinaria de Ca y P en este trabajo, por lo que se sugiere que realicen posteriormente. Desafortunadamente no se pudo contar con un grupo control debido a que la mayoría de los pacientes presentaron osteopenia.
El uso prolongado de NP no impide que se proporcionen aportes extra de minerales por vías alternas, con la finalidad de lograr aportes ideales. Sobre todo en prematuros con antecedentes de ser hijos de madres con preeclampsia, desnutrición o avitaminosis.
Actualmente, los fortificadores de la leche materna proporcionan la cantidad adecuada de Ca y P, así como un incremento en la densidad calórica, por lo que se sugiere su uso con la finalidad de disminuir la desmineralización. Se ha recomendado que desde las dos semanas de vida extrauterina el ingreso de Ca al día debe ser de 200 mg/ kg/día y de P de 100 mg/kg/día, y que es necesario continuar con ese aporte hasta al menos la semana 40 de edad postmenstrual y aún por más tiempo en los prematuros que se alimentan exclusivamente con leche materna.29 En los pacientes de este estudio, el promedio general de Ca recomendado si se dio. No así el de P, que estuvo por debajo de lo sugerido, lo que pudo ser un factor coadyuvante para la presentación de la enfermedad, además de los ya mencionados.
La FA sérica y las radiografías de huesos largos fueron los mejores indicadores de osteopenia en este estudio. No se empleó la densitometría por no contar con ese recurso. Por otro lado, es importante comentar que en el período neonatal la FA total corresponde casi por completo a la fracción ósea, por lo que puede utilizarse como elemento para el diagnóstico de osteopenia.28 También es importante determinar puntos de corte de referencia (normalidad) para el RNPT de acuerdo con la técnica utilizada en las diferentes unidades en que atienden a este tipo de pacientes.
Se concluye que la osteopenia del prematuro se puede detectar alrededor de la tercera semana de vida extrauterina, con exámenes paraclínicos asequibles en la mayoría de las unidades que atiende este tipo de pacientes. Con mayor razón cuando se encuentran en tratamiento diuréticos, metilxantinas y esteroides. Estos resultados ofrecen un panorama diferente al ya conocido y reportado en la literatura. Tomando en cuenta estos datos, la prevención de la desmineralización ósea debe ser más tempranamente. Esto se logrará iniciando con aportes de minerales (Ca y P entre otros) necesarios en el RNPT, para mantener los niveles de Ca, P y FA normales desde el momento del ingreso a una UCIN o a un servicio de cuidados especiales de prematuros.
REFERENCIAS
1. Rubin LP. Trastornos del metabolismo del calcio y del fósforo. En: Taeusch HW, Ballard RAS, eds. Tratado de Neonatología de Avery. Madrid: Ediciones Harcourt SA; 2000. pp. 1189-1206. [ Links ]
2. Hospital Británico. Departamento de Pediatría. Unidad Neonatal. Osteopenia del prematuro. Arch Pediatr Urug 2006;77:290-292. [ Links ]
3. Brooke OG, Lucas A. Metabolic bone disease in preterm infants. Arch Dis Child 1985;60:682-685. [ Links ]
4. McIntosh N, Livesey A, Brooke OG. Plasma 25-hydroxyvitamin D and rickets in infants of extremely low birthweight. Arch Dis Child 1982;57:848-850. [ Links ]
5. Rigo J, De Curtis M, Pieltain C, Picaud JC, Salle BL, Senterre J. Bone mineral metabolism in the micropremie. Clin Perinatol 2000;27:147-170. [ Links ]
6. Prestidge LL, Schanler RJ, Shulman RJ, Burns PA, Laine LL. Effect of parenteral calcium and phosphorus therapy on mineral retention and bone mineral content in very low birth weight infants. J Pediatr 1993;122(5 Pt 1):761-768. [ Links ]
7. Shrivastava A, Lyon A, McIntosh N. The effect of dexamethasone on growth, mineral balance and bone mineralization in preterm infants with chronic lung disease. Eur J Pediatr 2000;159:380-384. [ Links ]
8. Moyer-Mileur L, Luetkemeier M, Boomer L, Chan GM. Effect of physical activity on bone mineralization in premature infants. J Pediatr 1995;127:620-625. [ Links ]
9. Litmanovitz I, Dolfin T, Friedland O, Arnon S, Regev R, Shainkin-Kestenbaum R, et al. Early physical activity intervention prevents decrease of bone strength in very low birth weight infants. Pediatrics 2003;112(1 Pt 1):15-19. [ Links ]
10. Moyer–Mileur LJ, Brunstetter V, McNaught TP, Gill G, Chang GM. Daily physical activity program increases bone mineralization and growth in preterm very low birth weight infants. Pediatrics 2000;106:1088-1092. [ Links ]
11. Eliakim A, Nemet D. Osteopenia of prematurity —the role of exercise in prevention and treatment. Pediatr Endocrinol Rev 2005;2:675-682. [ Links ]
12. Eliakim A, Shiff Y, Nemet D, Dolfin T. The effect of neonatal sepsis on bone turnover in very-low birth weight premature infants. J Pediatr Endocrinol Metab 2003;16:413-418. [ Links ]
13. Chan GM. Growth and bone mineral status of discharged very low birth weight infants fed different formulas or human milk. J Pediatr 1993;123:439-443. [ Links ]
14. Rowe J, Rowe D, Horak E, Spackman T, Saltzman R, Robinson S, et al. Hypophosphatemia and hypercalciuria in small premature infants fed human milk: evidence for inadequate dietary phosphorus. J Pediatr 1984;104:112-117. [ Links ]
15. Miller ME. The bone disease of preterm birth: a biomechanical perspective. Pediatr Res 2003;53:10-15. [ Links ]
16. Steichen JJ, Gratton TL, Tsan RC. Osteopenia of prematurity: the cause and possible treatment. J Pediatr 1980;96(3 Pt 2):528-534. [ Links ]
17. Kulkarni PB, Hall RT, Rhodes PG, Sheehan MB, Callenbach JC, Germann DR, et al. Rickets in very low-birth-weight infants. J Pediatr 1980;96:249-252. [ Links ]
18. Campbell D, Fleischman AR. Rickets of prematurity: controversies in causation and prevention. Clin Perinatol 1988;15:879-890. [ Links ]
19. James JA, Mayne PD, Barnes IC, Kovar IZ. Growth velocity and plasma alkaline phosphatase activity in the preterm infant. Early Hum Dev 1985;11:27-32. [ Links ]
20. Kovar I, Mayne P, Barltrop D. Plasma alkaline phosphatase activity: a screening test for rickets in preterm neonates. Lancet 1982;1:308-310. [ Links ]
21. Lucas A, Brooke OG, Baker BA, Bishop N, Morley R. High alkaline phosphatase activity and growth in preterm neonates. Arch Dis Child 1989;64:902-909. [ Links ]
22. Glass EJ, Hume R, Hendry GM, Strange RC, Forfar JO. Plasma alkaline phosphatase activity in rickets of prematurity. Arch Dis Child 1982;57:373-376. [ Links ]
23. Faerk J, Peitersen B, Petersen S, Michaelsen KF. Bone mineralization in premature infants cannot be predicted from serum alkaline phosphatase or serum phosphate. Arch Dis Child Fetal Neonatal Ed 2002;87:F133-F136. [ Links ]
24. Ballard JL, Khoury JC, Wedig K, Wang L, Eilers-Walsman BL, Lipp R. New Ballard Score, expanded to include extremely premature infants. J Pediatr 1991;119:417-423. [ Links ]
25. Papile LA, Burstein J, Burstein R, Koffler H. Incidence and evolution of subependymal and intraventricular hemorrhage: a study of infants with birth weights less than 1500 g. J Pediatr 1978;92:529-534. [ Links ]
26. Chang GM, Mileur L, Hansen JW. Effects of increased calcium and phosphorus formulas and human milk on bone mineralization in preterm infants. J Pediatr Gastroenterol Nutr 1986;5:444-449. [ Links ]
27. Gandy GM, Roberton NC. Neonatología. México D.F.: El Manual Moderno; 1989. p. 324. [ Links ]
28. Román NA, Wilson SJ, Beca IJP, Cortés EJM, Polette BV, Espíndola AAM. Fosfatasas alcalinas en el estudio de osteopenia del prematuro. Rev Chil Pediatr 1993;64: 359-363. [ Links ]
29. Ceriani-Cernadas JM, Fustiñana CA, Mariani G, Jenik A, Lupo EA. Neonatología Práctica. Buenos Aires: Editorial Médica Panamericana; 2009. p. 260. [ Links ]














