ANTECEDENTES
La lesión pulmonar aguda relacionada con la transfusión (TRALI, por sus siglas en inglés) es un síndrome de dificultad respiratoria causada por la transfusión de sangre. 1 Tiene una incidencia de 1 por cada 173,000 concentrados eritrocitarios transfundidos y mortalidad de 5 a 40% del total de los casos. La Food and Drug Administration (FDA) ubica a la TRALI como la principal causa de muerte asociada con la transfusión. 2 Las embarazadas se encuentran en desventaja por los múltiples factores de riesgo de esta complicación. Se desconoce si el embarazo afecta la incidencia y el pronóstico de TRALI, pues no hay suficiente bibliografía. Se describe el presente caso clínico para apoyar la bibliografía universal referente al tratamiento de la TRALI en una embarazada.
CASO CLÍNICO
Paciente de 35 años, con antecedente de tres embarazos, una cesárea y un aborto, alérgica a Nulliteli®, vitamina K y butilhiosina. Se estableció el diagnóstico de placenta previa marginal a las 20 semanas de gestación. En otro hospital fue valorada por amenaza de parto pretérmino y sangrado transvaginal, donde se inició el tratamiento médico con respuesta adecuada. Se reportó anemia normocítica normocrómica, con hemoglobina de 7 g/dL; esta fue la razón de la transfusión de 2 unidades de concentrado eritrocitario. El esquema de maduración pulmonar se inició con betametasona; en las siguientes 12 horas tuvo disnea y tos mínima, que progresivamente se fue incrementando.
Ingresó al Centro Médico Naval con reporte de 33.2 semanas de gestación, conforme a la fecha de la última menstruación tipo 1 (regular), amenaza de parto pretérmino posthemotransfusión de concentrado eritrocitario y síndrome de dificultad respiratoria del adulto. En la valoración tocoquirúrgica se advirtieron: disnea, con saturación de aire ambiente de 75% con recuperación de 96% con la aplicación de una mascarilla facial con bolsa reservorio. La presión arterial era normal. Los campos pulmonares con ruido respiratorio bilateral, crepitantes, infraescapulares derechos. Los ruidos cardiacos rítmicos se notaron con tendencia a la taquicardia. Edema en el miembro pélvico derecho. El electrocardiograma mostró elevación del segmento ST en V5 y V6. La gasometría arterial reportó alcalosis respiratoria e hipoxemia moderada.
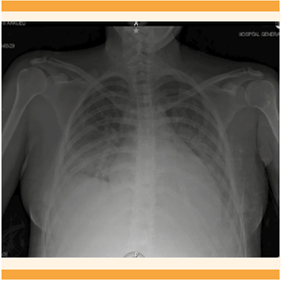
En la radiografía de tórax anteroposterior se observó un patrón reticular central, opacidad heterogénea basal interna y externa derecha, borramiento de los ángulos costodiafragmáticos bilaterales que sugerían derrame pleural bilateral mínimo. Figura 1
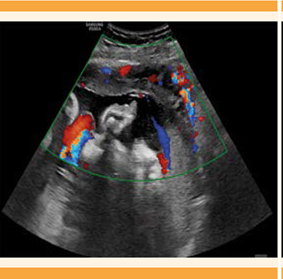
El ultrasonido obstétrico reportó embarazo de 30.6 semanas por fetometría, peso fetal estimado de 1984 g y líquido amniótico de 11.1 cc por Phelan, longitud cervical de 3.1 y placenta subcenturiata a 2.5 cm del orificio cervical interno, grado 1 de inserción baja, con datos de probable acretismo placentario, con interfase uterovesical hipervascularizada. Figura 2
El Doppler de los miembros pélvicos reportó datos de estasis venosa bilateral, negativo para trombosis. El ultrasonido hepático documentó incremento de la perfusión hepática arteriovenosa, quizá secundaria a sobrecarga hídrica. Figura 3

Figura 3 Doppler de miembro pélvico (izquierda). Ultrasonido hepático con incremento de la perfusión hepática arteriovenosa (derecha).
Se decidió ingresarla a terapia intensiva debido a insuficiencia respiratoria aguda y edema pulmonar. Glasgow de 15 puntos, Rass 0 puntos, sin datos de ingurgitación yugular, amplexión disminuida en ambas bases, estertores subcrepitantes bilaterales de predominio basal, con síndrome de derrame pleural bilateral de 20%. No se auscultó el tercer ruido cardiaco; diuresis normal por sonda Foley. Desde el punto de vista obstétrico no se encontró alteración, sin evidencia de actividad uterina.
Los signos y síntomas hicieron sospechar una reacción asociada con la transfusión: TRALI, sobrecarga de líquido asociada con la transfusión (TACO), neumonía o síndrome de dificultad respiratoria aguda, por eso se solicitaron exámenes complementarios.
El reporte fue de: péptido natriurético B (BNP) 135.7 ng/mL, CKmb 10 U/L, leucocitos en 13000, hemoglobina de 9.2 g/dL, plaquetas de 167 000, glucosa en 73 mg/dL, BUN de 6.6 mg/dL, creatinina con 0.5 mg/dL, Na 138 mmol/L, K 3.05 mmol/L.
El ecocardiograma reportó: corazón estructuralmente normal, movilidad segmentaria y global adecuada, función sistólica adecuada, fracción de eyección de 60%, fracción de acortamiento del 30%. Función diastólica adecuada, aparatos valvulares estructuralmente normales, competentes, insuficiencia tricuspídea leve con hipertensión arterial pulmonar leve y presión sistólica de la arteria pulmonar de 42 mmHg. Pericardio y grandes vasos de características normales. El septum en sus porciones interauricular e interventricular íntegro, sin evidencia de trombo intracavitario ni endocarditis vegetante.
Con el informe previo se estableció el diagnóstico de TRALI y se inició el tratamiento con furosemida y levosimendán, esquema con el que evolucionó clínica y paraclínicamente a la mejoría. Posterior a la estabilización hemodinámica y redistribución hemática se reportó anemia de 8 g/dL por lo que se le transfundieron dos concentrados eritrocitarios, sin contratiempos. Con las pruebas complementarias se descartó que tuviera anticuerpos atípicos.
La resonancia magnética documentó, nuevamente, placenta subcenturiata y acretismo placentario sin datos de invasión a la vejiga. Figura 4
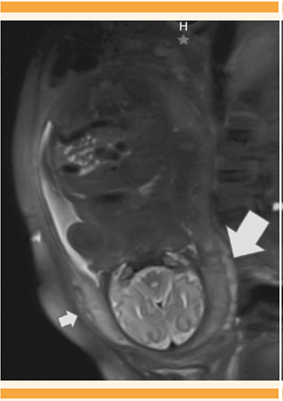
Figura 4 Placenta subcenturiata con lóbulo mayor posterior (flecha grande) y lóbulo menor en la parte anterior (flecha pequeña) en donde se sugiere acretismo placentario.
La cistoscopia reportó al fondo vesical y la pared anterior sin aumento de la vascularidad. La coloración del urotelio se encontró con características normales, el trígono vesical ligeramente hiperémico, y la uretra sin alteraciones; con esto se descartó la invasión vesical por placenta. Figura 5

Figura 5 (A y B) Meatos ureterales, (C) trígono y (D) fondo vesical sin evidencia de invasión placentaria.
Dos semanas posteriores a la recuperación de la alteración respiratoria y hemodinámica la paciente tuvo actividad uterina y ruptura prematura de membranas: se programó la finalización del embarazo mediante cesárea e histerectomía obstétrica, por acretismo placentario focal a nivel de la pared anterior a 2 cm del cuello uterino. El recién nacido, masculino, de 34 semanas de gestación por Capurro, con peso de 2590 gramos, Apgar 7/8 Silverman Anderson de 2. El sangrado se estimó en 1200 mililitros. (Figura 6) La paciente evolucionó satisfactoriamente y fue dada de alta del hospital sin contratiempos.
DISCUSIÓN
En 1964 Ashbaugh y su grupo describieron el síndrome de insuficiencia respiratoria aguda que comprende: dificultad respiratoria aguda, disminución de la adaptabilidad pulmonar, infiltrado alveolar difuso bilateral súbito e hiperemia. 3 Posteriormente, en 1985 Popovsky y sus colaboradores (citado por Kim y su grupo4) acuñaron el acrónimo TRALI (daño pulmonar relacionado con las transfusiones).2,4,5 En 2004 el consenso canadiense hizo mención de los criterios de TRALI: a) inicio agudo, b) hipoxemia (PaO2/ FiO2menor de 300 o SpO2 menor de 90%, sin oxígeno suplementario), c) radiografía de tórax con infiltrados bilaterales, d) sin evidencia de aumento de la presión en la aurícula izquierda. Todo esto sin lesión pulmonar aguda previa a la transfusión, con inicio en las primeras 6 horas de la transfusión y sin relación temporal con otros factores para lesión pulmonar aguda (aspiración de cuerpo extraño, neumonía, inhalación de toxinas, quemaduras, ahogamiento, politraumatismo, sobredosis de drogas, pancreatitis aguda, bypass cardiopulmonar). 6 A partir de este consenso los estudios y publicaciones posteriores definen al TRALI con estos criterios.7,8
Se reporta que la incidencia es de 1:432 unidades transfundidas para plaquetas, 1: 173,000 unidades transfundidas para concentrados eritrocitarios e incidencia general de 1.12%. La mortalidad se estima en 5 a 40% de los casos. Los datos estadísticos siguen siendo confusos porque en muchos centros hospitalarios no se tiene la cautela del reporte epidemiológico de los casos. 2,5,9,10
Cualquier componente sanguíneo puede originar TRALI, incluidos los productos derivados de la colecta de células madre y de algunos hemoderivados, como las gammaglobulinas endovenosas. En fin, todos los componentes ricos en plasma representan alto riesgo de inducción de TRALI. 2 Se reporta mayor riesgo de TRALI en: hemorragia posparto, leucemia mieloide aguda, trasplante hepático, trasplante alogénico y autólogo de células madre hematopoyéticas, politraumatismo y microangiopatía trombótica.11,12
En la paciente obstétrica se reporta que la incidencia de TRALI es de entre 0.7 y 15% en las receptoras. Como factores de riesgo se mencionan: sepsis obstétrica o puerperal, enfermedad hipertensiva del embarazo (con mayor incidencia en pacientes sin tratamiento) y hemorragia obstétrica. 2,13Los factores de riesgo dependientes del receptor incluyen: concentraciones elevadas de interleucina 6 y 8, disminución de la interleucina 10, edad avanzada, antecedentes de cirugía cardiotorácica y de cirugía hepática, choque, picos elevados de presión durante la ventilación mecánica, balance hídrico positivo, alcoholismo y tabaquismo. 11,14
La fisiopatología no está del todo definida, aunque se han descrito algunos mecanismos. Se describe que los polimorfonucleares secuestrados en la luz de los capilares pulmonares se activan y producen anión superóxido, que daña al endotelio, filtración capilar y daño pulmonar agudo. También en ausencia de neutrófilos; el factor de crecimiento endotelial vascular (VEGF) activa el endotelio pulmonar, daña los capilares pulmonares y de ello resultan el edema pulmonar no cardiogénico y daño pulmonar agudo. 14,15
El sistema antígeno leucocitario humano (HLA, por sus siglas en inglés) es una clase de genes que codifican para un grupo altamente polimórfico de moléculas del complejo HLA. El HLA se subdivide en 3 clases: a) los HLA de clase 1 con antígenos A, B y C se encuentran en todas las células nucleadas y plaquetas. b) Los HLA de clase II que portan los antígenos D, DR y DQ se localizan, predominantemente, en superficies dendríticas, macrófagos y células B. c) Los HLA clase III codifican los componentes del sistema del complemento.
Los antígenos de neutrófilos humanos (HNA, por sus siglas en inglés) son estructuras determinadas genéticamente en la superficie de neutrófilos, monocitos, linfocitos, plaquetas y células asesinas. Las personas pueden desarrollar anticuerpos HNA o HLA cuando su sistema inmunitario entra en contacto con un HNA o HLA externo; por ejemplo, durante el embarazo, la transfusión o el trasplante.4,12,16,17
Se habla de dos condiciones diferentes y relacionadas entre sí para el TRALI: “teoría de los dos golpes”. El primer golpe puede estar dado por una condición clínica del paciente que da como resultado el cebado de neutrófilos y su atracción al capilar pulmonar. El segundo golpe ocurre por la trasfusión de un producto sanguíneo que activa los neutrófilos y las vías de coagulación, lo que origina el TRALI. 5,10,18
La “teoría del modelo umbral” se basa en el nivel de cebado de los neutrófilos pulmonares y la capacidad de los mediadores en el producto de trasfusión para activar estos neutrófilos cebados. A mayor cantidad de neutrófilos activados secuestrados asociados con un hemocomponente de alto riesgo de TRALI, es menor el umbral, por lo que hay mayor riesgo de TRALI.9,12,18
El TRALI tiene una manifestación clínica indistinguible, salvo por su relación temporal con el acto de la transfusión, aparece entre la primera y la segunda hora de iniciada la transfusión y no más allá de 6 horas. 12
Los signos y síntomas asociados con TRALI pueden confundirse fácilmente con: sobrecarga de líquido asociada con la transfusión (TACO), neumonía y síndrome de dificultad respiratoria aguda. 19 Desde el punto de vista de la clínica hay taquipnea de aparición aguda, secreción pulmonar espumosa, hipotensión, fiebre, taquicardia y cianosis. 12
A la auscultación se encuentran estertores pulmonares diseminados. La presión venosa central y la presión en cuña de los capilares pulmonares resultan normales. La pauta para diferenciar el TRALI es que el edema pulmonar no es cardiogénico y que los pacientes no muestran sobrecarga de volumen, no se ausculta tercer ruido cardiaco de galope que haga sospechar una sobrecarga hemodinámica, tampoco hay ingurgitación de las venas yugulares, datos clínicos que pueden encontrarse en la sobrecarga de volumen relacionado con la transfusión (TACO) y con la insuficiencia cardiaca relacionada con la sobrecarga volumétrica de cualquier otro origen.15,19
Para el apoyo diagnóstico se utiliza el péptido natriurético-B como marcador bioquímico de sobrecarga de volúmenes y presiones. Este péptido natriurético-B se libera en los ventrículos cardiacos en respuesta a cambios en la presión intracavitaria cuando se llega a la insuficiencia cardiaca. Los valores ayudan a distinguir entre los diagnósticos diferenciales. El péptido natriurético-B menor de 150 pg/mL apoya el diagnóstico de TRALI. En cambio, el péptido natriurético-B mayor de 150 pg/mL apoya al diagnóstico de TACO. El péptido natriurético-B mayor de 250 pg/mL apunta al diagnóstico de insuficiencia cardiaca congestiva. En una paciente recién transfundida, la concentración absoluta de péptido natriurético-B mayor de 100 pg/dL con una razón péptido natriurético-B postransfusional-pretransfusional mayor de 1.5 hace descartar al TRALI como causa de daño pulmonar agudo. 4,5,15
La aparición relativamente súbita de infiltrado bilateral “algodonoso” en la radiografía anteroposterior simple de tórax no descarta TRALI. Los estudios de laboratorio tampoco aportan elementos que distingan entre un diagnóstico y otro. Se menciona a la leucopenia con neutropenia transitoria, acompañada o no de monocitopenia e hipocomplementemia durante la fase aguda del TRALI. El diagnóstico se basa en el conjunto de elementos clínicos, radiológicos y hemogasométricos sobre la base del descarte del resto de las posibles causas de daño pulmonar agudo.4,15
La prevención para eventos de TRALI se fundamenta en evitar transfusiones de hemoderivados provenientes de donantes implicados en TRALI, hacer pruebas anti HLA y de anticuerpos antigranulocitos a las unidades de los donantes implicados en TRALI, evitar hemoderivados provenientes de multíparas, uso universal de leucorreducción de las unidades de glóbulos rojos y transfusión de unidades frescas, exclusión de donantes mujeres, mujeres multíparas o donantes previamente transfundidos, lavado de productos de la transfusión y filtración.4,18,20,21
El tratamiento intensivo de la dificultad respiratoria con oxígeno y quizá ventilación mecánica no invasiva o invasiva, representa la primera línea del tratamiento del TRALI. 5,15,19,20En la Figura 1 se muestra el esquema propuesto para TRALI. 15

Figura 1 Diagrama para el diagnóstico y tratamiento de pacientes con ALI y TRALI. ALI = lesión pulmonar aguda. TACO = sobrecarga circulatoria por transfusión. TRALI = lesión pulmonar aguda por transfusión. PEEP = presión positiva al final de la expiración. BNP = péptido natriurético-B.
Hay suficiente evidencia de TRALI en pacientes en general, en menor cantidad hay evidencia en pacientes obstétricas, en quienes se reporta TRALI en el puerperio debido a transfusiones secundarias a hemorragia obstétrica; pero los reportes de casos de TRALI durante el embarazo son escasos. 21,22 Velázquez (2008) reportó una paciente de 19 años, con embarazo de 30 semanas, con anemia grave, diagnóstico en que se apoyó la indicación de trasfusión de concentrado eritrocitario, resultó con TRALI y requirió ventilación mecánica e inotrópicos durante 12 horas con dopamina, con buena evolución hasta que al quinto día tuvo trabajo de parto pretérmino, que no remitió con el tocolítico y el embarazo finalizó mediante cesárea, sin complicaciones. 20
Gibbs (2016) reportó el caso de una paciente de 35 años, con embarazo de 28.4 semanas, con hematoma espontáneo de rectos abdominales que requirió transfusión y resultó con TRALI. Se le indicó soporte ventilatorio no invasivo y tratamiento hemodinámico en terapia intensiva, con buena evolución hasta llegar a las 37 semanas y se indujo el parto. 23 En ambos casos, de la misma manera que nuestra paciente, tuvieron TRALI durante el embarazo, con asistencia ventilatoria y hemodinámica en terapia intensiva, hasta su normalización gradual y terminar el embarazo solo por indicación obstétrica. 4,20,21
CONCLUSIONES
El TRALI se asocia con hemorragia posparto y transfusión masiva. Existen muy pocos reportes documentados de TRALI en el periodo anterior al parto. Se desconoce si el embarazo afecta la incidencia y el pronóstico de TRALI, pues no hay suficiente bibliografía reportada. Las embarazadas se encuentran en desventaja por los cambios fisiológicos del embarazo: disminución del volumen residual, de la capacidad de reserva respiratoria y de la presión coloidosmótica capilar. Es importante establecer el diagnóstico de TRALI para tratarlo oportunamente y notificarlo para conocer la incidencia real y evaluar si el embarazo es causa de TRALI. El control y reversión de la insuficiencia respiratoria en TRALI debe efectuarse con un grupo multidisciplinario.











 nueva página del texto (beta)
nueva página del texto (beta)